Вплив супутньої терапії неврологічних і серцево-судинних уражень у хворих на цукровий діабет 2 типу
Цукровий діабет (ЦД) належить до патології, яка становить значну частку в структурі причин непрацездатності, інвалідності та смертності населення. За даними Всесвітньої організації охорони здоров’я (ВООЗ) та Міжнародної діабетичної федерації (IDF), чисельність хворих на ЦД у світі серед дорослого населення віком 20-79 років у 1985 р. становила 30 млн осіб, у 1995 р. цей показник сягнув 135 млн, у 2000 р. — 150,9 млн, у 2003 р. — 194 млн, у 2010 р. — 285 млн, у 2011 р. — 366 млн, у 2012 р. — 371 млн, у 2013 р. — 382 млн, що відповідає 8,3% населення, у 2015 р. зареєстровано 415 млн хворих, тобто 1 особа з 11 захворіла на ЦД, а на 2040 р. прогнозують 642 млн хворих, що охопить 10% населення Землі. Отже, показник поширеності цього захворювання у світі з 2003 р. і донині зріс більш ніж удвічі. Слід зазначити, що ця катастрофічна статистика поповнюється переважно за рахунок ЦД 2 типу, на який хворіють понад 90% осіб від загальної кількості виявлених.
У патогенезі ЦД 2 типу велике значення відіграє інсулінорезистентність (ІР). Мішенями її впливу є тканинні структури, які перебувають у прямій залежності від інсуліну щодо засвоєння глюкози (печінка, м’язи, жирова тканина, ендотелій). Добре відомо, що підтримання нормальної фізіологічної функції ендотелію — запорука здоров’я серцево-судинної системи. В осіб з ІР та гіперінсулінемією, що характеризує ЦД 2 типу, спостерігають переважання вазоконстрикторної властивості судин над вазодилатацією. В основі цієї схильності лежить активація симпатоадреналової та ренін-ангіотензинової систем. Активація однієї лише ренін-ангіотензинової системи, незалежно від інших впливів, відповідальна за підвищення артеріального тиску (АТ), чутливість до вазоконстрикторної дії глюкокортикоїдів, підвищений уміст кортизолу, зниження швидкості перетворення кортизолу на неактивні метаболіти.
Значну частину серед ускладнень ЦД 2 типу становить діабетична полінейропатія (складова хронічної мікроангіопатії), у патогенезі якої фіксують оксидативний стрес, глікування ліпідів, зростання рівнів факторів запалення (С-реактивний протеїн, інтерлейкіни, фактор некрозу пухлини-альфа), а порушення провідності нервовими волокнами пов’язують із втратою цілісності мієлінової оболонки тощо. За умови ІР надмір інтерлейкіну‑1β та фактора некрозу пухлини-альфа посилює адгезію лейкоцитів до ендотелію, прискорюючи атерогенез. Існує також патогенетична залежність між ІР та розвитком ангінозних приступів за ангіографічно незмінених, неуражених атеросклерозом коронарних артерій (так званий кардіальний синдром Х).
ІР є етіологічною складовою розвитку не лише ЦД 2 типу та його ускладнень, а й супутніх станів, таких як діабетична стопа, атеросклероз, артеріальна гіпертензія (АГ), ішемічна хвороба серця (ІХС). Окрім того, поєднуючись між собою, вони створюють умови для появи третіх патологічних станів. Наприклад, на тлі розвитку АГ та діабетичної енцефалопатії з’являється підвищена схильність до розвитку когнітивних порушень і хвороби Альцгеймера.
Окрім перелічених патогенетичних особливостей, простежують тісний зв’язок діабетичних ускладнень і коморбідних станів з ураженням вегетативної нервової системи (ВНС), що особливо помітно на прикладі гострих і хронічних форм ІХС, порушення мозкового кровообігу.
На початковій стадії ЦД 2 типу клінічна картина невиразна, а тому виявлення хвороби запізнюється. Як правило, на момент встановлення діагнозу діабетичні ускладнення досягають середнього ступеня тяжкості. Саме їх у вигляді яскравої неврологічної й серцево-судинної симптоматики супроводжують активним наглядом і медикаментозною терапією лікарі суміжних профілів. Препарати, які дали б змогу позитивно впливати на неврологічний статус, кардіоваскулярну патологію з погляду впливу на ІР, гіперінсулінемію, гіперглікемію та ВНС на момент відтермінованого початку лікування ЦД 2 типу, мали б значні переваги над іншими.
Аналіз літературних джерел свідчить, що іпідакрин (міжнародна назва), який належить до групи антихолінестеразних препаратів, виявляє універсальні нейрональні можливості, особливо актуальні при ЦД 2 типу з порушеннями ВНС.
Іпідакрин блокує проникнення крізь мембрану іонів калію, гальмує активність ацетилхолінестерази, відповідно збільшуючи тривалість життя ацетилхоліну й активність М-холінорецепторів, активує пре- й постсинаптичні ланцюги нейронної передачі імпульсу (Е.Ф. Лаврецька, 2002). Препарат здатний посилювати провідність нервовими волокнами й сприяти активації роботи гладком’язових волокон. Іпідакрин добре себе зарекомендував у лікуванні міастеній (Б.М. Гехт, А.Г. Санадзе, 2003).
До додаткових ефектів препарату належать незначна седативна й аналгетична дії, зумовлені пригніченням проникності нейронних мембран для іонів натрію (Б.М. Гехт, 2003; Д.И. Ромейко, 2009). Хоча на ринку існує значна кількість антихолінестеразних препаратів, іпідакрин, на відміну від інших, має не лише периферійний, а й центральний ефект, виявляючи водночас менше побічних ефектів.
За хвороби Альцгеймера головним чином уражаються великі півкулі мозку й гіпокамп. Іпідакрин із потоком крові накопичується в цих структурах, позитивно впливаючи на судинні когнітивні порушення, і пом’якшує перебіг хвороби. Під впливом іпідакрину спостерігали покращення пам’яті, уваги, концентрації, психічної активності, абстрактного мислення й конструктивних здібностей (В.В. Захаров, 2009). Існує достатньо доказів позитивного впливу іпідакрину на когнітивний статус під час реабілітації хворих після перенесеного ішемічного інсульту (Т.С. Мищенко, 2008).
Призначення іпідакрину хворим на діабетичну полінейропатію виявило низку позитивних ефектів. Засвідчено прискорення швидкості проведення збудження периферійними нервами, посилення нервово-м’язової провідності, відновлення рухових функцій і скоротливої здатності м’язів у хворих на діабетичну полінейропатію. Згідно з даними літературних джерел тривалий прийом іпідакрину не супроводжується серйозними побічними ефектами, добре переноситься хворими й може призначатися повторними курсами, що особливо важливо в умовах хронічного перебігу ЦД 2 типу. Саме тому низка авторів у алгоритмі лікування діабетичної полінейропатії окреслюють такі три напрями: 1) лікування больового синдрому (антидепресанти, антиконвульсанти); 2) корекція оксидативного стресу й ендотеліальної дисфункції (тіоктова кислота, гемодеривати, метаболічні засоби); 3) активація реіннервації за допомогою іпідакрину (И.А. Строков, 2013).
Якщо обговорювати докладніше другий пункт із перерахованих, слід розглянути коректор метаболізму мельдоній (міжнародна назва), здатний впливати на ендотеліальну функцію при ЦД 2 типу, його ускладненнях і супутніх станах (М. Dambrova, 2016). Зокрема, поєднане застосування препарату Мілдронат® (запатентована назва мельдонію, виробник – АТ «Гріндекс», Латвія) з еналаприлом у хворих на АГ сприяло нормалізації ендотеліальної дисфункції, добового профілю АТ, морфофункціонального стану міокарда лівого шлуночка (Ф.Е. Хлебодаров, 2009).
Препарат використовують у клінічній практиці протягом більш ніж 40 років, його ефекти є добре вивченими. Мілдронат® пригнічує перетворення гамма-бутиробетаїну (ГББ) на карнітин завдяки впливу на фермент ГББ-гідроксилазу. Цей процес сприяє оптимізації синтезу носіїв енергії в ішемізованих тканинах.
Окрім того, під впливом мельдонію відбувається активація ендотеліальної синтази оксиду азоту (NO) та його біосинтез, що запускає каскад NO-залежних ефектів із відновленням функції ендотелію. Зниження рівня карнітину під впливом препарату сприяє активації гліколізу, зменшенню потреби тканин у кисні, гальмуванню окислення жирних кислот (ЖК). Мельдоній активує холін- і катехоламінергічні рецептори в центральній і периферичній нервовій системах, водночас забезпечуючи селективну дію щодо певних відділів ВНС і часткове пригнічення симпатоадреналової системи (С.Г. Бурчинский, 2015). Вибірковість дії мельдонію зумовлює зменшення ризику розвитку побічних і небажаних ефектів. Останні клінічні дослідження вказують, що до нозологічних мішеней впливу мельдонію належать: серцева недостатність, атеросклероз, нейродегенеративні захворювання, ЦД.
Процеси окислення ЖК і глюкози перебувають у реципрокній залежності: якщо пригнічується окислення ЖК, то посилюється споживання глюкози. За умови нестачі кисню, що спостерігається при ІХС, клітині стає вигіднішим використовувати окислення глюкози, бо для цього необхідно менше кисню. Мілдронат®, сповільнюючи транспорт ЖК (саме довголанцюгових ЖК), зменшує їх окислення, а тому потреба клітини в кисні знижується. Слід зазначити, що коротколанцюгові ЖК проходять крізь мітохондріальну мембрану без обмежень. Знижується рівень карнітину та підвищується концентрація ГББ. Сповільнене використання ЖК запускає альтернативний механізм отримання енергії — окислення глюкози, яка на 12% ефективніше використовує кисень для синтезу АТФ. Мілдронат® стимулює аеробний гліколіз, зменшує вміст лактату та ІР, а також запобігає накопиченню проміжних продуктів обміну (ацилкарнітину й ацил-КоА) та їх шкідливому впливу (Н.Ф. Сорока, 2012). Дослідження останніх років засвідчують, що довголанцюгові ацилкарнітини беруть безпосередню участь у розвитку ІР та ЦД 2 типу (M.G. Schooneman, 2013). Відомий лише один терапевтичний засіб — Мілдронат®, здатний знижувати вміст ацилкарнітинів, і він може призначатися разом із різними протидіабетичними засобами для впливу на ІР.
M. Roustit і співавт. довели, що ендотеліальна дисфункція — це першочергова сполучна ланка між кардіоваскулярним ризиком і діабетичною полінейропатією. З огляду на дані літературних джерел обидва лікарські засоби — іпідакрин і мельдоній — здатні в той чи інший спосіб забезпечити вплив на васкулярні та неврологічні порушення, що супроводжують ЦД 2 типу у вигляді ускладнень (діабетична полінейропатія, діабетична енцефалопатія) та коморбідних станів (ІХС, АГ, атеросклероз), в основі патогенезу яких лежить пошкодження ендотелію.
Мета дослідження — оцінювання ефективності препарату Ипигрикс® (запатентована назва іпідакрину, виробник – АТ «Гріндекс», Латвія) самостійно та в комбінації з препаратом Мілдронат® на тлі основного лікування в пацієнтів із ЦД 2 типу, що страждають на діабетичну полінейропатію, діабетичну енцефалопатію, ІХС і АГ.
Матеріали та методи
Для досягнення мети було поставлено такі завдання: проаналізувати закономірності суб’єктивних клініко-неврологічних та ендокринологічних змін у хворих на ЦД 2 типу під впливом обраних медикаментів до та після терапії; зіставити динаміку об’єктивних клініко-неврологічних та ендокринологічних змін під впливом певного терапевтичного підходу у хворих на ЦД 2 типу з коморбідними станами; оцінити самостійний вплив препарату Ипигрикс® та вплив його комбінації з препаратом Мілдронат® на рівень АТ і клініко-лабораторні показники; уточнити наявність побічних ефектів і ступінь прихильності до лікування монотерапією та комбінацією препаратів хворих на ЦД 2 типу із супутньою патологією.
До критеріїв виключення з дослідження належали: ІХС зі стенокардією напруження IV функціонального класу, застійна серцева недостатність, тяжкі порушення ритму серця, злоякісна АГ, тяжкі порушення функції печінки й нирок, супутні ендокринні й психіатричні захворювання, гіперчутливість і/або алергічні реакції до препаратів, що аналізують.
Було залучено 135 хворих на ЦД 2 типу, які страждали на діабетичну полінейропатію, діабетичну енцефалопатію, ІХС і АГ (82 жінки й 53 чоловіки), віком від 45 до 69 років. Під час проведення спостереження впродовж перших тижнів лікування відсіяли 23 особи через такі причини: порушення хворими дієти та способу життя, шкідливі звички, самовільні зміни в дозуванні медикаментів, неявка на черговий огляд, помилки під час застосування препаратів. Відібраних 112 пацієнтів розподілили на дві групи.
Перша група охопила 58 хворих (32 жінки й 26 чоловіків), друга — 54 хворих (33 жінки й 21 чоловік). У першій групі пацієнти на тлі базисного лікування отримували Ипигрикс®, у другій — комбінацію препаратів Ипигрикс® та Мілдронат®. Ипигрикс® призначали внутрішньом’язово в дозі 15 мг/мл, а Мілдронат® — перорально в дозі 500 мг 2 р/добу. Курс супутнього лікування тривав 1,5 міс.
Протидіабетичну терапію проводили відповідно до Уніфікованого клінічного протоколу первинної та вторинної (спеціалізованої) медичної допомоги «Цукровий діабет 2 типу», затвердженого наказом МОЗ України № 1118 від 21 грудня 2012 р. Дозування та кратність прийому медикаментів (цукрознижувальних, антиаритмічних, гіпотензивних, антиангінальних тощо), які вживали хворі протягом періоду спостереження, не змінювалися.
До та після проведеної додаткової терапії здійснювали такі обстеження: неврологічні дослідження за допомогою шкали неврологічних розладів NDS (Neuropathy Disability Score), що включає в себе визначення порогу вібраційної чутливості на головці першої плеснової кістки, визначення температурної чутливості за допомогою тіп-термера на тильній поверхні стопи, аналіз больової чутливості шляхом дотикання гострим і тупим предметами проксимально до великого пальця стопи, спостереження за ахілловим рефлексом, оцінювання тактильної чутливості за допомогою монофіламенту 10 г шляхом дотикання до дистальних фаланг першого, третього, п’ятого пальців стопи, до проекцій на підошві головок першої, третьої, п’ятої плеснових кісток, до латеральної й медіальної точок склепіння, до підошовної поверхні п’ятки, до точки проекції на тильній поверхні стопи між другою та третьою плесновими кістками; дослідження суб’єктивних відчуттів і переживань пацієнта за допомогою опитувальника з визначення рівня болю PainDETECT, що містить 12 цілеспрямованих запитань; дослідження прихильності пацієнтів до призначення додаткової терапії за допомогою письмового опитувальника; якісні дослідження ІР за допомогою визначення рівня лактату як індикатора клітинної чутливості до інсуліну, насамперед впливу на м’язову ІР; визначення рівнів холестерину ліпопротеїнів високої (ЛПВГ) та низької густини (ЛПНГ), загального холестерину, тригліцеридів (ТГ), глюкози й інсуліну крові натще, HOMA-індексу ІР (НОМА-IR) як інтегральних показників печінкової ІР та атерогенезу; визначення рівнів мікроальбумінурії, креатиніну крові, швидкості клубочкової фільтрації (ШКФ) як маркерів ендотеліальної ІР та вказівок на функціональний стан гломерулярної функції нирок; контроль ефективності комбінованого лікування шляхом визначення рівня HbA1c; визначення рівня кортизолу як маркера впливу на гіпоталамо-гіпофізарно-наднирникову вісь.
Вміст глюкози, HbA1c, креатиніну, лактату, загального холестерину, ТГ, холестерину ЛПВГ і ЛПНГ визначали на біохімічному аналізаторі Cobas Integra 400 plus. Кількісне визначення рівня мікроальбуміну сечі проводили на біохімічному фотометр-аналізаторі ВА‑88. Вміст інсуліну, кортизолу визначали за допомогою імунохемілюмінесцентного методу на імунологічному аналізаторі Immulite 1000. Індекс НОМА-IR розраховували за формулою: глюкоза натще (ммоль/л) × інсулін натще (мкОд/мл) / 22,5. ШКФ розраховували за формулою CRD-EPI.
Для зручності контролю динаміки лікування неврологічного ураження застосовували прийняті системи бальної оцінки (шкали NDS, опитувальника PainDETECT, тактильної чутливості за допомогою монофіламенту).
Отож об’єктами нашого дослідження були неврологічні та васкулярні ураження при ЦД 2 типу, а предметом дослідження — вибір оптимального терапевтичного підходу з двох використаних.
Математичний аналіз результатів дослідження виконали за допомогою методів параметричної статистики з використанням програмного забезпечення Excel (Microsoft, США) та Statistica 6.0 (StatSoft, США), що ґрунтувалося на даних літературних джерел.
Різницю між порівнюваними вибірками оцінювали як достовірну за р<0,05. Для опису отриманих результатів також використовували тенденцію до вірогідної зміни 0,05<р<0,1, оскільки вважали, що такі спостереження можуть вказати шлях подальшого пошуку з більшою вибіркою та тривалішим часом спостереження.
Результати та їх обговорення
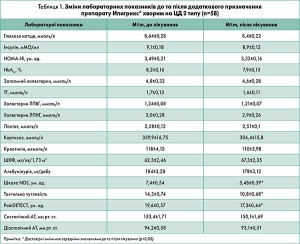
Під впливом призначення препарату Ипигрикс® спостерігали вірогідні зміни згідно з даними оцінювання тактильної чутливості стопи за допомогою монофіламенту, шкали NDS та опитувальника PainDETECT (табл. 1).
Вважають, що якщо чутливість (10 г/см2) не збережена в чотирьох із десяти локусів під час використання монофіламенту, то пацієнт належить до групи підвищеного ризику. У результаті комплексної терапії стан тактильної чутливості покращився: від 14,3±0,74 до 10,8±0,68 ум. од.
Застосування іпідакрину почалося в умовах неврологічної клініки, але з роками препарат добре себе зарекомендував і в ендокринології. Найчастіше іпідакрин призначають у діабетології, проте останнім часом з’явилися роботи, які засвідчують доцільність його використання і в тиреоїдології. Зокрема, з метою нейропротекції іпідакрин застосовують у комплексному лікуванні пацієнтів із гіпотиреозом і неврологічними ускладненнями, оскільки під дією препарату встановлено зменшення виразності координаторних розладів та поліневропатичних порушень (И.И. Шоломов, 2011). Позитивна динаміка щодо останніх не випадкова. Іпідакрин виявляє безпосередній вплив у пацієнтів з ураженням периферійних рухових нервів різної етіології. Його застосування сприяє достовірному посиленню швидкості проведення імпульсу нервовими волокнами, збільшенню амплітуди й частоти м’язових коливань під час довільних скорочень, що підтверджує процеси відновлення функції периферійних нервів (И.В. Дамулин, 2008).
З цього погляду визначення втрати чутливості за шкалою NDS, що має чотири складові (вібраційна, больова, температурна види чутливості, ахілловий рефлекс), є особливо актуальним.
Комплексна терапія з додаванням препарату Ипигрикс® виявила сприятливе зниження сумарної оцінки за шкалою NDS у досліджуваних пацієнтів: від 7,4±0,54 до 5,48±0,39 ум. од. Наші дані підтверджують думку низки вчених про те, що до алгоритму лікування діабетичних полінейропатій слід залучати іпідакрин, який покращує нервово-м’язову холінергічну передачу, нормалізує стан мембрани периферійних нервів, стимулюючи таким чином процеси регенерації й реіннервації в структурах периферичної нервової системи.
Суб’єктивний аналіз больових відчуттів хворих згідно з опитувальником PainDETECT також продемонстрував позитивну динаміку: показники знизилися з 19,6±0,57 до 17,3±0,44 ум. од. Наші спостереження збігаються з даними інших дослідників, які рекомендують застосовувати цей метод для аналізу неврологічних уражень, що супроводжуються болем та іншими суб’єктивними відчуттями, у тому числі у хворих на ЦД 2 типу.
Отже, результати нашого дослідження не мають розбіжностей із результатами інших учених і вказують на позитивну динаміку застосування препарату Ипигрикс® у хворих із комбінованою патологією та ускладненнями ЦД 2 типу, що раніше в такому ракурсі не вивчалися.
Водночас додавання препарату Ипигрикс® до основного лікування не вплинуло на такі показники вуглеводного обміну, як уміст глюкози, інсуліну, лактату, рівень HbA1c та індекс НОМА-IR. Ми також не спостерігали жодних змін систолічного та діастолічного АТ упродовж періоду спостереження. Концентрація кортизолу в крові, значення ліпідограми, рівень креатиніну в крові, ШКФ та альбумінурія до та після лікування не відрізнялися.
Аналіз прихильності до лікування препаратом Ипигрикс® та його переносимості засвідчив відсутність будь-яких негативних оцінок з боку пацієнтів. Більшість із них бажали продовжувати лікування препаратом завдяки виразному покращенню неврологічної симптоматики.
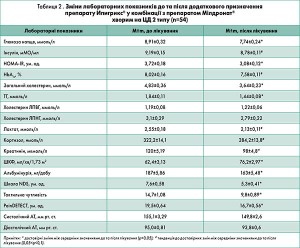
! Додаткове призначення препарату Мілдронат® у нашому дослідженні сприяло зниженню вмісту глюкози в крові натще (від 8,91±0,32 до 7,74±0,24 ммоль/л), індексу НОМА-IR (від 3,72±0,18 до 3,08±0,12 ум. од.), а рівні HbA1c, інсуліну та лактату мали тенденції до зниження (табл. 2). За свідченнями низки досліджень, мельдоній підвищує чутливість до інсуліну) (F. Inoue, 1999). Існують дані, які свідчать, що супутнє застосування препарату Мілдронат® упродовж 12 тиж у хворих із субкомпенсованим і компенсованим ЦД 2 типу на тлі прийому метформіну та глібенкламіду також дало змогу знизити вміст глюкози в крові на 11,85%, а рівень HbA1c — на 9,14% (М.В. Лобанова, 2008). Ці результати узгоджуються з результатами низки дослідників, що засвідчили достовірне зменшення рівнів HbA1c і ТГ після додаткового призначення препарату Мілдронат® хворим на ЦД 2 типу після тримісячного курсу терапії (М.Е. Стаценко, 2008).
Натомість наше спостереження виявило зменшення рівня не лише ТГ (із 1,84 до 1,44 ммоль/л), а й загального холестерину (з 4,83 до 3,64 ммоль/л). Схожі висновки отримано й у результаті лікування хворих на дисциркуляторну енцефалопатію атеросклеротичного генезу (Г.П. Хасенова, 2012). На тлі гіполіпідемічної терапії та додаткового застосування препарату Мілдронат® констатували зниження концентрації загального холестерину на 23,36% (-1,75 ммоль/л), ТГ — на 11,75% (-0,37 ммоль/л). Виявлена в нашій роботі тенденція до зниження рівнів інсуліну (від 9,19±0,15 до 8,78±0,11 мМО/мл) та HbA1c (від 8,02±0,16 до 7,58±0,11%), очевидно, пов’язана з коротким терміном спостереження. Попри це індекс НОМА-IR достовірно знизився.
Встановлено, що застосування мельдонію в режимі монотерапії чи в комбінації з метформіном у щурів Zucker із ожирінням сприяло зниженню вмісту лактату та запобігало метформін-індукованому лактат-ацидозу (Е. Liepinsh, 2011). Автори дослідження зробили висновок, що додавання мельдонію до метформіну має значні переваги в лікуванні гіперглікемії, гіперліпідемії та ІР. До певної міри ми також можемо погодитися з потенційними можливостями препарату Мілдронат®, оскільки спостерігали тенденцію до зниження рівня лактату після його додаткового призначення (2,55±0,18 до 2,13±0,11 ммоль/л).
Уперше в нашій роботі відзначено тенденцію до зменшення рівня кортизолу на тлі додаткового призначення препарату Мілдронат® хворим на ЦД 2 типу із супутньою серцево-судинною та неврологічною патологією (від 322,2±14,1 до 284,2±13,8 нмоль/л). Схожі дані отримано лише в одному з відомих нам досліджень у хворих на ІХС, хронічну серцеву недостатність зі збереженою систолічною функцією без ЦД 2 типу під впливом мельдонію (А.В. Курята, 2011).
У роботі М.Є. Стаценко і співавт. було виявлено, що прийом препарату Мілдронат® упродовж 16 тиж підвищував ШКФ, знижував рівні креатиніну крові та альбумінурію у хворих на ЦД 2 типу в постінфарктному періоді. У 12-тижневому дослідженні В.І. Паньківа з додаванням мельдонію в межах комплексного лікування хворих на ЦД 2 типу спостерігали значуще покращення функціонального стану нирок, на що вказувало виразне зниження рівнів альбумінурії, креатиніну й збільшення ШКФ. За даними нашого аналізу, встановлено вірогідне зменшення екскреції альбумінів із сечею (від 187±5,86 до 163±5,48 мг/добу), креатиніну крові (від 120±5,19 до 98±4,8 мкмоль/л) та зростання ШКФ (від 62,4±3,13 до 76,2±2,97 мл/хв/1,73 м2). Вважаємо, що нефропротективний ефект мельдонію можна пояснити впливом на ендотеліальну дисфункцію — патогенетичну складову ЦД 2 типу.
Цікавий аспект впливу препарату Мілдронат® на ендотеліальну дисфункцію продемонстровано в рандомізованому подвійному сліпому плацебо-контрольованому клінічному дослідженні MI&CI («Мілдронат® — ефективність і безпечність при лікуванні пацієнтів із переміжною кульгавістю»). Застосування препарату Мілдронат® упродовж 24 тиж у дозі 1 г/добу сприяло статистично достовірному зменшенню проявів переміжної кульгавості. Найчастіше на цю хворобу страждають пацієнти з ЦД 2 типу.
Автори спостереження вважають, що отримані результати позитивного впливу на ендотелій дають змогу рекомендувати Мілдронат® хворим на діабетичну ангіопатію нижніх кінцівок. Інше подвійне сліпе перехресне дослідження також виявило позитивний вплив мельдонію на функцію ендотелію завдяки стимуляції синтезу NO. Відзначено покращення ендотелій-залежної вазодилатації у хворих зі стабільною хронічною серцевою недостатністю.
Оцінювання симптомів діабетичної нейропатії за шкалою NDS дало змогу виявити виразні достовірні позитивні зміни вібраційної, температурної, больової, тактильної чутливості, а також ахіллового рефлексу. Наші дані підтверджуються низкою досліджень, у яких було з’ясовано, зокрема, що додаткове призначення препарату Мілдронат® супроводжується відчутнішою редукцією симптомів порівняно з монотерапією альфа-ліпоєвою кислотою.
Після додаткового супутнього лікування метаболічним коректором Мілдронат® нами зафіксовано меншу виразність больових ознак за даними опитувальника PainDETECT і відновлення тактильної чутливості на стопі, котру визначали за допомогою монофіламенту. Відкрите рандомізоване тримісячне клінічне дослідження хворих на ЦД 2 типу, яким додатково призначили мельдоній, також виявило, що препарат сприяє збільшенню швидкості поширення імпульсу нервовими волокнами, зниженню інтенсивності болю та відчуття оніміння кінцівок, чинить позитивний вплив на мікроциркуляцію шкіри (позитивний вплив на діабетичну нейропатію й мікроангіопатію).
Мілдронат® став лауреатом всеукраїнської премії «Панацея» (2011) як найкращий рецептурний препарат для лікування захворювань серцево-судинної системи. Вважають, що Мілдронат® посилює дію інгібіторів ангіотензинперетворювального ферменту, нітрогліцерину, блокаторів кальцієвих каналів, бета-адреноблокаторів та інших гіпотензивних препаратів, потенціює дію серцевих глікозидів. Під час нашого спостереження не виявлено впливу препарату Мілдронат® на рівень систолічного й діастолічного АТ.
Імовірно, розширення часових рамок могло би підтвердити дані тривалих спостережень інших учених.
Стосовно прихильності до лікування мельдонієм вдалося виявити роботу В.В. Пономарьова і співавт., які на базі клінічної лікарні м. Мінськ (Республіка Білорусь) провели рандомізоване дослідження 60 пацієнтів із хронічною судинно-мозковою недостатністю та визнали прихильність хворих до лікування препаратом і добру його переносимість.
Отже, проведене нами клінічне дослідження виявило виняткові сприятливі ефекти додаткового лікування комбінацією препаратів іпідакрину та мельдонію у хворих на ЦД 2 типу із супутньою серцево-судинною й неврологічною симптоматикою.
Тож, ураховуючи дані доказової бази препарату Мілдронат® і результати нашого дослідження, можна зробити такі висновки:
1. Аналіз клініко-неврологічних даних (тактильна чутливість, шкала неврологічних розладів NDS, опитувальник із визначення рівня болю PainDETECT) вказує на виразні позитивні зрушення під впливом додаткового призначення препарату Ипигрикс® хворим на ЦД 2 типу із супутньою серцево-судинною та неврологічною патологією.
2. Застосування препарату Мілдронат® на тлі основної терапії ЦД 2 типу в комбінації з препаратом Ипигрикс®, окрім позитивної динаміки змін тактильної чутливості, оцінки за шкалою NDS і опитувальника PainDETECT, сприяло зниженню альбумінурії, рівня креатиніну крові та збільшенню показників ШКФ, що свідчить на користь нефропротекції та пом’якшення перебігу ендотеліальної дисфункції.
3. Супутнє застосування препарату Мілдронат® у хворих на ЦД 2 типу супроводжувалося зниженням рівнів загального холестерину та ТГ, що забезпечило часткове відновлення ліпідного профілю й антиатерогенний ефект відповідно.
4. Призначення препарату Мілдронат® хворим на ЦД 2 типу з проявами мікро- та макроангіопатії характеризувалося зниженням концентрації глюкози та індексу НОМА-IR, що підтверджує здатність препарату впливати на вуглеводний обмін завдяки підвищенню чутливості тканин до інсуліну та покращенню утилізації глюкози. Рівні інсуліну, HbA1c, кортизолу та лактату виявили тенденцію до зниження.
5. В обох групах спостерігали позитивні зрушення після проведеного лікування, однак поєднана терапія іпідакрином і мельдонієм засвідчила значні переваги.
Список літератури знаходиться в редакції.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
21 березня в рамках II Міжнародної школи «Сучасний лікар: від теорії до практики» професор кафедри ендокринології Львівського національного медичного університету ім. Данила Галицького, лікар-ендокринолог вищої категорії, доктор медичних наук Вікторія Олександрівна Сергієнко представила доповідь, присвячену хронічним ускладненням цукрового діабету (ЦД). Зокрема, було акцентовано увагу на причинах розвитку діабетичної полінейропатії (ДП), розглянуто клінічні варіанти цього ускладнення, діагностичні підходи та основні принципи лікування. Пропонуємо огляд цієї доповіді у форматі «запитання – відповідь»....
Останніми десятиліттями в усьому світі спостерігалося значне зростання поширеності цукрового діабету (ЦД), що зумовило серйозні наслідки стосовно якості життя населення, а також спричинило певний тягар для системи охорони здоров’я та економічні витрати [1]. За даними Діабетичного атласу Міжнародної діабетичної федерації (International Diabetes Federation Diabetes Atlas), у 2021 р. ≈537 млн людей мали ЦД і, за прогнозами, до 2045 р. цей показник досягне 783 млн [2]. Значна захворюваність і підвищена смертність асоційовані з пов’язаними із ЦД макросудинними (інфаркт міокарда, інсульт) і мікросудинними (сліпота, ниркова недостатність, ампутації) ускладненнями [3]....
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....