Эзомепразол: новые аспекты клинического применения
Несмотря на большое количество публикаций, посвященных ингибиторам протонной помпы (ИПП), интерес к ним по-прежнему стабильно высок: в центре повышенного внимания многих ученых находятся ингибиторы водородно-калиевой аденозинтрифосфатазы (Н+-К+-АТФазы) последнего поколения, в частности эзомепразол. Первый чистый оптический изомер среди ИПП (S-стереоизомер омепразола), эзомепразол по праву считается препаратом с устойчивым метаболизмом, высокой биодоступностью, мощным, хорошо предсказуемым и продолжительным антисекреторным действием. Именно появление S-изомера омепразола связывают с разработкой новой эффективной схемы профилактики рецидивов гастроэзофагеальной рефлюксной болезни (ГЭРБ) – так называемой терапии по требованию. Заняв одно из лидирующих мест в терапии различных кислотозависимых заболеваний, эзомепразол продолжает укреплять свои позиции на фармацевтическом рынке.
Немаловажную роль в этом сыграли новые данные доказательной медицины. Результаты наиболее значимых рандомизированных контролированных исследований (РКИ) и метаанализов, раскрывающие достоинства и преимущества эзомепразола, приведены в данном обзоре.
ГЭРБ
Данные, полученные доказательной медициной за последние несколько лет, свидетельствуют, что эзомепразол успешно нивелирует проявления неэрозивной (НЭРБ) и эрозивной форм ГЭРБ. Например, в РКИ, проведенном Jing Sun и соавт. (2015), приняли участие пациенты с типичными симптомами гастроэзофагеального рефлюкса (изжога и/или регургитация), у которых при эндоскопическом обследовании не выявлено эрозивно-язвенного поражения слизистой оболочки пищевода. В инициальной фазе терапии всем пациентам рекомендовали принимать эзомепразол в суточной дозе 20 мг на протяжении 8 (n=154) или 2 нед (n=151). В случае эффективности назначенного лечения больных переводили во II фазу исследования, предполагавшую прием эзомепразола в режиме «по требованию» или проведение постоянной поддерживающей терапии на протяжении 24 нед. Общая длительность терапии составила 26 и 32 нед (для пациентов, принимавших эзомепразол в инициальной фазе на протяжении 2 и 8 нед соответственно). Первичной конечной точкой данного РКИ была эффективность контроля симптомов НЭРБ при проведении поддерживающей терапии / приеме препарата «по требованию». Вторичная конечная точка охватывала несколько показателей: количество рецидивов, эффективность назначенной терапии, время, прошедшее до появления первого рецидива НЭРБ, и удовлетворенность пациентов лечением.
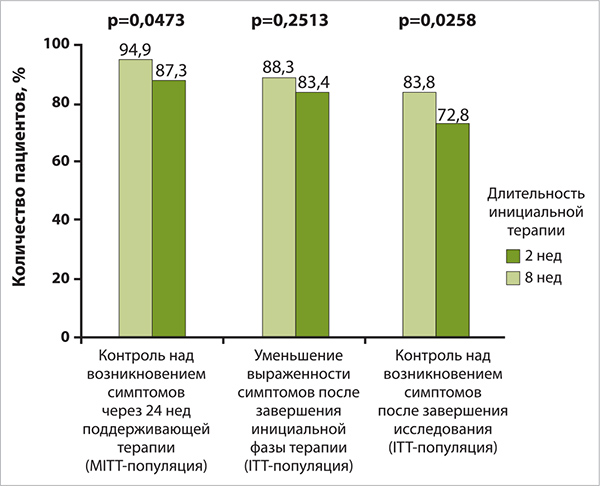
Полученные данные исследователи подвергли тщательному статистическому анализу, изучив эффективность эзомепразола в двух когортах больных: у начавших получать лечение (ITT-популяция; n=305), а также у тех, у кого инициальная терапия эзомепразолом способствовала уменьшению выраженности клинических проявлений НЭРБ (модифицированная ITT-популяция, МITT; n=262). В МITT-популяции ученые зафиксировали небольшие, но статистически достоверные различия, подтверждавшие превосходство 8-недельной инициальной терапии над 2-недельным режимом (94,9 vs 87,3%; р=0,0473).
Результаты, полученные в ITT-популяции, также подтвердили превосходство 8-недельной терапии, однако в данном случае межгрупповые различия оказались статистически недостоверными: 88,3 vs 83,4% (р=0,2513). В ITT-популяции результативность полного курса лечения (инициальной и поддерживающей терапии) при применении 8-недельного режима значительно превосходила аналогичный показатель при использовании 2-недельной схемы (83,8 vs 72,8%; р=0,0258). Еще одним неоспоримым преимуществом длительной инициальной терапии эзомепразолом оказалось снижение риска рецидива НЭРБ на 46% по сравнению с более короткой продолжительностью первоначального лечения (относительный риск (ОР) 0,543; 95% доверительный интервал (ДИ) 0,388-0,761). Меньшее количество внеплановых визитов больных к врачам и более высокая степень удовлетворенности пациентов проведенным лечением подтвердили превосходство 8-недельной терапии по сравнению с 2-недельным режимом. Приняв во внимание сопоставимую безопасность лечения в обеих группах, ученые рекомендовали назначать больным НЭРБ наиболее эффективную схему терапии эзомепразолом, предусматривающую 8-недельный инициальный курс приема препарата (рис.).
В настоящее время не только определена оптимальная длительность первоначального лечения эзомепразолом, но и разработана наиболее эффективная схема противорецидивного лечения НЭРБ. По мнению Е. Bayerdоrffer и соавт. (2016), таким режимом является терапия «по требованию». К данному выводу исследователи пришли, проанализировав результаты многоцентрового РКИ, в котором приняли участие больные с НЭРБ, не имеющие изжоги после 4-недельного инициального курса терапии эзомепразолом. В соответствии с дизайном исследования пациентов рандомизировали в 2 группы для проведения 6-месячного противорецидивного лечения: из 877 пациентов, ответивших на инициальную терапию эзомепразолом, 297 получали постоянную поддерживающую терапию, 301 пациенту рекомендована терапия «по требованию». Первичной конечной точкой РКИ являлось досрочное завершение лечения, обусловленное неудовлетворенностью пациентов результатами терапии.
Исследователи установили, что 9,8 и 6,3% пациентов из 1-й (n=297) и 2-й (n=301) группы соответственно, то есть находившихся на постоянной поддерживающей терапии и принимавших ИПП «по требованию», преждевременно прекратили прием препарата по причине неудовлетворенности лечением (межгрупповые различия (МГ) -3,5%; 95% ДИ от -7,1 до 0,2%). В общей сложности 82,1 и 86,2% больных, получавших терапию «по требованию» и постоянную поддерживающую терапию соответственно, были удовлетворены способностью эзомепразола купировать изжогу и регургитацию (р>0,05). В то же время среднесуточное количество таблеток эзомепразола при использовании такого вида противорецидивного лечения, как терапия «по требованию», составило 0,41 таблетки/сут, при применении постоянной поддерживающей терапии этот показатель был значительно больше – 0,91 таблетки/сут. Доказав сопоставимую эффективность двух видов противорецидивного лечения НЭРБ эзомепразолом, Е. Bayerdоrffer и соавт. отдали предпочтение методу, требующему минимальных экономических затрат: терапии «по требованию».
В настоящее время опубликовано достаточное количество результатов многих РКИ, доказавших эффективность эзомепразола в лечении эрозивной формы ГЭРБ, поэтому современные разработки в данной области направлены на определение наиболее результативной схемы приема препарата. Одной из таких работ является исследование, осуществленное под руководством P.I. Hsu (2015). В испытании приняли участие больные эрозивным эзофагитом степени А и В (по Лос-Анджелесской классификации), которых рандомизировали для 4- (n=207) или 8-недельной (n=201) инициальной терапии эзомепразолом в дозе 40 мг/сут. Пациентам, ответившим на первоначальное лечение, при повторном возникновении типичных проявлений ГЭРБ рекомендовали возобновить прием эзомепразола в виде терапии «по требованию» на протяжении 20 нед. После 20-й нед противорецидивного лечения всем больным проводилось контрольное эндоскопическое обследование верхнего отдела желудочно-кишечного тракта.
Сравнив субъективную эффективность 8- и 4-недельного курса инициальной терапии, исследователи не обнаружили значимых межгрупповых различий: количество пациентов, полностью избавившихся от типичных проявлений ГЭРБ, при применении краткого режима приема препарата достоверно не отличалось от такового при использовании длительной схемы (77,9 vs 82,1%; р>0,05). Тем не менее вероятность возникновения рецидива заболевания в течение 12 нед была гораздо выше у пациентов, рандомизированных для проведения 4-недельной инициальной терапии, по сравнению с больными, принимавшими эзомепразол на протяжении 8 нед (62,5 vs 47,8%; межгрупповые различия 14,7%; 95% ДИ 3,7-25,7%; р=0,009). Контрольная эндоскопия не выявила достоверных межгрупповых различий в заживлении эрозивно-язвенных поражений пищевода при использовании 4- и 8-недельной терапии (40,9 vs 49,6%; р=0,160). Проанализировав полученные данные, P.I. Hsu и соавт. считают 8-недельный курс лечения эзомепразолом наиболее целесообразным для больных рефлюкс-эзофагитом А и В, т. к. именно он позволяет существенно снизить риск рецидива заболевания.
Еще одним актуальным вопросом является подбор персонифицированной кислотосупрессивной терапии ГЭРБ в зависимости от генетически обусловленных особенностей метаболизма ИПП (генотипа CYP2C19). Доказано, что у быстрых метаболизаторов стандартные дозы ИПП не оказывают необходимого антисекреторного действия. S. Sahara и соавт. (2015) предположили, что должного ингибирования продукции соляной кислоты для достижения значимого клинического эффекта можно добиться посредством увеличения суточной дозировки ИПП. Высказанную гипотезу ученые проверили в ходе РКИ, рекомендовав Helicobacter pylori (Нр)-негативным волонтерам (n=30) принимать 20 мг эзомепразола 2 или 4 раза в сутки на протяжении 7 дней.
Проанализировав результаты суточной рН-метрии в зависимости от генотипа CYP2C19, исследователи установили, что у быстрых метаболизаторов средние значения рН были выше при 4-кратном приеме препарата, чем при 2-кратном режиме терапии (6,6 vs 5,3 соответственно; р=0,022). Подобная картина была зафиксирована и в остальных подгруппах: 4-кратный прием эзомепразола сопровождался более значимым ростом рН по сравнению с 2-разовым применением препарата как у промежуточных (6,8 vs 5,5 соответственно; р=0,005), так и у медленных (7,0 vs 6,2 соответственно; р=0,047) метаболизаторов. S. Sahara и соавт. отметили интересный факт: при 2-кратном режиме приема эзомепразола корреляционная связь между генотипом CYP2C19, кодирующим скорость метаболизма ИПП, и медианой рН являлась статистически значимой (р=0,004), а при 4-кратном приеме данная зависимость становилась недостоверной (р=0,384). Основываясь на полученных данных, ученые полагают, что обнаружение генотипа CYP2C19, кодирующего быстрый метаболизм ИПП, является показанием для назначения высоких доз блокаторов Н+-К+-АТФазы, в частности 160 мг эзомепразола в сутки.
Эрадикация Нр
Эзомепразол является неотъемлемым компонентом эрадикационных схем первой и второй линии. Среди множества исследований, выполненных в этой области, следует отметить работу А. Campillo и соавт. (2016).
Это испытание интересно тем, что в нем сравнивалась эффективность трех- и четырехкомпонентной схем антихеликобактерной терапии первой линии. Поначалу исследователи получили вполне ожидаемые результаты: эффективность квадротерапии (n=371) значительно превосходила результативность тройного режима (n=248) как по данным ITT-анализа (85,9 vs 65,7%; р<0,001), так и по результатам РР-анализа (92,5 vs 68,4%; р<0,001). Однако, когда ученые сопоставили эффективность эрадикационных схем, в которых в качестве ИПП использовался эзомепразол (40 мг 2 р/сут на протяжении 10 дней), оказалось, что результативность двух антихеликобактерных режимов значительно возросла, но при этом четырехкомпонентная схема (n=108) все так же превосходила трехкомпонентную (n=76; ITT-анализ: 90,7 vs 73,6%; р=0,003; РР-анализ: 92,5 vs 74,6%; р=0,002). На основании полученных данных ученые пришли к выводу, что 10-дневная сопутствующая квадротерапия с высокими дозами ИПП позволяет добиться гораздо лучших результатов, чем оптимизированная тройная схема. При этом А. Campillo и соавт. подчеркивают, что 90% уровня эрадикации можно достичь, если в качестве ИПП использовать эзомепразол (40 мг 2 р/сут).
Еще один заслуживающий внимания вывод был сделан в работе V. de Francesco и соавт. (2016), изучавших эффективность 14-дневной тройной антихеликобактерной терапии с использованием кларитромицина (500 мг 2 р/сут), амоксициллина (1000 мг 2 р/сут) и эзомепразола (20 или 40 мг 2 р/сут). По данным ITT-анализа (n=145), эрадикация Нр оказалась эффективной у 73,9% больных, получавших стандартную дозу эзомепразола (95% ДИ 63,9-84,0), и у 81,9% пациентов, принимавших двойную дозу ИПП (95% ДИ 73,0-90,80; МР недостоверны). Проанализировав выборку пациентов, завершивших исследование по протоколу (РР-анализ), ученые установили следующее: эффективность эрадикации при назначении стандартной (78,2%; 95% ДИ 68,5-87,9) и двойной (85,5%; 95% ДИ 77,2-93,8; МР недостоверны) дозы ИПП оказалась недостаточной, поскольку не достигала 90%. Получив такие неутешительные данные, исследователи рекомендуют использовать для эрадикационной терапии первой линии другие антибактериальные препараты, не меняя при этом ИПП, считая эзомепразол наиболее действенным препаратом среди всех ИПП.
Данные метаанализов
Относительно недавно было опубликовано большое количество метаанализов, где сравнивалась эффективность эзомепразола и других ИПП в лечении различных кислотозависимых заболеваний. Одной из таких работ является метаанализ, выполненный J. Mei и соавт. (2016). Он основан на тщательном изучении результатов 11 исследований, в которых приняли участие больные ГЭРБ. Исследователи доказали, что прием эзомепразола в дозе 20 мг в сутки в качестве поддерживающей терапии позволяет значительно сократить вероятность рецидива заболевания в течение первых 6 мес по сравнению с другими ИПП (отношение рисков, ОР, 0,67; 95% ДИ 0,55-0,83). Подобная картина наблюдалась в отношении некоторых клинических проявлений ГЭРБ: изжога (ОР 0,72; 95% ДИ 0,57-0,92) и эпигастральная боль (ОР 0,82; 95% ДИ 0,70-0,96) достоверно реже беспокоили пациентов, получавших эзомепразол, в отличие от больных, принимавших иные ИПП. Еще одним преимуществом терапии эзомепразолом явилась низкая вероятность развития побочных действий (РО 1,40; 95% ДИ 1,04-1,88) по сравнению с другими ИПП. Получив такие впечатляющие результаты, J. Mei и соавт. считают эзомепразол наиболее эффективным ИПП для лечения ГЭРБ.
Еще один метаанализ, в котором сравнивалась эффективность различных ИПП в лечении ГЭРБ, доказал превосходство эзомепразола. Q. Qi и соавт. (2015) провели анализ данных 10 исследований (n=10 286), где для купирования симптомов ГЭРБ использовались эзомепразол и омепразол. Оказалось, что представитель последнего поколения ИПП значительно превосходил своего прародителя (ОР 1,06; 95% ДИ 1,01-1,10; I2=72%; р=0,01) в лечении ГЭРБ. Даже сделав поправку на использование различных суточных доз (эзомепразол – 40 мг, омепразол – 20 мг), исследователи доказали, что применение эзомепразола сопровождается более быстрым заживлением эрозивно-язвенных поражений пищевода по сравнению с омепразолом (ОР 1,07; 95% ДИ 1,004-1,14; I2=78%; р=0,04). Более того, низкие дозы эзомепразола (20 мг/сут) превосходили высокие дозы омепразола (40 мг/сут) в способности нивелировать клиническую симптоматику ГЭРБ (ОР 0,68; 95% ДИ 0,47-0,97; р=0,03). В заключение ученые резюмировали: «Высокие дозы эзомепразола позволяют восстановить целостность поврежденной слизистой оболочки и эффективно контролировать симптомы ГЭРБ».
В другом метаанализе, выполненном A.G. McNicholl и соавт. (2012), рассматривалась эффективность эрадикационной терапии в зависимости от использованного ингибитора Н+-К+-АТФазы: результативность ИПП последнего поколения (эзомепразол, рабепразол) сравнивалась с таковой препаратов-предшественников (омепразол, лансопразол, пантопразол). Проанализировав результаты 35 РКИ (n=5998), ученые установили, что эффективность эрадикационных схем с использованием эзомепразола достоверно превосходила таковую режимов, предусматривавших применение ИПП первых поколений: 82,3 vs 77,6% (ОР 1,32; 95% ДИ 1,01-1,73; NNT=21). Подобные данные были получены в отношении рабепразола: он оказался эффективнее своих предшественников (80,5 vs 76,2%; ОР 1,21; 95% ДИ 1,02-1,42; NNT=23). Проведя сравнительный анализ результативности эзомепразола и рабепразола (данные 5 РКИ), ученые отметили недостоверное превосходство эзомепразола: 78,7 vs 76,7% (ОР 0,90; 95% ДИ 0,70-1,17; NNT=50). Назначение эзомепразола сопровождалось значимым увеличением эффективности эрадикационной терапии по сравнению с ИПП первых поколений (83,5 vs 72,4% соответственно; ОР 2,27; 95% ДИ 1,07-4,82; NNT=9). Подводя итоги проведенной работы, A.G. McNicholl и соавт. рекомендуют в схемы антихеликобактерной терапии включать эзомепразол или рабепразол, а не ИПП первых поколений, а также подчеркивают, что назначение эзомепразола (40 мг 2 р/сут) приводит к увеличению эффективности эрадикационной терапии.
Сопутствующая патология
Известно, что ИПП применяются для лечения и профилактики гастропатии, индуцированной приемом нестероидных противовоспалительных препаратов. Однако некоторые ученые считают, что дополнительное включение ИПП в схему лечения пациентов с заболеваниями опорно-двигательного аппарата не только защищает слизистую оболочку гастродуоденальной зоны, но и увеличивает эффективность противовоспалительной терапии. Подобный вывод сделали R.J. Holt и соавт. (2015), авторы широкомасштабного РКИ, дизайн которого предусматривал рандомизацию больных (старше 50 лет) остеоартритом коленных суставов для одновременного приема 500 мг напроксена и 20 мг эзомепразола 2 р/сут (n=487), или 200 мг целекоксиба (n=486), или плацебо (n=246). Конечными точками в этом исследовании были: время до первого значимого уменьшения интенсивности болевого синдрома (БС), значения индекса WOMAC (подшкалы «боль», «скованность») и RAPID3 (рутинного индекса самооценки исходов ревматоидного артрита), данные опросников APS-POQ (шкала оценки результатов лечения, разработанная Американским обществом по изучению боли) и PGA (шкала оценки общего впечатления пациента об изменении состояния своего самочувствия) в динамике лечения.
Ученые установили, что сочетанный прием напроксена и эзомепразола способствовал более значимому снижению интенсивности БС: значения индекса WOMAC ко 2-7-му дню лечения, а также через 6 и 12 нед терапии значительно уменьшились по сравнению с плацебо (во всех случаях р<0,05). Анализ данных опросника APS-POQ также подтвердил эффективность комбинации напроксена и эзомепразола в купировании БС ко 2-7-му дню лечения по сравнению плацебо (во всех случаях р<0,05). Значения индексов RAPID3, WOMAC (скованность/функциональность) и шкалы PGA у пациентов, принимавших напроксен и эзомперазол, значительно улучшились к 6-й и 12-й нед лечения (во всех случаях р<0,05). Выраженность обезболивающего эффекта напроксена и эзомепразола была сопоставима с таковой целекоксиба. Основываясь на полученных результатах, R.J. Holt и соавт. рекомендуют назначать больным остеоартритом коленных суставов комбинацию напроксена и эзомепразола, т. к. ее использование приводит к значимому уменьшению интенсивности БС при сохранении длительности обезболивающего эффекта до 12 нед.
Безопасность терапии
Активные дискуссии о безопасности длительного применения ИПП ведутся на протяжении нескольких лет. Наибольшие опасения вызывает безвредность поддерживающей терапии ИПП из-за существующей вероятности развития хронического атрофического гастрита, который, в свою очередь, способен трансформироваться в неопластическое поражение желудка. Научные споры по этому поводу разгорелись с новой силой после публикации результатов некоторых экспериментальных исследований, доказавших увеличение вероятности развития гиперплазии энтерохромаффиноподобных клеток (ГЭК) и карциноидных опухолей у мышей, получавших высокие дозы ИПП. Четкий ответ на вопрос о безопасности длительной терапии ИПП и связи между их приемом и развитием неопластических/предопухолевых состояний желудка дали L. Eslami и соавт. (2013). Исследователи провели метаанализ данных 6 РКИ (n=785): в 2 из них безопасность терапии эзомепразолом сравнивалась с таковой плацебо, в 1 РКИ сопоставлялись профили безопасности омепразола и антацида / антирефлюксного хирургического вмешательства, в 2 РКИ сравнивался омперазол с ранитидином, в 1 РКИ – лансопразол с ранитидином. Количество пациентов, у которых на фоне приема ИПП развились прогрессирующая атрофия тела желудка, интестинальная метаплазия и хроническое воспаление в антральном отделе желудка, достоверно не отличалось от числа больных, у которых перечисленные патологии возникли при применении контрольных препаратов. Подобные результаты были получены в отношении ГЭК. Исследователи констатировали: «По данным клинических исследований, поддерживающая терапия ИПП не взаимосвязана с увеличением риска атрофии желудка или ГЭК в течение трех лет».
Еще одним камнем преткновения длительной терапии ИПП являются данные о нежелательности одновременного приема ингибиторов Н+- и К+-АТФазы и антитромбоцитарных препаратов (аспирин/клопидогрель) по причине возможного ослабления антиагантного действия последних. Среди множества работ, опровергающих эту точку зрения, следует отметить исследование, выполненное L.P. Liu и соавт. (2016), где сравнивалась эффективность 30-дневной двойной антитромбоцитарной терапии у пациентов, принимавших эзомепразол или рабепразол (20 мг/сут), с аналогичными показателями у больных, не получавших указанные ИПП. Оценку функциональной активности тромбоцитов проводили при помощи АДФ-индуцированной световой трансмиссионной агрегометрии (СТА), индекса реакционной способности тромбоцитов, стимулированной вазодилататором фосфопротеина (VASP-PRI) на 1-й, 3-й и 30-й день после старта двойной антитромбоцитарной терапии.
Интересно, что через 30 дней от момента начала двойной антиагрегантной терапии исследователи не зафиксировали статистически значимых межгрупповых различий в значениях СТА и VASP-PRI у пациентов, получавших ИПП, по сравнению с больными, не принимавшими такие препараты. В группе рабепразола на 3-й и 30-й день лечения было выявлено снижение эффективности антиагрегантной терапии, тогда как подобных отклонений в группе эзомепразола не отмечали: значения СТА и VASP-PRI достоверно не изменились в динамике лечения. В заключение L.P. Liu и соавт. подчеркнули: «Несмотря на то что эффективность двойной антитромбоцитарной терапии не подверглась значимым изменениям на фоне сопутствующего приема ИПП в течение всех 30 дней лечения, эзомепразол значительно меньше влияет на результативность антитромбоцитарной терапии по сравнению с рабепразолом».
Продолжаются дебаты о возможном развитии инфекционных заболеваний органов дыхания, в частности пневмонии, при приеме ИПП. Работа шведских ученых расставила все точки над «i» относительно наличия этого побочного действия у эзомепразола. Проведя ретроспективный анализ данных 24 РКИ, в которых безопасность эзомепразола (n=9602) сопоставлялась с таковой плацебо (n=5500), L. Estborn и соавт. (2015) не зафиксировали значимых межгрупповых различий в частоте развития инфекционных заболеваний дыхательных путей у пациентов, получавших эзомепразол, и у больных, принимавших плацебо (соответственно, появление субъективных признаков / объективных симптомов, потенциально связанных с инфекционной патологией дыхательных путей: 0,278 и 0,296 пациенто-лет; инфекции нижних отделов респираторного тракта – 0,048 и 0,058 пациенто-лет; пневмония – 0,006 и 0,009 пациенто-лет).
Относительный риск развития любой респираторной инфекции у пациентов, получавших эзомепразол, не превышал такового при применении плацебо (ОР 0,94; 95% ДИ 0,86-1,04). Инфекции нижних дыхательных путей (ОР 0,82; 95% ДИ 0,65-1,03) и пневмонии (ОР 0,66; 95% ДИ 0,36-1,22) на фоне приема эзомепразола возникали с такой же частотой, что и при использовании плацебо. Приняв во внимание демографические характеристики, дозу и показания для приема ИПП, L. Estborn и соавт. получили аналогичные результаты. На основании полученных данных исследователи сделали вывод: «Не зафиксировано причинно-следственной связи между приемом эзомепразола и развитием внебольничных инфекций дыхательный путей, в том числе пневмонии».
Таким образом, по совокупности кислотосупрессивного действия и безопасности длительной поддерживающей терапии эзомепразол является препаратом выбора для лечения различных кислотозависимых заболеваний, в том числе ГЭРБ, а также для эрадикации Нр.
Медична газета «Здоров’я України 21 сторіччя» № 20 (393), жовтень 2016 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...