Лечение гастроэзофагеальной рефлюксной болезни – сравнительная эффективность и результаты применения декслансопразола с модифицированным высвобождением
Определение ГЭРБ
Определение гастроэзофагеальной рефлюксной болезни (ГЭРБ) изменялось с течением времени. Первоначально между термином ГЭРБ и тканевым повреждением ставился знак равенства, однако затем было признано, что многие пациенты с ГЭРБ испытывают стойкие симптомы заболевания (включая изжогу и регургитацию) при отсутствии эндоскопических и гистологических повреждений. По мере роста распространенности рефлюксной болезни, а также с учетом ее разнообразных клинических проявлений, возникла необходимость сформулировать краткое определение проблемы и дать рекомендации по лечению для пациентов и специалистов здравоохранения. В 2006 г. Монреальский консенсус определил ГЭРБ как «состояние, которое развивается, когда рефлюкс желудочного содержимого вызывает беспокоящие пациента симптомы и/или осложнения» [1]. Исходя из этого унифицированного определения, ведение пациентов с ГЭРБ должно быть направлено на лечение как осложнений рефлюкса, так и значимых симптомов, связанных с данным расстройством.
Эпидемиология ГЭРБ
Недавно обновленный обзор эпидемиологических данных по ГЭРБ, включающий исследования с 1997 по 2011 гг., выявил, что распространенность ГЭРБ в США составляет 18,1-27,8% [2], в Южной Америке – 23%. Для Европы и Ближнего Востока характерен аналогичный диапазон показателей. В Европе распространенность составляла 8,8-25,9%, тогда как на Ближнем Востоке была в пределах от 8,7 до 33,3%. Напротив, в Восточной Азии и в Австралии наблюдалась меньшая распространенность ГЭРБ, при этом в Восточной Азии она варьировала в диапазоне от 2,5 до 7,8%, а в Австралии составляла 11,6% [3].
Факторы риска и патогенез ГЭРБ
Существует много факторов риска, которые способствуют развитию ГЭРБ. Было показано, что ожирение (в особенности абдоминальное) достоверно повышает риск ГЭРБ, предположительно – посредством повышения внутрибрюшного давления [4]. Старение также может играть определенную роль, поскольку у пожилых пациентов чаще отмечается более выраженное повреждение слизистой оболочки пищевода [5]. Как и определение ГЭРБ, которое изменилось с течением времени, изменились представления о механизмах, лежащих в основе патогенеза заболевания. Они включают аномалии функции желудочно-пищеводного соединения, в том числе влияние транзиторного расслабления нижнего пищеводного сфинктера, гипотонию нижнего пищеводного сфинктера и грыжу пищеводного отверстия диафрагмы, а также сниженный пищеводный клиренс кислоты и рефлюкс, связанный с постпрандиальным кислотным карманом [4].
Современное лечение ГЭРБ
Современные подходы к лечению ГЭРБ сфокусированы на изменении образа жизни, а также на фармакологической терапии. Традиционные рекомендации по изменению образа жизни включают снижение массы тела, поднятие изголовья кровати и избегание приема пищи за 2-3 ч до сна. Рекомендуется отказаться от табакокурения и употребления алкоголя, а также изменить рацион, в том числе – избегать употребления шоколада, кофеина, острой пищи, цитрусовых и газированных напитков [6, 7]. В последних руководствах, опубликованных Американской коллегией гастроэнтерологов (American College of Gastroenterology) и Американской гастроэнтерологической ассоциацией (American Gastroenterological Association), для пациентов с ГЭРБ с ночными симптомами рекомендуется снижение массы тела (для имеющих избыточную массу тела и ожирение), а также поднятие изголовья кровати и отказ от приема пищи перед сном, поскольку имеются доказательства в поддержку этих мер [6, 7]. К сожалению, отсутствуют исследования, в которых было бы продемонстрировано клиническое улучшение у пациентов с ГЭРБ на фоне других изменений образа жизни и диеты; поэтому рекомендуются скорее изменения, специфичные для определенного течения ГЭРБ, нежели советы по широкому применению этих мер у каждого пациента с ГЭРБ. Действующие в настоящее время руководства Американской коллегии гастроэнтерологов и Американской гастроэнтерологической ассоциации рекомендуют использование ингибиторов протонной помпы (ИПП) как для лечения, так и для поддержания процесса заживления эрозивного эзофагита. Пациентам с неэрозивной формой заболевания следует рекомендовать применение антагонистов Н2-рецепторов или ИПП с целью облегчения симптоматики [6, 7].
Неудовлетворенные потребности
при ведении больных с ГЭРБ
Очевидно, что ведение больных с ГЭРБ значительно улучшилось после появления ИПП. Однако многие пациенты все равно продолжают страдать от изжоги, несмотря на терапию ИПП, что обусловлено фармакокинетическими и фармакодинамическими ограничениями, присущими традиционным препаратам этой группы [8-11]. Например, при опросе 1013 пациентов с ГЭРБ 35% больных, получавших терапию ИПП один раз в сутки, сообщили, что их текущий режим приема ИПП не смог обеспечить полное купирование симптоматики. При опросе компактно проживающей группы из 617 пациентов с ГЭРБ 42% тех, кто получал терапию один раз в сутки, дополнительно к своему ИПП принимали другой лекарственный препарат (безрецептурный или рецептурный), а 22% – принимали ИПП два раза в сутки [9]. Эта тенденция не является исключительной только для популяции стран Запада. Данные опроса 450 пациентов с ГЭРБ в Азиатско-Тихоокеанском регионе выявили, что 45% респондентов сообщили об ограниченном ослаблении ночных симптомов, а у 49% пациентов симптомы сохранялись и для их устранения требовалась дополнительная терапия [12].
Обзор фармакологии, механизма действия и фармакокинетики декслансопразола
ИПП с модифицированным высвобождением (MR) действующего вещества представляют собой слабые основания, которые захватываются в кислой среде, подвергаются перестройке катализируемой кислотой и в последующем необратимо связываются с активной протонной помпой париетальной клетки и ингибируют ее [13]. Секреция кислоты восстанавливается, когда новые протонные помпы переходят из своего неактивного состояния в активную форму [10]. Традиционные ИПП не полностью устраняют секрецию кислоты; однако однократные дозы этих препаратов обычно ингибируют 70-80% активных помп [10]. Хотя разработка ИПП совершила революцию в лечении кислотозависимых заболеваний, к сожалению, у традиционных ИПП имеются изначально присущие им ограничения, и многие пациенты страдают от сохраняющихся симптомов несмотря на терапию ИПП, как было отмечено выше. Недостатки терапии традиционными ИПП в первую очередь связаны с ограничениями в основополагающих фармакокинетических и фармакодинамических свойствах препаратов [11]. Это проявляется в необходимости дозирования во время приема пищи и коротких периодах полувыведения этих препаратов. Декслансопразол MR (прим. ред. – в Украине зарегистрирован под торговым названием Дексилант) был разработан с целью эффективного решения этих проблем путем пролонгирования фармакокинетических и фармакодинамических профилей ИПП [14].
Проблема № 1: традиционные ИПП имеют короткий период полувыведения, периодически приводящий к возникновению симптомов прорыва и требующий более частого дозирования.
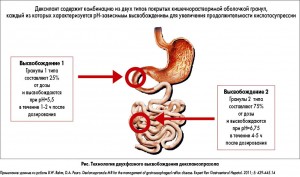
Декслансопразол представляет собой R-энантиомер лансопразола [15]. Он в высокой степени связывается с белками и подвергается элиминации путем биотрансформации в печени. В последующем R-энантиомер ассоциируется со сниженным клиренсом по сравнению с S-энантиомером; однако это не является единственным механизмом, который продлевает эффект декслансопразола MR, поскольку период полувыведения декслансопразола аналогичен таковому у других ИПП (приблизительно 1-2 ч) [14, 16-18]. Время, в течение которого декслансопразол MR присутствует в плазме крови, увеличивается благодаря системе доставки действующего вещества, а не благодаря изначально более медленному печеночному клиренсу. Технология двухфазного высвобождения подразумевает наличие двух отличающихся друг от друга наборов покрытых кишечнорастворимой оболочкой гранул, которые специально разработаны для того, чтобы обеспечить рН-зависимое высвобождение в различных отделах ЖКТ. После приема внутрь содержащая гранулы желатиновая капсула растворяется в желудке, и первый набор гранул (~25% от дозы лекарственного препарата) высвобождается в проксимальном отделе двенадцатиперстной кишки (рН=5,5). Это приводит к быстрому повышению плазменной концентрации препарата (1-2 ч), аналогичному таковому при применении других ИПП. Остальные гранулы (75%) специально разработаны для высвобождения в дистальных отделах тонкого кишечника (рН=6,75), что приводит к получению второго пика концентрации препарата через 4-5 ч после его приема внутрь. Эта система доставки действующего вещества обеспечивает увеличение продолжительности кислотосупрессии и помогает ограничить необходимость дозирования препарата чаще, чем один раз в сутки (рис.) [14, 17-19].
В ходе рандомизированного открытого перекрестного исследования с двумя периодами сравнивали фармакодинамические эффекты, которые оказывают однократные дозы декслансопразола MR 60 мг и эзомепразола 40 мг на значения внутрижелудочного рН в течение 24 ч у здоровых взрослых лиц. Его результаты продемонстрировали, что среднее 24-часовое значение внутрижелудочного рН после приема однократной дозы декслансопразола MR было выше по сравнению с таковым после приема однократной дозы эзомепразола (58 в сравнении с 48%; р=0,0003). Наиболее выраженное различие было отмечено во второй половине дня – предположительно по причине большей продолжительности действия декслансопразола MR [20].
Проблема № 2: для достижения максимальной эффективности обычные ИПП следует принимать до еды.
Протонные помпы париетальных клеток активируются на фоне приема пищи, а большинство помп – во время утреннего приема пищи. Обычные ИПП ингибируют стимулированную секрецию соляной кислоты и, чтобы обеспечить максимальную кислотосупрессию, их рекомендуется принимать перед приемом пищи, в частности, за 30-60 мин до завтрака. Это требование может быть обременительным для многих пациентов, что приведет к проблемам, связанным с сохранением симптомов. С другой стороны, ввиду своего пролонгированного действия декслансопразол MR ингибирует как базальную, так и стимулированную секрецию соляной кислоты в желудке, и будет эффективен независимо от употребления пищи [21]. При использовании рандомизированного открытого перекрестного дизайна исследования с целью оценки влияния пищи на фармакодинамику декслансопразола MR участники исследования принимали натощак плацебо за 30 минут до, за 5 минут до или через 30 минут после употребления завтрака с высоким содержанием жиров в 1-й день исследования, а на 3-й день исследования – получали декслансопразол MR в течение каждого перекрестного периода. Плазменные концентрации декслансопразола измерялись в 1-й и 3-й дни исследования. Также измеряли 24-часовые значения внутрижелудочного рН. Между двумя периодами не наблюдалось каких-либо клинически значимых различий в фармакокинетических или фармакодинамических показателях. Исследователи пришли к выводу, что пища, равно как и время приема декслансопразола MR по отношению ко времени приема пищи, не влияют на способность препарата к ингибированию секреции соляной кислоты в желудке [22]. В ходе дополнительного рандомизированного открытого перекрестного 4-этапного исследования 48 здоровых лиц получали декслансопразол MR 60 мг один раз в сутки за 30 минут до завтрака, второго завтрака, обеда или вечернего приема пищи. Не отмечалось клинически значимых различий в среднем 24-часовом значении внутрижелудочного рН или в выраженном в процентах времени, в течение которого 24-часовое значение внутрижелудочного рН было более 4, что означает отсутствие влияния времени приема пищи на контроль секреции соляной кислоты в желудке в течение дня [23].
Безопасность, эффективность
и переносимость декслансопразола MR
Декслансопразол MR хорошо переносится; было показано, что он имеет профиль безопасности, аналогичный таковому у лансопразола. Данные шести контролируемых исследований с участием 4 270 пациентов и данные 12-месячного исследования безопасности продемонстрировали меньшее количество нежелательных явлений на 100 пациенто-месяцев в группе декслансопразола MR в сравнении с группами лансопразола и плацебо (15,64-18,75 в сравнении с 21,06 и 24,49 соответственно) [20]. Кроме того, меньшее число пациентов, получавших декслансопразол MR, прекратили терапию в сравнении с плацебо (р<0,05) [24]. При выполнении биопсий слизистой оболочки желудка не было обнаружено ничего, что могло бы вызвать беспокойство [21]. Наиболее частым нежелательным явлением была диарея; за ней следовали абдоминальная боль, тошнота, инфекция верхних дыхательных путей, рвота и вздутие живота [17]. В таблице 1 приведены наиболее частые нежелательные явления, которые наблюдались у пациентов во время клинических исследований декслансопразола MR.
Кроме того, существует несколько потенциальных рисков, ассоциированных с ИПП как с классом, а именно: вероятность возникновения инфекции, вызванной Clostridium difficile, и других кишечных инфекций, возможное повышение риска внебольничной пневмонии у лиц, получающих короткие курсы лечения, а также неясная ассоциация между переломами костей и применением ИПП.
Декслансопразол MR и эрозивный эзофагит
Эрозивный эзофагит представляет собой тяжелое осложнение ГЭРБ. Было показано, что применение ИПП является наиболее эффективным лечением для эрозивного эзофагита, которое способно поддерживать достигнутое заживление [26]. В ходе двух идентичных двойных слепых рандомизированных контролируемых исследований была оценена роль декслансопразола MR в заживлении эрозивного эзофагита. Пациенты с эндоскопически подтвержденным эрозивным эзофагитом (как минимум 30% участников имели умеренный или тяжелый эзофагит – степень C или D согласно Лос-Анджелесской классификации) из 188 центров США и из 118 центров, расположенных в других странах, были рандомизированы на три группы для получения в течение 8 недель одного из следующих видов лечения: декслансопразол MR 60 мг или 90 мг либо лансопразол 30 мг. Первичной конечной точкой оценки эффективности являлось количество пациентов, у которых наблюдалось полное эндоскопическое заживление эрозивного эзофагита в течение 8 недель. Анализ таблиц вероятности дожития в популяции пациентов, которые начали получать назначенное лечение, свидетельствовал о том, что заживление наступило у 92-95% пациентов, получавших декслансопразол MR в сравнении с 86-92% пациентов в группе лансопразола. Индивидуальные результаты исследования с использованием более консервативных статистических методов (анализ общего коэффициента) продемонстрировали, что показатели частоты заживления эзофагита при использовании обеих доз декслансопразола MR (60 мг и 90 мг) на 8-й неделе превосходили таковые у лансопразола в одном исследовании, тогда как в другом исследовании декслансопразол MR в дозе 60 мг обладал не меньшей эффективностью, а в дозе 90 мг – превосходил лансопразол [26]. При объединенном анализе частота заживления умеренного и тяжелого эзофагита (степень C или D согласно Лос-Анджелесской классификации) была достоверно выше при использовании декслансопразола MR 90 мг, чем лансопразола. Во всех группах лечения отмечался хороший контроль симптомов и переносимость исследуемых препаратов [26]. Декслансопразол MR продемонстрировал не только эффективность в обеспечении первоначального облегчения симптомов и заживлении эрозивного эзофагита, но и способность обеспечивать постоянное облегчение симптомов и поддерживать эндоскопическое заживление у пациентов с эрозивным эзофагитом. В процессе рандомизированного двойного слепого многоцентрового плацебо-контролируемого исследования III фазы продолжительностью 6 месяцев оценивали эффективность декслансопразола MR в дозе 30 мг и 60 мг в сутки при заживлении эрозивного эзофагита и обеспечении облегчения симптоматики. В него были включены пациенты, которые ранее участвовали в одном из двух исследований по изучению лечения эзофагита и достигли полного заживления слизистой оболочки. Первичной конечной точкой оценки эффективности являлось число пациентов, у которых сохранялось заживление эзофагита в течение 6 месяцев согласно эндоскопической оценке. Декслансопразол MR был достоверно более эффективен в поддержании процесса заживления эрозивного эзофагита, чем плацебо. Кумулятивные показатели частоты заживления в течение 6 месяцев на основе анализа в популяции в соответствии с исходно назначенным лечением и анализа времени до наступления события (таблицы дожития) составили 74,9 и 82,5% в группах декслансопразола MR 30 мг и 60 мг соответственно по сравнению с 27% в группе плацебо. Кроме того, декслансопразол MR в дозе как 30 мг, так и 60 мг был высокоэффективен в купировании имеющихся у пациентов симптомов. Медиана выраженного в процентах количества дней без изжоги в течение 24 ч в течение 6-месячного исследования составляла 96 и 91% у пациентов, получавших декслансопразол MR 30 мг и 60 мг соответственно, по сравнению с 29% у пациентов, получавших плацебо [21].
Декслансопразол MR и неэрозивная ГЭРБ
Неэрозивная ГЭРБ (НЭРБ) – термин, использующийся для описания симптомов, которые свидетельствуют о наличии ГЭРБ у пациентов без эндоскопических доказательств эзофагита [18]. Лечение НЭРБ может быть проблематичным, поскольку многие пациенты не отвечают на терапию традиционными ИПП. Рандомизированное двойное слепое плацебо-контролируемое исследование сравнивало 4-недельный курс лечения декслансопразолом MR 30 мг и 60 мг с применением плацебо у пациентов с НЭРБ. Требовалось, чтобы включенные в исследование пациенты испытывали симптомы изжоги в течение как минимум 6 месяцев до включения в исследование, а также отмечали их в течение ≥4 дней из 7 дней до рандомизации. Также требовалось, чтобы у этих пациентов отсутствовали доказательства эрозий пищевода при эндоскопии. Первичной конечной точкой исследования являлось выраженное в процентах количество дней без изжоги в течение 24-х часов. Результаты исследования продемонстрировали достоверное различие в купировании симптомов (оцененное по количеству дней без изжоги в течение 24-х часов) у пациентов, которые получали декслансопразол MR в сравнении с теми, кто получал плацебо (54,9 и 50% в сравнении с 18,5% соответственно; р>0,00001) [18]. Кроме того, достоверно большее число пациентов в группах декслансопразола MR (30 мг и 60 мг) достигали стойкого избавления от изжоги на момент окончания лечения в сравнении с плацебо (59 и 42% в сравнении с 14% соответственно; р<00001). Систематический обзор и непрямое сравнение рандомизированных контролируемых исследований, в которых оценивалась эффективность декслансопразола MR и эзомепразола у пациентов с НЭРБ, свидетельствовали о достоверно лучшем контроле симптомов у пациентов с НЭРБ, получавших декслансопразол MR 30 мг в сравнении с эзомепразолом 20 мг или 40 мг [27].
Декслансопразол MR и индекс массы тела
Более высокое значение индекса массы тела (ИМТ) является мощным и независимым фактором риска развития ГЭРБ, а также осложнений этого заболевания, таких как эрозивный эзофагит, пищевод Барретта и аденокарцинома пищевода [28]. Влияние ИМТ на ответ на терапию ИПП изучалось лишь в незначительном количестве исследований. Результаты этих исследований были противоречивыми; при этом некоторые исследования показывали положительное влияние ИМТ на ответ на терапию ИПП, а другие – отсутствие либо отрицательное влияние ИМТ на терапию ИПП [28]. Проведенное в 2012 г. исследование с участием как пациентов с НЭРБ, так и пациентов с эрозивным эзофагитом подтвердило ассоциацию между более высокими значениями ИМТ и тяжестью эзофагита, а также с увеличением частоты возникновения симптомов ГЭРБ, оцениваемой с помощью дневника регистрации симптомов [28]. Пациенты с НЭРБ и более высокими значениями ИМТ, которым было назначено лечение декслансопразолом MR, имели большее преимущество в плане купирования симптомов по сравнению с теми, у кого были меньшие значения ИМТ. Это преимущество было достоверно более выражено у пациентов с эрозивным эзофагитом, которые получали лечение декслансопразолом MR. Более того, показатели частоты заживления у пациентов, получавших лечение декслансопразолом (но не лансопразолом), были выше у пациентов с ожирением в сравнении с теми, у кого ИМТ составлял <30 кг/м2 [28]. В результате исследования было отмечено, что как пациенты с НЭРБ, так и пациенты с эрозивным эзофагитом имели более выраженную симптоматику по мере увеличения ИМТ. В то время как у пациентов с НЭРБ это являлось тенденцией, у пациентов с эрозивным эзофагитом это было статистически достоверным. Хотя преимущество от лечения декслансопразолом MR получали все пациенты, у лиц с более высокими значениями ИМТ оно, по-видимому, было наиболее выраженным [28].
Декслансопразол MR, ночная изжога
и связанные с ГЭРБ нарушения сна
Многие пациенты с ГЭРБ страдают от ночных симптомов и ассоциированных с ними нарушений сна. Фактически, почти 89% пациентов с ГЭРБ испытывают ночные симптомы [29]. Была отмечена эффективность декслансопразола MR в отношении уменьшения этих ночных симптомов. В процессе проспективного рандомизированного двойного слепого плацебо-контролируемого исследования оценивали эффект применения декслансопразола MR 30 мг для облегчения ночных симптомов во время 4-недельного периода у пациентов, которые отмечали умеренные или тяжелые симптомы изжоги в течение трех или более ночей в неделю до рандомизации. Вторичная конечная точка исследования оценивала результат применения декслансопразола MR для купирования связанных с ГЭРБ нарушений сна. Декслансопразол MR 30 мг был достоверно эффективнее, чем плацебо, в уменьшении ночных симптомов: в группе декслансопразола было зарегистрировано 73,1 ночи без изжоги в сравнении с 35,7 ночами без изжоги в группе плацебо (р<0,0001) [29]. Кроме того, у большего числа пациентов в группе декслансопразола (47,5%) отмечалось облегчение ночных симптомов изжоги в течение последней недели исследуемого периода в сравнении с плацебо (19,6%; р<0,001) [29]. Наконец, было обнаружено, что декслансопразол был более эффективен в снижении выраженности связанных с ГЭРБ нарушений сна (69,7% в группе декслансопразола в сравнении с 47,9% в группе плацебо; р<0,001) [29].
Декслансопразол MR и ступенчатый переход к терапии один раз в сутки
Многие пациенты с ГЭРБ имеют симптомы, которые недостаточно хорошо контролируются на фоне терапии ИПП один раз в сутки. Проведенный в 2009 г. опрос 619 пациентов с ГЭРБ выявил, что 22,2% пациентов с ГЭРБ использовали режим приема ИПП два раза в сутки ввиду неконтролируемых симптомов ГЭРБ либо персистирующих ночных симптомов [9]. Возможность уменьшения частоты дозирования при сохранении контроля симптомов могла бы быть полезна в силу многих причин, включая удобство, комплайенс и стоимость лечения. Многоцентровое простое слепое исследование оценивало эффективность приема декслансопразола MR 30 мг один раз в сутки в поддержании контроля изжоги у пациентов с симптомами изжоги, которые ранее хорошо контролировались на фоне приема ИПП два раза в сутки. Исследование выявило, что после ступенчатого перехода с терапии два раза в сутки на прием декслансопразола MR 30 мг один раз в сутки контроль симптомов сохранялся у 88% пациентов [30].
Декслансопразол MR и регургитация
Регургитация является значимым симптомом манифестации ГЭРБ и, к сожалению, она часто не поддается адекватному лечению традиционными ИПП [31]. Фактически, регургитация может быть важной причиной развития неполного ответа на лечение ИПП у пациентов с ГЭРБ. Симптомы регургитации были недавно оценены в ходе апостериорного анализа (post hoc analysis) данных пациентов с НЭРБ и эрозивным эзофагитом, получавших декслансопразол MR, плацебо или лансопразол. Это исследование использовало опросник PAGI-SYM (оценка пациентом выраженности симптомов со стороны верхних отделов желудочно-кишечного тракта) для анализа эффективности воздействия терапии ИПП на симптомы регургитации. Пациенты с НЭРБ с наличием как минимум легких симптомов регургитации получали декслансопразол MR 30 мг, 60 мг или плацебо в течение 4-х недель. Через 2 и 4 недели декслансопразол MR в дозе как 30 мг, так и 60 мг обеспечивал статистически значимое ослабление симптомов регургитации по сравнению с плацебо. Пациенты с эрозивным эзофагитом и как минимум легкой регургитацией получали декслансопразол MR 60 мг либо лансопразол 30 мг. Отмечалось статистически значимое ослабление симптомов регургитации на 4-й неделе лечения в группе декслансопразола по сравнению с лансопразолом. В обеих группах аналогичное ослабление симптомов регургитации было зафиксировано на 8-й неделе [32].
Декслансопразол MR и качество жизни
Было показано, что у пациентов с ГЭРБ декслансопразол MR улучшает несколько показателей качества жизни, связанных со здоровьем. В ходе проспективного рандомизированного двойного слепого плацебо-контролируемого исследования в параллельных группах сравнивали декслансопразол MR 30 мг с плацебо и выявили достоверно большее снижение производительности труда и повседневной деятельности в группе декслансопразола MR, а также уменьшение количества часов, в течение которых была нарушена трудовая деятельность по сравнению с плацебо [29]. В исследовании с участием 178 пациентов с хорошо контролируемыми симптомами ГЭРБ на фоне приема ИПП два раза в сутки, которые были впоследствии переведены на маскированный прием декслансопразола MR 30 мг один раз в сутки и плацебо в течение 6 недель, наблюдалось статистически значимое улучшение показателей балльной оценки качества жизни (р=0,16) (PAGI-QOL) у пациентов с хорошо контролируемыми симптомами на фоне применения декслансопразола MR 30 мг [30].
Вывод – место декслансопразола MR в терапии
Декслансопразол MR представляет собой ИПП с уникальной системой доставки действующего вещества, которая увеличивает продолжительность его действия. Было показано, что он эффективен в контроле многих аспектов симптоматики ГЭРБ. Его отличительные фармакокинетические и фармакодинамические свойства делают его полезным инструментом в арсенале средств терапии ГЭРБ. Применение декслансопразола MR может рассматриваться у пациентов с различными клиническими проявлениями ГЭРБ, в том числе у пациентов с впервые установленным диагнозом ГЭРБ, эрозивным эзофагитом (или при необходимости поддержания заживления эрозивного эзофагита), а также у пациентов с симптомной НЭРБ. Кроме того, превосходными кандидатами для лечения декслансопразолом MR являются пациенты, которые нуждаются в 24-часовом купировании симптомов, испытывают ночные симптомы, имеют неполный ответ на терапию традиционным ИПП при его приеме один раз в сутки, страдают ожирением, а также те, кому необходима гибкость дозирования препарата (табл. 2).
Статья печатается в сокращении.
Список литературы находится в редакции.
Therapeutics and Clinical Risk Management 2015: 11 1649-1656.
Перевод с англ. Елена Терещенко
UA/(PPIF)/0316/0004
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...