Неонатальний вовчак
 Під неонатальним вовчаком (НВ) розуміють симптомокомплекс, що діагностують у новонароджених, матері яких страждають на системні захворювання сполучної тканини (СЗСТ) із наявністю антитіл (АТ) до антигенів Ro(SS-A) і La(SS-B), і найчастіше проявляється двома ознаками – ураженням шкіри та провідної системи серця. НВ трапляється з частотою 1 на 15-20 тис. новонароджених і частіше серед білого населення планети [7]. Проблема своєчасної діагностики й насамперед запобігання НВ тісно пов’язана з підвищенням якості надання медичної допомоги жінкам з аутоімунними захворюваннями та позитивними змінами у питаннях планування вагітності в таких жінок.
Під неонатальним вовчаком (НВ) розуміють симптомокомплекс, що діагностують у новонароджених, матері яких страждають на системні захворювання сполучної тканини (СЗСТ) із наявністю антитіл (АТ) до антигенів Ro(SS-A) і La(SS-B), і найчастіше проявляється двома ознаками – ураженням шкіри та провідної системи серця. НВ трапляється з частотою 1 на 15-20 тис. новонароджених і частіше серед білого населення планети [7]. Проблема своєчасної діагностики й насамперед запобігання НВ тісно пов’язана з підвищенням якості надання медичної допомоги жінкам з аутоімунними захворюваннями та позитивними змінами у питаннях планування вагітності в таких жінок.
З історії вивчення. У 1954 році C.H. McCuistion і E.P. Schoch уперше описали типові шкірні прояви в дитини, мати якої страждала на системний червоний вовчак (СЧВ), й запропонували термін «neonatal lupus erythematosus», що надовго закріпило цей не зовсім точний термін у світовій літературі. Пізніше, у 1983 році, J.S. Scott, P.J. Maddison і співавт. уперше припустили наявність взаємозв’язку між материнськими АТ до рибонуклеопротеїдів та вродженою блокадою серця (ВБС) у новонароджених. Наразі в Міжнародній класифікації хвороб 10-го перегляду (МКХ‑10) НВ міститься в рубриці Р.83 («Інші зміни зовнішніх покривів, специфічні для плоду та новонародженого»), в англомовній літературі використовують як синоніми терміни «neonatal lupus syndrome», «congenital lupus», «congenital lupus erythematosus», «neonatal lupus erythematosus», із яких, на нашу думку, найближчим до сутнісної характеристики цього синдрому є перший.
Клінічні прояви. За даними світових літературних джерел, переважна більшість випадків НВ проявляється у вигляді ізольованих форм, серед яких найчастіше трапляються шкірні висипання (25-32% у загальній картині) та ураження серця (15-24%). Шкірна висипка зазвичай представлена поліциклічними зливними елементами, які локалізуються на шкірі голови, шиї та верхніх кінцівок, з’являються протягом перших 6-8 тиж життя і нерідко посилюються на тлі інсоляції. Що стосується ураження серця, то воно включає міокардит із порушеннями серцевого ритму та провідності (атріовентрикулярні блокади 1, 2 ступеня); повну поперечну блокаду серця з поєднанням або без клапанних вад (у 15-20% випадків призводять до загибелі плода); дилатаційну кардіоміопатію, ендокардіофіброеластоз тощо. Прояви з боку інших систем та органів, такі як тромбоцитопенія, анемія, гепатомегалія, транзиторна гіпербілірубінемія, спленомегалія, пневмоніт, становлять близько 15-18% випадків і зазвичай мають минущий характер. У 30-40% випадків НВ маніфестує поєднанням різних клініко-лабораторних проявів. Наявність в анамнезі дитини НВ не є передумовою розвитку аутоімунного захворювання в підлітковому чи дорослому віці, хоча в літературі описано випадки розвитку СЧВ або хвороби Шегрена у таких дітей.
Вважається, що саме АТ до Ro(SS-A) і La(SS-B) належить провідна роль у патогенезі НВ, при цьому розвиток шкірних проявів пов’язують насамперед з АТ до La(SS-B), а ВБС – із наявністю АТ до Ro(SS-A). Останні представлені білками з молекулярною масою 52 і 60 кДа, із яких більш патогенними є поліпептиди масою 52 кДа. E. Jaeggi, C. Laskin і співавт. у своєму дослідженні довели наявність кореляції між титрами АТ до Ro(SS-A) та розвитком ВБС і зазначили, що клінічно значущим є титр АТ ≥50 Од/мл.
Матері новонароджених із НВ. АТ до Ro(SS-A) та La(SS-B) виявляються при таких аутоімунних захворюваннях, як СЧВ із синдромом Шегрена чи (рідше) без нього, дискоїдний червоний вовчак, що асоціюється з наявністю АТ до La(SS-B), хвороба Шегрена (первинний синдром Шегрена), системна склеродермія із синдромом Шегрена, ревматоїдний артрит із синдромом Шегрена, інші аутоімунні захворювання (первинний біліарний цироз печінки, аутоімунний тиреоїдит) із синдромом Шегрена.
Слід зазначити, що не в усіх матерів, які мають АТ до Ro(SS-A) та La(SS-B), народжуються діти з НВ: усього лише у 2-5% новонароджених діагностують це захворювання, в 1-3% випадків розвивається ВБС. Це дає змогу припустити, що, крім материнських АТ, є й інші фактори, які зумовлюють розвиток НВ. Встановлено, що ризик народження хворої дитини підвищується за умови наявності HLA-B8 і HLA-DR3. Імовірно, певну роль відіграють статеві гормони: співвідношення хворих дівчаток до хлопчиків становить 2:1, що пов’язують із посилювальним ефектом естрадіолу. Цікаво, що ризик народження другої дитини з ВБС у хворої матері зростає у 6-10 разів, навіть якщо перша дитина мала лише шкірні прояви, асоційовані з материнськими АТ до Ro(SS-A) та La(SS-B). Шкірна форма трапляється частіше в дітей, матері яких не мали діагностованого СЗСТ. За різними даними, у 70-90% матерів, що не мали СЗСТ на момент народження хворої дитини, протягом десяти років розвивається аутоімунне ревматичне захворювання.
Лікування та профілактика. Наразі протоколу лікування НВ не розроблено, але з урахуванням результатів останніх досліджень сформульовано рекомендації щодо запобігання розвитку та лікування цього синдрому. Вони містять такі пункти:
1. Хворим жінкам зі встановленим діагнозом рекомендовано приймати профілактичні дози гідроксихлорохіну за 6 тиж до планованої вагітності й увесь час упродовж вагітності. Ефективність застосування високих доз дексаметазону, плазмаферезу та внутрішньовенного введення імуноглобуліну не було доведено.Починаючи з 16-го тижня вагітності забезпечити щотижневу доплерометрію судин пуповини для вчасної діагностики затримки внутрішньоутробного розвитку та ехокардіографічне (ЕхоКГ) дослідження для моніторингу розвитку серця плода, адже маніфестація кардіальних ускладнень зазвичай настає з 18-го по 24-й тиждень гестації, що пов’язано з підвищенням трансплацентарного транспортування IgG у II триместрі.
2. Пологи мають бути заплановані в закладах третинного рівня задля вчасного встановлення електрокардіостимулятора в разі ВБС.
3. У разі діагностування ізольованої шкірної форми, гематологічних проявів або поодиноких проявів з боку інших органів та систем дитина лікування не потребує.
4. Дитину спостерігати до 6-7 міс (в окремих випадках – до 9) з контрольним аналізом крові для підтвердження елімінації материнських АТ.
Випадок із клінічної практики
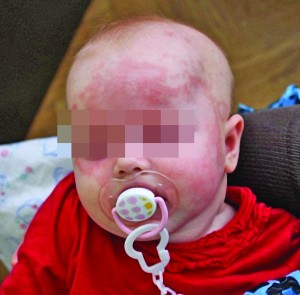
Наведемо клінічний випадок НВ у 3-місячної дівчинки, мати якої звернулася в клініку в серпні 2016 року зі скаргами на висипку на обличчі дитини (фото).
Анамнез дитини: народилася здоровою, але у віці 6 тиж було помічено появу яскраво-рожевої плями в скроневій ділянці зліва, яка поступово збільшувалася, стала кільцеподібною, з часом на обличчі з’явилися нові плямисто-кільцеподібні елементи з тенденцією до злиття, збільшення. Підвищення температури, погіршення загального стану дівчинки не спостерігали, укусів кліщів і комах не зафіксовано. Мати дитини зазначила, що під впливом сонячних променів висипка стає більш яскравою.
У зв’язку з прогресуванням висипки дитину було госпіталізовано в стаціонарну педіатричну установу, де за результатами оглядів спеціалістів, загальноклінічних лабораторних обстежень встановлено діагноз токсикоалергічного дерматиту. Унаслідок лікування дексаметазоном спостерігалася позитивна динаміка: значне зменшення інтенсивності екзантеми, проте після відміни препарату висипка поновилася.
 У матері на момент обстеження скарги відсутні. З анамнезу: вагітностей – 3, пологів – 2, має здорового сина 8 років, друга вагітність – викидень. Два роки тому перенесла «паротит» – спостерігалося припухання привушних слинних залоз, переважно лівої, без ознак інфекційного захворювання. Лікування не отримувала, припухання залоз регресувало за 2 тиж. Під час цілеспрямованого опитування не отримано інформації про наявність скарг або симптомів «ревматологічного кола», включаючи артралгії, шкірну висипку, гіпертермію, сухість у роті та очах, проте жінка зазначила, що під час тривалої роботи за комп’ютером або читання з’являється відчуття «піску в очах», частіше виникає бажання зморгнути. На комп’ютерній томограмі щелепно-лицевої ділянки, яку виконували за 3 міс до звернення, зафіксовано збільшення піднижньощелепних лімфатичних вузлів зліва.
У матері на момент обстеження скарги відсутні. З анамнезу: вагітностей – 3, пологів – 2, має здорового сина 8 років, друга вагітність – викидень. Два роки тому перенесла «паротит» – спостерігалося припухання привушних слинних залоз, переважно лівої, без ознак інфекційного захворювання. Лікування не отримувала, припухання залоз регресувало за 2 тиж. Під час цілеспрямованого опитування не отримано інформації про наявність скарг або симптомів «ревматологічного кола», включаючи артралгії, шкірну висипку, гіпертермію, сухість у роті та очах, проте жінка зазначила, що під час тривалої роботи за комп’ютером або читання з’являється відчуття «піску в очах», частіше виникає бажання зморгнути. На комп’ютерній томограмі щелепно-лицевої ділянки, яку виконували за 3 міс до звернення, зафіксовано збільшення піднижньощелепних лімфатичних вузлів зліва.
Під час огляду матері клінічно значущих відхилень з боку доступних для фізикального обстеження органів і систем не знайдено. В результатах призначених лабораторних та інструментальних досліджень виявлено низку діагностично значущих змін: швидкість осідання еритроцитів (ШОЕ) – 42 мм/год (референтні значення – до 20 мм/год); С-реактивний білок (СРБ) – 34 мг/л (референтні значення – до 5 мг/л); ревматоїдний фактор – 72 МО/мл (референтні значення – до 14 МО/мл); антинуклеарні антитіла (АНА) – позитивні (норма – негативні); АТ до Ro(SS-A) 52/60 і La(SS-B) >8 Од (негативний результат – до 1 Од), інші АТ до ядерних антигенів – негативний результат; тимолова проба – 14 Од/л (референтні значення – до 4 Од/л). Проба Ширмера показала істотне зменшення продукції слізної рідини з обох боків: ОD – 5 мм, OS – 7 мм (норма – не менше 15 мм за 5 хв). Рентгенографія органів грудної клітки, електрокардіографія (ЕКГ) та ЕхоКГ патології не виявили.
Зважаючи на дані анамнезу (неасоційований з інфекцією епізод припухання привушних слинних залоз у дорослому віці, збільшення піднижньощелепних лімфатичних вузлів, непрямі ознаки зниження сльозопродукції), лабораторних обстежень (ознаки активного запального процесу – підвищення ШОЕ та рівня СРБ, високий рівень ревматоїдного фактора без ознак артриту, позитивні АНА, значне підвищення рівня АТ до Ro(SS-A) і La(SS-B), тимолової проби за відсутності відхилень в інших печінкових тестах), підтверджене за допомогою проби Ширмера двобічне зниження продукції слізної рідини, матері було встановлено діагноз: хвороба Шегрена, хронічний перебіг, 2 ступінь активності, з ураженням слинних (сіалоаденіт, лімфаденопатія) і слізних залоз (ксерофтальмія). АНА (+), АТ-Ro(SS-A) (+), АТ-La(SS-B) (+), РФ (+). Рекомендовано провести ультразвукове дослідження слинних залоз та біопсію дрібних слинних залоз слизової оболонки рота.
Після отримання результатів обстеження матері було прийнято рішення дообстежити дитину. В клінічному аналізі крові – всі показники в межах вікової норми, рівень СРБ не підвищений, виявлено АНА (позитивні) й АТ до Ro(SS-A) 52/60 і La(SS-B) >8 Од/л, інші лабораторні параметри, включаючи РФ і тимолову пробу – без патологічних змін. Результати ЕКГ та ЕхоКГ дитини нормальні.
З огляду на наявність у матері хвороби Шегрена з високими титрами АТ до Ro(SS-A) та La(SS-B), виявлення в крові дівчинки таких самих АТ за відсутності клініко-лабораторних ознак СЗСТ дитині встановлено діагноз: неонатальний вовчаковий синдром з ураженням шкіри (еритематозний дерматит). АНА (+), АТ-Ro(SS-A) (+), АТ-La(SS-B) (+).
Отже, можна зробити висновок, що розвиток НВ у цієї дитини був зумовлений трансплацентарною передачею материнських АТ до Ro(SS-A) і La(SS-B). Клінічна картина буде наявна доти, доки не елімінуються материнські АТ – орієнтовно протягом 3-4 міс, тому було рекомендовано спостерігати дитину до 6-місячного віку й очікувати зменшення висипки до повного її зникнення.
Системне лікування в цьому випадку не показано, варто лише уникати потрапляння на шкіру дитини прямих сонячних променів, що може спровокувати появу нових висипань чи посилити їх вираженість. Можливе місцеве застосування глюкокортикоїдних кремів або мазей. Матері було рекомендовано після дообстеження спостерігатися у ревматолога для лікування захворювання в майбутньому, узгоджуючи його ініціацію із закінченням грудного вигодовування. Хоча, згідно із сучасними рекомендаціями Європейської протиревматичної ліги (EULAR) із фармакотерапії ревматичних захворювань під час вагітності та лактації, жінка може без шкоди для дитини приймати глюкокортикоїди та деякі інші лікарські засоби, відносно доброякісний перебіг захворювання у матері дає змогу на кілька місяців відтермінувати початок лікування.
СТАТТІ ЗА ТЕМОЮ Ревматологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....
Зв’язок між рівнем сироваткової сечової кислоти (ССК) і ризиком серцево-судинних захворювань (ССЗ) упродовж багатьох років є предметом вивчення дослідників. Установлено, що рівень ССК – незалежний предиктор смерті від усіх причин і серцево-судинної смерті, зокрема від гострого коронарного синдрому, інсульту та серцевої недостатності (СН). Також опубліковано багато робіт про зв’язок між ССК і функцією нирок. Попри значну кількість публікацій, деякі моменти, а саме: яким є оптимальний поріг ССК для визначення ризику ССЗ, чи необхідна корекція значень ССК для функції нирок, чи є ССК ключовим патологічним елементом метаболічної дисрегуляції, потребують прояснення....




