Антибиотикотерапия инфекций мочевыводящих путей: место цефалоспоринов
В структуре инфекционной заболеваемости инфекции мочевых путей (ИМП) занимают второе место, уступая по частоте лишь респираторным инфекциям. В структуре внутрибольничных инфекций доля ИМП может достигать 40% (Ермоленко В. М., Филатова Н. Н. и соавт., 2012). Терапия ИМП должна быть направлена на эрадикацию возбудителя, профилактику реинфекции, быстрое устранение клинических симптомов и при этом соответствовать международным рекомендациям.
Первой линией терапии является назначение антибиотиков. Рациональный выбор стартового антибактериального препарата представляется непростой задачей с учетом разных уровней эффективности и переносимости антибиотиков, а также резистентности к ним основных уропатогенов.
Риск развития ИПМ повышается при (Ермоленко В. М., Филатова Н. Н. и соавт., 2012):
- нарушении уродинамики (в случае аномалий развития мочеполовой системы, обструкции, нефролитиаза, аденомы простаты, нефроптоза);
- бессимптомной бактериурии;
- обменных нарушениях (сахарном диабете, подагре, гиперкортицизме);
- иммуносупрессиях любого генеза;
- беременности;
- атонии кишечника.
В диагностике ИМП ведущими методами являются общий анализ мочи и бактериологическое исследование мочи. Неосложненную инфекцию нижних мочевых путей (острый цистит) можно установить без проведения бактериологического исследования мочи.
Посев мочи назначают:
- при подозрении на острый пиелонефрит;
- в случае, если симптомы сохраняются на фоне терапии или рецидивируют в течение 2-4 нед после лечения;
- при наличии атипичных симптомов;
- беременным;
- у мужчин с подозрением на ИМП.
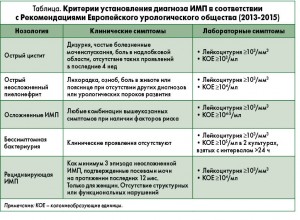
Наиболее частым возбудителем ИМП является Escherichia coli, которая вызывает неосложненную ИМП в 80-90% случаев. Значительно реже при неосложненной ИМП выделяют Staphylococcus saprophyticus (3-5%), Klebsiella spp., Proteus mirabilis и др. Осложненные ИМП чаще обусловлены Proteus spp., Pseudomonas spp., Klebsiella spp., Candida albicans. При этом этиологическая значимость E. coli достигает 30%. Карбункул почки в 90% случаев вызван Staphylococcus aureus, основными возбудителями апостематозного нефрита, абсцесса почки с локализацией в медуллярном веществе являются E. сoli, Klebsiella spp., Proteus spp. Диагностическое значение при ИМП имеет не только вид возбудителя, но и его концентрация в единице объема исследуемой мочи (табл.).
В последние годы накапливается все больше данных о распространении резистентных штаммов уропатогенов, которые выделяются не только в условиях стационара, но и при внебольничных ИМП. Так, в большинстве стран отказались от использования аминопенициллинов и триметоприма/сульфаметоксазола в качестве препаратов выбора при амбулаторных ИМП. В некоторых государствах отмечается высокий уровень резистентности к традиционно используемым для терапии ИМП препаратам, таким как фторхинолоны и нитрофураны (Ляхова О. А., Остроумова М. В. и соавт., 2008). В связи с этим в современной клинической практике одной из наиболее востребованных групп антибиотиков являются цефалоспорины (ЦС), обладающие высокой активностью в отношении наиболее вероятных возбудителей амбулаторных ИМП – бактерий семейства Enterobаcteriaceae. Одним из представителей ЦС III поколения является цефиксим – полусинтетический пероральный ЦС, обладающий благоприятным профилем фармакокинетики и оптимальным спектром антимикробной активности.
При приеме 400 мг цефиксима натощак биодоступность составляет 40-50%. Максимальные концентрации в сыворотке крови определяются через 3-5 ч. Среди других пероральных ЦС цефиксим выделяется наиболее длительным периодом полувыведения (3,7 ч), что позволяет назначать его в режиме 1 р/сут. Выведение препарата из организма осуществляется преимущественно в неизмененном виде через гепатобилиарную систему (60%) и почки (40%). Содержание препарата в моче во много раз превышает минимальную подавляющую концентрацию (МПК) для большинства возбудителей ИМП. При почечной недостаточности период полувыведения цефиксима возрастает в 2-4 раза, что требует коррекции дозы (Белов Б. С., 2013).
Из грамположительных микроорганизмов наиболее чувствительны к цефиксиму стрептококки (МПК для более чем 90% штаммов S. pyogenes и S. agalactiae составляет <0,5 мг/л). Препарат малоактивен в отношении S. aureus, энтерококков, P. aeruginosa и анаэробов. Однако наибольшей чувствительностью к цефиксиму среди энтеробактерий обладают E. coli, Proteus spp., K. pneumoniae, включая штаммы, продуцирующие β-лактамазы. Чувствительность штаммов основного возбудителя ИМП – E. coli – к цефиксиму остается высокой. Так, резистентные к цефиксиму штаммы E. coli выделяются в 4,2% случаев в Испании и в 2,6% в Германии. В исследовании О. А. Ляховой, М. В. Остроумовой и соавт. (2008) на территории России частота выделения чувствительных к цефиксиму штаммов уропатогенной E. coli составляла 98,9%, умеренно чувствительных – 1,1%. Не выделено ни одного резистентного к цефиксиму штамма E. coli. Авторами также отмечено, что цефиксим обладает более высокой активностью in vitro по отношению к уропатогенной E. coli, чем ципрофлоксацин, и может рассматриваться как один из препаратов выбора для терапии внебольничных ИМП. В отличие от ципрофлоксацина цефиксим демонстрирует лучшие фармакодинамические качества. МПК для 90% исследованных штаммов (МПК90) цефиксима составляет 0,5 мг/л, тогда как у ципрофлоксацина данный показатель равняется 6,4 мг/л, причем цефиксим создает МПК90 уже через 12-24 ч.
Высокая клиническая и бактериологическая эффективность цефиксима продемонстрирована в клинических исследованиях у пациентов как с неосложненными уроинфекциями (Togashi M. et al., 1989; Sonoda T. et al., 1989; Sanchez M. et al., 2002), так и с осложненными ИМП (Levenstein J., Summerfield P. J. et al., 1986; Ho M. W., Wang F. D. et al., 2001).
Этот препарат может назначаться в таких случаях:
- лечение острого цистита у детей;
- лечение острого пиелонефрита у детей и взрослых;
- в качестве препарата второй линии при неэффективности фосфомицина или производных нитрофурантоина в терапии острого неосложненного цистита;
- лечение осложненных ИМП у детей и взрослых при подтвержденной чувствительности выделенного возбудителя.
Следует отметить благоприятный профиль безопасности цефиксима. Препарат разрешен к использованию у детей и подростков. В отличие от ципрофлоксацина и норфлоксацина его применение не вызывает побочных эффектов со стороны сердечно-сосудистой системы и опорно-двигательного аппарата. Элиминация препарата в неизмененном виде почками и отсутствие кумулятивного эффекта практически предотвращают развитие побочных действий.
На рынке Украины препарат Цефикс представлен компанией «Мегаком» с 2006 г. Он имеет удобные формы выпуска и дозировки (порошок для приготовления суспензии 100 мг/5 мл по 30 и 60 мл и капсулы по 400 мг № 5), что позволяет подобрать оптимальную дозу как для взрослого, так и для ребенка.
Цефикс (цефиксим) является цефалоспориновым антибиотиком III поколения с широким спектром действия. Это дает возможность применения цефиксима в качестве второй (пероральной) составляющей при проведении ступенчатой антибиотикотерапии препаратами цефалоспоринового ряда, главным образом при лечении ИМП, что следует отнести к несомненным достоинствам препарата. Основная идея ступенчатой терапии заключается в сокращении длительности парентерального введения антибиотика. Такой подход обеспечивает значительное уменьшение стоимости лечения, сокращение срока пребывания в стационаре при сохранении высокой клинической эффективности терапии. Современные ЦС характеризуются высокой биодоступностью, что позволяет достичь терапевтических концентраций в биологических средах и тканях при пероральном приеме препарата. Благодаря высокой эффективности, снижению частоты осложнений и уменьшению количества дополнительных обследований использование современных пероральных антибактериальных препаратов в клинической практике является целиком оправданным и по показателям фармакоэкономического эффекта. Кроме того, уменьшение количества инъекций делает лечение более комфортным, устраняя психологические проблемы и уменьшая риск возникновения постинъекционных осложнений. Как возможный вариант ступенчатой терапии может быть использовано внутримышечное введение ЦС ІІІ поколения в течение 3-4 дней, а затем переход на 7-дневный прием Цефикса (Иванов Д. Д., Кушниренко С. В., 2011).
Таким образом, ИМП, прочно удерживающие второе место по распространенности после респираторных инфекций, остаются актуальной проблемой современной медицины. Ключевые возбудители ИМП – представители семейства Enterobаcteriaceae – сохраняют высокую чувствительность к ЦС III поколения, в частности к цефиксиму. Высокая эффективность и безопасность цефиксима доказаны в клинических исследованиях, а наличие пероральных лекарственных форм открывает возможность проведения ступенчатой антибиотикотерапии. Препарат цефиксима Цефикс («Мегаком») может быть рекомендован в лечении как неосложненных, так и осложненных (если выделен чувствительный к цефиксиму возбудитель) ИМП у взрослых и детей в возрасте от 6 мес.
Подготовила Мария Маковецкая
СТАТТІ ЗА ТЕМОЮ Урологія та андрологія
У лютому відбулася щорічна Всеукраїнська науково-практична конференція «Малоінвазивні технології в урології», присвячена актуальним проблемам сучасної урології. Пропонуємо огляд найцікавіших доповідей, що прозвучали в рамках заходу....
Інфекції сечовивідних шляхів (ІСШ) у всьому світі посідають провідне місце серед інфекційних захворювань дорослого населення. Поряд із тим серед фахівців зростає занепокоєння щодо триваючого зростання стійкості бактерій до більшості антибіотиків. Експерти провідних міжнародних товариств наголошують на необхідності розсудливого і виваженого призначення антимікробних препаратів. Про основні принципи раціональної антибіотикотерапії в урології, зокрема при проведенні діагностичних і хірургічних втручань, ми попросили розповісти завідувача відділу відновної урології та новітніх технологій ДУ «Інститут урології ім. акад. О.Ф. Возіанова НАМН України», доктора медичних наук, професора В’ячеслава Миколайовича Григоренка. ...
Процедура трансректальної біопсії простати супроводжується високим ризиком інфекційних ускладнень, тому проведення антимікробної профілактики при цьому втручанні є обов’язковим. Однак зростання антибіотикорезистентності, а також нещодавні рекомендації щодо обмеження призначень фторхінолонів значно звужують спектр можливих варіантів такої профілактики. Міжнародною мультидисциплінарною групою експертів на основі літературних джерел та клінічного досвіду було розроблено ряд настанов стосовно запобігання інфекційним ускладненням при біопсії простати та обґрунтовано доцільність і переваги призначення з цією метою фосфоміцину ...
Кількість людей, які страждають і помирають від вірусного гепатиту В (ВГВ), можна порівняти з кількістю хворих на коронавірусну хворобу 2019 року (COVID‑19), яка наразі викликає велике занепокоєння в усьому світі. Тому вкрай важливим залишається питання передачі вірусу, у тому числі через статеві клітини. Попередніми дослідженнями встановлено, що гени ВГВ, інтегровані в людські сперматозоїди, здатні до реплікації та експресії після передачі ембріонам. Однак досі це явище не було підтверджено клінічними дослідженнями у пацієнтів. Автори вивчали особливості інтеграції ВГВ у геном сперматозоїдів пацієнтів та аналізували можливі клінічні наслідки для потомства ...