Инфекции мочевыводящей системы у детей: обновление клинических рекомендаций
21-23 сентября во Львове состоялась ежегодная Всеукраинская научно-практическая конференция «Актуальные вопросы педиатрии» – XVІІІ Сидельниковские чтения. В рамках форума прозвучал доклад заведующего кафедрой нефрологии и почечно-заместительной терапии НМАПО им. П. Л. Шупика (г. Киев), доктора медицинских наук, профессора Д.Д. Иванова, в котором докладчик акцентировал внимание аудитории на обновлении клинических рекомендаций по лечению инфекций мочевыводящих путей (ИМП).
В этиологии ИМП в последние годы изменений не наблюдается – лидирующие позиции по-прежнему занимает кишечная палочка. Так, в 75-80% случаев ИМП вызваны Escherichia сoli. Значительно реже, в 10-15% случаев, возбудителем выступают Proteus mirabilis, Klebsiella, Enterococcus, Pseudomonas. При гематогенном пути инфицирования в 6-8% случаев причиной ИМП могут быть Staphylococcus aureus, Candida sрp., Salmonella sрp. и Mycobacterium tuberculosis, в 2-4% – другие возбудители. Соответственно, назначаемые антимикробные препараты должны быть активны в первую очередь в отношении грамотрицательной флоры.
Согласно классификации Европейской ассоциации урологов (European Association of Urology – EAU, 2012) ИМП у детей подразделяют по:
• уровню поражения мочевыводящих путей: верхние (пиелонефрит) и нижние;
• эпизодичности: первый эпизод, рецидивирующая ИМП (рецидивирующая, неизлеченная, реинфекция);
• степени тяжести: легкая, тяжелая (с гипертермией);
• наличию симптомов: бессимптомная, с симптомами;
• наличию осложнений: осложненная, неосложненная.
Однако эта классификация не очень удобна для применения в клинической практике. Поэтому в Украине используется видоизмененный ее вариант:
• по типу течения: острые ИМП (до 3 мес) и хронические (более 3 мес);
• по локализации: цистит, пиелонефрит, уросепсис, без определения локализации.
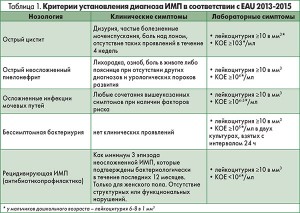
Диагноз ИМП базируется на определении количества лейкоцитов в 1 мм3 мочи и результатах ее бактериологического исследования (табл. 1.). Диагностические критерии различных типов ИМП также остались без изменений.
В новых рекомендациях (EAU, 2016) появилось указание, что бактериологическое исследование мочи является рекомендуемым методом для определения наличия или отсутствия клинически значимой бактериурии у пациентов, которым планируется проведение урологических вмешательств. Ранее бактериологическое исследование рекомендовалось только при подозрении на пиелонефрит или осложненную ИМП. На сегодняшний момент даже при остром цистите рекомендовано по возможности провести бактериологическое исследование мочи. В случае рецидивирующего течения цистита этот метод дает возможность сравнить культуры микроорганизмов, выделенных в каждом из эпизодов заболевания.
Однако бактериологическое исследование занимает не менее 48 часов, а этиотропное лечение должно быть назначено безотлагательно. Поэтому можно широко использовать тест-полоски для определения рН мочи, эстеразы лейкоцитов, уровня нитритов. Данный метод может быть полезен при получении сомнительных результатов общего анализа мочи. Например, когда нет уверенности в том, расценивать ли показатель лейкоцитов, равный 8-10, как вариант нормы или маркер ИМП.
Бессимптомная бактериурия во время беременности может осложниться преждевременными родами (ранее 37-й недели), значительным увеличением числа новорожденных с низкой массой тела (менее 2500 г), а также неонатальной смертностью. В связи с этим при выявлении бессимптомной бактериурии у беременных показана антибактериальная терапия, которая существенно снижает риск развития указанных осложнений.
Для лечения бессимптомной бактериурии и цистита у беременных европейские клинические рекомендации (EAU, 2011) придерживаются старых схем:
• нитрофурантоин 100 мг 2 р/сут 3-5 дней (не применять при дефиците глюкозо‑6-фосфатдегидрогеназы);
• амоксициллин 500 мг 3 р/сут 3-5 дней – (высокий уровень резистентности);
• амоксициллин/клавуланат 500 мг 2 р/сут 3-5 дней;
• цефалексин 500 мг 3 р/сут 3-5 дней (высокий уровень резистентности);
• фосфомицин 3 г однократно;
• триметоприм-сульфаметоксазол 2 р/сут 3-5 дней (не применять триметоприм в 1-м триместре и сульфаметоксазол в 3-м триместре).
Большинство этих опций имеют значительные ограничения. В итоге для лечения бессимптомной бактериурии и цистита у беременных европейские рекомендации указывают только на фосфомицин и амоксициллин/клавуланат при выявлении чувствительной флоры.
Для лечения пиелонефрита у беременных применяют:
• цефтриаксон 1-2 г/сут парентерально;
• азтреонам 1 г в/в 2-3 р/сут;
• пиперациллин-тазобактам 3,375-4,5 г в/в 4 р/сут;
• цефепим 1 г в/в 2 р/сут;
• имипенем-циластатин 500 мг в/в 4 р/сут;
• ампициллин 2 г в/в 4 р/сут + гентамицин 3-5 мг/кг/сут в/в.
Если у беременной не удается установить локализацию инфекционно-воспалительного процесса, назначают цефалоспорин ІІІ поколения, при необходимости – парентерально по ступенчатой схеме. Опыт нашей клиники говорит о том, что оптимальным цефалоспорином для лечения ИМП у беременных является цефиксим (Цефикс). В отечественных и европейских рекомендациях этот препарат не внесен в схемы лечения ИМП у беременных, однако в российских протоколах он поставлен в один ряд с фосфомицином и цефтриаксоном. Для лечения острого цистита у беременных препаратами выбора являются фосфомицина трометамол и 7-дневные курсы цефалоспоринов ІІ-ІІІ поколения: фосфомицина трометарол 3 г однократно внутрь, цефиксим внутрь 400 мг 1 р/сут 7 дней или цефуроксим внутрь 250-500 мг 2 р/сут 7 дней. Альтернативными препаратами служат цефтибутен внутрь 400 мг 1 р/сут 3-7 дней, цефиксим внутрь 400 мг 1 р/сут 5-7 дней, амоксициллин/клавуланат (только при известной чувствительности возбудителя) внутрь 625 мг 3 р/сут 3-7 дней.
Для лечения острого цистита рекомендованы (EAU, 2015):
• цефиксим 8-12 мг/кг 3-5 дней или
• фурагин 0,1 г 3 р/сут 5 дней или
• нифурател 0,2 г 3 р/сут 5 дней.
При рецидиве цистита:
• цефиксим 8-12 мг/кг 5 дней или
• фурагин 0,1 г 3 р/сут 7 дней или
• нифурател 0,2 г 3 р/сут 7 дней.
Детям с рецидивирующим циститом показана консультация уролога/гинеколога, микционная цистография, обследование на наличие внутриклеточных возбудителей путем определения сывороточного уровня иммуноглобулинов класса G.
Профилактическое лечение при рецидивирующих циститах применяют у всех девочек. Мальчики практически не болеют острыми циститами, а если такая ситуация и случается, то уроантисептики у них не применяют, так как отсутствует восходящий путь проникновения инфекции. Поэтому лечение ИМП у мальчиков сразу начинают Цефиксом и профилактические дозы уроантисептиков не назначают.
Для профилактического лечения у девочек применяют фурагин, нифурател, фитопрепараты сроком от 3 до 6 месяцев.
Что касается лечения острого пиелонефрита у детей, то оно включает три обязательных компонента: дезинтоксикационную и цитопротективную терапию (инфузионные растворы), противовоспалительное лечение (парацетамол), антибактериальную терапию. Cроки лечения и антибиотики выбора для лечения острого пиелонефрита приведены в таблице 2. Сегодня наиболее обоснованным считается длительность антибиотикотерапии не более 10 дней. Даже при сохранении лейкоцитурии после 10-го дня противомикробной терапии продлевать прием антибиотиков не следует. Такие пациенты должны находиться под наблюдением врача и получать профилактическую терапию в течение 1-12 месяцев.
Амбулаторное лечение пиелонефрита должно включать:
1. Дезинтоксикационную терапию в течение 3-7 дней.
2. Противовоспалительное лечение (парацетамол, нимесулид для детей старше 12 лет).
3. Антимикробную терапию per os: цефалоспорины III поколения в течение 10 дней или левофлоксацин 750 мг/сут в течение 7 дней.
4. Профилактическую терапию в течение 3-12 мес.
Среди цефалоспоринов (табл. 3) одним из наиболее удачных для применения в урологии является Цефикс (цефиксим). Цефикс имеет пероральную лекарственную форму, что позволяет широко применять его для ступенчатой терапии. Основная идея ступенчатой терапии заключается в сокращении длительности парентерального введения антибиотика. Такой подход обеспечивает значительное уменьшение стоимости лечения, сокращение срока пребывания в стационаре при сохранении высокой клинической эффективности лечения.
Кроме того, уменьшение количества инъекций позволяет устранить психологический дискомфорт и уменьшить риск возникновения постинъекционных осложнений. Как возможный вариант ступенчатой терапии может быть использовано в/м введение ЦС ІІІ поколения в течение 3-4 дней, а затем переход на 7-дневный прием Цефикса.
Профилактическое лечение показано при наличии 2 рецидивов пиелонефрита в течение года или осложненного течения и назначается сроком на 3-12 месяцев:
• фурагин 50-100 мг на ночь;
• нифурател 0,2 г на ночь;
• бисептол 120-480 мг на ночь;
• фитопрепараты.
Подготовила Мария Маковецкая
СТАТТІ ЗА ТЕМОЮ Урологія та андрологія
Кількість людей, які страждають і помирають від вірусного гепатиту В (ВГВ), можна порівняти з кількістю хворих на коронавірусну хворобу 2019 року (COVID‑19), яка наразі викликає велике занепокоєння в усьому світі. Тому вкрай важливим залишається питання передачі вірусу, у тому числі через статеві клітини. Попередніми дослідженнями встановлено, що гени ВГВ, інтегровані в людські сперматозоїди, здатні до реплікації та експресії після передачі ембріонам. Однак досі це явище не було підтверджено клінічними дослідженнями у пацієнтів. Автори вивчали особливості інтеграції ВГВ у геном сперматозоїдів пацієнтів та аналізували можливі клінічні наслідки для потомства ...
За визначенням робочої групи Міжнародного товариства з проблем утримання сечі (ICS), у чоловіків термін «урологічний синдром хронічного тазового болю (СХТБ)» включає хронічний простатит (ХП) або СХТБ (ХП/СХТБ). Серед пацієнтів, які перебувають під амбулаторним спостереженням із приводу простатиту, понад 90% осіб мають діагноз ХП/СХТБ, що свідчить про високу поширеність цього урологічного захворювання в загальній структурі (Yang C.C. et al., 2018). Саме з наявністю ХП пов’язують підвищений ризик розвитку нетримання сечі, доброякісної гіперплазії передміхурової залози (ДГПЗ), запальних процесів сечостатевої системи, утворення каменів, кіст у ПЗ та виникнення раку ПЗ (РПЗ). Адже відомо, що в генезі останнього відіграють роль різні фактори, зокрема ампліфікація та мутація генів, що кодують гени-супресори пухлини, онкогени, а також фактори росту та цитокіни [1, 2]. Учені довели, що інгібування запалення, у тому числі за допомогою нестероїдних протизапальних препаратів (НПЗП), може зменшувати прогресування ХП та опосередковано впливати на зменшення ризику виникнення РПЗ. Водночас потужні анальгетичні властивості НПЗП дозволяють ефективно усувати хронічний тазовий біль та асоційовані з ним симптоми...
Хвороба Пейроні (ХП) — це захворювання сполучної тканини, що вражає білкову оболонку статевого члена, може спричиняти біль і пенільну деформацію; при цьому відомо, що поширеність патології зростає з віком. Хоча хірургічне втручання є золотим стандартом лікування хронічної фази ХП, існує низка методів консервативної терапії, однак оптимальний менеджмент пацієнтів із гострою фазою захворювання залишається предметом дискусії. У статті узагальнено дані останніх досліджень, що стосуються тенденцій нехірургічного лікування ХП ...
Симптоми з боку нижніх сечових шляхів (СНСШ), викликані доброякісною гіперплазією передміхурової залози (ДГПЗ), суттєво впливають на якість життя чоловіків. Динамічне спостереження та медикаментозне лікування з використанням широкого спектра препаратів можуть давати терапевтичний ефект. Проте хірургічне втручання залишається одним із найбільш ефективних рішень у пацієнтів із тяжкими формами цього захворювання. Трансуретральна резекція простати (ТУРП) є золотим стандартом хірургічного лікування. Утім з’являються й альтернативні методи, зокрема лазерна абляція простати за допомогою гольмієвого й тулієвого лазера (HoLEP і ThuLEP), а також роботизована водоструминна терапія (акваабляція), спрямовані на зниження післяопераційної захворюваності. Мінімально інвазивні хірургічні процедури (МІХП), що проводяться амбулаторно під місцевою анестезією або седацією, мають усе ширше застосування, особливо у хворих із високим хірургічним ризиком через супутню патологію. ...