Стаття у форматі PDF
Виразковий коліт (ВК) – це хронічне рецидивуюче ідіопатичне запальне захворювання кишечнику (ЗЗК). І хоча етіопатогенез ВК ще потребує докладного вивчення, зараз визнано, що його основою є складна взаємодія між генетичними, мікробними та зовнішніми факторами [1-3]. ВК характеризується прогресуючим перебігом: у багатьох пацієнтів вже під час дебюту захворювання відмічаються тяжкі клінічні симптоми, які згодом полегшуються, однак приблизно у половини з них захворювання поступово прогресує до більш тяжкої форми, що супроводжується поширенням ураження, погіршенням клінічного перебігу або рецидивуючими симптомами [4, 5]. Під час надання спеціалізованої допомоги раннє виявлення на етапі діагностики тих пацієнтів, які належать до груп ризику, є одним із найбільш складних завдань; і незважаючи на те що поширеність уражень слизової оболонки кишечнику, вочевидь, є раннім предиктором потенційної тяжкості перебігу ВК, поки що немає істотного консенсусу щодо його ролі порівняно з іншими чинниками ризику, які визначають несприятливий прогноз [6-8].
Типовий перебіг ВК характеризується тим, що захворювання починається з появи кров’янистої діареї. Пік маніфестації ВК спостерігається на 3 та 4-му десятиріччі життя [9]. Однак до 15% випадків ВК діагностують у людей віком старше 60 років, які становлять значну когорту пацієнтів; враховуючи більшу поширеність у цій популяції поліпрагмазії та супутніх захворювань, у таких пацієнтів затребувані так звані таргетні підходи до лікування, що характеризуються мінімальною кількістю ефектів, за межами їх високоспецифічного впливу [10]. Що стосується географічних особливостей, то показники захворюваності ВК знижуються з півночі на південь та із заходу на схід: при цьому найвища захворюваність реєструється у Північній Америці та Північній Європі, де частота ВК у загальній популяції становить до 0,5%. Одночасно з появою нових даних, котрі свідчать, що захворюваність у регіонах із високою частотою ВК, ймовірно, вже досягла плато, в інших регіонах вона, навпаки, зростає. І це зумовлює те, що проблема ВК стає дедалі більш значущою [11].
Вплив ВК на життя пацієнтів не можна недооцінювати; 73% із них повідомляють про те, що захворювання негативно позначається на їх активності під час дозвілля, дві третини – на їх професійній діяльності, а понад чверть хворих були змушені змінити роботу з цієї причини [12]. Серед низки емоційних, фізичних та соціальних факторів, які впливають на якість життя пацієнтів, саме активність захворювання є основним фактором, що чинить негативний вплив на їх самопочуття [13]. Тому терапевтичні стратегії мають бути націлені на зменшення тягаря хвороби кожної конкретної людини та відновлення якості її життя; до того ж поступово збільшується масив доказів того, що усунення запалення та загоєння слизової оболонки кишечнику дають можливість не лише досягти цих цілей, а й знизити ризик рецидиву захворювання у майбутньому [14]. Відомо, що персистуюче активне захворювання асоціюється з віддаленими ускладненнями, такими як анемія [15], дисфункція кишечнику та підвищений ризик розвитку колоректального раку [16]. Крім того, персистуюче запалення може призводити до розвитку системних побічних ефектів, таких як тромбоемболічні ускладнення [17], також існує ймовірність його самостійного внеску в розвиток серцево-судинних захворювань [18]. Згідно з даними Державної служби охорони здоров’я Великої Британії (NHS), орієнтовна вартість лікування ЗЗК становить ≥700 млн британських фунтів на рік, а за відсутності соціального медичного обслуговування (як, наприклад, у США) ця цифра може бути значно вищою [19, 20]. Окрім цього, витрати, пов’язані з ВК, зростають через значне зниження продуктивності праці окремих осіб унаслідок негативного впливу захворювання на їх здатність виконувати свої обов’язки – і це демонструє його вплив на більш широкі верстви суспільства [21]. Хоча вартість лікування ЗЗК загалом істотно не змінилася протягом 2 років, доступність більшості терапевтичних варіантів змінює структуру цих витрат – від переважання витрат на госпіталізацію та хірургічне втручання до збільшення частки, яку становить вартість лікарських засобів [21].
Найбільш важливе значення для зниження смертності від ВК свого часу мало застосування кортикостероїдів; однак властивий їм несприятливий профіль побічних ефектів та нездатність підтримувати ремісію роблять тривалу терапію цими препаратами неприйнятною [22]. У значної частки пацієнтів контролю захворювання можна досягти на фоні підтримувального лікування препаратами 5-аміносаліцилової кислоти (5-АСК) [23], хоча деякі хворі потребують імуномодуляції, яка найчастіше досягається завдяки призначенню азатіоприну [24]. Зараз накопичена істотна доказова база щодо терапії блокаторами фактора некрозу пухлини (ФНП), які підтримують безстероїдну ремісію [25, 26]. Проте як азатіоприн [27], так і блокатори ФНП [28] характеризуються обмеженою ефективністю та несприятливим профілем побічних ефектів. Більше того, хоча зараз у міжнародних керівництвах як варіант лікування рекомендовано інгібітори кальциневріну, їх застосування асоційоване з широким спектром можливих побічних ефектів [29].
У пацієнтів, які не відповідають на лікування або не можуть досягти безстероїдної ремісії на фоні медикаментозної терапії, важливим варіантом лікування є колектомія; незважаючи на останні терапевтичні досягнення, частота виконання колектомії з приводу хронічного активного захворювання істотно не змінюється [30, 31]. Таким чином, потреби пацієнтів із ВК у більш ефективному лікуванні дотепер залишаються незадоволеними.
Нещодавно перелік лікарських засобів, доступних для терапії ВК, доповнив новий препарат – ведолізумаб. Він чинить цілеспрямовану дію на рекрутінг (тобто накопичення у вогнищі запалення) лейкоцитів у кишечнику шляхом блокування α4β7-інтегрину, що зменшує запалення та запобігає рецидиву у пацієнтів із ВК. У цьому огляді подано обґрунтування застосування ведолізумабу при ВК, а також наведено дані щодо його використання у клінічній практиці.
Блокада рекрутінгу лімфоцитів: обґрунтування
Фактори, які ініціюють ВК, не є достатньо вивченими. Подальші адаптивні відповіді частково несуть відповідальність за підтримання запалення, доказом чого є накопичення лімфоцитів в ураженому кишечнику [32]. Наївні Т-лімфоцити активуються CD103+дендритними клітинами у периферичних лімфоїдних органах, де вони розпізнають антиген, діляться і дозрівають, тобто визначається їх шлях міграції до кишечнику завдяки реалізації механізму, який залежить від ретиноєвої кислоти [33, 34]. У нормі цей процес, згідно з сучасними уявленнями, має стимулювати формування толерантності та утворення Т-регуляторних клітин, які допомагають підтримувати наявний в кишечнику гомеостаз; однак за умов локального запалення дендритні клітини здійснюють активацію Т-ефекторних відповідей, котрі під дією неадекватного стимулу можуть спричиняти персистуюче запалення [35].
Інтегрин α4β7, на який ведолізумаб чинить цілеспрямований вплив, є рецептором, участь якого необхідна при переміщенні клітин до кишечника [36]. Його експресія не обмежується тільки циркулюючими звичайними Т-клітинами – вона також має місце на В-клітинах, мієлоїдних, лімфоїдних і нетипових γδ Т-клітин вродженого імунітету; всі вони (хоча і менш вивченим чином) мають потенційну здатність посилювати неналежну імунну відповідь [37-39]. Експресія молекули клітинної адгезії типу «адресин» у слизових оболонках (MAdCAM‑1) переважно обмежена ендотелієм судин, асоційованих із Пейєровими бляшками та власною пластинкою (lamina propria) слизової оболонки кишечнику. MAdCAM‑1 є основним лігандом для опосередкованої α4β7 адгезії та захоплення з кровотоку Т-клітин [40-42]. Його експресія стає неконтрольованою при ВК, тому, враховуючи специфічну для кишечнику експресію MAdCAM‑1, таргетний підхід до блокади взаємодії між ним та α4β7 можна вважати привабливою терапевтичною стратегією [43].
Інтегрин α4β7 – це гетеродимер; отже, α- та β-субодиниці можуть бути спільними з іншими інтегринами [44]. Наталізумаб – гуманізоване моноклональне антитіло до α4-субодиниці. Хоча відомо про ефективність наталізумабу при хворобі Крона (ХК) [45], він також блокує й α4β1-інтегрин, запобігаючи міграції лейкоцитів до центральної нервової системи (ЦНС), внаслідок чого можуть виникнути серйозні побічні ефекти [46]. Для порівняння, ведолізумаб чинить таргетну дію на α4β7 гетеродимер, а отже, є специфічним відносно саме тих лейкоцитів, які тропні до кишечнику. Призначення ведолізумабу здоровим нелюдиноподібним приматам призводить до зменшення накопичення β7+ мононуклеарних клітин у тонкій та товстій кишках, а також до реципрокного збільшення кількості циркулюючих β7+ Т-клітин пам’яті [47]. Більше того, оскільки ведолізумаб – селективний відносно шлунково-кишкового тракту (ШКТ), встановлено, що він зв’язується з мононуклеарними клітинами у ШКТ (цей ефект найбільш виражений у тонкій, товстій кишках та шлунку), але не зв’язується з ними поза кишечником, у тому числі в головному мозку, шкірі та легенях [47]. Таким чином, ведолізумаб може відігравати особливу роль у лікуванні тих пацієнтів, у яких небажана або протипоказана системна імуносупресія, що зазвичай досягається завдяки застосуванню стероїдів, імуносупресантів і блокаторів ФНП.
Однак слід зазначити, що головний «гравець» – інтегрин α4β7 – не є унікальним за своєю здатністю спрямовувати лейкоцити до кишечнику. Нещодавно отримані дані свідчать про превалювання CCR9+ T-клітин та його ліганда CCL25 у власній пластинці запаленої слизової оболонки у хворих на ВК порівняно зі здоровими особами контрольної групи [48]. Нещодавно був опублікований огляд потенційних функцій CCR9 [49]. Однак хоча це питання поки що не вивчали у клінічних дослідженнях за участю хворих на ВК, клінічні результати блокади CCR9 при ХК були неоднозначними [49]. Інші потенційні мішені, такі як GPR15 [50], демонструють потенційну здатність порушувати міграцію лейкоцитів; однак, на відміну від таргетного впливу на α4β7, їх можливе застосування – віддалена перспектива для реальної клінічної практики. У той час як лікування ЗЗК покращувалось завдяки застосуванню препаратів, розроблених для лікування інших патологічних станів, можливо, ведолізумаб матиме більш значущий вплив на здоров’я людини, а здатність ведолізумабу впливати на міграцію Т-лімфоцитів до кишечнику може мати і інші сфери застосування. Зокрема, відомо, що тонка кишка – це і місце локалізації інфекції, і резервуар для ВІЛ; в експериментальній моделі на тваринах продемонстровано, що блокада α4β7 у поєднанні з антиретровірусною терапією (АРТ) дозволяє досягти стійкої вірусологічної відповіді та запобігти вірусному рикошету в разі припинення АРТ [51].
Фармакологія
Ведолізумаб має високу ефективність з точки зору блокади α4β7; застосування однократної дози ведолізумабу через 4 тижні призводило до зв’язування >90% рецепторів на поверхні циркулюючих CD4+CD45RO+ T-клітин [52]. Фармакокінетичне моделювання, виконане в ході клінічних досліджень ефективності ведолізумабу II та III фази [53], дозволило встановити, що його Т 1/2 становить 25,5 діб (діапазон – 14,6-36 діб; 5%-95% перцентілі). Розподіл препарату найкраще описує двокомпонентна фармакокінетична модель, у якій має місце нелінійна елімінація, регульована насичуваними механізмами, такими як зайнятість рецепторів, а інші ненасичувані механізми відповідають за лінійну елімінацію [53]. Основними клінічними чинниками, які негативно впливають на концентрацію ведолізумабу, є низький сироватковий рівень альбуміну та маса тіла >120 кг [53].
Значний обсяг наших знань про застосування моноклональних антитіл при ВК ґрунтується на досвіді терапії блокаторами ФНП, при якій на клінічну відповідь впливали певні клінічні параметри, рівні препарату та антитіл до препарату (АП) [54]. Хоча АП відіграють значну роль у терапії блокаторами ФПН, їх значення для фармакокінетики ведолізумабу поки що є не з’ясованим. У ранніх дослідженнях високі показники частоти формування АП супроводжувалися відповідями на лікування, аналогічними отриманим при застосуванні плацебо [52]. Однак зі зміною методу виробництва препарату значно зменшилася частота формування АП (зареєстровано у 11% пацієнтів) [55], а об’єднані дані досліджень III фази за участю пацієнтів із ВК (GEMINI 1) і з ХК (GEMINI 2) свідчать про формування АП лише у 16% пацієнтів [56, 57]. Незначна кількість осіб із персистуючими АП і низькі титри АП, виявлені у більшості таких пацієнтів (<1:15), ускладнюють оцінку внеску формування АП у неефективність лікування [55].
Відомо, що комбінована терапія із застосуванням імуномодулятора не тільки зменшує ризик формування АП при терапії блокаторами ФНП, а й може також змінювати фармакокінетику цих антитіл [58, 59]. Однак існують докази того, що імуномодуляція чинить незначний вплив на фармакокінетику ведолізумабу або взагалі не впливає на неї [60]. Кліренс ведолізумабу збільшується на 12% за наявності АП [53], тоді як кліренс інфліксімабу – на 47,1% [54]. Таким чином, хоча АП можуть чинити клінічно значущий вплив на ефективність лікування ведолізумабом, слід бути обережним при спробі екстраполювати дані щодо «поведінки» різних ліків на основі моноклональних антитіл, а, враховуючи відносно низьку імуногенність ведолізмабу, з метою визначення істинного значення АП необхідно провести ґрунтовні дослідження.
Ефективність
Дослідження GEMINI 1
Ефективність застосування ведолізумабу з метою індукції або підтримання ремісії при ВК продемонстровано у ході багатоцентрового рандомізованого плацебо-контрольованого дослідження III фази GEMINI 1, участь у якому взяли понад 800 пацієнтів із 34 країн світу [54]. Його учасники мали активне захворювання середньої тяжкості або тяжке, ураження слизової оболонки кишечнику поширювалося як мінімум на 15 см від ануса; також попереднє лікування у них було неефективне (тобто наявність активного захворювання, відсутність відповіді на лікування або виникнення неприйнятних небажаних явищ) при застосуванні одного або більшої кількості кортикостероїдів, імуносупресивних препаратів (тобто тіопурину) або блокаторів ФНП.
Фаза індукції ремісії
Дослідження GEMINI 1 включало дві когорти індукції ремісії: подвійну сліпу когорту (n=374), рандомізовану для отримання плацебо або ведолізумабу в дозі 300 мг внутрішньовенно (в/в) на 0-му та 2-му тижні, а також відкриту когорту (n=521), сформовану для набору потрібної кількості пацієнтів, котрі відповіли на лікування, з метою забезпечення достатньої статистичної потужності дослідження у фазі підтримання ремісії.
Дослідження GEMINI 1 досягло своєї первинної кінцевої точки у фазі індукції ремісії, продемонструвавши достовірну клінічну відповідь на 6-му тижні лікування у групі терапії порівняно з групою плацебо (47,1% порівняно з 25,5%, p<0,001). Враховуючи збільшення масиву доказів того, що загоєння слизової оболонки кишечнику може бути клінічно значущим [61, 62], його було включено в аналіз як вторинну кінцеву точку. Загоєння слизової оболонки кишечнику, визначене як показник за ендоскопічною субшкалою 0 або 1 бал, достовірно частіше зустрічалося у групі ведолізумабу, ніж у групі плацебо (40,9% порівняно з 24,8%, p=0,001).
Фаза підтримання ремісії
На момент включення у підтримувальну фазу дослідження GEMINI 1 пацієнти, які відповіли на терапію ведолізумабом у фазі індукції ремісії, були повторно рандомізовані для отримання плацебо або ведолізумабу (300 мг в/в), що призначали з 4- або 8-тижневими інтервалами до кінця 52-го тижня дослідження. Всіх пацієнтів, які не відповіли на терапію ведолізумабом у фазі індукції ремісії, переведено на більш інтенсивне лікування з 4-тижневим інтервалом між введеннями препарату; ті пацієнти, які відповіли на призначення плацебо під час фази індукції, продовжували отримувати його і у підтримувальній фазі. Рандомізація пацієнтів була стратифікована залежно від 3 факторів: когорта індукції, супутнє застосування кортикостероїдів та імуносупресивних засобів або попереднє застосування блокаторів ФНП.
Первинною кінцевою точкою у підтримувальній фазі дослідження була клінічна ремісія на 52-му тижні, визначена як показник оцінки за шкалою клініки Мейо 2 бали чи менше (за умови відсутності за жодною субшкалою значення вище 1 балу). Результати підтримувальної фази виявилися так само вражаючими, як і результати фази індукції: на фоні терапії ведолізумабом достовірно більша кількість пацієнтів досягли ремісії порівняно з тими, хто отримував плацебо (41,8% порівняно з 15,9% при застосуванні кожні 8 тижнів ведолізумабу порівняно з плацебо, p<0,001); частота досягнення стійкої клінічної відповіді (як через 6, так і через 52 тижні) становила 56,6% порівняно з 23,8% (p<0,001). На фоні введення ведолізумабу кожні 8 тижнів на 52-му тижні загоєння слизової оболонки кишечнику вдалося досягти у 51,6% пацієнтів порівняно з 19,8% пацієнтів у групі плацебо (p<0,001).
Кокранівський систематичний огляд та метааналіз
Кокранівський систематичний огляд та метааналіз об’єднали дані, отримані у дослідженні GEMINI 1 [56], з даними трьох досліджень III фази, виконаних протягом більш ніж 12-річного періоду [52, 55, 63, 64]. Вони включали дослідження з визначення оптимального режиму дозування, а також дослідження, основною метою яких було отримання даних, що дозволили б глибше зрозуміти аспекти безпеки та фармакологічні властивості ведолізумабу. Аналіз об’єднаних даних підтвердив, що ведолізумаб достовірно переважає плацебо, зменшуючи частоту випадків неможливості досягти ремісії (відносний ризик (ВР) 0,86; 95% довірчий інтервал (ДІ) 0,80-0,91), відсутності клінічної відповіді (ВР 0,82; 95% ДІ 0,75-0,91) та недосягнення ендоскопічної ремісії (ВР 0,82; 95% ДІ 0,75-0,91).
Обсерваційні дослідження з вивчення ефективності
Хоча ефективність визначається за показниками досягнення клінічних кінцевих точок у висококонтрольованих умовах клінічного дослідження, зараз зростає розуміння важливості обсерваційних досліджень лікарських засобів, що виконуються в умовах реальної клінічної практики [65, 66]. Враховуючи це, декілька груп експертів із США та Європи опублікували свої дані щодо отриманого ними досвіду застосування ведолізумабу в широкій популяції хворих із ЗЗК для того, щоб доповнити результати, отримані у ході досліджень GEMINI (рис.).
Досвід застосування у США
Клініцисти з Чиказького університету повідомили про досвід лікування 110 пацієнтів із ЗЗК (78 – з ХК та 32 – з ВК) [67]. З метою оцінки ефективності терапії вони застосували Простий клінічний індекс активності коліту (Simple Clinical Colitis Activity Index, SCCAI) [68]: відповідь була визначена як зменшення початкової оцінки на 3 пункти, а ремісія – як значення SCCAI <3 балів. Незважаючи на відносно рефрактерні групи пацієнтів (у більшості пацієнтів із ВК застосування монотерапії блокатором ФНП виявилося неефективним – 47%, а у значної частини хворих спостерігалася неефективність декількох блокаторів ФНП – 19%), проаналізувавши ефективність лікування пацієнтів з активним захворюванням (n=23), вони повідомили про показники клінічної відповіді та досягнення ремісії на 14-му тижні, що становили 52 та 39% відповідно. Загалом встановлено зменшення середнього значення SCCAI з 4,5 балів на 0-му до 2,9 балів на 14-му тижні із подальшим його зниженням до 1,7 балів на 30-му тижні.
В інше дослідження було включено 172 пацієнти (107 – з ХК, 59 – з ВК та 6 – з некласифікованим ЗЗК), проспективна оцінка стану яких проводилась у двох великих академічних центрах м. Бостона [69]. Важливо, що дослідники встановили той факт, що лише 36% пацієнтів, які узяли у ньому участь, відповідали тим критеріям включення, які використовували в дослідженнях GEMINI (вказавши при цьому причини, такі як наявність ілеостоми/колостоми або ілеоанального резервуару як критерію виключення). Ці дані ще більше підкреслюють важливість проведення реальних обсерваційних досліджень. Дослідники, використавши ту саму методологію, що й в дослідженні Чиказької групи, повідомили про показники частоти досягнення клінічної відповіді та ремісії, що становили 54 та 29% відповідно, у 58 пацієнтів, за даними, доступними станом на 14-й тиждень лікування. Крім того, дані щодо використання кортикостероїдів на 14-му тижні продемонстрували частоту досягнення безстероїдної ремісії, що становила 23%.
Група дослідників із Центру ЗЗК Вашингтонського університету здійснила додатковий внесок у розуміння клінічної ефективності ведолізумабу, проаналізувавши її у 102 пролікованих пацієнтів [70]. Проведене обсерваційне дослідження включало як проспективні, так і ретроспективні когорти, а також дозволило отримати певні ендоскопічні дані. З числа пацієнтів із ВК у проспективній когорті, які завершили 14 тижнів лікування, 55% досягли ремісії (частковий показник за бальною шкалою Мейо ≤2 балів за умови відсутності показників за жодною субшкалою вище ніж 1 бал). Ці пацієнти також продемонстрували статистично достовірне покращення показників часткової бальної оцінки за шкалою Мейо на 6-му тижні (–2,6, p=0,002) та на 14-му тижні лікування (–2,9, p=0,0002). Крім того, також у них було досягнуто ендоскопічну відповідь; у 29 пацієнтів із показником оцінки за ендоскопічною субшкалою Мейо 2 (помірна) або 3 (тяжка) бали у початковому стані в 69% випадків спостерігалося загоєння слизової оболонки кишечнику (визначалося як значення оцінки за ендоскопічною субшкалою Мейо 0 або 1 бал).
Європейський досвід
У лютому 2016 р. французька дослідницька група з вивчення підходів до терапії запальних уражень травного тракту GETAID (Groupe d’Etude Therapeutique des Affections Inflammatoires du tube Digestif) надрукувала результати багатоцентрового дослідження за участю 121 пацієнта з ВК, які отримували ведолізумаб у рамках благодійної програми раннього доступу до лікування [71]. Знову таки, ця когорта включала значну частку пацієнтів із рефрактерним захворюванням; 98% пацієнтів вже отримували один блокатор ФНП, а 69% – два препарати цієї групи. Використовуючи визначення кінцевих точок, аналогічні точкам у дослідженні GEMINI 1, на 14-му тижні було повідомлено про частоту досягнення ремісії, що становила 39% (36% – безстероїдна ремісія), та про відповідь на лікування у 57% пацієнтів. Крім того, дослідники вивчили предиктори клінічної ефективності та встановили, що прогностичними факторами досягнення безстероїдної ремісії на 14-му тижні лікування були: клінічна відповідь на 6-му тижні (p<0,001), бальна оцінка за шкалою клініки Мейо >9 балів (p=0,002), рівень C-реактивного білку >20 мг/л (p=0,005), кількість лейкоцитів >8500×10–9/л (p=0,02) та чоловіча стать (p=0,09).
Спираючись на досвід, отриманий групою GETAID, та використавши аналогічну методологію дослідження, Німецький консорціум із вивчення ведолізумабу (German vedolizumab consortium) оприлюднив результати загальнонаціонального когортного дослідження, у ході якого було здійснено проспективний збір даних у когорті із 115 пацієнтів із ВК [72]. Німецькі дослідники повідомили про ефективність препарату, що була аналогічною вказаним результатам: на 14-му тижні лікування показники частоти досягнення відповіді на терапію та частоти ремісії становили 57 та 24% відповідно. Однак при цьому набір предикторів клінічної ефективності, визначений німецькою групою дослідників, відрізнявся від набору в дослідженні групи GETAID. Отримані дані свідчать про те, що активне тютюнопаління або тютюнопаління в анамнезі (p=0,044/0,028) та відсутність попереднього впливу блокаторів ФНП (p=0,023) асоційовані з клінічною ремісією на 14-му тижні. В подальшому ці дані були доповнені результатами тривалого дослідження, в яке включили вибірку пацієнтів з оригінальної когорти, а також додатково набраних осіб [73]. Як і результати на 14-му тижні, що загалом були аналогічні отриманим у раніше зазначених дослідженнях (рис.), результати 1-річного спостереження за 60 пацієнтами із ВК продемонстрували показники частоти досягнення клінічної ремісії та безстероїдної ремісії, які становили 25 та 22% відповідно. Слід зазначити, що відсутність відповіді на лікування на 14-му тижні вказувала на низьку ймовірність досягнення клінічної ремісії на 54-му тижні.
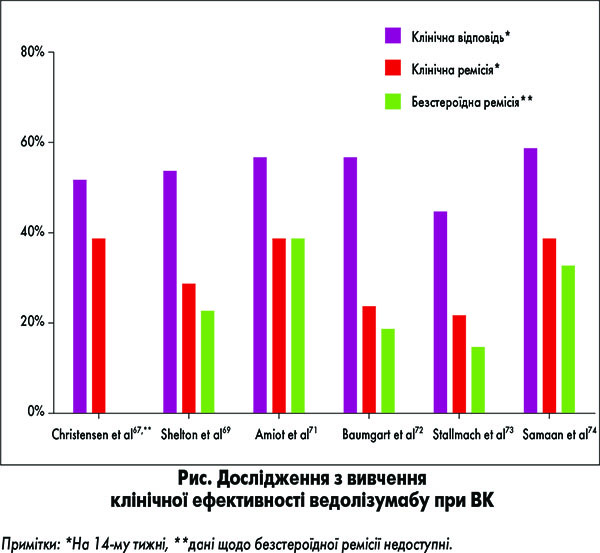
Загалом дані ретроспективного обсерваційного дослідження, отримані у Центрі ЗЗК (Лікарня Гая та Св. Томаса) та у госпіталі Королівського коледжу з використанням вимірювання активності захворювання за індексом SCCAI, продемонстрували ефективність ведолізумабу, яка була аналогічною результатам описаних досліджень [74]. Встановлено зниження клінічної активності захворювання у 23 пацієнтів із ВК: медіана SCCAI зменшилась із початкового значення 6 балів до 4 балів на 14-му тижні (p=0,005) та до 2 балів у 10 пацієнтів, спостереження за якими здійснювалося до 30-го тижня (p=0,023); наслідком цього стало досягнення показника ремісії на 14-му тижні, який становив 39% (33% – безстероїдна ремісія), та відповіді на лікування у 55% пацієнтів. До 30-го тижня ремісія спостерігалася у 50% пацієнтів (у всіх – без застосування кортикостероїдів), а відповідь на лікування – ще у 10%. За даними комбінованого аналізу з включенням пацієнтів із ХК також встановлено значне зниження медіани рівня фекального кальпротектину у початковому стані порівняно зі станом на 14-му тижні лікування (1076 мкг/г порівняно з 476 мкг/г, p=0,010).
Порівняльні дослідження
Сьогодні дані прямих порівняльних досліджень ефективності біологічних препаратів при ВК є недоступними, хоча наразі триває активне вивчення цього питання. Наприклад, зараз проводиться пряме порівняльне дослідження ефективності етролізумабу (селективний інгібітор молекули адгезії лейкоцитів, який має механізм дії, аналогічний ведолізумабу) та інфліксімабу в пацієнтів, які раніше не отримували терапію блокаторами ФНП [75].
З огляду на відсутність відповідних даних Danese та співавт. виконали системний метааналіз рандомізованих контрольованих досліджень (РКД), у яких вивчили застосування біологічних препаратів як терапії, яка має на меті індукцію або підтримання ремісії, у пацієнтів із середньою або вираженою активністю ВК [76]. В аналіз із використанням методів байєсової статистики було включено 8 РКД із вивчення ефективності інфліксімабу, адалімумабу, голімумабу та ведолізумабу. Методологічні розбіжності в дизайні досліджень ускладнювали порівняння цих препаратів при їх застосуванні як підтримувальної терапії; однак у пацієнтів, які раніше не отримували блокаторів ФНП, ефективність ведолізумабу та блокаторів ФНП при їх застосуванні з метою підтримання ремісії загалом була аналогічною.
Однак, як визнають автори, цінність цього типу аналізу обмежена, тому існує необхідність у прямих порівняльних дослідженнях терапевтичних засобів, так само як і в дослідженнях в умовах реальної клінічної практики, предметом яких була б оцінка як клінічної ефективності препаратів, так і властивого їм співвідношення вартість/ефективність.
Аналіз релевантних серій клінічних випадків
У масштабних клінічних дослідженнях не оцінюють користь від застосування ведолізумабу в особливих випадках, таких як запалення резервуару після реконструктивної проктоколектомії та за наявності ілеоанального резервуарного анастомозу. Підгрупа дослідників із Бостонської когорти описала ефекти ведолізумабу у 8 пацієнтів із запаленням резервуару (внаслідок рефрактерного запального процесу в резервуарі або внаслідок ураження резервуару при ХК) [69]. Шість (75%) пацієнтів відповіли на лікування (зниження модифікованого індексу активності запалення резервуару (mPDAI) на 2 бали або більше), а в одного пацієнта (13%) досягнуто ремісії (mPDAI ≤4 бали).
Як відомо, з ВК асоційоване аутоімунне захворювання печінки (АІЗП) – у формі первинного або аутоімунного склерозуючого холангіту (ПСХ та АІСХ). Більше того, АІЗП пов’язане з аберантною експресією MADCAM‑1 на ендотелії печінки [77] – і саме цим можна обґрунтувати доцільність застосування ведолізумабу в цій клінічній ситуації, а також у лікуванні ПСХ [78].
В одному з досліджень здійснено оцінку лікування ведолізумабом у когорті з 10 хворих на ВК та АІЗП, половині з яких проведено трансплантацію печінки. Клінічна відповідь (зниження SCCAI на 3 бали та більше) на 14-му тижні спостерігалася у 4/10 (40%) пацієнтів, а ремісія (SCCAI <3 балів) – у 1/10 (10%) пацієнтів. Важливо, що у групі пацієнтів, у яких вже здійснювалася імуносупресія, не було отримано даних про те, що терапія ведолізумабом приводить до збільшення частоти інфекційних ускладнень [79], хоча, вочевидь, ця когорта є нечисленною і спостереження за пацієнтами було порівняно незвичайним.
Безпека та переносимість
Дані про безпеку
Як було описано вище, наталізумаб є ефективним препаратом для лікування ХК, а завдяки його здатності запобігати міграції лейкоцитів у ЦНС – і для лікування розсіяного склерозу. На жаль, у незначної кількості пацієнтів його застосування призводило до розвитку прогресуючої мультифокальної лейкоенцефалопатії (ПМЛ), зумовленої реактивацією віруса Джона Каннінгема, яка супроводжується катастрофічною неврологічною дегенерацією та може мати фатальні наслідки. Це стало причиною інтенсивної перевірки під час розробки ведолізумабу і зумовило створення всеосяжної програми моніторингу безпеки – RAMP (Оцінка та мінімізація ризику ПМЛ), що передбачає детальний скринінг та моніторинг клінічних ознак неврологічної дисфункції на фоні застосування препарату.
Використовуючи дані про частоту клінічних випадків ПМЛ, асоційованих із застосуванням наталізумабу, можна екстраполювати, що очікувана частота ПМЛ у пацієнтів, котрі отримують лікування ведолізумабом, становитиме приблизно 2,1 випадків на 1000 пацієнтів [80]; однак у рамках реалізації програми RAMP не повідомлялося про жодний випадок цього ускладнення у 2884 хворих, на ЗЗК. Також дотепер не описано жодного випадку ПМЛ на фоні застосування препарату в реальній клінічній практиці. Експериментальні дані демонструють, що, на відміну від наталізумабу, ведолізумаб не запобігає розвитку запальних уражень на моделях розсіяного склерозу у тварин [81] і не впливає на рекрутінг лейкоцитів у ЦНС [82]. Отже, ґрунтуючись на експериментальних даних та даних обсерваційних спостережень за пацієнтами, можна припустити, що ймовірність наявності будь-якої асоціації між терапією ведолізумабом і розвитком ПМЛ є вкрай низькою.
Системні імуносупресивні ефекти ведолізумабу також було оцінено; в 2014 р. Wyant та співавт. виконали дослідження з витонченим дизайном, у якому використовувалася оральна (проти холери) та парентеральна (проти гепатиту В) вакцинація у пацієнтів, які отримували ведолізумаб або плацебо [83]. Як і можна було очікувати, на фоні застосування ведолізумабу спостерігалося послаблення імунних відповідей збоку слизової оболонки (судячи з титрів IgA) на пероральне введення вакцини, але він не чинив ефекту на імунні відповіді на парентеральну вакцинацію. Отримані результати підтвердили, що ця селективна терапія характеризується меншою кількістю системних ефектів.
Дані найбільш масштабного дослідження довгострокової безпеки ведолізумабу були надруковані на початку 2016 р. До нього було включено понад 2800 пацієнтів, які отримували лікування терміном до 5 років включно у рамках 6 клінічних досліджень (два дослідження II фази та чотири дослідження III фази) [84]. Результати цього дослідження підтвердили, що серед хворих, яких лікували ведолізумабом, ризик серйозних опортуністичних інфекцій (4,3/100 пацієнто-років) і частота злоякісних новоутворень (0,1/100 пацієнто-років) порівнянні з відповідними показниками у загальній популяції пацієнтів із ЗЗК. Кишкові інфекції рідко реєструвалися у пацієнтів, які отримували лікування ведолізумабом, і у разі їх виникнення вони зазвичай перебігали у формі неспецифічного гастроентериту. Інші кишкові інфекції, такі як абсцеси ШКТ або періанальної зони, загалом рідше виникали у пацієнтів, які приймали ведолізумаб, ніж у тих, хто отримував плацебо.
Реальні запобіжні заходи
В обсерваційному дослідженні, проведеному Vivio та співавт., небажані явища зареєстровано у 6 пацієнтів із 21 (29%) у проспективній когорті та у 2 із 30 пацієнтів (7%) у ретроспективній когорті [70]. Шість із цих небажаних явищ були пов’язані з посиленням активності ВК, що потребувало хірургічного втручання, тоді як інші два – це були захворювання з фебрильною температурою тіла, які минули без лікування, та епізод кон’юнктивіту. Чиказька група дослідників повідомляла про побічні реакції у 41% пацієнтів, хоча більшість із них мали відносно незначну вираженість або були пов’язані з посиленням активності захворювання. Однак у цьому дослідженні наявне застереження, пов’язане з 4 епізодами інфекції, спричиненої Clostridium difficile, серед 110 пролікованих пацієнтів (4%); хоча слід зазначити, що їх зареєстровано у зоні з високою поширеністю C. difficile.
Перспективи пацієнтів
Якість життя, пов’язана зі здоров’ям (HRQL), була включена як пошукова кінцева точка в аналіз результатів дослідження GEMINI 1. Її оцінку здійснювали на 6-му, 30-му та 52-му тижні за допомогою опитувальника для пацієнтів із ЗЗК – IBDQ [56]. IBDQ – добре валідований опитувальник, який широко застосовується; чим вища сума бальної оцінки за IBDQ (діапазон – від 0 до 224 балів), тим кращою є якість життя [85]. Збільшення бальної оцінки за IBDQ між початковим станом та станом на 6-му тижні було достовірно більш істотним у пацієнтів, які отримували лікування ведолізумабом, аніж у тих, хто отримував плацебо (p<0,0001). Більше того, під час підтримувальної фази лікування відзначалося покращення декількох оцінок HRQL (у тому числі – за IBDQ) порівняно з пацієнтами, котрі отримували плацебо, особливо у групах пацієнтів із низькою початковою активністю захворювання або у пацієнтів, які раніше не отримували терапію блокаторами ФНП [86].
З точки зору пацієнта переносимість терапії має вирішальне значення. Цей аспект оцінювали непрямим шляхом в обсерваційній когорті з м. Вашингтона: дослідники встановили, що ведолізумаб загалом добре переноситься, і 90% пацієнтів продовжували лікування до 14-го тижня, а 84% – до 52-го тижня. Інфузійні реакції на введення ведолізумабу виникали відносно рідко, і більшість із них були легкими або помірними та не потребували припинення лікування. Довгострокові дані про безпеку свідчать про їх наявність у менш ніж 5% пацієнтів; при цьому найчастіше повідомляли про такі симптоми, як нудота та головний біль. У переважній більшості випадків (>99%) інфузії не переривали та завершили, незважаючи на реакції [84].
Вивчивши дані 102 пацієнтів із ЗЗК (45 – з ВК, 57 – з ХК), Vivio та співавт. встановили, що показники частоти випадків продовження лікування на 52-му тижні становили 84 та 74% при ВК та ХК відповідно. Це свідчить про те, що більшість пацієнтів загалом добре переносили лікування препаратом [70]. Більше того, досвід, отриманий при застосуванні інфліксимабу, демонструє, що частота випадків відсутності прихильності до схеми введення препарату кожні 8 тижнів при ЗЗК є низькою [87] і може бути ще нижчою, порівняно з частотою, встановленою на фоні підшкірного введення аналогічних препаратів [88].
Персоналізована терапія
Ідентифікація осіб, які мають отримати користь від застосування специфічних видів терапії, є складним завданням, проте її здійснення має першочергову важливість. Ефективне застосування таргетних, тканинно-специфічних засобів терапії потребує більшої концентрації на розумінні механізмів захворювання та може полегшити розробку біомаркерів відповіді на лікування. Наприклад, етролізумаб – інше моноклональне антитіло, що чинить таргетний вплив на міграцію імуноцитів – зв’язується з β7 і у такий спосіб блокує як α4β7, так і інтегрин епітеліального хомінгу αЕβ7. Більш високі рівні початкової експресії гена ITGAE (гена, що кодує αE-інтегрин) та GZMA (гранзим A) були асоційовані з відповіддю на етролізумаб у нещодавно виконаному дослідженні II фази [89]. Хоча цей тип даних поки що недоступний щодо ведолізумабу, розуміючи патогенез ВК, можна сподіватися на розробку аналізів, які даватимуть змогу виявляти тих пацієнтів, у яких очікується найбільша користь від таргетної терапії.
Висновок
Позиціонування ведолізумабу в алгоритмах лікування ВК
В ідеалі стратегія лікування ВК має бути адаптована до потреб кожного конкретного пацієнта. Враховуючи відносну неспроможність визначити прогноз захворювання на момент його дебюту, згідно з рекомендаціями Європейської організації з вивчення ХК та ВК, при виборі варіанта лікування слід брати до уваги декілька факторів [29]. Слід враховувати активність та поширеність захворювання, частоту рецидивів та ступінь їх тяжкості, а також вплив попередніх видів лікування. Крім цього, слід розглянути відносні ризики та переваги різних стратегій лікування. Вибір препарату для першої лінії біологічної терапії, виходячи з його механізму дії при ВК, сьогодні викликає значний інтерес. Однак через відсутність даних прямих порівнянь вибір терапії зводиться до комбінованої оцінки клінічної ситуації та вибору самого пацієнта. Плюси та мінуси у кожній конкретній клінічній ситуації, вочевидь, має оцінювати мультидисциплінарна команда фахівців із лікування ЗЗК. Ми, зокрема, розглядаємо всі релевантні аспекти конкретних клінічних випадків [90], які включають специфічні для ЗЗК фактори, такі як позакишкові прояви або періанальне захворювання (у випадках можливої переваги блокаторів ФНП), а також супутню патологію, таку як схильність або наявність у анамнезі злоякісного новоутворення чи інфекції (у випадку можливої переваги ведолізумабу). Крім того, може виникнути потреба у врахуванні таких практичних факторів, як побажання пацієнта щодо шляху введення препарату та здатність контролювати тиск у інфузійному пакеті.
Таким чином, ведолізумаб – це ефективний препарат для терапії ВК. Враховуючи це, слід сконцентрувати увагу на визначенні його позиції у терапевтичній ніші, яка продовжує розширюватися, а також на пошуку біомаркерів відповіді на терапію. Це сприятиме реалізації персоналізованого підходу до лікування, котрий належить застосовувати у XXI сторіччі.
Clinical and Experimental Gastroenterology 2017: 10 57-66
Стаття друкується у скороченні.
Список літератури знаходиться в редакції.
Переклала з англ. Олена Терещенко
За підтримки ТОВ «Такеда Україна»
UA/EYV/0917/0050
Тематичний номер "Гастроентерологія, Гепатологія, Колопроктологія" № 3 (45) вересень 2017 р.



