8 грудня, 2017
Клиническая эффективность тамсулозина при синдроме хронической тазовой боли у мужчин

 Актуальность проблемы хронических воспалительных заболеваний мужских половых органов не подлежит сомнению в связи с тем, что каждый второй мужчина страдает этим заболеванием в какой-либо период своей жизни [21, 28]. Такие больные, как правило, достаточно молоды, болезнь сопровождается симптоматикой различной тяжести и в результате может осложняться психологическими проблемами.
Актуальность проблемы хронических воспалительных заболеваний мужских половых органов не подлежит сомнению в связи с тем, что каждый второй мужчина страдает этим заболеванием в какой-либо период своей жизни [21, 28]. Такие больные, как правило, достаточно молоды, болезнь сопровождается симптоматикой различной тяжести и в результате может осложняться психологическими проблемами.
 В Украине простатит поражает около 19% мужского населения в возрасте от 20 до 60 лет [31]. Сам термин «хронический простатит» (ХП) может обозначать широкий спектр состояний предстательной железы (ПЖ) и нижних мочевых путей (инфекционный простатит, синдром хронической тазовой боли (СХТБ), простатодиния при абактериальном простатите (АП), нейрогенный мочевой пузырь, инфекционно-аллергические и обменные нарушения железы и т.д.). ХП рассматривают как «мультифакторный каскад» патологических превращений, которые инициируются тем или иным агентом и приводят к возникновению симптомов и боли [17].
В Украине простатит поражает около 19% мужского населения в возрасте от 20 до 60 лет [31]. Сам термин «хронический простатит» (ХП) может обозначать широкий спектр состояний предстательной железы (ПЖ) и нижних мочевых путей (инфекционный простатит, синдром хронической тазовой боли (СХТБ), простатодиния при абактериальном простатите (АП), нейрогенный мочевой пузырь, инфекционно-аллергические и обменные нарушения железы и т.д.). ХП рассматривают как «мультифакторный каскад» патологических превращений, которые инициируются тем или иным агентом и приводят к возникновению симптомов и боли [17].
Существует несколько классификаций данного заболевания. Одной из основных, принятых в Европе, является классификация К. Nickel [18]. В 1995 году Институтом национального здоровья США (NIH) была разработана современная классификация ХП. Согласно последней категории I (острый бактериальный простатит) и II (бактериальный ХП) соответствуют традиционному выделению острого и бактериального ХП. Выделение новых категорий, например СХТБ, воспалительного и невоспалительного простатита (категория III), бессимптомного воспалительного простатита (категория IV), направлено на решение проблем и устранение упущений традиционной классификации.
Лечение больных ХП I и II категории подробно описано в большинстве руководств по воспалительным заболеваниям мужских половых органов. Значительную сложность представляет собой выбор груп лекарственных препаратов для лечения больных хроническим АП (ХАП), относящимся, согласно классификации NIH, к IIIА и IIIВ категориям. Это объясняется неопределенностью понятия «хронический абактериальный простатит», неясностью этиологии и патогенеза данного заболевания. Прежде всего перечисленные группы лекарственных препаратов касаются простатита категории IIIВ (ХАП/СХТБ).
 Обычно даже для лечения ХАП многие авторы предлагают применять антибактериальные средства [17]. Это связано с недостаточностью изучения этиопатогенеза заболевания, влиянием инфекции на его развитие и противоречивостью принятой терминологии.
Обычно даже для лечения ХАП многие авторы предлагают применять антибактериальные средства [17]. Это связано с недостаточностью изучения этиопатогенеза заболевания, влиянием инфекции на его развитие и противоречивостью принятой терминологии.
К настоящему времени нет единой концепции лечения больных ХАП/СХТБ, поэтому в специализированной литературе предлагается многообразие различных лекарственных средств.
Медикаментозная терапия ХАП/СХТБ должна иметь этиопатогенетическую направленность, учитывать активность, категорию и степень распространенности процесса, быть комплексной и индивидуальной для каждого больного.
В настоящее же время лечение, как правило, подбирается эмпирически, посимптомно, что, с точки зрения доказательной медицины, недопустимо. Гарантировать полное излечение ХАП невозможно, поэтому целью лечения, особенно для пациентов категории IIIВ, является, как считает J.C. Nickel (1999), улучшение качества жизни.
По нашему мнению, антибактериальную терапию необходимо рекомендовать при наличии клинических, бактериологических или иммунологических признаков инфекции в ПЖ, и выбор антимикробного агента базируется на его активности против предполагаемого возбудителя, возможности достижения им очага инфекции в адекватной концентрации [2, 22]. Достаточно широко в лечении ХП используются α1-адреноблокаторы, поскольку их применение обеспечивает восстановление дисфункционального мочеиспускания [4].
Наиболее эффективным является этиопатогенетическое лечение α1-адреноблокаторами у больных СХТБ, воздействующих путем блокады постсинаптических нервных волокон.
Вопросы патогенеза ХАП
Для уточнения точек приложения α1-адреноблокаторов при СХТБ рассмотрим механизмы патогенеза ХАП.
1. Конгестивный механизм. Стойкие застойные явления в венах малого таза приводят к нарушению дренирования предстательных ацинусов и воспалению ПЖ. У больных регистрируются изменения микроциркуляции, гемокоагуляции и фибринолиза. Причинами конгестии являются половые нарушения и дизритмия половой жизни. К причинам простатовезикулита относят сексуальные повторные возбуждения без физиологического опорожнения ПЖ от секрета. Длительное половое воздержание, ведущее к задержке секрета в ПЖ, также способно стать причиной асептического воспаления.
2. Иммунные нарушения и аллергический статус. Возникновение ХАП может быть обусловлено иммунологическими процессами, ускоренными неизвестным антигеном или аутоиммунной реакцией [17]. Развитие воспалительного процесса в ПЖ вызывает изменения в системе микроциркуляции, в результате чего повышается сосудистая проницаемость, обусловливающая возможность выхода белков сыворотки крови в окружающие ткани и даже в секрет ПЖ. В зависимости от состояния ее гистогематологических барьеров при различных формах ХП в секрете могут появляться в большем или меньшем количестве белковые фракции сыворотки крови с различной молекулярной массой, что позволяет косвенно судить о транскапиллярном обмене и состоянии мембранных структур органа.
При длительном течении заболевания может возникнуть сенсибилизация организма тканями ПЖ, влекущая за собой аллергизацию организма как местного, так и общего характера.
Второй механизм, предусматривающий возникновение воспалительных реакций замедленного типа к живым возбудителям – микроорганизмам и их токсинам, связан с непосредственным воздействием агента и продуктов распада на ткани органа. В дальнейшем воспалительный процесс в ПЖ поддерживается за счет аутоиммунных механизмов. При рецидивирующем простатите образуются комплексы антиген-антитело, которые оседают на базальных мембранах, в результате чего патологический процесс прогрессирует.
В последнее время все больше внимания уделяется роли цитокинов в развитии и поддержании ХП. Сообщается об обнаружении в секрете простаты повышенного по сравнению с контролем уровня интерферона, интерлейкинов‑2, -6, -8 и ряда других цитокинов. A. Doble и соавт. (1999) установили, что при ХАП категории IIIB наблюдается увеличение соотношения CD8 (цитотоксических) к CD4 (хелперов) типов Т-лимфоцитов, а также уровня цитокинов [9].
3. Нарушения барьерной функции предстательной железы. ПЖ выполняет барьерную функцию, а ее секрет обладает антимикробным действием, препятствующим проникновению инфекции в верхние отделы мочеполового тракта. Барьерная функция ПЖ ассоциируется с содержанием в ней цинка (Zn), который оказывает in vitro антибактериальный эффект на грампозитивные и грамнегативные бактерии. Известно, что ПЖ наиболее богата Zn, потому как накапливает его в своих тканях. Антибактериальная активность ПЖ связана с наличием в ней свободного Zn. При бактериальном простатите уровень Zn снижается и не изменяется даже после перорального приема препаратов Zn. Напротив, при АП уровень Zn восстанавливается при его пероральном приеме [21].
Другими факторами, обеспечивающими барьерную функцию органа, являются факторы клеточного иммунитета (макрофаги и др.), иммуноглобулины IgA, IgG, IgM, которые вырабатываются в железе или проникают через простатический барьер в семенную жидкость, лизоцим, спермин. В норме рН секрета составляет 6,6. При воспалении показатель рН увеличивается до 7-8. На фоне ХП отмечается достоверное снижение уровня лимонной кислоты.
В случае развития воспалительного процесса ПЖ утрачивает свою защитную функцию, превращается в постоянно или длительно действующий очаг инфекции.
4. Нейровегетативные расстройства моторной функции ПЖ и нижних мочевых путей. Некоторые формы ХП связаны с первоначальным нарушением функции симпатической нервной системы и гиперактивностью α1-адренорецепторов. Описан интрапростатический протоковый рефлюкс, вызванный турбулентным мочеиспусканием с высоким внутриуретральным давлением [8]. Рефлюкс мочи в протоки долек ПЖ способен стимулировать стерильную воспалительную реакцию.
5. Нейрогенные нарушения функции мышц тазового дна. Существует также нейромышечная теория патогенеза ХАП. Изучение симптомов и неврологическое обследование могут указывать на наличие симпатической рефлекторной дистрофии мышц промежности и тазового дна. Различные повреждения на уровне регуляторных центров спинного мозга способны приводить к изменению мышечного тонуса, чаще по гиперспастическому типу, при которых нарушения уродинамики (спазм шейки мочевого пузыря, псевдодиссинергия) сопутствуют или являются следствием этих состояний.
6. Нарушение психосоматического статуса. Клиническую картину заболевания у пациентов с ХАП довольно часто сопровождает депрессия. Ее могут вызывать постоянный, плохо поддающийся лечению болевой синдром, половые расстройства и др.
Клинические проявления СХТБ
Клинически боль и ощущение дискомфорта в промежности считаются самыми распространенными симптомами СХТБ. Второе и третье места занимают надлобковая боль и дискомфорт и боль и дискомфорт при эякуляции соответственно. Среди симптомов, связанных с мочеиспусканием, самым распространенным симптомом является мучительная повышенная частота мочеиспускания, затем затрудненное мочеиспускание и императивный позыв к мочеиспусканию. По средней частоте проявления симптомов на первом месте – частота мочеиспускания, за ней идут боль и/или дискомфорт в промежности, боль и/или дискомфорт в надлобковой области и затрудненное мочеиспускание.
Впервые α1-адреноблокаторы были применены в конце ХХ века. В литературе можно найти сведения, что α1-адреноблокаторы, мышечные релаксанты и физиотерапия снижают степень проявления симптомов у больных ХАП/СХТБ [17, 18]. D.E. Osborn и соавт. (1981) одними из первых применили с положительным эффектом при простатодинии неселективный препарат феноксибензамин в ходе плацебо-контролируемого исследования. Улучшение оттока мочи при блокаде α1-адренорецепторов шейки мочевого пузыря и ПЖ приводят к ослаблению симптомов простатодинии [4, 6]. Согласно результатам небольших исследований α1-адреноблокаторов клинический прогресс наблюдается в 48-80% случаев [4, 6]. Большинство авторов сообщают, что трехмесячного курса приема αl-адреноблокаторов недостаточно для получения стойкого и выраженного снижения симптомов патологии ПЖ [1, 7, 16, 19].
Данные специализированной литературы указывают на то, что при СХТБ применяется несколько α1-адреноблокаторов.
А.В. Сивков (2002) приводит данные, что монотерапия теразозином у наблюдавшихся мужчин с ХАП/СХТБ способствует симптоматическому улучшению у большинства из них (96%), в том числе к уменьшению дизурии у 82% пациентов, частоты мочеиспусканий – у 96% и боли – у 93% больных. α1-адреноблокаторы способствовали уменьшению частоты дизурии на 40-65% и боли в промежности на 25-35% по сравнению с исходным уровнем.
Изучение выраженности симптомов с использованием линейных шкал продемонстрировало суммарное уменьшение дизурии на 35% от исходного уровня, в то время как снижение интенсивности боли составило 85%. Столь высокий уровень ответа на лечение указывает на тесную связь боли при ХП с расстройствами уродинамики, а не только с изменениями воспалительного характера. В результате монотерапии теразозином было достигнуто более чем двухкратное уменьшение (66%) показателя качества жизни по шкале NIH-CPSI. Указанные данные позволяют иначе взглянуть на подходы к диагностике и лечению ХП категории IIIВ [30].
В одном из проспективных рандомизированных плацебо-контролируемых исследований применялся препарат альфузозин. Исследование продолжалось 12 мес и включало 6 мес активного лечения и еще столько же времени наблюдения [15]. Через 6 мес у пациентов, принимавших альфузозин, было зарегистрировано более выраженное снижение симптомов по шкале NIH-CPSI, достигшее статистической значимости, по сравнению с группами плацебо и контроля: 9,9; 3,8 и 4,3 балла соответственно (р=0,01). Внутри этой шкалы только симптомы, характеризующие боль, уменьшились достоверно, в отличие от других, связанных с мочеиспусканием и качеством жизни.
В группе альфузозина у 65% пациентов наблюдалось улучшение по шкале NIH-CPSI более чем на 33% по сравнению с 24 и 32% в группах плацебо и контроля (р=0,02). Через 6 мес после отмены препарата симптомы стали постепенно нарастать как в группе альфузозина, так и плацебо [15].
Применение селективного α1-адреноблокатора тамсулозина при ХАП/СХТБ также демонстрирует хороший клинический эффект. В.В. Дьяков и А.В. Говоров (2002) приводят данные собственного исследования по изучению длительного применения тамсулозина у больных ХП. Так, 39 пациентов в возрасте от 31 до 62 лет и продолжительностью заболевания 1,5-10 лет принимали тамсулозин в течение 12 мес.
Положительный эффект был достигнут у 71,8% пациентов. Через год терапии снижение по шкале IPSS составило 5,3 балла (52%), а снижение показателя QoL – 3,1 пункта (79%). Количество побочных эффектов было сравнимо в группах тамсулозина и плацебо [24].
В целом складывается впечатление, что у больных СХТБ клиническая эффективность всех α1-адреноблокаторов практически одинакова, а различаются они только профилем своей безопасности. В то же время, как свидетельствуют наши наблюдения, несмотря на то что применение α1-адреноблокатора не позволяет полностью избежать рецидива заболевания после отмены препарата, на фоне его терапии существенно снижается выраженность симптомов и увеличивается время до возникновения рецидива [30].
В клинической практике используется несколько препаратов группы α1-адреноблокаторов. Для лечения ХАП/СХТБ они имеют приблизительно равную ценность. Однако практическому врачу необходимо обратить внимание на то, что доксазозин требует жесткого контроля исходного артериального давления крови, даже у больных гипертонической болезнью. Этот препарат имеет так называемый «эффект первой дозы», другими словами, у нормотензивных пациентов снижает артериальное давление значительно сильнее теразозина. Теразозин также способствует снижению артериального давления, хотя и в меньшей степени, учитывая его более высокую селективность.
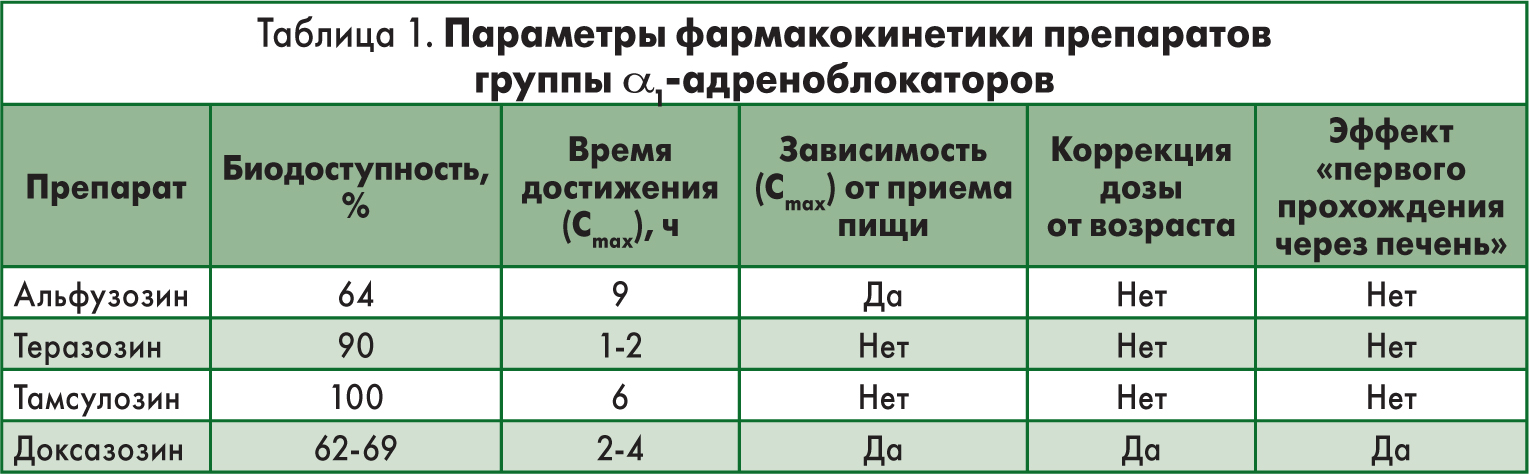
В таблице 1 приведены параметры фармакокинетики препаратов группы α1-адреноблокаторов.
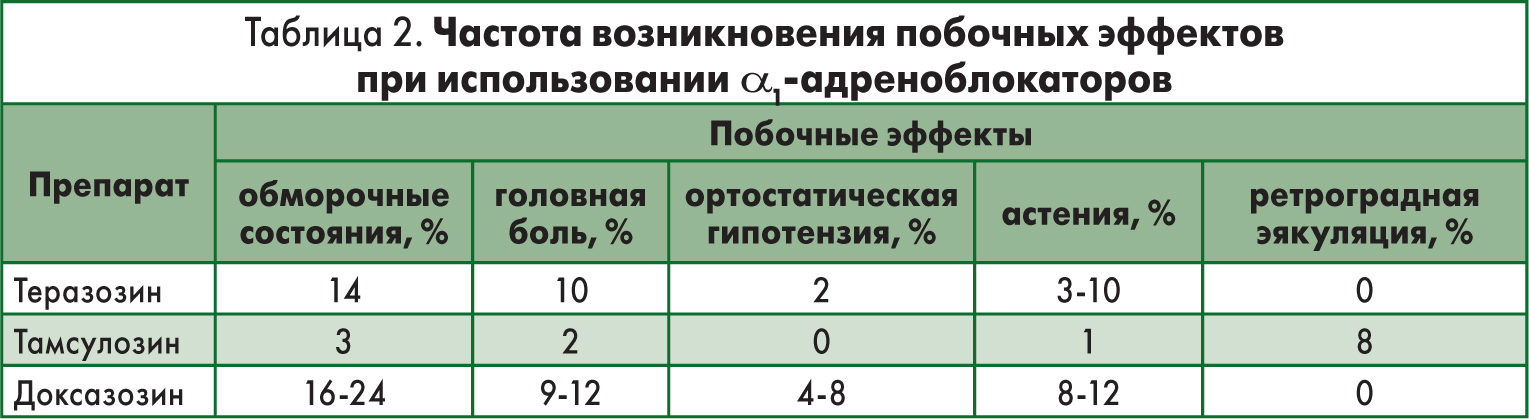
В таблице 2 приведена частота возникновения побочных эффектов α1-адреноблокаторов, в частности, теразозина, тамсулозина, доксазозина [3, 11, 13, 14, 20, 26].
Тамсулозин является наиболее простатоселективным α1-адреноблокатором в медикаментозном лечении ХАП. Его эффективность при почти отсутствии побочных явлений, отсутствии необходимости в титровании дозы и отсутствии влияния на артериальное давление могут быть отнесены к терапевтической дозе 0,4 мг при соотносительной клинической эффективности [29]. Тамсулозин является препаратом первого выбора для купирования острой задержки мочи любой этиологии [12, 13].
Кроме α1-адреноблокаторов, в лечении ХАП используются миорелаксанты и спазмолитики [19], нестероидные противовоспалительные средства и аналгетики [17], растительные экстракты [30], ингибиторы 5α-редуктазы, антихолинергические средства, препараты для иммунотерапии [17, 18], биорегуляторные пептиды, витамины и микроэлементы [21], препараты энзимотерапии.
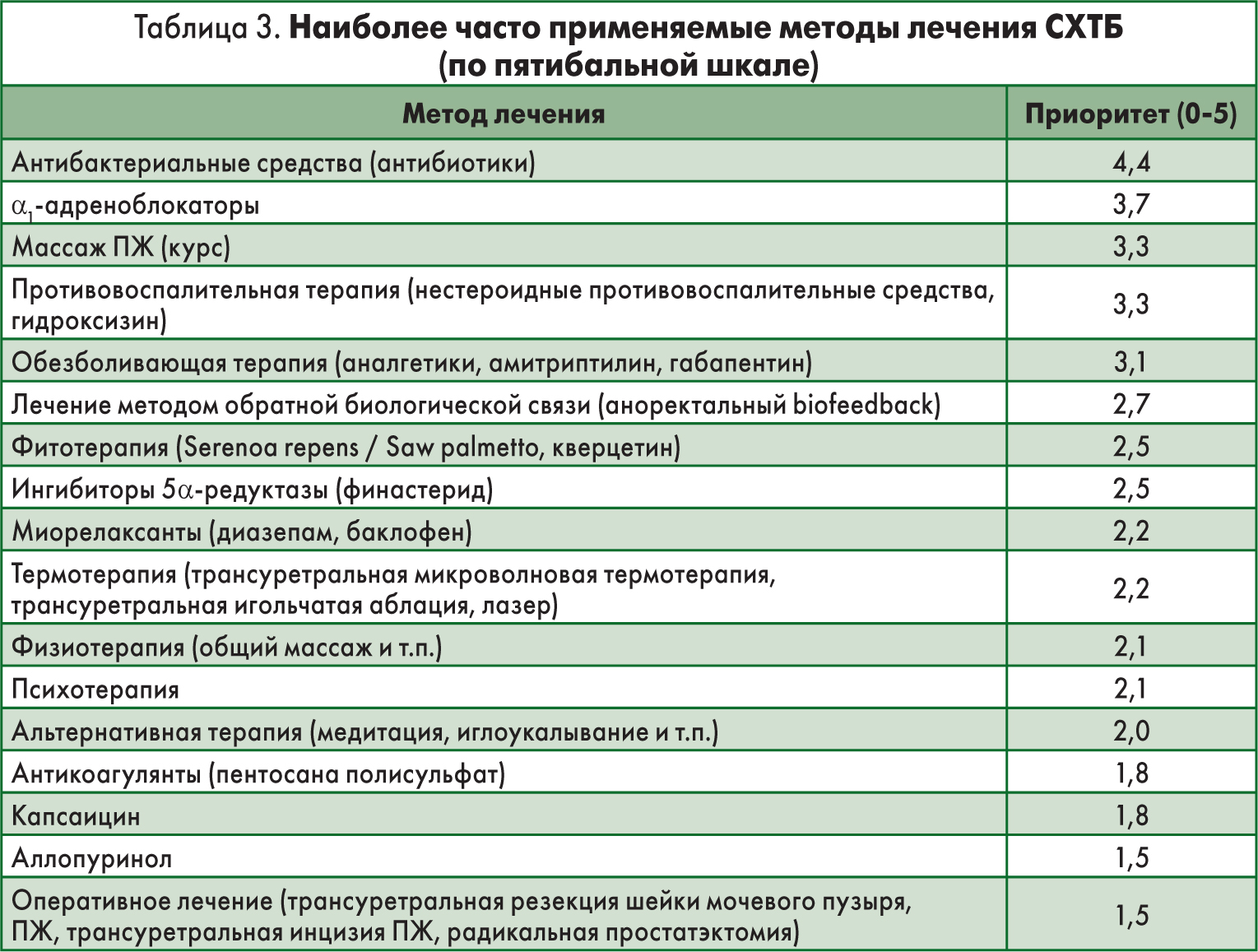
Сегодня в странах с развитыми системами здравоохранения рекомендации по диагностике и лечению заболеваний составляются с учетом принципов доказательной медицины. В таблице 3 по приоритету и в соответствии с критериями доказательной медицины представлены наиболее часто применяемые методы лечения АП (согласно рекомендациям NIH).
Таким образом, для лечения ХАП/СХТБ рекомендовано большое число разных препаратов и групп препаратов, применение которых основывается на изучении их влияния на различные звенья патогенеза заболевания.
Материалы и методы
В отделении сексопатологии и андрологии ГУ «Институт урологии НАМН Украины» в динамике было обследовано и пролечено 34 пациента в возрасте от 24 до 53 лет по поводу ХАП/СХТБ (продолжительность заболевания составляла от 2 до 8 лет). Для монотерапии был использован препарат ТАМСИН ФОРТЕ (тамсулозин), который относится к высокоселективным α1-адреноблокаторам длительного действия.
Всем больным было проведено стандартное урологическое обследование: пальцевое ректальное исследование до и после лечения, измерение гемодинамических показателей, ультрасонография (определение количества остаточной мочи в мочевом пузыре), урофлоуметрия в динамике, а также анкетирование больных по шкале ІPSS и определение качества жизни по шкале QoL. Параметры, приведенные выше, контролировались на протяжении исследования два раза: до начала приема препарата и через 3 мес лечения.
После осмотра врачом больные были включены в группу, получающую 1 раз в сутки перорально 0,4 мг ТАМСИНа ФОРТЕ в виде монотерапии. Эффективность препарата оценивалась на основании первичных критериев (уменьшение баллов по шкалам IPSS и QoL) и вторичных параметров (увеличение максимальной скорости потока мочи, уменьшение количества остаточной мочи, оценка безопасности и переносимости препарата при каждом посещении). При последнем визите регистрировалась субъективная оценка пациентами и лечащими врачами эффективности и переносимости препарата.
По результатам проведенного комплексного обследования у всех 34 пациентов был диагностирован ХАП, сопровождавшийся СХТБ. Наряду с жалобами на дизурию и выраженный болевой синдром (n=34; 100% больных) у 10 (29,4%) пациентов диагностировано снижение адекватных эрекций, у 7 (20,6%) – относительное ускорение эякуляции. При ректальной пальпации ПЖ болезненность отмечалась у всех 34 (100%) пациентов, у 14 (41,1%) больных пальпировались расширенные и болезненные семенные пузырьки.
Исследование секрета ПЖ не выявило развития воспалительной лейкоцитарной реакции. Также при бактериологическом обследовании патологической микрофлоры виявлено не было, то есть у больных диагностирован ХАП.
Ультразвуковое исследование (УЗИ) позволило объективно определить размеры ПЖ; у 6 (17,6%) пациентов были диагностированы патологические включения – камни ПЖ, что можно рассматривать в качестве осложнения ХП и одной из причин развития дизурии и алгического синдрома.
Результаты и их обсуждение
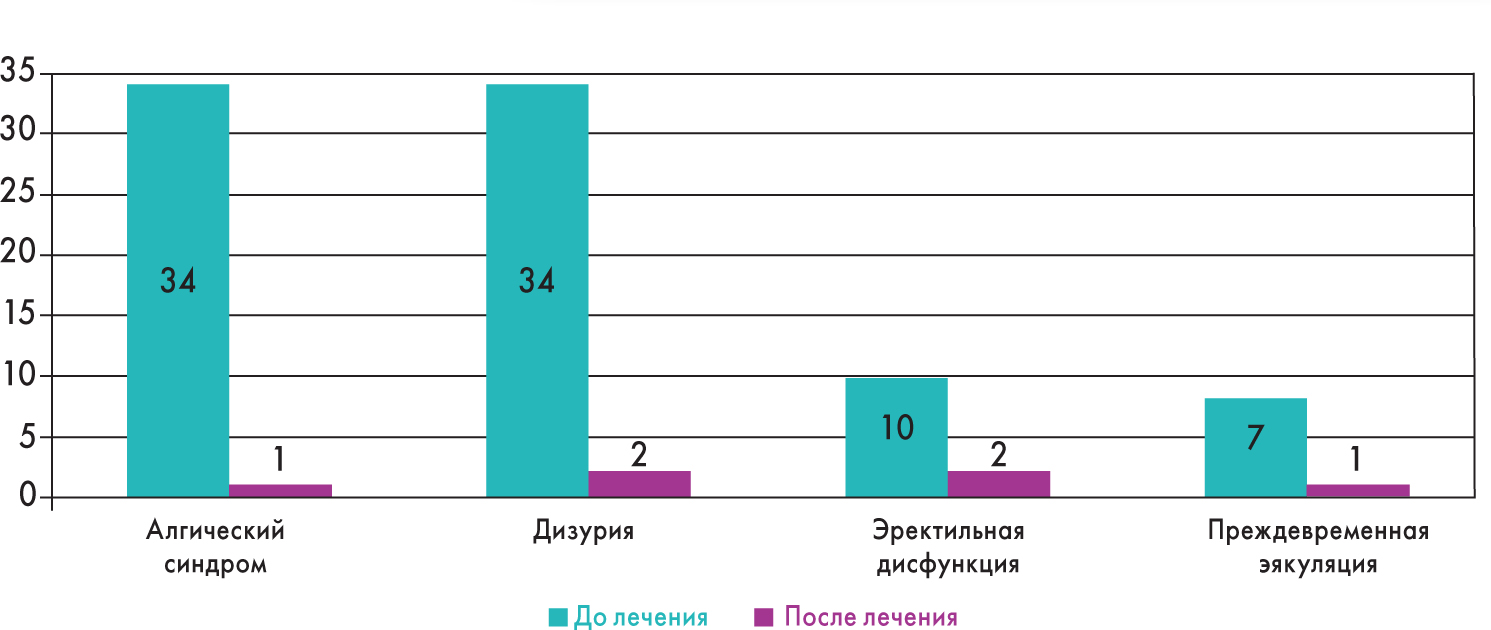
В результате лечения состояние больных довольно быстро улучшилось. Применение монотерапии тамсулозином (ТАМСИН ФОРТЕ) обеспечило быстрый клинический эффект (рис.). Болевые ощущения были ликвидированы по окончании трехмесячного курса лечения у 33 (97,1%) из 34 обследованных, дизурические явления купированы у 32 (94,1%) из 34 больных. У 8 (80,0%) из 10 участников улучшилась эректильная функция, преждевременная эякуляция купирована у 6 из 7 пациентов (85,7%).
Рис. Динамика клинических проявлений при лечении препаратом ТАМСИН ФОРТЕ
УЗИ проводилось с целью определения продольного и поперечного размеров ПЖ, ее консистенции, обнаружения конкрементов.
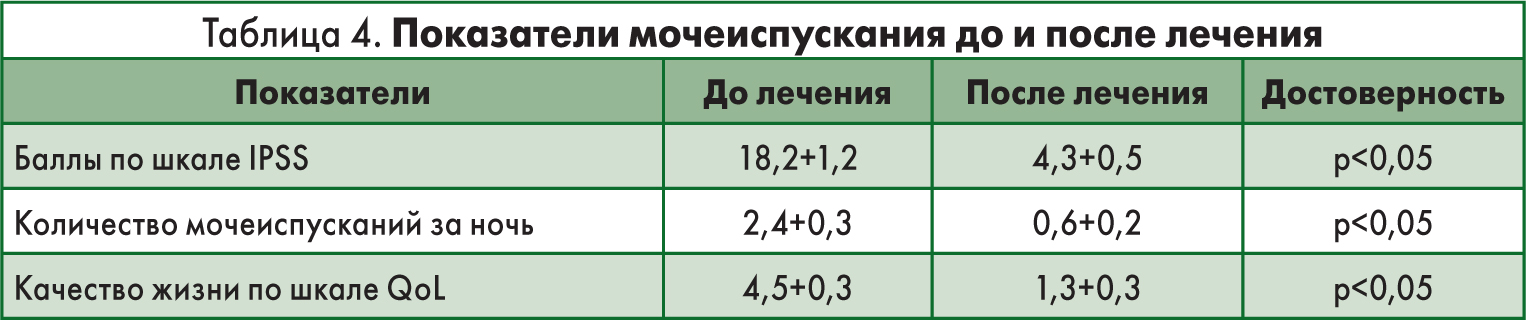
Достоверных различий продольного и поперечного размеров ПЖ до и после лечения выявлено не было. Вероятно, для получения более выраженных положительных изменений необходим продолжительный прием исследуемого препарата. В таблице 4 приведены показатели, характеризующие мочеиспускание. Данные показывают достоверное их улучшение.
Наряду с субъективной оценкой больными эффективности препарата теразозин было проведено объективное измерение ряда показателей до и после терапии.
После лечения препаратом ТАМСИН ФОРТЕ достоверно увеличилась максимальная скорость мочеиспускания.
На фоне терапии препаратом ТАМСИН ФОРТЕ у 2 (5,9%) больных были отмечены побочные эффекты в виде нарушения эякуляции. Однако ни один из них не прекратил лечение.
Препарат ТАМСИН ФОРТЕ достаточно эффективен при использовании в виде монотерапии у больных ХАП, сопровождающимся СХТБ, как по оценке врача (91,2%), так и по оценке пациентов (94,2%).
Таким образом, из материалов исследования можно сделать вывод, что препарат ТАМСИН ФОРТЕ достаточно эффективен при использовании в виде монотерапии ХАП/СХТБ как по оценке врача (91,2%), так и по оценке пациентов (94,2%). Препарат хорошо переносится больными, а побочные эффекты отмечались всего лишь у 5,9% пациентов. Препарат ТАМСИН ФОРТЕ может быть рекомендован для лечения больных ХАП/СХТБ.
Продолжение следует.