7 червня, 2016
Прошлое и будущее в мониторинге и лечении хронической миелоидной лейкемии
 Для лечения хронической миелоидной лейкемии (ХМЛ) сегодня существует широкий спектр лекарственных средств. Правильное применение имеющихся терапевтических возможностей важно для получения хороших клинических результатов. Перспективой развития данной терапии является отмена лечения при достижении стойкой и длительной молекулярной и клинической ремиссии.
Для лечения хронической миелоидной лейкемии (ХМЛ) сегодня существует широкий спектр лекарственных средств. Правильное применение имеющихся терапевтических возможностей важно для получения хороших клинических результатов. Перспективой развития данной терапии является отмена лечения при достижении стойкой и длительной молекулярной и клинической ремиссии.
Основа успешной терапии – эффективная интеграция клинического и лабораторного мониторинга больных ХМЛ. Определение уровня молекулярного ответа во время лечения через установленные временные промежутки служит важным критерием для оптимального ведения больных, а скрининг мутации домена BCR‑ABL1 киназы – для пересмотра схемы лечения пациентов, которые не достигли оптимального молекулярного ответа при терапии ингибиторами тирозинкиназы (ИТК).
 Более глубокий молекулярный ответ (ниже 4,5 log) связан с улучшением долгосрочной выживаемости пациентов и рассматривается как путь к достижению клинико-молекулярной ремиссии и возможность прекращения специфического лечения. Для оценки результативности лечения ХМЛ используются автоматизированные аналитические системы, эволюция методов продолжается. В литературе последних лет активно обсуждаются аспекты улучшения существующих методов мониторинга ХМЛ, направленные на создание предпосылок для отмены терапии при клинико-молекулярной ремиссии у пациентов с ХМЛ. Технологии, применяемые для оценки молекулярного ответа, постоянно совершенствуются, позволяя определять меньшее число репликации BCR-ABL домена, что в свою очередь дает возможность установить молекулярный ответ ниже 4,5 log.
Более глубокий молекулярный ответ (ниже 4,5 log) связан с улучшением долгосрочной выживаемости пациентов и рассматривается как путь к достижению клинико-молекулярной ремиссии и возможность прекращения специфического лечения. Для оценки результативности лечения ХМЛ используются автоматизированные аналитические системы, эволюция методов продолжается. В литературе последних лет активно обсуждаются аспекты улучшения существующих методов мониторинга ХМЛ, направленные на создание предпосылок для отмены терапии при клинико-молекулярной ремиссии у пациентов с ХМЛ. Технологии, применяемые для оценки молекулярного ответа, постоянно совершенствуются, позволяя определять меньшее число репликации BCR-ABL домена, что в свою очередь дает возможность установить молекулярный ответ ниже 4,5 log.
Широкое применение ИТК (иматиниба, нилотиниба, дазатиниба и других препаратов) резко изменило исход для пациентов с ХМЛ. Пациенты с ХМЛ, получающие ИТК, имеют почти «нормальную» продолжительность жизни. В настоящий момент рассматриваются два важных вопроса: качество жизни при приеме специфического лечения и экономические последствия лечения пациентов на протяжении их жизни.
С увеличением продолжительности жизни пациентов с ХМЛ экономическая составляющая таргетной терапии возрастает с каждым годом, существенно влияя на систему здравоохранения.
В то же время отмена терапии при ХМЛ ведет к развитию резистентности, что сужает арсенал возможностей для пациента, т.е. снижает шансы больного на контроль заболевания и повышает риск прогрессии. В данном аспекте возникает естественный вопрос о целесообразности отмены терапии и возможных последствиях данного решения.
Такая стратегия активно изучается в настоящее время. Более 900 пациентов официально прекратили прием ИТК для оценки молекулярной эффективности в условиях клинических испытаний. Однако многие вопросы, касающиеся глубины молекулярной ремиссии, длительности лечения, прогнозирующих факторов, а также безопасности, по-прежнему остаются открытыми.
Основной вопрос при проведении данных исследований лежит в плоскости определения клинико-молекулярного ответа при ХМЛ, а также мониторинга эффективности лечения и длительности сохранения молекулярного ответа.
Поэтому методология мониторинга молекулярного ответа является важной составляющей проведения данных исследований. Кроме того, подбор кандидатов для отмены терапии требует тщательной оценки динамики сохранения молекулярного ответа перед вынесением решения об отмене терапии.
Для оценки молекулярного ответа определяется уровень транскриптов BCR-ABL1 посредством полимеразной цепной реакции в режиме реального времени (ПЦР-РВ). Рабочие протоколы исследований и используемое оборудование могут варьировать в зависимости от лаборатории.
 В 2005 г. была введена международная шкала (IS) для стандартизации измерений BCR-ABL1, полученных в разных лабораториях, и создания преемственности в отчетах о результатах исследований. Использование шкалы IS позволяет стандартизировать значения BCR-ABL1, полученные с применением разнообразных аналитических систем, что значительно повышает точность определения молекулярного ответа. Также обеспечивается возможность проведения межлабораторных исследований. По шкале IS стандартизированный базовый уровень соответствует 100%; большой молекулярный ответ (MMR или MR3, где индекс указывает на порядок уменьшения) соответствует уровню BCR-ABL1 ≤0,1% (рис.).
В 2005 г. была введена международная шкала (IS) для стандартизации измерений BCR-ABL1, полученных в разных лабораториях, и создания преемственности в отчетах о результатах исследований. Использование шкалы IS позволяет стандартизировать значения BCR-ABL1, полученные с применением разнообразных аналитических систем, что значительно повышает точность определения молекулярного ответа. Также обеспечивается возможность проведения межлабораторных исследований. По шкале IS стандартизированный базовый уровень соответствует 100%; большой молекулярный ответ (MMR или MR3, где индекс указывает на порядок уменьшения) соответствует уровню BCR-ABL1 ≤0,1% (рис.).
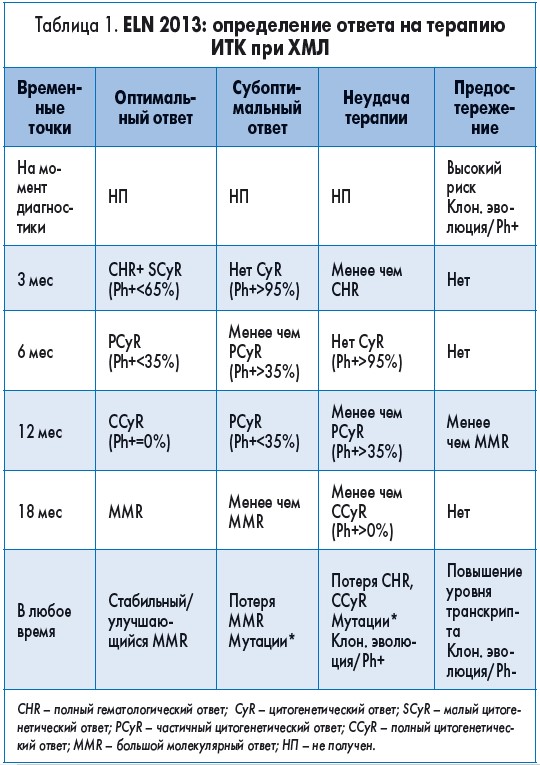
В соответствии с рекомендациями ELN от 2013 г. по лечению ХМЛ, достижение MMR, а также других ключевых уровней наличия транскриптов BCR-ABL1 (10 и 1%) в настоящее время используется для определения оптимального ответа, прогноза результатов терапии или неудачи лечения. При оценке эффективности терапии большое значение придается достижению молекулярного ответа. Самые последние рекомендации по ХМЛ (NCCN 2015, ELN 2013) предлагают продолжать лечение ИТК на неопределенное время у всех больных, ответивших на терапию (табл. 1).
Результаты не стандартизированной по IS лаборатории являются полезными для понимания динамики молекулярного ответа. Адаптация таких лабораторий к системе стандартизации IS требует либо экспериментального расчета (и периодического контроля) фактора преобразования путем обмена партий образцов между референтным центром и лабораторией, занимающейся мониторингом состояния пациента с ХМЛ (Muller et al., 2009; Balasubramanian et al., 2012; Yoshida et al., 2012), либо, возможно, использования одного из коммерческих наборов, содержащих контрольные материалы, откалиброванные по международным стандартам (White et al., 2010, 2013, 2015).
Основные этапы молекулярного ответа, определяемые у пациентов, получающих терапию ИТК, базируются на сроках его достижения и выраженности.
Помимо MMR, недавно были определены два дополнительных этапа достижения MR: «ранний MR» и «глубокий MR».
Ранний MR определяет достижение уровня транскриптов BCR-ABL1 ≤10% через 3 мес и ≤1% через 6 мес от начала лечения.
Несколько независимых исследований (Hanfstein, 2012; Ohm, 2012; Jain, 2013; Huges, 2014; Jabbour, 2014; Brummendorf, 2015) согласованно показали, что уровень молекулярного ответа 10% предсказывает скорость и глубину любого последующего ответа и коррелирует с клиническими результатами. Пациенты с уровнями транскриптов BCR-ABL1 ≤10% через 3 мес (и ≤1% через 6 мес) достоверно имели более высокую вероятность достижения полного цитогенетического ответа (CCyR) и MMR, а также более глубокого MR и показали достоверно лучшую выживаемость без прогрессии и общую выживаемость. Поэтому критерий раннего MR является важным аргументом при оценке ближайших и отдаленных результатов лечения.
Прогностическое значение BCR-ABL1 ≤10% через 3 мес справедливо для пациентов, получающих ИТК 2‑го поколения во 2‑й линии терапии после переключения с иматиниба (Brandford, 2012; Kim, 2013; Boquimpani, 2014; Shah, 2014). Данный факт подтвержден и для пациентов, получающих в 1‑й линии терапии ИТК 2‑го поколения (нилотиниб или дазатиниб) (Marin, 2012; Jain, 2013; Huges, 2014; Jabbour, 2014; Brummendorf, 2015).
Кроме понятия раннего MR существует определение оптимального молекулярного ответа. Рекомендации ELN от 2013 г. определяют достижение BCR-ABL1 ≤10% через 3 мес и ≤1% за 6 мес как «оптимальный ответ».
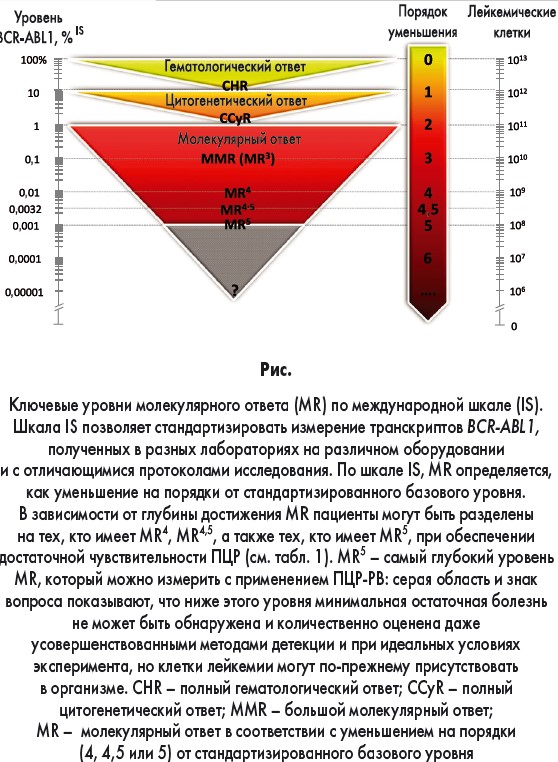 Глубокий MR соответствует MR4 или более (рис.). Под глубиной молекулярного ответа понимают степень снижения уровня транскриптов BCR-ABL1. Результаты оценки нижнего уровня MR зависят от уровня детекции тест-системы 4,5 log или 4 log.
Глубокий MR соответствует MR4 или более (рис.). Под глубиной молекулярного ответа понимают степень снижения уровня транскриптов BCR-ABL1. Результаты оценки нижнего уровня MR зависят от уровня детекции тест-системы 4,5 log или 4 log.
Глубокий MR достигается у значительной части пациентов, получавших иматиниб, и у еще большей части пациентов, получавших нилотиниб и дазатиниб в 1‑й линии терапии (Cortes, 2014; Hughes, 2014; Castagnetti, 2015; Gugliotta, 2015; Hjorth-Hansen, 2015; Kalmanti, 2015). Исследования последних лет, в ходе которых изучалась эффективность применения ИТК 2-го поколения в 1‑й линии терапии ХМЛ, показали достоверно более высокий потенциал в плане сроков и глубины достижения молекулярного ответа у больных ХМЛ.
Три независимых исследования продемонстрировали, что достижение самых глубоких уровней MR (подтвержденный MR4,5 и/или неопределяемый уровень транскрипта BCR-ABL1) связано со значительно лучшими долгосрочными результатами для пациентов с ХМЛ, получавших ИТК (Press, 2007; Etienne, 2014; Hehlmann, 2014). С другой стороны, исследование с участием большого количества пациентов с ХМЛ, получавших терапию иматинибом и ИТК 2‑го поколения, показало, что глубокий MR на протяжении 18 или 24 мес не являлся предиктором достижения ремиссии, при которой можно было бы рекомендовать отмену терапии (Falchi, 2013). Более того, достижение устойчивого MR4,5 не влияло на сокращение в будущем риска дальнейшей трансформации ХМЛ или смерти (Falchi et al., 2013). Исходя из этого, глубокий MR в настоящее время не включен в определение оптимального ответа на лечение в рекомендациях ELN от 2013 г.
Кроме того, преимущества с точки зрения долгосрочных результатов достижения MR5 против MR4,5 или MR4,5 против MR4 в настоящее время не доказаны. В перспективе долгосрочное наблюдение за большим количеством пациентов с глубоким молекулярным ответом позволит пролить свет на эти вопросы. Тем не менее в настоящее время точная оценка глубокого MR представляет несомненный интерес, поскольку глубокий MR считается «воротами» к достижению главной цели будущего лечения ХМЛ – свободной от лечения ремиссии (Mahon, Etienne, 2014).
Достижение свободной от лечения ремиссии становится приоритетной задачей терапии ХМЛ как с точки зрения пациентов, так и по причине фармакоэкономической целесообразности. Безопасное и полное прекращение терапии ИТК (с учетом возможности наступления беременности, предотвращения потенциальных поздних осложнений лечения) является важной задачей, особенно при лечении молодых пациентов с ХМЛ, которым желательно обеспечить высокую продолжительность и оптимальное качество жизни. Актуальность прекращения терапии при ХМЛ также высока, если речь идет о системе здравоохранения. Поэтому в настоящее время инициирован ряд исследований, которые позволят разработать критерии отмены терапии при ХМЛ. Некоторые из них уже имеют результаты, другие еще только в процессе набора данных (табл. 2).
В последние годы пилотные клинические исследования определили перспективы прекращения ИТК‑терапии у больных с длительным глубоким молекулярным ответом. В экспериментальных исследованиях была показана возможность прекращения назначения иматиниба пациентам с ХМЛ с полным молекулярным ответом (CMR) на протяжении не менее 2 лет. Имеются данные многочисленных исследований (Merante, 2005; Breccia, 2006; Okabe, 2007; Russelot, 2007; Verma, 2008; Guastafierro, 2009), а также клинического исследования STIM (STop IMatinib) о случаях прекращения терапии у пациентов, достигших стабильного MR (Mahon, 2010). Они впоследствии были дополнены новыми результатами (Takahashi, 2012; Ross, 2013; Thielen, 2013; Russelot, 2014). В качестве факторов, потенциально связанных с успешным прекращением терапии иматинибом, рассматривается скорость достижения молекулярного ответа. При более коротком периоде достижения BCR-ABL1-негативного статуса и значительной продолжительности глубокого MR рассматривается возможность прекращения терапии. В то же время, нет четких критериев для стратификации пациентов с целью выделения группы претендентов для отмены терапии. По этим причинам несколько текущих исследований рассматривают достижение MR4 (или глубже) в качестве первичного обязательного условия для включения в исследование.
Промежуточный анализ первых 200 пациентов, включенных в исследование European Stop Kinase Inhibitor (EURO-SKI), который был представлен в 2014 г. на заседании Американского общества гематологии, показал, что экономия средств для восьми стран – участниц данного проекта составила 7 млн евро только в первый год исследования (Mahon et al., 2014). Эффективность и безопасность стратегий отмены лечения ИТК и факторы прогнозирования для успешного прекращения терапии продолжают исследоваться в ряде клинических испытаний.
Кроме того, продолжительность сохранения ответа и глубина MR, а также другие факторы могут быть использованы для прогноза возможностей прерывания лечения ИТК. В исследовании STIM ретроспективно оценивали несколько потенциальных предикторов развития молекулярного рецидива. Вероятность сохранения стабильного CMR после прекращения терапии была выше в группе больных с низкими показателями по шкале Сокаля по сравнению с промежуточными или высокими группами риска. В исследовании TWISTER показано, что высокий риск по шкале Сокаля на момент постановки диагноза был самым сильным предиктором молекулярного рецидива при отмене терапии (Ross, 2012).
Представляет определенный интерес и тот факт, что показатели по шкале Сокаля иллюстрируют агрессивность заболевания на момент постановки диагноза и до сих пор имеют значение для прогноза исходов заболевания на фоне проводимого лечения. Другими известными модифицирующими факторами является возраст пациента и низкий показатель риска по шкале Сокаля (Ross, 2012; Takahashi, 2012).
Выявление других прогностических факторов требует глубокого статистического анализа большего контингента больных, что является дальнейшей целью исследований EURO-SKI и STIM2.
Исследование STIM2 стартовало во Франции в 2011 г. и в настоящее время продолжается. В это исследование были включены пациенты с ХМЛ, получающие терапию только иматинибом в качестве единственного агента, с теми же критериями включения, как в STIM1, т.е. поддержание CMR на протяжении по крайней мере 2 лет терапии. Критерии молекулярного рецидива также были идентичные. Предварительные результаты показали, что кумулятивная частота молекулярного рецидива в группе из 127 пациентов составила 46% (95% ДИ 38-56) в течение 24 мес наблюдения (Mahon, 2013).
Поскольку идентификация пациентов, которые могли бы получить наибольшую выгоду от прекращения терапии ИТК, остается ключевой задачей, важно определить оптимальную продолжительность молекулярного ответа, позволяющую прекратить лечение. Данный аргумент имеет решающее значение для инициирования новых исследований. Этот же аспект является одним из направлений организованного ELN исследования EURO-SKI, в котором участвуют более десяти стран. Критерии включения в исследование не такие строгие, как в исследованиях STIM: длительность терапии ИТК до включения ≥3 лет и отсутствие результатов ПЦР BCR-ABL >0,01% в течение последнего года, то есть устойчивый глубокий молекулярный ответ MR4 должен быть подтвержден. Нулевая гипотеза данного исследования заключается в том, что безрецидивная выживаемость в течение 6 мес будет ≤40%.
Предварительные результаты исследования EURO-SKI были представлены EHA в 2014 г. Среди первых 200 пациентов из 8 стран у 123 не было молекулярного рецидива на протяжении первых 6 мес наблюдения. Таким образом, безрецидивная выживаемость к 6 мес прекращения лечения составила 61,5% (95% ДИ [54,4%; 68,3%]), что доказывает несостоятельность нулевой гипотезы (р<0,0001) (Saussele, 2014).
Таким образом, ранний молекулярный ответ, глубина молекулярного ответа, а также сохранение глубокого молекулярного ответа в динамике (по крайней мере на протяжении ≥2 лет) являются важными критериями в разработке будущей стратегии отмены лечения ИТК у пациентов с ХМЛ. В то же время стратегия отмены лечения ИТК требует создания сертифицированного лабораторного контроля молекулярного ответа при терапии ХМЛ. Поэтому в настоящее время особую важность приобретает раннее назначение ИТК пациентам с ХМЛ, эффективный контроль и мониторинг результатов лечения, чтобы у пациентов был шанс на отмену специфической терапии в будущем.