22 березня, 2017
Торемифен – эффективная и безопасная альтернатива тамоксифену в адъювантной эндокринной терапии рака молочной железы
В отличие от тамоксифена, эффективность и побочные эффекты торемифена в адъювантной терапии рака молочной железы (РМЖ) не были изучены в полной мере. С целью более точной оценки эффективности и вероятности возникновения серьезных побочных эффектов торемифена в сравнении с тамоксифеном был проведен метаанализ, объединивший результаты четырех рандомизированных исследований. Было показано, что торемифен является убедительной и безопасной альтернативой тамоксифену в адъювантной эндокринной терапии.
В метаанализ были включены в общей сложности данные 1890 пациенток с РМЖ, получавших терапию торемифеном, и 1857 пациенток, принимавших тамоксифен. По сравнению с пациентками, принимающими тамоксифен, в группе торемифена не было статистически значимой разницы в общей выживаемости – ОВ (относительный риск – ОР – 1,07; 95% доверительный интервал – ДИ – 0,97-1,19; р=0,994) или выживаемости без болезни – ВББ (ОР 1,05; 95% ДИ 0,95-1,17; р=0,431). Показатели количества тромбоэмболических событий в группе торемифена, включающих тромбоз глубоких вен (ОР 0,68; 95% ДИ 0,40-1,17; р=0,926), нарушения мозгового кровообращения (ОР 0,59; 95% ДИ 0,32-1,09; р=0,438) и эмболию легочной артерии (ОР 0,91; 95% ДИ 0,42-2,01; р=0,618), незначительно отличались от таковых в группе тамоксифена. Количество осложнений в виде полипов и рака эндометрия в двух группах было почти одинаковым. Результаты данного метаанализа позволили авторам утверждать, что торемифен столь же эффективен в адъювантной терапии пери- и постменопаузального РМЖ, как тамоксифен, и имеет аналогичный профиль серьезных осложнений.
Тамоксифен, антиэстрогенный препарат, который используется в адъювантной эндокринной терапии РМЖ, может значительно улучшить показатели ВББ и ОВ (C.K. Osborne, 1998; EBCTCG, 2005). Торемифен, другой нестероидный селективный модулятор рецептора эстрогена, показал равноценные эстроген-рецептор-связывающий и противоопухолевый эффекты в доклинических исследованиях (S. Kallio et al., 1986). Торемифен оказывает эстрогенные или антиэстрогенные эффекты в зависимости от органа-мишени, дозы препарата и длительности лечения. Этот препарат в основном используется у больных с прогрессирующим РМЖ. По данным предшествующего метаанализа, торемифен и тамоксифен в равной степени эффективны и хорошо переносятся при лечении прогрессирующего РМЖ у женщин в постменопаузе. Однако эффективность торемифена в адъювантной эндокринной терапии не была достаточно изучена. До сих пор лишь немногие рандомизированные клинические исследования (K. Holli et al., 2000; O. Pagani et al., 2004; J.D. Lewis et al., 2010) сообщали об эффективности торемифена в адъювантной терапии по сравнению с тамоксифеном. В то же время тамоксифен способен вызывать серьезные побочные эффекты, такие как тромбоэмболические события, гинекологические осложнения и осложнения со стороны органов зрения, которые могут представлять угрозу жизни пациенток. Важно отметить, что торемифен, хлорированное производное тамоксифена, может иметь другую фармакокинетику и более благоприятный профиль переносимости (J.D. Lewis et al., 2010; P. Hirsimaki et al., 2002). Данные о побочных эффектах, представленные в предыдущих исследованиях, были противоречивыми. По результатам исследований Международной группы по изучению рака молочной железы (IBCSG), большее количество нарушений мозгового кровообращения и гинекологических осложнений были зарегистрированы у пациенток, получавших терапию торемифеном, но в двух других исследованиях продемонстрированы прямо противоположные результаты.
Данный метаанализ был проведен с целью более точного определения эффективности торемифена в качестве адъювантной терапии по сравнению с тамоксифеном. Более серьезные побочные эффекты от приема торемифена по сравнению с тамоксифеном также были оценены в данном исследовании. Установлено, что торемифен был эффективной и безопасной альтернативой тамоксифену в адъювантной гормонотерапии РМЖ.
В метаанализ были включены результаты четырех рандомизированных мультицентровых исследований, описанные в трех публикациях (K. Holli et al., 2000; O. Pagani et al., 2004; J.D. Lewis et al., 2010). Это исследования, проведенные Финской исследовательской группой по изучению РМЖ, Международной группой по изучению РМЖ, а также Североамериканское исследование сравнительной эффективности тамоксифена и торемифена (North American Fareston versus Tamoxifen Adjuvant – NAFTA) соответственно. Для оценки эффективности препаратов в метаанализ были включены 1890 случаев использования торемифена и 1857 случаев лечения тамоксифеном. Кроме того, были оценены побочные эффекты путем сопоставления 1864 случаев в группе торемифена и 1845 случаев в группе тамоксифена.
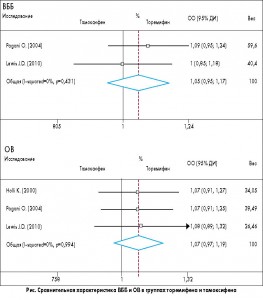
По сравнению с группой тамоксифена, у пациенток в группе торемифена не было существенной разницы в ОВ за период наблюдения (ОР 1,07; 95% ДИ 0,97-1,19; р=0,994 для гетерогенности) (рис.). Данные о ВББ были приведены только в двух исследованиях. По аналогии, показатели ВББ существенно не отличались в обеих группах (ОР 1,05; 95% ДИ 0,95-1,17; р=0,431 для гетерогенности) (рис.).
Торемифен и тамоксифен могут вызывать такие побочные явления, как потливость, приливы, слабость, а также тромбоэмболические и гинекологические осложнения. Тяжелые неблагоприятные осложнения, в том числе тромбоэмболии, полипы и рак эндометрия, оказывают серьезное влияние на качество жизни пациенток. Показатели уровня тромбоза глубоких вен в группе торемифена существенно не отличались от таковых в группе тамоксифена (ОР 0,68; 95% ДИ 0,40-1,17; р=0,926). Также не было значительных отличий между показателями возникновения острых нарушений мозгового кровообращения в группе торемифена по сравнению с группой тамоксифена (ОР 0,59; 95% ДИ 0,32-1,09; р=0,438 для гетерогенности). Кроме того, показатели эмболии легочной артерии в обеих группах не отличались (ОР 0,91; 95% ДИ 0,42-2,01; р=0,618 для гетерогенности). В целом у пациенток, получавших торемифен, не было зафиксировано существенной разницы в количестве тромбоэмболических событий по сравнению с группой тамоксифена (ОР 0,81; 95% ДИ 0,66-1,01; р=0,799 для гетерогенности). Показатели возникновения полипов эндометрия в двух группах были почти такими же (ОР 1,03; 95% ДИ 0,61-1,73; р=0,831 для гетерогенности). Кроме того, не было значительной разницы в заболеваемости раком эндометрия (ОР 0,99; 95% ДИ 0,36-2,73; р=0,297 для гетерогенности). Стоит отметить, что осложнения со стороны органов зрения были освещены только в исследовании NAFTA.
Проведенный метаанализ, который объединил результаты четырех рандомизированных исследований, позволяет дать более точную оценку эффективности и серьезных побочных эффектов торемифена в качестве адъювантной терапии по сравнению с тамоксифеном. Доказано, что пациентки в группе приема торемифена имели сходные показатели ОВ и ВББ с таковыми в группе приема тамоксифена. Кроме того, не было продемонстрировано значительной разницы в количестве тромбоэмболических событий у пациенток групп торемифена и тамоксифена. Гинекологические осложнения возникали почти в равной степени в обеих группах. Результаты исследования позволяют предположить, что торемифен является эффективной и безопасной альтернативой тамоксифену в адъювантной эндокринной терапии РМЖ у пациенток в пери- и постменопаузе. И торемифен и тамоксифен, связываясь с рецептором эстрогена, оказывают эстрогенные или антиэстрогенные эффекты (S. Kallio et al., 1986). Данные препараты достаточно эффективны в эндокринной терапии РМЖ, но в то же время имеют множество побочных эффектов (S. Pyrhonen et аl., 1999). Данный метаанализ показал, что торемифен является таким же эффективным антиэстрогенным препаратом, как и тамоксифен. Несмотря на то что существенных различий в выживаемости выявлено не было, в обеих группах зафиксированы различные показатели ОВ и ВББ. Необходимы дальнейшие широкие клинические испытания, чтобы подтвердить этот предварительный вывод.
Тамоксифен до настоящего времени используется в качестве адъювантной эндокринной терапии, особенно у пациенток в пременопаузе и пожилых пациенток с низким риском рецидива (J.D. Lewis et al., 2010). К сожалению, не у всех пациенток с гормон-рецептор-положительными опухолями отмечается позитивный эффект после терапии тамоксифеном. В некоторых исследованиях (M.P. Goetz et. al., 2007; M. Ingelman-Sundberg, 2005; R. Carpenter, 2008) сообщается, что полиморфизм гена CYP2D6 цитохрома Р450 оказывает влияние на метаболизм тамоксифена, что может ухудшить результаты. Хотя метаболизм торемифена не изучен в достаточной степени, торемифен может потенциально быть альтернативой тамоксифену в этой ситуации.
Тромбоэмболические и гинекологические осложнения серьезно влияют на качество жизни больных. Обнаружено, что частота тромбоэмболических осложнений у пациенток, получавших торемифен, не отличалась от таковой у пациенток, получавших тамоксифен. В соответствии с данными предыдущего метаанализа (S. Pyrhonen, 1999), частота тромбоэмболических событий была одинаковой в двух группах. Тем не менее по-прежнему является необходимым проведение больших клинических испытаний с фокусом на тромбоэмболических событиях, вызванных применением торемифена и тамоксифена. Два гинекологических осложнения, рассмотренных в метаанализе, возникали почти в равной степени в обеих группах. Предыдущие исследования (O. Pagani et al., 2004; J.D. Lewis et al., 2010; T. Saarto et al., 1996) показали, что серьезная окулотоксичность возникала очень редко в обеих группах. Более низкая генотоксичность (S. Shibutani et al., 2001) может быть потенциальным преимуществом для торемифена по сравнению с тамоксифеном (S. Shibutani et al., 2000). Следовательно, торемифен является достойной заменой тамоксифену. Некоторые исследования сообщают о более низком эстрогенно-антиэстрогенном соотношении у торемифена, чем у тамоксифена, что могло бы объяснить различия в количестве тромбоэмболических событий, вызванных двумя препаратами. В случае возникновения тяжелых побочных эффектов при использовании тамоксифена в качестве альтернативного варианта может быть рассмотрен торемифен. Однако проведение дальнейших клинических исследований с целью систематизации побочных эффектов этих двух препаратов является крайне необходимым.
С другой стороны, данный метаанализ имеет некоторые недочеты. Во-первых, доза торемифена 40 мг/сут, которую принимали пациентки в течение 3 лет в Финской исследовательской группе (K. Holli et al., 2000), отличалась от таковой в остальных трех рандомизированных исследованиях. Во-вторых, многие пациентки не завершили лечение или проверку исполнения в исследовании NAFTA. В-третьих, в то время когда было начато исследование NAFTA, химиотерапия не входила в стандарты лечения больных с гормон-рецептор-положительными опухолями молочной железы, и, следовательно, часть пациенток не получали лечения цитостатиками. В-четвертых, результаты исследования были основаны на нескорректированных статистических показателях, и более точная оценка может быть дана с учетом таких факторов, как возраст пациенток, индекс массы тела и менопаузальный статус.
Результаты представленного метаанализа подтверждают, что торемифен столь же эффективен, как и тамоксифен, в адъювантной терапии пациенток в пери- или в постменопаузе и характеризуется сходным уровнем побочных эффектов. Таким образом, торемифен представляет собой действенную и безопасную альтернативу тамоксифену в адъювантной эндокринной терапии РМЖ. Дальнейшие рандомизированные клинические исследования с большим размером выборки крайне необходимы для более точной оценки эффективности и побочных эффектов торемифена по сравнению с тамоксифеном.
Статья печатается в сокращении.
Zhou W.-B., Ding Q., Chen L., Liu X.-A., Wang S. Toremifene is an effective and safe alternative to tamoxifen in adjuvant endocrine therapy for breast cancer: results of four randomized trials. Breast Cancer Res Treat (2011), 128: 625-631.
Перевела с англ. Мария Стафейчук