2 липня, 2017
Сосудистые когнитивные нарушения и эндотелиальная дисфункция: современные подходы к терапии
По материалам XIX Международной конференции «Возрастная стратегия профилактики, терапии
и реабилитации в неврологии» (25-27 апреля, г. Трускавец)
 Мозговой инсульт и его последствия стабильно занимают лидирующие позиции в структуре причин смертности и инвалидности населения. Актуальным направлением является изучение ранних форм цереброваскулярных заболеваний, когда патологические процессы еще обратимы, а патогенетически обоснованные лечебно-профилактические мероприятия помогают надолго сохранить человеку активную жизнедеятельность и уменьшить риск мозговой катастрофы. Вопросам терапии дисциркуляторной энцефалопатии (ДЭ) и сосудистых когнитивных нарушений посвятила лекцию заведующая кафедрой неврологии № 1 Харьковского национального медицинского университета (ХНМУ), доктор медицинских наук, профессор Ирина Анатольевна Григорова.
Мозговой инсульт и его последствия стабильно занимают лидирующие позиции в структуре причин смертности и инвалидности населения. Актуальным направлением является изучение ранних форм цереброваскулярных заболеваний, когда патологические процессы еще обратимы, а патогенетически обоснованные лечебно-профилактические мероприятия помогают надолго сохранить человеку активную жизнедеятельность и уменьшить риск мозговой катастрофы. Вопросам терапии дисциркуляторной энцефалопатии (ДЭ) и сосудистых когнитивных нарушений посвятила лекцию заведующая кафедрой неврологии № 1 Харьковского национального медицинского университета (ХНМУ), доктор медицинских наук, профессор Ирина Анатольевна Григорова.
Хронические нарушения мозгового кровообращения традиционно объединяют термином «дисциркуляторная энцефалопатия», под которой подразумевается прогрессирующая недостаточность кровоснабжения головного мозга, приводящая к развитию множественных мелкоочаговых повреждений нервной ткани и нарушений неврологических и психических функций.
Особенности клинических проявлений ДЭ обусловлены мультифокальным характером поражения мозга. Симптоматика ДЭ формируется в результате нарушения связей между корой и подкорковыми структурами. Причина «разобщения» – диффузные изменения белого вещества головного мозга, коры, базальных ядер. При ДЭ в наибольшей степени страдают функция лобных долей и их связи с подкорковыми и стволовыми отделами. Это поясняет доминирующую роль когнитивных расстройств лобного типа и сложных нарушений двигательного контроля в клинической картине ДЭ.
Клинические изменения при ДЭ характеризуются стадийностью и без лечения имеют тенденцию к прогрессированию.
При ДЭ I стадии преобладают неврастенические нарушения, а явные неврологические нарушения, как правило, отсутствуют. Но тестирование с применением простых скрининговых инструментов, например мини-теста психического статуса (MMSE), выявляет легкие (26-27 баллов) или умеренные (24-25 баллов) когнитивные нарушения.
На II стадии ДЭ нарастает частота нарушений памяти. Результат MMSE ухудшается до 20-23 баллов, что соответствует деменции легкой степени выраженности. Отчетливой становится очаговая неврологическая симптоматика. Например, следствием поражения пирамидной, экстрапирамидной систем и мозжечка являются нарушения ходьбы и равновесия.
На III стадии ДЭ когнитивный дефицит приобретает тотальный характер и накладывает ограничения на жизнедеятельность больных. Тест MMSE выявляет умеренную (11-19) или тяжелую деменцию (>10 баллов). Наблюдается дальнейшее прогрессирование неврологических нарушений вплоть до утраты контроля тазовых органов.
Первыми шагами в диагностике ДЭ являются выделение основных синдромов – неврологических, когнитивных, эмоционально-аффективных и их подтверждение инструментальными и психометрическими методами.
На втором этапе диагностики проводится оценка сосудистых факторов риска. Они могут быть неустранимыми (возраст,
наследственность) и устранимыми или потенциально модифицируемыми (артериальная гипертензия, сахарный диабет, ожирение, курение, злоупотребление алкоголем).
По возможности следует стремиться к точной идентификации сосудистого процесса, вызывающего ДЭ (по данным допплерографии, нейровизуализации и ангиографии). Диагноз ДЭ и сосудистой деменции правомочен лишь в тех случаях, когда доказана временная причинно-следственная связь нарушений гемодинамики с развитием клинической, неврологической, нейропсихологической и психиатрической симптоматики, а также исключены другие (не сосудистые) причины наблюдаемых симптомов.
Соответственно в клинико-патогенетической картине выделяют следующие цели терапии ДЭ:
– снижение темпов прогрессирования цереброваскулярной недостаточности;
– устранение или уменьшение выраженности неврологических и психических проявлений;
– предупреждение развития транзиторной ишемической атаки, первого или повторного инсульта, инфаркта миокарда, заболеваний периферических артерий;
– предотвращение развития и прогрессирования деменции.
Сосудистая деменция – это не единое состояние, а несколько клинико-морфологических и клинико-патогенетических синдромов, общей для которых является взаимосвязь цереброваскулярной патологии с когнитивными нарушениями. Деменция патогенетически тесно связана с ключевыми факторами развития и прогрессирования сердечно-сосудистых заболеваний – дисфункцией эндотелия, артериальной гипертензией, атеросклерозом.
Эндотелий в настоящее время рассматривается не просто как эпителиальная выстилка сосудов, а как автономный сердечно-сосудистый и эндокринный орган. Его общий вес (1,5-2 кг) сопоставим с весом печени, а площадь достигает размеров футбольного поля. Эндотелий продуцирует более 30 важнейших медиаторов, которые участвуют в фибринолизе, регуляции тонуса сосудов, пролиферации, иммунного ответа.
Эндотелиальная дисфункция признана экспертными ассоциациями, включая Европейское общество кардиологов, ключевым звеном в развитии кардио- и цереброваскулярной патологии – атеросклероза, ишемической болезни сердца, острых и хронических нарушений мозгового кровообращения, облитерирующих заболеваний сосудов нижних конечностей.
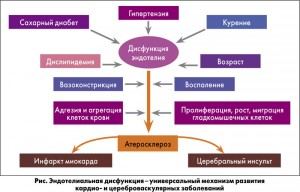
Под воздействием различных модифицируемых и немодифицируемых факторов способность эндотелиальных клеток синтезировать вазодилатирующие субстанции снижается, тогда как синтез сосудосуживающих факторов сохраняется или усиливается. При участии системной воспалительной реакции, усиленной пролиферации гладкомышечных клеток, адгезии и агрегации клеток крови эндотелиальная дисфункция становится прямым предшественником прогрессирования атеросклероза и связанной с ним сосудистой патологии (рис.).
Основным проявлением эндотелиальной дисфункции является нарушение биодоступности универсального вазодилататора оксида азота (NO) за счет дефицита субстрата для его синтеза – L-аргинина. На кафедре неврологии № 1 ХНМУ проведено новаторское исследование, направленное на поиск дополнительных маркеров дисфункции эндотелия сосудов у пациентов с ишемическим инсультом (ИИ). Для этого производился подсчет количества циркулирующих десквамированных эндотелиоцитов (ЦДЭ) венозной крови по методу J. Hladovеc (1978) с определением их морфологических характеристик (площади, максимального размера) у больных в раннем восстановительном периоде каротидного ИИ (Патент на корисну модель № 66974 від 25.01.2012 «Спосіб визначення циркулюючих ендотеліоцитів крові», О.О. Гелетка, І.А. Григорова, О.Ю. Степаненко). Выявлена взаимосвязь между количеством ЦДЭ, их морфологическими показателями и сосудистыми факторами риска у пациентов с ИИ. Так, была выделена группа из 19 больных, перенесших ИИ в возрасте от 30 до 42 лет, которые являлись заядлыми курильщиками. Показатель количества ЦДЭ у них составлял 19,6±5,2×105 в 1 л крови, а среднее значение площади фрагмента десквамированного эндотелиоцита – 38279±9521 условных единиц (пикселей). Это значительно отличается от показателей некурящих больных, перенесших ИИ, у которых количество ЦДЭ составило 9,4±2,62×105 в 1 л крови, а площадь десквамированного эндотелиоцита – 27353±9745 условных единиц. Таким образом, было выявлено, что кроме увеличения количества ЦДЭ в группе курящих пациентов достоверно выше степень их фрагментации за счет увеличения площади и максимального размера. Эти дополнительные маркеры эндотелиальной дисфункции у лиц, перенесших ИИ (в том числе молодого возраста), были более выражены у курильщиков, а также пациентов, которые нерегулярно принимали антигипертензивные препараты и статины.
Основой ведения пациентов с ДЭ являются адекватная терапия атеросклеротического заболевания сосудов и контроль модифицируемых факторов риска: назначение статинов, подбор эффективной антигипертензивной терапии, модификация образа жизни и питания с целью нормализации массы тела. Регулярные умеренные физические нагрузки, кроме того, благотворно влияют на функционирование сосудистого эндотелия.
Кроме того, для симптоматической терапии когнитивных нарушений у пациентов с ДЭ применяются препараты с нейропротективными и ноотропными свойствами:
– антагонисты NMDA-рецепторов (ме-мантин);
– модуляторы ГАМК-эргической нейротрансмиссии (гопантеновая кислота – ГПК);
– ингибиторы холинэстеразы (донепезил, ривастигмин);
– препараты с метаболическим механизмом действия (мельдоний);
– донаторы L-аргинина для синтеза эндотелиального NO;
– предшественники фосфолипидов нейрональных мембран (цитиколин) и др.
Для коррекции когнитивных расстройств, наблюдаемых при І и ІІ стадии ДЭ, мы рекомендуем применять препарат отечественного производства Когнум (кальция гопантенат). Фармакологические свойства ГПК обусловлены наличием в структуре молекулы гамма-аминомасляной кислоты (ГАМК) – основного тормозного медиатора центральной нервной системы. Посредством модуляции ГАМК-рецептор-канального комплекса ГПК повышает устойчивость нейронов к гипоксии и действию токсических веществ, способствует нормализации обменных процессов в стенке церебральных сосудов, проявляет антивазоспастическое и мембраностабилизирующее действия, стимулирует белок-синтетические процессы в нейронах.
Терапевтические эффекты ГПК:
– улучшает память, внимание;
– регулирует уровень бодрствования (умеренное седативное действие);
– регулирует тонус мышц, уменьшает моторную возбудимость;
– противосудорожное действие;
– противотревожное действие;
– улучшает эмоциональный фон;
– предотвращает побочные эффекты фенобарбитала, карбамазепина, нейролептиков.
Рекомендованные суточные дозы препарата Когнум у взрослых пациентов – 1500-3000 мг. Препарат можно применять
у детей с 3 лет, начиная с дозы 750 мг/сут, что свидетельствует о его безопасности. Курс лечения составляет от 1 до 4 мес, в отдельных случаях – до 6 мес. Через 3-6 мес возможно повторение курса лечения.
У пациентов с деменцией в схему лечения мы рекомендуем добавлять отечественный препарат мемантина гидрохлорида – Мембрал. Субстанция для его производства поставляется компанией Merz Pharma GmbH (Германия). Остановимся на действии мемантина.
Действие мемантина связано с улучшением межнейрональной передачи и предохранением нейронов от повреждения в условиях избыточного выброса глутамата. Мемантин является неконкурентным низкоаффинным антагонистом N-метил-D-аспартатных (NMDA) рецепторов с низкой селективностью по отношению к различным подтипам NMDA-рецепторов и быстрой кинетикой связывания с ними. Одним из основных лигандов NMDA-рецепторов является возбуждающий нейромедиатор глутамат. Модулирующий эффект мемантина в отношении NMDA-рецепторов сглаживает негативные последствия усиленной глутаматергической трансмиссии, которая наблюдается как при ишемии мозга (сосудистой деменции), так и в результате токсического действия β-амилоида (при деменции альцгеймеровского типа). Вторичные механизмы действия связаны с влиянием мемантина на серотониновые рецепторы подтипа 5-HT3, ацетилхолиновые, дофаминовые (D2) рецепторы, а также потенциал-зависимые каналы для ионов Na+. Посредством перечисленных механизмов мемантин снижает уровень окислительного стресса в нервной ткани, подавляет образование патологического β-амилоида и фосфорилирование тау-протеинов, уменьшает выраженность нейровоспаления, улучшает нейрогенез. Все перечисленные эффекты противостоят дисфункции нейрональных сетей, которая наблюдается при деменции, и, возможно, замедляют прогрессирование патологического процесса.
Мембрал применяется с постепенным повышением дозы на 5 мг/нед в течение первых 3 нед по следующей схеме:
1-я неделя (1-7-й день) – 5 мг/сут (0,5 таблетки);
2-я неделя (8-14-й день) – 10 мг/сут (1 таблетка);
3-я неделя (15-21-й день) – 15 мг/сут (1,5 таблетки);
начиная с 4-й недели – 20 мг/сут (2 таблетки). В дальнейшем рекомендованная поддерживающая доза составляет 20 мг/сут.
В клинической практике часто возникает вопрос о том, в каких ситуациях следует назначать комбинированную нейропротекторную терапию. Ответ на этот вопрос был получен, в частности, при проведении на базе нашей кафедры исследования с участием 120 больных с додементными когнитивными расстройствами и сосудистой деменцией. Все обследованные были разделены на две группы: І группа – больные с гипертензивной энцефалопатией ІІ стадии в возрасте 50-60 лет, ІІ группа – больные с гипертензивной энцефалопатией ІІ-ІІІ стадии в возрасте 65-80 лет. У пациентов І группы выявлялись додементные когнитивные нарушения, а у пациентов ІІ группы – деменция легкой и средней степени тяжести.
Больные были обследованы согласно украинскому протоколу. Психодиагностическое обследование проводилось с использованием Монреальской шкалы, применяемой для выявления когнитивных нарушений (шкала MoCA), степень выраженности психоэмоциональных расстройств и депрессии определялась при помощи шкал Спилберга-Ханина и Бека. У пациентов І группы отмечено снижение когнитивных функций на 3 балла по шкале MoCA (уменьшение концентрации внимания, ухудшение кратковременной и долговременной памяти, дезориентация, апрактические расстройства). У больных ІІ группы выявлено снижение когнитивных функций на 5 баллов по шкале МоСА. У данного контингента больных к аналогичным расстройствам, имеющимся у больных І группы, присоединялись эхолалия, обедненность речи, трудность в самообслуживании. У 50% пациентов І группы и у 80% пациентов ІІ группы выявлялись психоэмоциональные нарушения в виде тревоги и депрессивного синдрома. Нами отмечен положительный эффект при применении препарата Когнум у больных І группы. У больных ІІ группы частичный регресс когнитивных расстройств наблюдался при применении комбинации препаратов Когнум и Мембрал. Таким образом, у лиц среднего возраста с додементными сосудистыми расстройствами в ряде случаев достаточно назначения одного препарата – Когнум. У более пожилых пациентов и у лиц с деменцией, даже легкой и средней степени, целесообразно назначать препарат Когнум и ингибитор NMDA-рецепторов Мембрал. Это подтверждает мнение о целесообразности комбинированной терапии у лиц с когнитивными сосудистыми расстройствами, особенно в старших возрастных группах при деменции.
Таким образом, своевременный и адекватный выбор терапевтической тактики при ДЭ позволит предупредить прогрессирование цереброваскулярной недостаточности и обеспечит положительную динамику нарушений в интеллектуально-мнестической, эмоционально-мотивационной и двигательной сферах.
Подготовил Дмитрий Молчанов