21 жовтня, 2017
Таксаны в химиотерапии рака молочной железы

Таксаны (доцетаксел и паклитаксел), как и винкаалкалоиды, относятся к цитостатикам растительного происхождения. Эти препараты являются митотическими ядами и влияют на пролиферацию раковой клетки путем блокирования внутриклеточного белка тубулина.
Оба препарата были введены в клиническую онкологию в 90-х гг. прошлого столетия и прочно утвердились в протоколах лечения рака молочной железы (РМЖ). Вслед за оригинальными препаратами на рынке появились их многочисленные генерические формы, что создало известные проблемы в оценке результатов клинических исследований, а также породило вопрос, все ли таксаны одинаковы.
В настоящем обзоре проводится анализ эффективности, безопасности и экономической целесообразности использования двух препаратов из группы таксанов – доцетаксела и паклитаксела.
История открытия цитостатиков естественного происхождения
История появления таксанов связана с так называемой инициативой Гордона Зуброды, который в течение двух десятилетий руководил отделом терапии опухолей Национального института рака США. Он проявлял особый интерес к натуральным продуктам и создал широкую программу по сбору различных растений и проверке противоопухолевого эффекта, обеспечиваемого их применением. Одним из результатов этой программы стало открытие паклитаксела (1964). Вначале паклитаксел добывали из коры тихоокеанского тиса (Taxus brevifolia), для чего приходилось уничтожать целые леса из этого растения. В 1990-х гг. возник конфликт между экологами и медицинской промышленностью, и производство паклитаксела пришлось остановить. В целом от открытия противоопухолевого эффекта паклитаксела до его клинического применения прошло 24 года.
Почти одновременно с американскими исследованиями в лаборатории французской компании «Рон Пуленк» из биомассы игл европейского тиса Taxus baccata был получен алкалоид бакатин – основа для химического синтеза таксанового производного доцетаксела (препарат Таксотер).
Для производства таксанов сегодня используются современные биотехнологии.
Фармакологические открытия конца ХХ века повторили уже известные эмпирические наблюдения о токсичности ягод тисового дерева. Taxus baccata (от греч. Toxin – яд) считался деревом смерти во всех европейских странах. В Центральных Гималаях растение издавна используется в народной медицине для лечения женщин с РМЖ и раком яичника.
Химические различия и механизм действия
Молекулы доцетаксела и паклитаксела имеют разную структуру, и даже ранние исследования выявили значительные различия между этими препаратами. По механизму действия таксаны представляют собой митотические яды: они обратимо связываются с b-субъединицей тубулина, димеры которого образуют микротрубочки. По сравнению с паклитакселом, доцетаксел демонстрирует большую афинность к β-тубулин связывающему участку и другой механизм полимеризации микротрубочек (накапливает тубулин в микротрубочках, препятствуя их распаду). Доцетаксел также отличается высокой активностью на ключевых этапах клеточного цикла, воздействуя на клетки в трех фазах (S/G2/M), тогда как паклитаксел действует только в фазах G2 и M. Все эти эффекты сопровождаются более мощной индукцией фосфорилирования Bcl‑2 и апоптоза, и в результате приводят к более выраженной противоопухолевой активности в моделях in vitro и in vivo.
Исследователи предполагают, что более выраженный противоопухолевый эффект доцетаксела может быть связан с фармакокинетическими/фармакодинамическими характеристиками. На доклинических моделях показано, что доцетаксел активно поглощается опухолевыми клетками и скорость его выведения из клетки ниже, чем паклитаксела. В результате доцетаксел накапливается в клетке в более высокой концентрации.
Генерические формы доцетаксела
В ходе исследования, проведенного независимой лабораторией (Vial J. et al., 2008) и посвященного сравнению оригинального препарата Таксотер и 31 его генерической формы производства Азии, Африки, стран Ближнего Востока и Латинской Америки, было изучено содержание активного доцетаксела и его примесей в лекарственной форме. Использовали метод хроматографии.
Оказалось, что более 2/3 генерических препаратов имели недостаточное содержание доцетаксела, а 74% генериков – недопустимо высокое суммарное содержание примесей. Все генерические формы характеризовались температурной нестабильностью.
Результаты исследования показали, что генерические формы доцетаксела существенно отличаются от оригинала и могут оказаться непредсказуемыми по клиническому эффекту и осложнениям. В данном обзоре используется оригинальное название препарата – Таксотер.
Клинические исследования
По данным метаанализа, комбинации таксанов с антрациклинами значительно увеличивают общую эффективность лечения и время до прогрессирования у больных РМЖ по сравнению с антрациклинсодержащими схемами без таксанов, но не влияют на продолжительность жизни. В монорежиме таксаны не превосходят антрациклины по эффективности. И доцетаксел и паклитаксел были одобрены для применения у пациенток с метастатическим РМЖ.
В 2005 г. опубликованы первые результаты прямого сравнения эффективности доцетаксела и паклитаксела. В рандомизированном исследовании III фазы TAX 311 проведено прямое сравнение доцетаксела (n=225) в дозе 100 мг/м2 (инфузия в течение 1 ч каждые 3 недели) и паклитаксела (n=224) в дозе 175 мг/м2 (инфузия 3 ч каждые 3 недели) у пациенток с метастатическим РМЖ, ранее получавших терапию антрациклинами. В этом исследовании была доказана более высокая эффективность доцетаксела: медиана общей выживаемости (ОВ) пациенток с метастатическим РМЖ увеличивалась до 15,4 мес по сравнению с 12,7 мес на фоне терапии паклитакселом, то есть достигнуто достоверное увеличение ОВ на 2,7 мес. Выживаемость в течение 1 года также была выше на фоне применения доцетаксела.
Общая частота ответа в группе доцетаксела была 37%, в группе паклитаксела – 26% (p<0,05). В пользу доцетаксела также свидетельствовала продолжительность регрессии опухоли на фоне лечения, которая в каждой из групп достигла 7,5 и 4,6 мес (p<0,01) соответственно; период времени до прогрессирования составил 5,7 и 3,6 мес.
Количество и степень тяжести побочных эффектов и осложнений при использовании доцетаксела (Таксотер) и паклитаксела различались.
Фебрильная нейтропения при лечении препаратом Таксотер развивалась чаще, чем при лечении паклитакселом (15 и 2%), однако важно отметить, что больным не назначалось профилактическое применение антибиотиков и гранулоцитарного колониестимулирующего фактора (Г-КСФ). Несмотря на побочные явления, медиана числа циклов химиотерапии в группе доцетаксела превосходила паклитаксел (6 против 4), что свидетельствует о более раннем прекращении лечения в группе паклитаксела в связи с прогрессированием заболевания. Кроме того, при более высокой частоте нежелательных явлений в группе доцетаксела эта разница не сказывалась на измеряемых результатах оценки качества жизни больных. Многочисленные изменения в лечении, которые появились в течение 11 лет с момента рандомизации первых пациенток в исследовании Tax 311, возможно, уменьшили значимость достигнутого результата – в первую очередь относительно профиля побочных эффектов. Клиницисты с тех пор чаще вводили более низкие дозы доцетаксела, кроме того, был изменен режим применения паклитаксела: было показано, что еженедельный режим инфузии в течение 1 ч превосходит стандартную схему назначения паклитаксела (трехчасовая инфузия 1 раз в 3 недели) при местнораспространенном и метастатическом РМЖ. Новая схема позволила улучшить ответ, но отрицательно повлияла на стоимость лечения и качество жизни пациенток. Последним новшеством стало появление паклитаксела, связанного с наночастицами.
Непрямое сравнение эффективности паклитаксела (Slamon et al., 2001) и доцетаксела (Marty et al., 2005) в комбинации с таргетной терапией трастузумабом при HER2-позитивном РМЖ также показало преимущества доцетаксела. При сопоставлении результатов двух исследований II фазы было показано, что доцетаксел является предпочтительным для применения в комбинации с таргетной терапией.
В адъювантной терапии РМЖ с инвазией в лимфоузлы доцетаксел продемонстрировал превосходство над схемами на основе антрациклинов. В исследованиях BCIRG 001 и PACS01 адъювантная химиотерапия на основе доцетаксела у больных операбельным РМЖ с поражением регионарных лимфоузлов показала значительное преимущество в общей и беспрогрессивной выживаемости.
В ходе исследования BCIRG 001 выяснилось, что режим TAC (доцетаксел, доксорубицин, циклофосфамид) превосходит режим FAC (фторурацил, доксорубицин, циклофосфамид) при использовании в адъювантной терапии (6 курсов) у больных РМЖ с вовлечением лимфоузлов и наличием минимум одного фактора высокого риска рецидива. Первичной конечной точкой была длительная безрецидивная выживаемость. При медиане наблюдения 77 мес доля пациенток без рецидива была выше в группе TAC (n=539, 87,8%), чем в группе FAC (n=521, 81,8%), что свидетельствует о снижении риска прогрессирования на 32% при применении режима, содержащего доцетаксел. Немаловажно, что преимущество доцетаксела сохранялось независимо от статуса гормональных рецепторов, наличия менопаузы, количества факторов высокого риска. Токсичность, связанная с ТАС, уменьшалась при первичной профилактике с применением Г-КСФ.
В исследовании PACS01 в адъювантной терапии раннего РМЖ с вовлечением лимфоузлов сравнивались два режима: FEC (фторурацил, эпирубицин и циклофосфамид) 6 курсов, а также 3 курса FEC с последующими 3 курсами монотерапии доцетакселом (FEC-D). Медиана наблюдения составила 60 мес. Пятилетние показатели выживаемости до прогрессирования составили 73,2 и 78,4% на фоне FEC и FEC-D соответственно. Многовариантный анализ, скорректированный с учетом прогностических факторов, показал снижение относительного риска рецидива на 18% при применении режима FEC-D. Пятилетняя ОВ составила 86,7 и 90,7% при FEC и FEC-D соответственно, что говорит о снижении относительного риска смерти на 27%. Режим FEC-D также продемонстрировал преимущество с точки зрения нейтропении и побочных эффектов со стороны сердца.
C. Frias и соавт. провели исследование, посвященное изучению экономической эффективности терапии паклитакселом и доцетакселом при метастатическом РМЖ. Это исследование показало, что доцетаксел обеспечивает более высокую пользу для здоровья (QALY), чем препарат сравнения. Авторы исследования утверждают: несмотря на разницу в стоимости препаратов, если принимать во внимание необходимость еженедельного введения паклитаксела и другие обстоятельства лечения, терапия доцетакселом экономически более эффективна.
В течение более 10 лет активных исследований доцетаксел изучен и одобрен для применения по 8 показаниям, проведено 19 клинических испытаний, показывающих улучшение выживаемости пациенток при опухолях молочной железы разной степени распространенности в разных линиях терапии. Помимо РМЖ, эффективность доцетаксела продемонстрирована в отношении широкого спектра различных опухолей, в том числе при немелкоклеточном раке легкого, раке предстательной железы, желудка, яичника, опухолях головы и шеи.
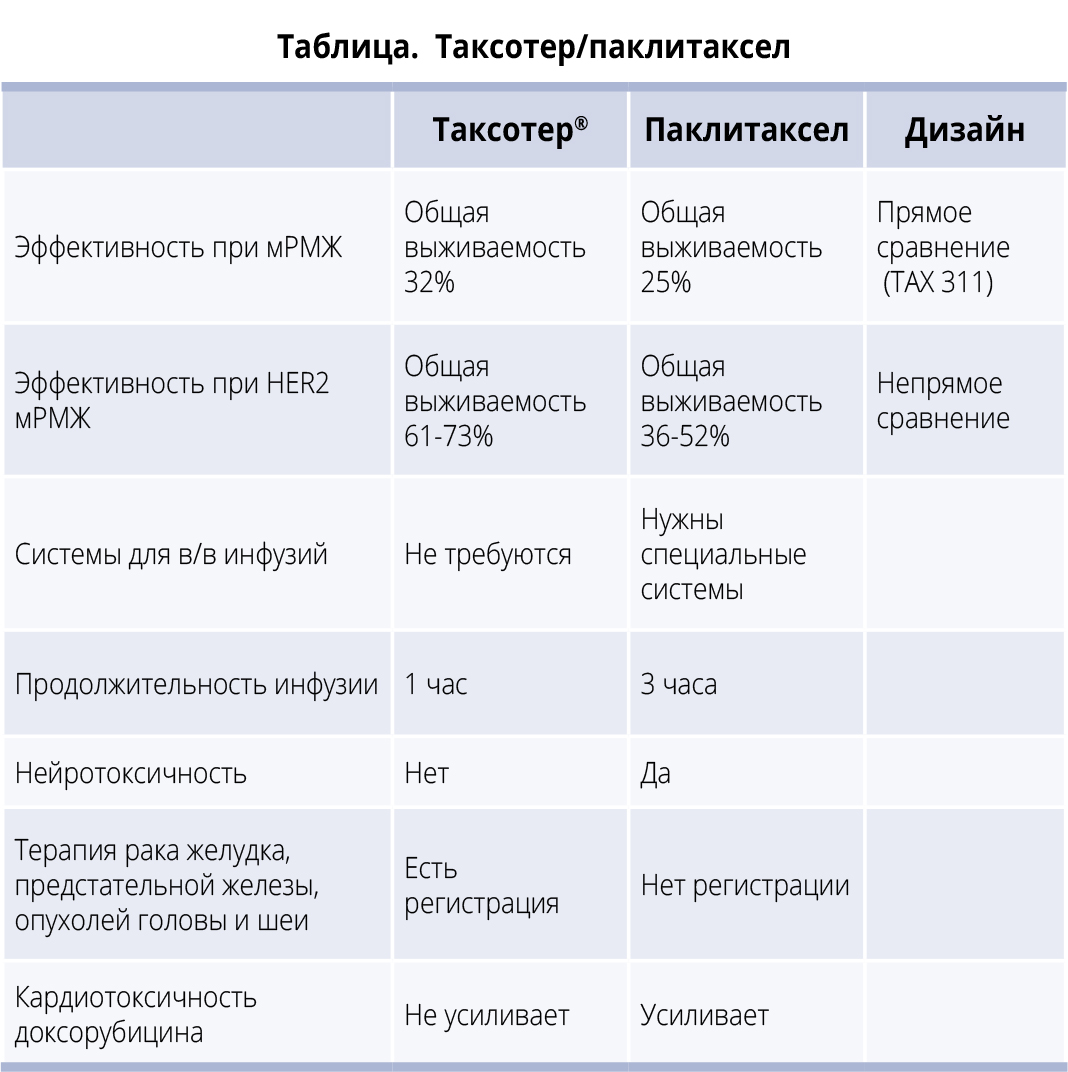
Сравнительные преимущества и недостатки каждого препарата (доцетаксел/паклитаксел) приведены в таблице.
Таким образом, доцетаксел (Таксотер) является эффективным средством терапии при различных анатомических локализациях опухоли и особенно при РМЖ. Таксотер входит в стандарты терапии метастатического РМЖ в адъювантном и неоадъювантном режимах как в комбинации с другими цитостатиками, так и при сочетании с анти-HER/2 агентами. Препарат не требует дополнительных систем для инфузии, не повышает кардиотоксичность доксорубицина и не проявляет кумулятивной нейротоксичности.
Повышение частоты нейтропений во время терапии препаратом Таксотер легко предотвращается профилактическим использованием колониестимулирующих факторов (ленограстим).
Экономическое преимущество препарата Таксотер перед паклитакселом проявляется в достижении его клинической эффективности не при еженедельном применении (паклитаксел), а при трехнедельном режиме терапии.
Литература
1. Vial J. et al. Pharmaceutical quality of docetaxel generics versus originator drug product: a comparative analysis. Curr Med Res Opin 2008; 24: 2019-33.
2. Jones S., Erban J., Overmoyer B. et al. Randomized phase III study of docetaxel compared with paclitaxel in metastatic breast cancer. J Clin Oncol; 23: 5542, 2005-5551.
3. Hudis С., More S. Testing chemotherapy for breast cancer: Timing is everything. Journal of Clinical Oncology 23, № 24 (August 2005); 5434-5436.
4. Slamon D., Leyland-Jones B., Shak S. et al. Use of chemotherapy plus a monoclonal antibody against HER2 for metastatic breast cancer that overexpresses HER2.
5. Marty M., Cognetti F., Maraninchi D. et al. Randomized phase II trial of the efficacy and safety of trastuzumab combined with docetaxel in patients with human epidermal growth factor receptor 2 – positive metastatic breast cancer administered as first-line treatment: The M77001 study group. Journal of Clinical Oncology 23, № 19 (July 2005); 4265-4274.
6. Sparano J.A., Wang M., Martino S. et al. Weekly paclitaxel in the adjuvant treatment of breast cancer. N Engl J Med, 2008.
7. Martin M., Segui M., Anton A. et al. Adjuvant docetaxel for high-risk, node-negative breast cancer. N Engl J Med, 2010 December 2; 363: 2200-2210.
8. Roche H., Fumoleau P., Spielmann M. et al. Sequential adjuvant epirubicin-based and docetaxel chemotherapy for node-positive breast cancer patients: The FNCLCC PACS01 trial. Journal of Clinical Oncology 24, № 36 (December 2006); 5664-5671.
9. Frias C., Cortes J., Segui M.A., Oyaguez I., Casado M.A. Cost-effectiveness analyses of docetaxel versus paclitaxel once weekly in patients with metastatic breast cancer in progression following anthracycline chemotherapy, in Spain. Clin Transl Oncol, 2010 Oct; 12(10): 692-700.
10. Brufsky A. Nab-Paclitaxel for the treatment of breast cancer: an update across treatment settings. Experimental Hematology & Oncology, 2017.
Спеціальний випуск тематичного номеру газети «Здоров’я України» «Онкологія, гематологія, хіміотерапія» 2017 р.