17 грудня, 2017
Елімінація вірусного гепатиту С: міжнародний досвід
Згідно з даними ВООЗ, вірусом гепатиту С (HCV), за різними оцінками, інфіковані 130-150 млн осіб. Щороку близько 700 тис. хворих помирають від хвороб, пов’язаних із хронічним гепатитом С (ХГС). Вакцини проти HCV поки що не існує, проте завдяки появі нових противірусних препаратів прямої дії (direct-acting antivirals – DAAs) елімінація ХГС стала можливою.
10 листопада компанії Gilead Sciences і Delta Medical організували телесимпозіум, присвячений сучасним досягненням у лікуванні ХГС, із прямою трансляцією в 5 містах України – Львові, Одесі, Вінниці, Харкові та Запоріжжі. У рамках заходу активно обговорювалися актуальні питання тактики ведення особливих популяцій пацієнтів із ХГС, рекомендації щодо застосування препаратів DAAs для лікування дитячої популяції, а також результати реалізації програми елімінації гепатиту С.
 Модератором заходу була завідувач кафедри інфекційних хвороб Національного медичного університету імені О.О. Богомольця, доктор медичних наук, професор Ольга Голубовська. Вона подякувала зарубіжним експертам за тісну співпрацю з українськими фахівцями та ознайомила присутніх із насиченою програмою телесимпозіуму. Формат заходу дозволив одночасно реалізувати кілька важливих завдань: перейняти досвід ведення пацієнтів із гепатитом С у зарубіжних колег, а також провести активну дискусію між спікерами та учасниками телесимпозіуму з різних регіонів нашої країни.
Модератором заходу була завідувач кафедри інфекційних хвороб Національного медичного університету імені О.О. Богомольця, доктор медичних наук, професор Ольга Голубовська. Вона подякувала зарубіжним експертам за тісну співпрацю з українськими фахівцями та ознайомила присутніх із насиченою програмою телесимпозіуму. Формат заходу дозволив одночасно реалізувати кілька важливих завдань: перейняти досвід ведення пацієнтів із гепатитом С у зарубіжних колег, а також провести активну дискусію між спікерами та учасниками телесимпозіуму з різних регіонів нашої країни.
 Виступ почесного професора медицини Королівської загальнодоступної клінічної лікарні та медичного факультету Університетського коледжу Лондона (Велика Британія) Джеффрі Душейко охоплював питання терапії гепатиту С у різних категорій пацієнтів. Спікер також приділив особливу увагу огляду рекомендацій Європейської асоціації з вивчення захворювань печінки (European Association for the Study of the Liver – EASL) із лікування ХГС.
Виступ почесного професора медицини Королівської загальнодоступної клінічної лікарні та медичного факультету Університетського коледжу Лондона (Велика Британія) Джеффрі Душейко охоплював питання терапії гепатиту С у різних категорій пацієнтів. Спікер також приділив особливу увагу огляду рекомендацій Європейської асоціації з вивчення захворювань печінки (European Association for the Study of the Liver – EASL) із лікування ХГС.
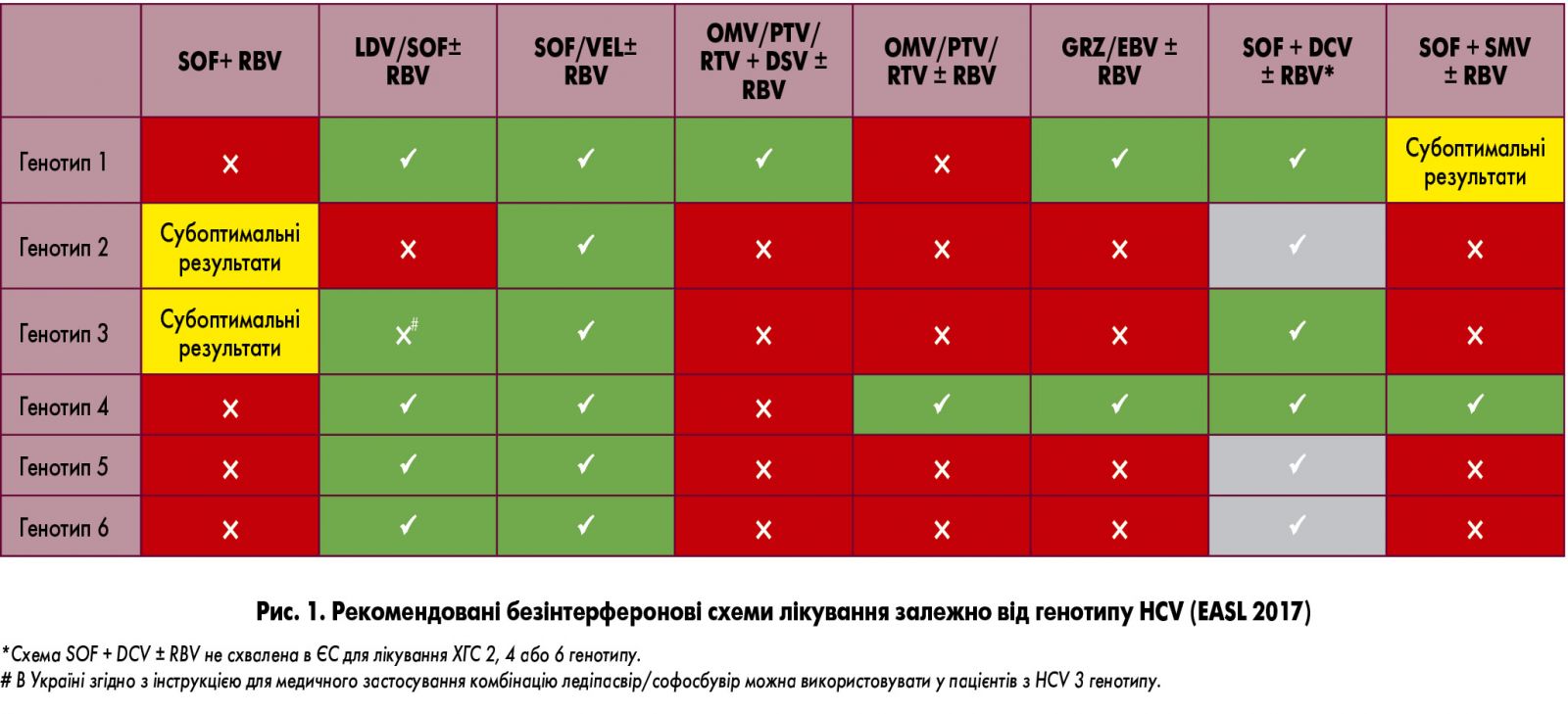
Тривалий час стандартом лікування ХГС вважали комбінацію пегінтерферону з рибавірином. Обидва препарати чинять противірусний ефект, але вони не націлені специфічно на вірус гепатиту С. Ця комбінація дозволяє досягти стійкої вірусологічної відповіді (СВВ) лише приблизно в половини пацієнтів і асоціюється зі значними побічними ефектами. Тож очевидною була необхідність у більш ефективному і безпечному лікуванні, націленому безпосередньо на вірус. Справжній прорив стався нещодавно завдяки розробленню та клінічному впровадженню препаратів DAAs. Вони впливають безпосередньо на білки вірусу, специфічно блокуючи їх функціональність і перериваючи цикл реплікації вірусу. Ці препарати використовують у комбінації з рибавірином та/або один з одним (рис. 1).
У хворих на ХГС терапія препаратами DAAs дозволила досягти: СВВ через 12 тижнів після закінчення лікування (СВВ12) у понад 90% випадків у пацієнтів з усіма генотипами вірусу; скорочення тривалості лікування ХГС до 8 тижнів; одужання від ХГС пацієнтів, які важко піддаються терапії, а також таких, які мали невдалий попередній досвід терапії DAAs; підвищення прихильності до терапії гепатиту С, зокрема завдяки зручності схеми лікування препаратами DAAs.
Відповідно до рекомендацій EASL (2017), для лікування пацієнтів з 1, 4, 5 і 6 генотипами HCV оптимальною вважається комбінація ледіпасвір/софосбувір ± рибавірин. Нещодавно проведене дослідження також показало високу ефективність режимів на основі фіксованої комбінації ледіпасвір/софосбувір у лікуванні пацієнтів із 3 генотипом HCV (n=2200; 54% із цирозом) в умовах реальної клінічної практики, частота СВВ становила близько 97% (T. Tsertsvadze et al., 2017). В Україні згідно з інструкцією для медичного застосування комбінацію ледіпасвір/софосбувір можна використовувати у пацієнтів з HCV 3 генотипу.
Що стосується ХГС 2 і 3 генотипу, то у низці досліджень комбінація софосбувір/велпатасвір дозволяла досягти високих показників СВВ – 91-100% після 12 тижнів лікування, зокрема в пацієнтів із цирозом і таких, які раніше отримували противірусну терапію.
Дж. Душейко зауважив, що у пацієнтів з декомпенсованим цирозом без гепатоцелюлярної карциноми, які очікують трансплантації печінки, початок терапії ХГС залежить від показника за шкалою MELD (моделі термінальної стадії захворювання печінки): <18-20 – противірусне лікування ХГС до трансплантації печінки, >18-20 – спочатку трансплантація печінки, а потім – терапія HCV-інфекції. Проте пацієнтам останньої групи може бути також рекомендовано лікування ХГС до проведення трансплантації печінки, якщо період очікування операції становить понад 6 міс.
Схеми лікування пацієнтів з декомпенсованим цирозом без гепатоцелюлярної карциноми (індекс MELD <18-20) з показаннями до трансплантації печінки або без таких включають: комбінацію ледіпасвір/софосбувір з рибавірином протягом 12 тижнів (генотипи вірусу 1, 4-6), софосбувір/велпатасвір з рибавірином або софосбувір + даклатасвір + рибавірин протягом 12 тижнів (генотипи вірусу 1, 2, 4-6) або 24 тижнів (генотип вірусу 3).
Професор Дж. Душейко також зупинився на питаннях, пов’язаних з терапією ХГС у пацієнтів з коінфекцією HCV/ВІЛ, представивши результати клінічних досліджень ефективності препаратів DAAs у таких хворих. Зокрема, дослідження ION-4 продемонструвало досягнення СВВ12 на рівні 96% у пацієнтів з коінфекцією HCV/ВІЛ (1 або 4 генотип HSV) після терапії комбінацією ледіпасвір/софосбувір. Софосбувір не має клінічно значимих взаємодій з антиретровірусними препаратами, що дозволяє проводити одночасне лікування обох інфекцій. Поєднання фіксованої комбінації ледіпасвір/софосбувір з більшістю схем антиретровірусної терапії також є безпечним; додатковий моніторинг може проводитися лише у разі одночасного застосування з ефавірензом або тенофовіром дизопроксилом.
Великий інтерес в української фахової аудиторії викликали представлені Дж. Душейко дані про схеми терапії ХГС в дитячій популяції. Згідно з рекомендаціями EASL, всі діти, народжені HCV-позитивними жінками, мають проходити тестування на HCV-інфекцію. Тести на основі антитіл можуть застосовуватись починаючи з 18 міс життя, тести для визначення РНК HCV – у більш ранні терміни. Діти, позитивні щодо анти-HCV у віці 18 міс, потребують тестування на РНК HCV у віці 3 років для підтвердження ХГС.
У дітей у віці 3-11 років для лікування ХГС EASL рекомендує застосовувати безінтерферонові схеми лікування (препарати DAAs), які схвалені для цієї вікової групи. У дітей віком від 12 років або з масою тіла ≥35 кг можна застосовувати софосбувір + рибавірин (2, 3 генотипи HCV) або фіксовану комбінацію ледіпасвір/софосбувір (1, 4-6 генотипи HCV) протягом 12-24 тижнів.
У багатоцентровому відкритому дослідженні II фази Balistreri і співавт. (2017) оцінювали ефективність і безпеку фіксованої комбінації ледіпасвір/софосбувір у дітей у віці 12-17 років із хронічною HCV-інфекцію 1 генотипу (n=100). Більшість пацієнтів (80%) раніше не отримували лікування ХГС, 84% були інфіковані перинатальним шляхом. Пацієнти отримували ледіпасвір/софосбувір 90/400 мг 1 р/добу протягом 12 тижнів. СВВ досягли 98% пацієнтів (98/100; два пацієнти без СВВ дочасно вибули з-під спостереження), не зареєстровано жодного випадку вірусологічної невдачі. Найчастішими небажаними подіями були головний біль (27%), діарея (14%) і підвищена втомлюваність (13%), серйозних побічних ефектів не спостерігалось. Отже, результати дослідження свідчать про високу ефективність і добру переносимість підлітками з ХГС 1 генотипу «дорослої» дози фіксованої комбінації ледіпасвір/софосбувір.
Пацієнтам із ХГС і хронічною хворобою нирок (ХХН) 4 і 5 стадії (швидкість клубочкової фільтрації (ШКФ) <30 мл/хв/ 1,73 м2 або термінальна стадія хвороби нирок) рекомендовано призначати фіксовані комбінації елбасвір/гразопревір (генотипи 1а, 1b, 4) протягом 12 тижнів або глекапревір/пібрентасвір (усі генотипи) упродовж 8-16 тижнів (EASL, 2017).
У дослідженні HCV-TARGET за участю 1789 пацієнтів в умовах реальної клінічної практики оцінювали ефективність і безпеку схем на основі софосбувіру залежно від ниркової функції. Серед пацієнтів із ШКФ ≤45 мл/хв/ 1,73 м2 було більше жінок (55 vs 36%), осіб віком ≥65 років (24 vs 16%), пацієнтів із декоменсованим цирозом (73 vs 24%) і хворих після трансплантації печінки (49 vs 10%) порівняно із пацієнтами з ШКФ >45 мл/хв/ 1,73 м2. Незважаючи на те що нирковий кліренс є головним шляхом елімінації софосбувіру, показник СВВ12 при лікуванні схемами на основі цього препарату істотно не відрізнявся між двома групами із різними показниками ШКФ і становив 82-83%. Незалежно від застосування рибавірину в пацієнтів із ШКФ ≤45 мл/хв/ 1,73 м2 частіше спостерігали анемію, погіршення ниркової функції, а також тяжкі небажані явища.
Як зазначив професор Дж. Душейко, всі препарати DAAs можна застосовувати в пацієнтів із ШКФ >30 мл/хв/1,73 м2. Схеми на основі софосбувіру продемонстрували високу ефективність і безпеку в цій популяції, тому можуть призначатись у разі протипоказань до застосування інгібіторів протеази.
Формат телесимпозіуму дозволив вітчизняним лікарям-інфекціоністам з різних куточків України взяти участь у професійній дискусії із зарубіжними колегами, а також презентувати інформацію щодо тягаря ХГС в різних регіонах нашої країни.
Згідно з представленими даними, тягар гепатиту С відрізняється залежно від регіону України; в декількох областях кількість пацієнтів із ХГС, які перебувають на обліку в лікувальному закладі, становить понад 10 тис. Однак, коментуючи надану інформацію, О. Голубовська зазначила, що реальні цифри значно відрізняються від даних офіційної статистики через низький показник виявлення таких хворих і відсутність єдиного реєстру пацієнтів із ХГС. За даними ВООЗ, в Україні зареєстровано 5% інфікованих ХГС в загальній популяції. Крім того, наша країна входить до переліку 17 країн з високою поширеністю хронічних гепатитів.
Найбільш поширеним генотипом вірусу гепатиту С в українських пацієнтів є 1 генотип, проте у багатьох хворих генотип вірусу досі є не визначеним.
Що ж стосується хворих на ХГС, які отримують лікування, зокрема за бюджетні кошти, їх кількість варіює залежно від регіону і становить від 431 до 1503 пацієнтів. У деяких регіонах нашої країни всі хворі на ХГС, які перебувають на обліку в лікувальному закладі і проходять лікування, отримують його за кошти державного бюджету.
У різних регіонах найбільш широко застосовуються різні схеми терапії ХГС, втім, основні з них – це схеми лікування на основі препаратів DAAs, зокрема софосбувіру і фіксованої комбінації ледіпасвір/софосбувір. На вибір терапії для кожного конкретного пацієнта впливають такі фактори, як генотип HCV, стадія фіброзу печінки та ін.
 Доповідь Шорени Двалі, лікаря-інфекціоніста Дослідницького центру з питань інфекційних захворювань, СНІДу та клінічної імунології, консультанта з інфекційних захворювань гепатологічного центру НЕРА (м. Тбілісі), була присвячена досягненням Грузії на шляху елімінації гепатиту С, а також ролі препаратів DAAs у цьому процесі.
Доповідь Шорени Двалі, лікаря-інфекціоніста Дослідницького центру з питань інфекційних захворювань, СНІДу та клінічної імунології, консультанта з інфекційних захворювань гепатологічного центру НЕРА (м. Тбілісі), була присвячена досягненням Грузії на шляху елімінації гепатиту С, а також ролі препаратів DAAs у цьому процесі.
Спікер зазначила, що, згідно з даними за 2014 рік, Грузія займала 5-те місце у світі за поширеністю гепатиту С з найвищим показником захворюваності серед країн пострадянського простору. У зв’язку з високим рівнем поширеності захворювання уряд Грузії прийняв рішення про необхідність впровадження державної програми із боротьби з гепатитом С. Це стало можливим завдяки допомозі іноземних партнерів – Gilead Sciences і Center for Disease Control and Prevention.
У квітні 2015 року генеральний директор Gilead Sciences Джон Мартін і прем’єр-міністр Грузії Іраклій Гарібашвілі підписали меморандум про взаємну співпрацю, в рамках якого компанія Gilead Sciences зобов’язалася надавати Грузії софосбувір і фіксовану комбінацію ледіпасвір/софосбувір на безоплатній основі для лікування пацієнтів з гепатитом С. Це стало основою для реалізації державної програми із боротьби з гепатитом С в цій країні.
За словами Ш. Двалі, вибір Грузії як зразкової країни для елімінації гепатиту С був зумовлений: високою поширеністю HCV серед населення в цілому і невеликою площею країни; чітким курсом уряду на припинення епідемії гепатиту С; необхідними трудовими ресурсами і технічними можливостями для діагностики та лікування гепатиту С; наявними системами і механізмами для реалізації аналогічних проектів; практичним досвідом боротьби з ВІЛ/СНІДом.
Метою реалізації державної програми з елімінації гепатиту С в Грузії є досягнення показників «90-95-95», тобто виявлення 90% інфікованих, проведення лікування 95% таких пацієнтів і досягнення відповіді на лікування в 95% випадків. Досягти таких амбітних цілей країна планує шляхом виявлення і лікування всіх пацієнтів із гепатитом С, посилення ефективних профілактичних втручань і скорочення кількості нових випадків захворювання.
При цьому відмінність програми з боротьби з гепатитом С в Грузії порівняно з іншими країнами полягає в активному пошуку інфікованих, лікуванні всіх пацієнтів з гепатитом С (включаючи хворих з фіброзом печінки F0), повторному лікуванні хворих у тих випадках, якщо попередня противірусна терапія була невдалою, реалізації масштабних програм із профілактики гепатиту С.
У рамках реалізації державної програми з елімінації гепатиту С в Грузії у протоколах лікування пацієнтів за період із квітня 2015 по березень 2016 року зазначено про застосування інтерфероновмісних і безінтерферонових схем лікування із включенням софосбувіру. Починаючи з березня 2016 року на підставі результатів клінічних досліджень для лікування пацієнтів з гепатитом C всіх генотипів HCV рекомендується фіксована комбінація ледіпасвір/софосбувір.
Алгоритм обстеження пацієнтів із ХГС до початку лікування включає клінічну оцінку, кількісне визначення РНК HCV, генотипування HCV, загальний аналіз крові, біохімічні показники (АЛТ, АСТ, креатинін, білірубін, альбумін, лужна фосфатаза, глюкоза, міжнародне нормалізоване співвідношення), тестування на HBs-антиген, анти-HBc та анти-HBs, визначення рівнів антинуклеарних антитіл, тиреотропного гормону та індексу FIB-4, а також ультразвукове дослідження органів черевної порожнини.
Індекс FIB-4 розраховується за формулою:
FIB4 = вік (роки) × АСТ / (тромбоцити (109/л) × √(АЛТ)).
Показник <1,45 із достовірністю 90% свідчить про відсутність значного фіброзу печінки, натомість показник >3,25 вказує на наявність фіброзу 4-6 стадії за шкалою Ishak.
Моніторинг противірусної терапії передбачав оцінку та контроль ефективності та побічних ефектів протягом лікування.
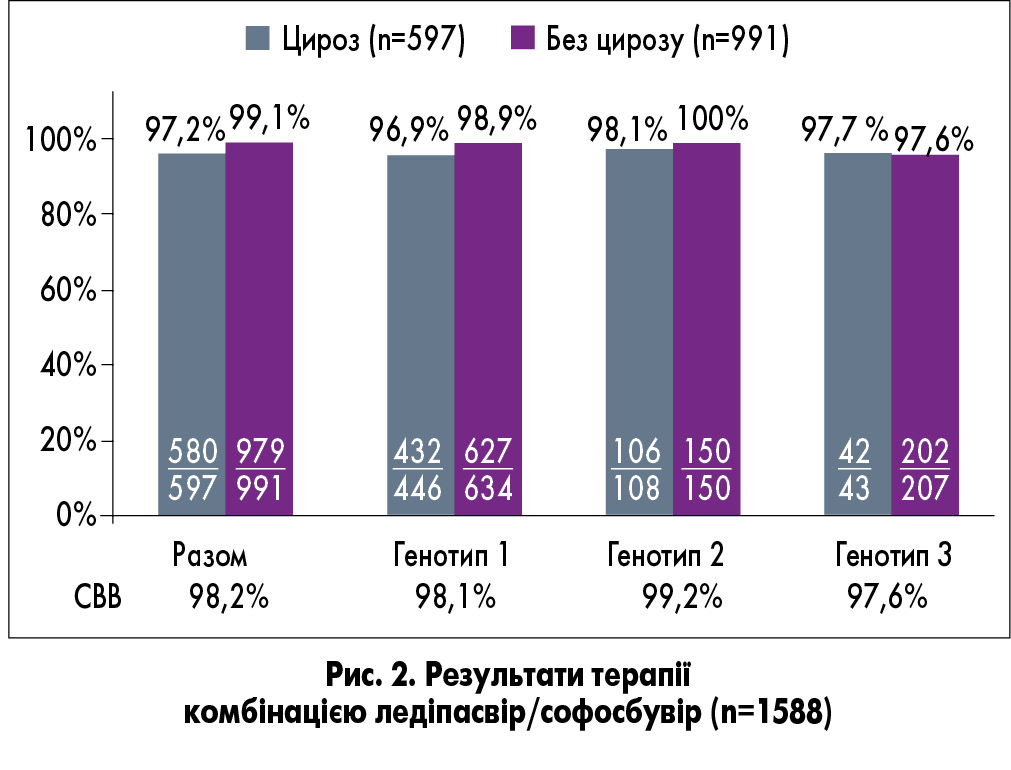
У рамках реалізації програми із елімінації ХГС в Грузії були отримані визначні результати щодо ефективності фіксованої комбінації ледіпасвір/софосбувір ± рибавірин (12-24 тижні) у лікуванні пацієнтів з ХГС 1-4 генотипів: при 1 генотипі – в 98,1% випадків, 2 генотипі – у 99,2%, 3 генотипі – у 97,6%, 4 генотипі – у 100%. Ефективність лікування не відрізнялася у пацієнтів із цирозом і без нього (рис. 2).
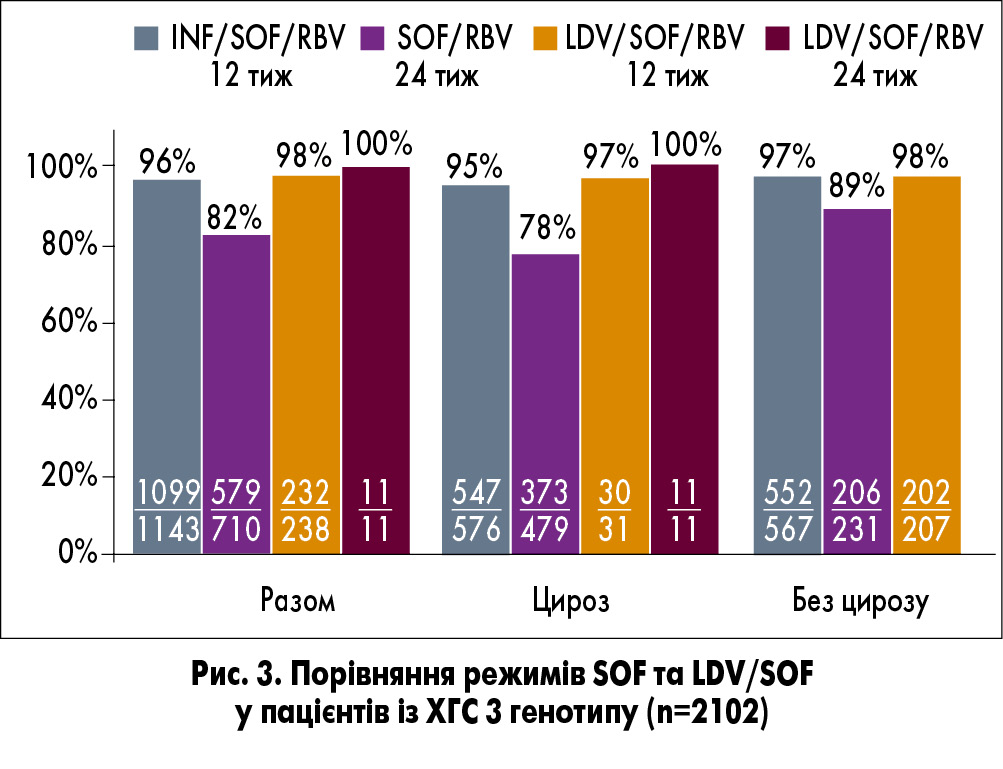
У популяції хворих на ХГС 3 генотипу (n=2102) ефективність комбінації ледіпасвір/софосбувір з рибавірином становила: у пацієнтів без цирозу печінки – 98%, з цирозом печінки – 97% (при режимі терапії протягом 12 тижнів); у пацієнтів з ХГС 3 генотипу з цирозом печінки – 100% (при режимі терапії протягом 24 тижнів; рис. 3).
На завершення заходу О. Голубовська представила основні меседжі за результатами проведення Всесвітнього саміту з вірусних гепатитів, який відбувся 1-3 листопада в м. Сан-Паулу (Бразилія). Міжнародний альянс із боротьби з гепатитом і його 252 організації підписали Сан-Паулську декларацію із вірусних гепатитів, висуваючи до урядів країн вимогу пріоритетності проблеми вірусних гепатитів, так само як ВІЛ/СНІДу, малярії та туберкульозу.
Cьогодні українські пацієнти мають можливість лікуватися оригінальними препаратами DAAs для терапії хронічного гепатиту С, зокрема за рахунок коштів державного бюджету. Отже, цілковите одужання від ХГС стало реальністю і в нашій країні.
Підготував Олексій Терещенко
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 4 (46), листопад 2017 р.