25 грудня, 2017
Вітамін D у різні періоди дитинства: що знаємо, що треба пам’ятати і що забули
Нельзя не отметить, что одним из наиболее распространенных видов витаминной недостаточности у детей и беременных женщин в настоящее время является D-гиповитаминоз, который возникает из-за недостаточного поступления этого витамина с пищевыми продуктами или нарушения его эндогенного синтеза и обмена. Наиболее склонны к гиповитаминозу дети, родившиеся от матерей с экстрагенитальной и акушерской патологией, недоношенные младенцы, дети в период интенсивного роста и развития: первые два года жизни, периоды первого и второго вытяжения.
Е.М. Лукьянова (2005)
 Відомо, що недостатня забезпеченість організму вітаміном D, навіть незначна, може бути причиною розвитку багатьох захворювань. Тому своєчасне визначення ступеня забезпеченості організму вітаміном D і корекція його дефіциту має велике значення для підтримки здоров’я людини та клінічної практики. На сьогодні ідентифіковано низку метаболітів вітаміну D, які мають гормоноподібну дію та беруть участь практично в усіх видах обміну речовин людини. Саме тому D-вітамінна недостатність та вітамін D-дефіцитні стани впливають на функціонування всіх органів і систем організму, «вирішуючи» питання здоров’я чи патології.
Відомо, що недостатня забезпеченість організму вітаміном D, навіть незначна, може бути причиною розвитку багатьох захворювань. Тому своєчасне визначення ступеня забезпеченості організму вітаміном D і корекція його дефіциту має велике значення для підтримки здоров’я людини та клінічної практики. На сьогодні ідентифіковано низку метаболітів вітаміну D, які мають гормоноподібну дію та беруть участь практично в усіх видах обміну речовин людини. Саме тому D-вітамінна недостатність та вітамін D-дефіцитні стани впливають на функціонування всіх органів і систем організму, «вирішуючи» питання здоров’я чи патології.
Доведено, що формуванню вітамін D-дефіцитного стану сприяють періоди активного росту дитини, коли має місце прискорення метаболізму вітаміну D зі швидким вичерпанням його запасів в організмі. Клінічні ознаки дефіциту вітаміну D залежать від віку дитини: у дітей раннього віку він проявляється рахітом, а у старших дітей – остеопенією, остеопорозом і функціональними розладами життєво важливих органів і систем.
Вивчення ролі вітаміну D в організмі людини тісно пов’язане з розвитком знань про рахіт. Уже в XV ст. рахіт був одним із поширених захворювань у Європі. Деякий час рахіт називали «англійською хворобою», оскільки в Англії відзначалася висока частота поширення його тяжких форм. Класичний опис рахіту подав у 1650 р. англійський анатом і хірург Гліссон (Glisson) у трактаті «De rachitide sive morbo puerili, qui vulgo the rickets dicitur». Однак історія пошуку причин рахіту і методів його лікування тривала практично 270 років від перших описів клінічної картини захворювання. У 1822 р. Sniadecki зробив припущення про те, що сонячне світло відіграє роль у запобіганні розвитку рахіту, на підставі свого спостереження. Він відзначив, що діти, народжені у м. Варшава, частіше хворіють на рахіт, ніж немовлята, народжені у сільській місцевості [3]. Але тільки у 1919 р. Huldschinsky вперше показав, що захворювання у дітей усувається під впливом променів «штучного гірського сонця» (кварцової лампи). Водночас антирахітичну дію риб’ячого жиру пов’язували з наявністю у ньому вітаміну А. І тільки у 1922 р. McCollum вказав на наявність у риб’ячому жирі іншого вітаміну. Пропускаючи струмінь кисню через жир тріски й інактивуючи вітамін А, він виявив, що антирахітична дія жиру зберігалася. Згодом із жиру тріски був виділений вітамін, який володів антирахітичною дією й отримав назву вітаміну D [4, 5].
Сьогодні вітаміном D називають дві речовини – D2 і D3 – ергокальциферол і холекальциферол. Холекальциферол (вітамін D3) надходить в організм людини з їжею та синтезується під дією ультрафіолетових променів у шкірі. Під час перебування на сонці 7-дигідрохолестерин у шкірі перетворюється у провітамін D, а потім – у вітамін D3. Ергокальциферол (вітамін D2) надходить в організм тільки з їжею, він виробляється рослинами і грибами, міститься у дріжджах і хлібі. Кількість холекальциферолу, яка синтезується під впливом ультрафіолетових променів, залежить від багатьох чинників: довжини світлової хвилі, віку (з віком знижується здатність шкіри синтезувати вітамін D), пігментації (чим менше пігментована шкіра, тим більша кількість вітаміну D синтезується).
Активне вивчення протягом останніх 20 років метаболізму вітаміну D показало, що крім добре відомої ключової ролі вітаміну D у мінеральному обміні, його активні метаболіти чинять значний вплив на всі види обміну речовин. Це пов’язано з двома механізмами дії вітаміну D3 на фізіологічні процеси: негеномним і на рівні генома [9, 12]. На рівні генома метаболіти вітаміну D3 проявляють фізіологічний ефект подібно до дії стероїдних гормонів.
Дигідроксиметаболіти, потрапляючи в клітину-мішень, зв’язуються зі своїми специфічними рецепторними білками. Встановлено, що у вільному стані рецептор міститься у цитоплазмі, де відбувається його зв’язування з гормоном. Утворений гормоно-рецепторний комплекс переноситься до ядра клітини і вступає у взаємодію з певними ділянками молекули ДНК. Результатом такої взаємодії є біосинтез нових молекул мРНК і трансляція відповідних білків, що беруть участь у гормональній відповіді.
Другий механізм дії вітаміну D3 проявляється через мембрану. Встановлено, що гормонально-активні форми вітаміну D3 регулюють активність ферментів in vitro на ізольованих мембранних везикулах при відсутності гормонального рецептора, генної транскрипції та синтезу нових білків; це вказує на їх вплив безпосередньо на плинність мембран і їх функцію, тобто мембранотропний ефект [9, 12].
При потраплянні в організм вітамін D всмоктується в проксимальному відділі тонкого кишечника: ступінь всмоктування безпосередньо залежить від кількості жовчі, при цьому біодоступність становить близько 60-90%. Транспортування вітаміну D обумовлене вітамін D-зв’язуючим білком (VDBP).
Незалежно від шляху надходження – з їжею або унаслідок ендогенного синтезу під дією ультрафіолетових променів – вітамін D стає біологічно активним після того, як пройде два етапи ферментативних перетворень у вигляді гідроксилювання. У купферових клітинах печінки, під впливом мембранного ферменту сімейства цитохрому Р450 25-гідроксилази (СYР3А4), холекальциферол перетворюється у перший активний метаболіт – 25-гідроксихолекальциферол (25(ОН)D3), або кальцидіол. У реалізації цієї реакції також задіяні цитохроми СYР2С9 і СYР2D6 [4, 5].
25(ОН)D3 є основною формою вітаміну D, що циркулює у крові. Утворення 25(ОН)D3 у печінці регулюється за механізмом зворотного зв’язку і підтримується на відносно сталому рівні. Саме тому рівень цього метаболіту в крові може служити критерієм забезпеченості організму вітаміном D3 [4].
Другий етап метаболізму відбувається у нирках за допомогою ферменту 1а-гідроксилази (СYР27В1), що перетворює 25(ОН)D3 у біологічно активний гормон кальцитріол – 1,25-дигідроксихолекальциферол (1,25(ОН)2D3). Саме 1,25(ОН)2D3 разом з паратгормоном і кальцитоніном забезпечує фосфатно-кальцієвий гомеостаз, процеси мінералізації та зростання кісток, регулюючи відкладення кальцію в кістковій тканині та дентині.
Добре доведена реалізація численних ефектів вітаміну D на рівні імунної відповіді [7]. Рецептори вітаміну D (VDR), як мембранні, так і нуклеарні, виявлено майже у всіх типах клітин імунної системи – нейтрофілах, моноцитах, макрофагах, дендритних клітинах, Т- (CD4 і CD8) і В-лімфоцитах, а також епітеліальних клітинах [3-6].
Висока концентрація рецепторів вітаміну D відзначається у популяціях Т-лімфоцитів і макрофагів, особливо у незрілих імунних клітинах тимуса і зрілих CD8 Т-лімфоцитах. Вітамін D стимулює вироблення трансформуючого фактора росту (ТGF-β) та інтерлейкіну‑4 (IL‑4), що в свою чергу пригнічує запальну активність Т-клітин [4]. Все більше фахівців визнають, що крім впливу вітаміну D на відповідь Тh1 і Тh2 цей вітамін сприяє індукції регуляторних Т-клітин [8].
Доведено, що вітамін D чинить виражений вплив на проліферацію, диференціювання і функціональну активність опасистих клітин, тим самим беручи участь в алергічних реакціях [1, 2]. Відповідно до сучасних даних, 1,25(ОН)2D3 можна розглядати як імуномодулятор, орієнтований на різні клітини імунної системи [8].
Крім безпосередньо імуномодулюючого впливу, вітамін D бере участь у виробленні дефензинів і кателіцидину – антимікробних пептидів, які забезпечують природний захист від патогенів. Проведені дослідження довели ефективну дію кателіцидину проти внутрішньоклітинних мікобактерій туберкульозу. Це пояснює ті історичні факти, що до появи антибіотиків туберкульоз шкіри успішно лікували за допомогою ультрафіолетового опромінення, а у 20-ті роки минулого століття при туберкульозі легенів рекомендували регулярне перебування на сонці.
Ефекти вітаміну D на рівні імунних клітин кишечника можуть реалізовуватися за участю бактерій кишкової мікробіоти. Передбачається, що модуляція кишкової мікробіоти шляхом використання пробіотиків може змінювати реакцію імунних клітин під стимулюючим впливом вітаміну D за рахунок підвищення експресії його рецепторів і таким чином пригнічувати запальні реакції тканин [5].
Дослідження останніх років, присвячені впливу вітаміну D на імунну відповідь, показали, що забезпеченість вітаміном D критично важлива для формування адекватної імунної відповіді у всі періоди дитинства, особливо в критичні періоди розвитку. Нині існує гіпотеза про те, що скорочення протягом останніх 40 років часу перебування людей на сонці (а також використання сонцезахисних кремів) призводить до більшості хвороб, при цьому проблема має світові масштаби. В епідеміологічних дослідженнях показано зв’язок недостатності вітаміну D з імунними порушеннями: підвищеною схильністю до інфекцій, у тому числі хронічних, а також до розвитку аутоімунних захворювань [9]. Нормальний рівень вітаміну D, навпаки, формує адекватну імунну відповідь, забезпечуючи нормальне співвідношення про- та протизапальних цитокінів. Показано, що 1,25(ОН)2D3 може запобігати або значно сповільнювати розвиток експериментального аутоімунного енцефаломієліту, ревматоїдного артриту, системного червоного вовчаку, цукрового діабету 1 типу і запальних захворювань кишечника [8].
Вітамін D3 впливає на ядра клітин-мішеней і стимулює транскрипцію ДНК та РНК, що супроводжується посиленням синтезу специфічних протеїнів. Дефіцит вітаміну D у плода, пов’язаний з його недостатністю у вагітної, значно підвищує ризик розвитку не тільки вроджених аномалій (вроджена катаракта, вроджені аномалії будови головного мозку), а й ризиком розвитку цілої низки інших захворювань у майбутньому (аутоімунні, алергічні захворювання, цукровий діабет, ожиріння, онкологічна патологія – рак молочної залози, товстої кишки; хвороби серцево-судинної системи, запальні захворювання кишечника) [5]. Це може бути пов’язане з тим, що вітамін D індукує понад 3 тис. генів, багато з яких дуже важливі для розвитку плода. Отже, ця унікальна речовина надзвичайно важлива для плодового «програмування», при якому чинники середовища визначають розвиток дитини і ризик подальшого виникнення захворювань у дитинстві та дорослому віці. Можливо, тут мають значення епігенетичні механізми, які призводять до зміни структури та функції різних органів і систем організму [24].
Встановлено, що рівень 25(OН)D3 у вагітної практично не змінюється, натомість рівень його активного метаболіту 1,25(ОН)2D3 зростає удвічі вже в першому триместрі. Разом із пролактином і плацентарним лактогеном 1,25(ОН)2D3 відповідає за посилену абсорбцію кальцію у травному каналі та збільшення його реабсорбції нирками з перших тижнів вагітності [21-23].
25(OН)D проходить через плаценту, а його рівень у пуповинній крові дорівнює рівню цього метаболіту вітаміну D у матері або є трохи нижчим. Натомість активний метаболіт вітаміну D 1,25(OН)2D3 практично не проникає через плаценту й утворюється самою плацентою, а пізніше – й печінкою плода з материнського 25(OН)D3. Отже, якщо у матері наявна недостатність вітаміну D, то у дитини виникає виражений гіповітаміноз.
Функції вітаміну D у період вагітності дуже різноманітні і не обмежуються підтримкою стабільності кісткової системи матері та плода. Важливість цієї речовини для обміну кальцію загалом підтверджує той факт, що її значний дефіцит у матері під час вагітності призводить до вродженого рахіту, а в критичних випадках – до глибокої гіпокальціємії та неонатальних судом у новонародженого. Однак дія цього вітаміну поширюється і на інші системи, що було зазначено вище.
Недостатність вітаміну D у популяції є звичайним явищем, тому не дивно, що вона характерна і для вагітних. Виділяють такі групи ризику гіповітамінозу D:
- пацієнтки з надлишковою масою тіла;
- жінки, що уникають перебування на сонці, застосовують креми з ультрафіолетовими фільтрами або носять одяг, який закриває більшість поверхні тіла;
- пацієнтки, госпіталізовані на тривалий час у період вагітності;
- особи, які додатково не приймають вітамін D або приймають його у недостатніх дозах.
Недавні дослідження вказують на зв’язок дефіциту вітаміну D у матері та ускладнень вагітності: прееклампсії, гестаційного діабету, необхідності кесаревого розтину, передчасних пологів, бактеріального вагінозу, малої для гестаційного віку дитини маси тіла, малої маси тіла дитини при народженні.
За даними багатьох дослідників, вітамін D опосередковано впливає на нормалізацію артеріального тиску. Нормотонічний ефект вітаміну D забезпечується за рахунок деяких молекулярних механізмів (зменшення секреції реніну, нефропротекції, протизапальної дії), нормалізації ліпідного обміну й ендотеліальної дисфункції [9, 10, 18-20].
Сьогодні очевидно, що рекомендована до останнього часу профілактична доза вітаміну 400-500 МО на добу достатня для підтримки оптимального рівня метаболізму Са і Р при нормальному початковому рівні 25(ОН)D3 (>30 нг/мл), але недостатня для реалізації інших функцій холекальциферолу і його активних метаболітів: чого достатньо для кісток, недостатньо для всього тіла (Enough for the bones, not for the body) [11].
! Враховуючи, що більш ніж 80% дитячого населення України має рівень 25(ОН)D3 нижчий за 30 нг/мл, V Конгрес педіатрів України ухвалив: профілактична доза вітаміну D для дітей має становити 1000 МО [17].
Ступінь забезпеченості вітаміном D організму людини сьогодні визначають за вмістом 25(ОН)D3 у сироватці крові. Вважається, що оптимальною концентрацією 25(ОН)D3 у сироватці крові є 40-60 нг/мл, це відмічається при прийомі добової дози вітаміну 1000-2000 МО (B. Dawson-Hughes, 2004). При введенні таких доз вітаміну D3 протягом 30-45 діб (залежно від початкового вмісту 25(OH)D3 у сироватці крові) його фізіологічний рівень підтримується в організмі протягом 2-3 міс після закінчення прийому. Цей факт обґрунтовує доцільність використання курсового методу 2-3 рази на рік з профілактичною або (за необхідності) лікувальною метою.
На підставі власних досліджень, які проводяться в ДУ «Інститут педіатрії, акушерства і гінекології НАМН України», встановлено особливості забезпечення організму вітаміном D і рівень 25(OH)D3 у сироватці крові у здорових дітей різних вікових груп (табл. 1).
З таблиці 1 видно, що знижена забезпеченість вітаміном D (D-гіповітаміноз, D-вітамінна недостатність і вітамін D-дефіцит) переважає в усій дитячій популяції і становить 72-90% залежно від віку, тоді як бажана забезпеченість вітаміном D спостерігається лише у 9-28% дітей залежно від віку (однак слід зазначити, що в деяких вікових групах цей показник не визначався).
В останні роки широко обговорюється питання щодо фізіологічної дози вітаміну D3. Служба продовольства та харчування (Food and Nutrition Service) США вважає, що безпечною добовою дозою для дітей першого року життя є 1000 МО вітаміну D3, а для дітей старшого віку, вагітних, матерів, що годують груддю, – 2000 МО. У 2013 р. надруковані рекомендації щодо доз вітаміну D для вагітних і жінок, що годують груддю, які проживають у країнах Східної Європи (табл. 2) [25].
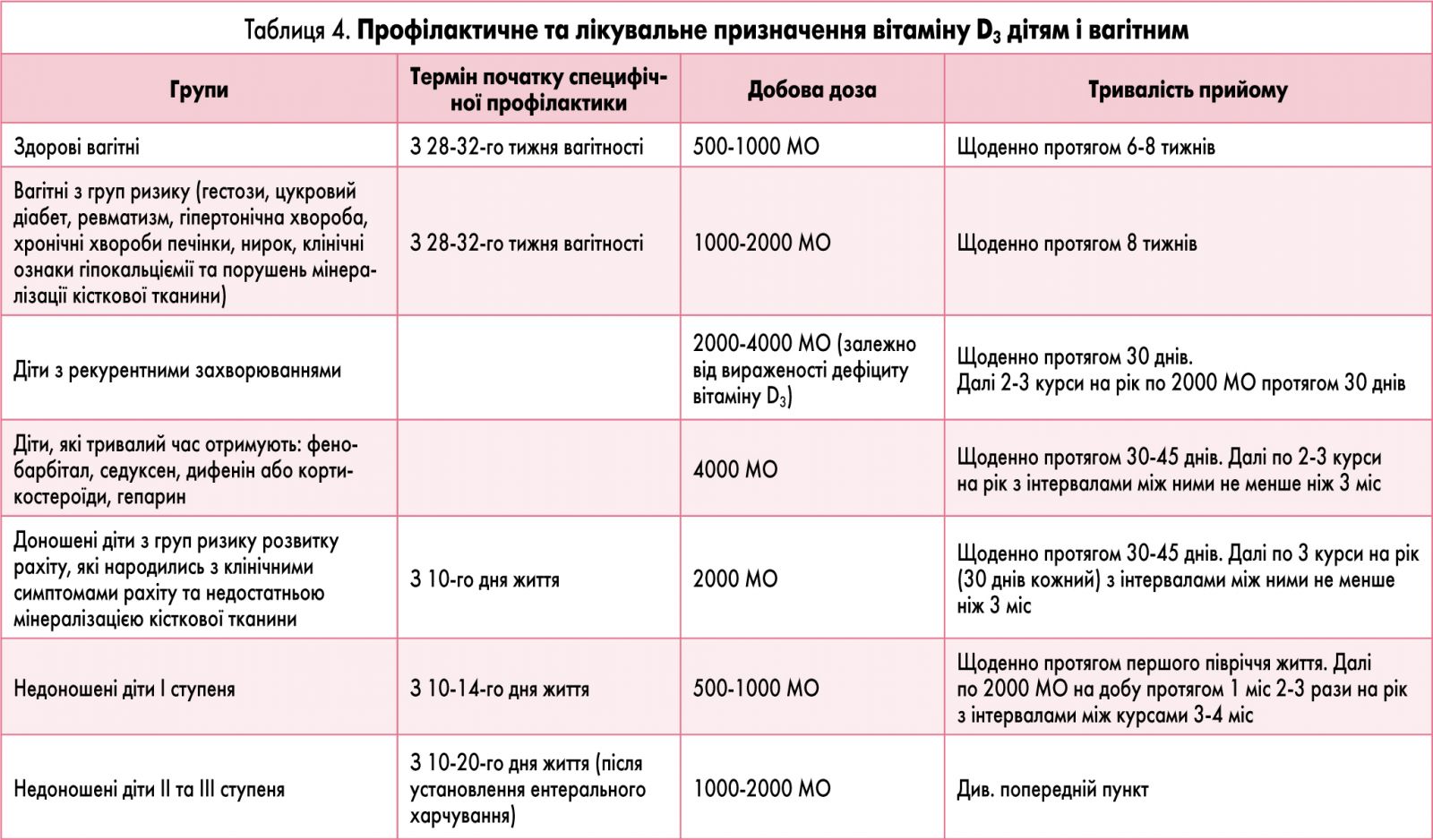
На V Конгресі педіатрів України, відповідно до досліджень і думок провідних вітамінологів світу, профілактичною дозою вітаміну D3 для дітей перших трьох років життя визначена доза 1000-2000 МО на добу з урахуванням клінічного перебігу вагітності у матері та здоров’я дитини (табл. 3, 4). Добове вживання вітаміну D3 у такій дозі забезпечує фізіологічний рівень його активних метаболітів у крові дітей, є ефективним для запобігання рахіту у здорових малюків.
Однак важливо відзначити, що необхідною умовою успішного здійснення вітаміном D його винятково важливих функцій є повноцінне забезпечення організму людини всіма іншими вітамінами, необхідними для утворення гормонально активної форми вітаміну D [12]. Саме тому корекція забезпеченості вітаміном D має бути комплексною і супроводжуватися призначенням всіх інших вітамінів [12].
На жаль, не тільки проживання в країнах з недостатньою інсоляцією, а й сам «західний» урбаністичний спосіб життя призводить до недостатньої забезпеченості населення вітаміном D. Так, результати досліджень забезпеченості вітаміном D показали, що поширеність дефіциту вітаміну D в розвинених країнах становить у середньому близько 10%, недостатньої забезпеченості – 50% [13, 14].
Визнаним критерієм оцінювання екзогенної забезпеченості вітаміном D є дослідження рівня 25(ОН)D3 у крові. Вивчення більшості взаємозв’язків між споживанням вітаміну D, станом здоров’я і різними захворюваннями дало змогу зробити висновок, що бажаний (або достатній) рівень циркулюючого вітаміну D (який визначається як 25(ОН) D3) становить як мінімум 30-40 нг/мл (75-100 нмоль/л). Рівні 25(ОН)D у діапазоні 20-30 нг/мл (50-75 нмоль/л) розглядаються як відносна недостатність. Отже, для оптимального функціонування імунної системи та підтримки загального здоров’я потрібна концентрація 25(ОН)D більше 40 нг/мл (100 нмоль/л). Середній рівень 25(ОН)D3 в крові вище за 100 нг/мл відповідає надлишковій забезпеченості, а вище за 150 нг/мл вважається токсичним [15].
Дефіцит вітаміну D документально підтверджений у багатьох популяціях у всьому світі, включаючи дітей. Особливо високий ризик дефіциту вітаміну D спостерігається у новонароджених, дітей молодшого віку, вагітних і матерів-годувальниць. Так, у дослідженні, проведеному університетом Мічигану, показано, що 50% матерів і 65% новонароджених у пологовому відділенні міської лікарні мали дефіцит вітаміну D. Його рівень у крові становив менше 12 нг/мл (або <30 нмоль/л), незважаючи навіть на те, що більшість матерів під час планування вагітності приймали полівітамінні комплекси [13]. Рівень вітаміну D у пуповинній крові корелював з таким у крові матері [13].
! Водночас показано, що низький рівень 25(ОН)D3 у пуповинній крові має сильну зворотну кореляцію з кількістю епізодів гострих респіраторних вірусних інфекцій у перші 3 міс життя дитини, а також із захворюваністю респіраторно-синцитіальною інфекцією у перший рік життя [16].
Проведене у 2013-2014 рр. багатоцентрове дослідження із визначення забезпеченості вітаміном D дітей раннього віку [16] дало змогу виявити наявність гіповітамінозу D у 90% дітей віком 2-3 роки [16].
У людей з темною шкірою (негроїдної раса, засмаглі люди) синтез вітаміну D у шкірі знижений. Така ж проблема існує й у людей літнього віку (у них здатність перетворювати провітаміни у вітамін D знижується вдвічі) і осіб, що дотримуються вегетаріанської дієти або вживають недостатню кількість жирів. Негативно впливають на засвоєння вітаміну D розлади функцій кишечника та печінки, жовчного міхура.
Уявлення про біологічну роль вітаміну D в організмі людини, що значно розширилися за останні роки, дозволяють пов’язати з недостатньою забезпеченістю цим вітаміном багато захворювань і патологічних станів.
Основними препаратами, що застосовуються для профілактики та лікування дефіциту вітаміну D, є насамперед препарати холекальциферолу (вітаміну D3). Препарати вітаміну D2 останнім часом в усьому світі майже не використовуються. Це пов’язано з тим, що вітамін D2 щодо людського організму є чужорідною речовиною, його зв’язок із транспортними та рецепторними білками і перетворення в активні метаболіти значно нижчі, ніж у вітаміну D3. Цим і пояснюється відносно низька профілактична та лікувальна ефективність вітаміну D2. Підвищення дози вітаміну D2 з метою досягнення ефекту категорично протипоказано, оскільки активність ферментів, під впливом яких вітамін D2 перетворюється на активні метаболіти, інгібується самим вітаміном D. Тому при використанні високих доз зменшується частка утворення активних метаболітів і збільшується кількість неперетвореної форми вітаміну, який зазнаючи окиснення, може чинити токсичну дію.
Активність препаратів вітаміну D виражається в міжнародних одиницях (40 МО = 1 мкг холекальциферолу).
У пацієнтів з муковісцидозом, холестазом та іншими порушеннями функції печінки (стеатогепатоз та ін.) секреція жовчних кислот знижується, окрему групу становлять недоношені діти різного гестаційного віку. Зазначені порушення ускладнюють міцелоутворення і, отже, різко знижують засвоєння вітаміну D (у тому числі з масляних розчинів) та інших жиророзчинних вітамінів. Синтез жирних кислот знижується в осіб літнього віку, а також при дотриманні певних дієт, включення в раціон блокаторів міцелювання і засвоєння вітаміну D – пальмітинової кислоти, насичених жирів, маргарину.
! Міцельовані (водорозчинні) розчини вітаміну D (до них належить препарат Аквадетрим® вітамін D3) характеризуються добрим всмоктуванням у пацієнтів практично всіх вікових груп.
В ДУ «Інститут педіатрії, акушерства і гінекології НАМН України» були проведені дослідження щодо визначення ефективності застосування препарату Аквадетрим® вітамін D3 (водний розчин, що в 1 краплі містить 500 МО вітаміну D3) з метою корекції недостатності цього вітаміну. Дітям першого року життя препарат призначали у дозі 1000 МО на добу, молодшого шкільного віку – 2000 МО на добу протягом 30-45 діб (залежно від початкового рівня забезпеченості). У дітей шкільного віку після 45-добового курсу рівень вітаміну D3 підвищився з 17,7 до 38,1 нг/мл, що підтверджує ефективність лікування.
При проведенні курсової профілактики у пропонованих дозах вміст вітаміну D в організмі підтримується на фізіологічному рівні протягом 2-3 міс. Це пов’язано з тим, що вітамін D3 має властивості до кумуляції. Він накопичується у печінці в непаренхімних клітинах, із яких далі транспортується у гепатоцити, де відбувається його метаболізм. Через 3 міс після прийому рівень вітаміну може значно знижуватися, внаслідок чого пропонується проведення повторних курсів лікування (2-3 курси на рік).
! Курсове застосування вітаміну D3 (препарат Аквадетрим® вітамін D3) у запропонованих дозах для корекції D-вітамінної недостатності та вітамін D-дефіцитних станів протягом всього періоду дитинства сприяє усуненню цих станів у 97% здорових дітей незалежно від віку.
Треба пам’ятати, що:
- дефіцит вітаміну D дуже розповсюджений і неминуче розвивається у дітей та вагітних;
- необхідно проводити антенатальну профілактику рахіту вагітним з 28-32-го тижня вагітності та вирішити питання, хто повинен її проводити;
- надходження вітаміну D в організм людини з природних джерел (сонячне опромінення, харчування) є недостатнім, тому для підтримки його бажаної концентрації (30-50 нг/мл) потрібен додатковий прийом цієї речовини;
- доказові дані обґрунтовують доцільність суплементації вітаміном D у дітей (особливо з рекурентними захворюваннями, в критичні періоди розвитку) і вагітних у дозах до 4000 МО на добу, що значно знижує ризик ускладнень перебігу вагітності та пологів (гестаційного діабету, гіпертензії, прееклампсії) та необхідності розродження шляхом кесаревого розтину, а також розвитку у дітей гострої та хронічної патології.
Література
1. Ребров В.Г., Громова О.А. Витамины, макро- и микроэлементы. – М.: ГЭОТАР-Медиа, 2008. – 960 с.
2. Спиричев В.Б., Коденцова В.М., Вржесинская О.А. и др. Методы оценки витаминной обеспеченности населения. – М., 2001. – 70 с.
3. Yu C., Fedoric B., Anderson P.H., Lopez A.R, Grimbaldeston M.A. Vitamin D(3) signalling to mast cells: A new regulatory axis // Int J Вiochem Cell Biol. 2011; 43(1): 41-6.
...
26. Антипкін Ю.Г., Квашніна Л.В., Омельченко Л.І. Обґрунтування доз вітаміну D3 для профілактики D-вітамінної недостатності та вітамін D-дефіцитних станів у здорових дітей різного віку. Інформаційний лист № 63-2017. – Київ, 2017.
Повний список літератури знаходиться в редакції.
Тематичний номер «Педіатрія» №4 (43), грудень 2017 р.