19 березня, 2018
Пембролизумаб в первой линии терапии метастатической уротелиальной карциномы
Рак мочевого пузыря – наиболее распространенное онкологическое заболевание мочевыделительной системы, занимающее второе место среди всех злокачественных опухолей мочеполовых органов после рака предстательной железы. Преобладающим гистологическим типом является уротелиальная (переходноклеточная) карцинома, на нее приходится 90% всех злокачественных новообразований мочевого пузыря. Гораздо реже уротелиальный рак берет свое начало в почечной лоханке, мочеточнике или уретре. Приблизительно у 25% пациентов на момент первичной диагностики уже имеется инвазия в мышечный слой, а у 4% присутствуют метастазы [1].
До внедрения современных схем химиотерапии (ХТ) медиана общей выживаемости (ОВ) у пациентов с метастатической уротелиальной карциномой не превышала 6 мес. Системная ХТ позволяет достичь медианы ОВ 9-15 мес и на сегодняшний день является стандартным подходом к лечению неоперабельной местнораспространенной или метастатической уротелиальной карциномы [2].
Стоит отметить, что ряд клинических и молекулярных характеристик коррелируют с выживаемостью пациентов. Прогностические маркеры имеют большое значение для интерпретации клинических исследований и выявления пациентов, проведение терапии у которых будет наиболее эффективно. Так, плохой функциональный статус и наличие висцеральных метастазов (печень, легкие, костная ткань) ассоциированы с плохой выживаемостью.
Стандартом первой линии терапии пациентов с метастатическим уротелиальным раком мочевого пузыря и мочевыводящих путей является ХТ на основе цисплатина, включающая режимы MVAC, GC, PGC. В рандомизированном исследовании режим MVAC продемонстрировал преимущество перед монотерапией цисплатином, показав значительное увеличение частоты общего ответа (39 против 12%), медианы выживаемости без прогрессирования (10 против 4 мес) и медианы ОВ (13 против 8 мес). В связи с этим режим MVAC был утвержден для использования в первой линии терапии. С целью улучшения терапевтических возможностей оценивалась также интенсификация дозы MVAC (ddMVAC каждые 2 недели) при поддержке гранулоцитарным колониестимулирующим фактором.
В ходе рандомизированного исследования III фазы сравнивались режимы MVAC и ddMVAC, при медиане наблюдения 7,3 года ОВ составила 13,2 и 24,6% соответственно. Кроме того, при интенсификации дозы отмечалось уменьшение токсичности лечения. Согласно руководству Национальной онкологической сети США (NCCN) 2018 г., обычный режим MVAC уже не рекомендован при данной патологии. Токсичность является серьезной проблемой для пациентов пожилого возраста и больных с наличием сопутствующей патологии. Сопроводительная терапия гранулоцитарным колониестимулирующим фактором улучшает ситуацию, особенно в отношении миелосупрессии и мукозита.
Комбинация гемцитабина и цисплатина (GC) имеет схожую эффективность, но характеризуется меньшей токсичностью по сравнению с MVAC. Добавление третьего агента (паклитаксела) к GC показало свое преимущество у пациентов с происхождением опухоли из мочевого пузыря, таким образом режим PGC является еще одним вариантом терапии пациентов с метастатическим уротелиальным раком [3].
Более половины больных не могут получать ХТ на основе цисплатина в связи с нарушением функции почек, плохим функциональным статусом или наличием других сопутствующих состояний, включая нарушение слуха, нейропатию и сердечную недостаточность. Альтернативным вариантом для таких пациентов является режим ХТ на основе карбоплатина, предпочтение отдается его сочетанию с гемцитабином. ОВ при этом составляет 9 мес, 21% пациентов прекращают лечение в связи с неприемлемой токсичностью.
Около 50% пациентов с распространенным уротелиальным раком не могут получать ХТ, что подчеркивает потребность в эффективных альтернативных вариантах первой линии терапии.
Исходя из результатов исследований, злокачественные новообразования с большим количеством соматических мутаций лучше отвечают на терапию ингибиторами контрольных точек. По данным «Атласа ракового генома», рак мочевого пузыря находится на третьем месте по количеству мутаций, следовательно, ингибиторы контрольных точек будут эффективны при этом виде онкологического заболевания [1].
Рецептор PD‑1 является терапевтической мишенью при раке мочевого пузыря, в особенности у пациентов с рецидивом уротелиального рака на поздних стадиях. Рецептор PD‑1 и его лиганды, PD-L1 и PD-L2, экспрессируются опухолевыми клетками, взаимодействие рецептора с его лигандами приводит к подавлению функции эффекторных Т-клеток и позволяет опухолевым клеткам уклоняться от иммунной системы.
Пембролизумаб – антитело, действие которого направленно на PD‑1, – обладает выраженной противоопухолевой активностью в отношении нескольких типов опухолей, и при этом характеризуется благоприятным профилем безопасности. В ходе исследования I фазы KEYNOTE‑012 у пациентов с PD-L1-положительным прогрессирующим уротелиальным раком был получен ответ на пембролизумаб в 26% случаев. В исследовании III фазы KEYNOTE‑045 пембролизумаб улучшил ОВ по сравнению с ХТ (10 против 7 мес, p=0,0022) у пациентов с рецидивирующим прогрессирующим уротелиальным раком во второй линии терапии. Другие представители этой группы препаратов, такие как ниволумаб (ингибитор PD‑1) и атезолизумаб (ингибитор PD-L1), также обладают активностью при распространенном уротелиальном раке.
В ходе исследования ІІ фазы KEYNOTE‑052 получены данные об эффективности пембролизумаба в первой линии терапии у пациентов с местнораспространенным и неоперабельным или метастатическим уротелиальным раком почечной лоханки, мочеточника, мочевого пузыря или уретры, которые не могут получать цисплатин по тем или иным причинам [4].
В исследование были включены больные ≥18 лет с гистологически или цитологически подтвержденным локально распространенным и неоперабельным или метастатическим уротелиальным раком почечной лоханки, мочеточника, мочевого пузыря или мочеиспускательного канала. Невозможность проведения ХТ на основе цисплатина определялась такими показателями: функциональный статус ECOG 2, клиренс креатинина 30-60 мл/мин, потеря слуха по данным аудиометрии 2 и более степени, периферическая нейропатия или сердечная недостаточность III степени. В исследовании приняли участие пациенты, которые ранее не получали системной ХТ или у которых наблюдалось прогрессирование заболевания через 12 мес после периоперационной ХТ на основе платины. Критериями также были возможность измерения опухоли (RECIST, версия 1.1), функциональный статус ECOG 0-2, приемлемые показатели крови (абсолютное количество нейтрофилов, тромбоциты и гемоглобин), функции почек (креатинин или клиренс креатинина) и печени (общий билирубин, аспартатаминотрансфераза и аланинаминотрансфераза), а также ожидаемая продолжительность жизни >3 мес.
В качестве первичной конечной точки был выбран объективный ответ (полный или частичный ответ согласно RECIST, версия 1.1, по оценке независимой централизованной радиологической проверки) у пациентов с экспрессией PD-L1. В ходе исследования протокол был изменен, что позволило включить в анализ пациентов независимо от их PD-L1-статуса. Вторичные конечные точки включали оценку ответа у пациентов с высокой экспрессией PD-L1, а также ОВ, выживаемость без прогрессирования, безопасность и переносимость терапии.
В исследование было включено 374 пациента, из них 370 получили как минимум одну дозу пембролизумаба. На момент анализа данных (сентябрь 2016 г.) 63% пациентов прекратили лечение, а 37% все еще продолжали прием пембролизумаба, при этом медиана лечения составила 3 мес, а медиана наблюдения – 5 мес.
У 29% из 370 пациентов был получен объективный ответ, медиана времени до ответа на терапию составляла 2 мес (95% доверительный интервал – ДИ – 2,0-2,1) (табл.) [5]. Контроль над заболеванием был достигнут у 47% пациентов. На момент промежуточного анализа медиана продолжительности ответа не была достигнута (95% ДИ, 12 мес – не достигнуто), ответ на терапию продолжался у 67% пациентов. По результатам исследования, 6-месячная выживаемость без прогрессирования составила 30%, а 6-месячная ОВ – 67% (95% ДИ 62-73) (рис.).
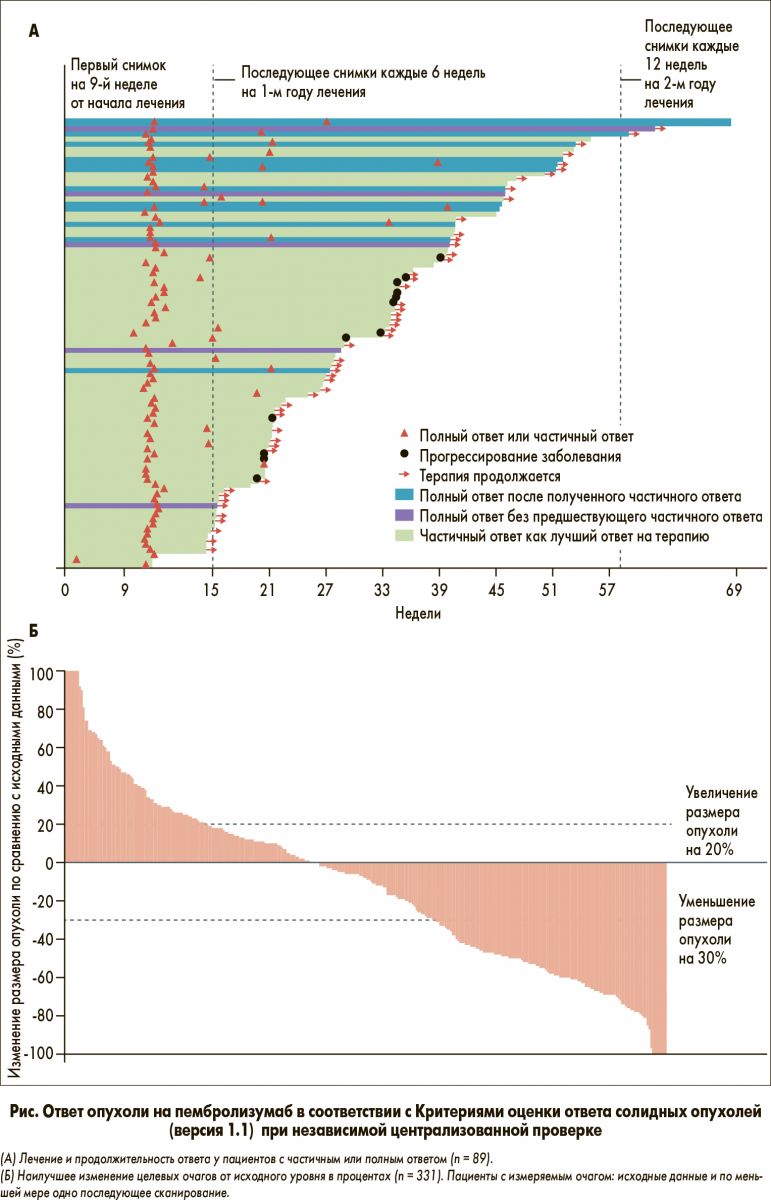 Экспрессия PD-L1 при уротелиальной карциноме коррелирует с результатами терапии пембролизумабом. Ее оценивали с помощью индекса CPS (Combined positive score – процент опухолевых клеток, макрофагов или лимфоцитов c экспрессией PD-L1). В зависимости от показателя CPS (экспрессии PD-L1) количество пациентов с низким (<1%), средним (1-10) и высоким (>10%) показателями составило 17, 52 и 30% соответственно. Объективный ответ у пациентов с высоким уровнем экспрессии PD-L1 достиг 51%, при этом у 18% пациентов был получен полный ответ.
Экспрессия PD-L1 при уротелиальной карциноме коррелирует с результатами терапии пембролизумабом. Ее оценивали с помощью индекса CPS (Combined positive score – процент опухолевых клеток, макрофагов или лимфоцитов c экспрессией PD-L1). В зависимости от показателя CPS (экспрессии PD-L1) количество пациентов с низким (<1%), средним (1-10) и высоким (>10%) показателями составило 17, 52 и 30% соответственно. Объективный ответ у пациентов с высоким уровнем экспрессии PD-L1 достиг 51%, при этом у 18% пациентов был получен полный ответ.
В ходе исследования было установлено, что пембролизумаб в первой линии терапии имеет противоопухолевую активность в отношении местнораспространенного, неоперабельного или метастатического уротелиального рака у пациентов, которым цисплатин не может быть назначен. При этом у 29% пациентов был достигнут полный или частичный ответ, а у 19% – стабилизация заболевания. Ответ на терапию не зависел от возраста, функционального статуса по шкале ECOG, локализации первичной опухоли и метастазов, наличия метастазов в печени и от причины, по которой пациент не может получать цисплатин, тем самым демонстрируя активность пембролизумаба у широкого круга пациентов.
Пембролизумаб имел приемлемый профиль безопасности: сообщалось о нескольких побочных эффектах 3 класса или выше, связанных с лечением, которые возникали более чем у одного пациента; только 5% пациентов прекратили лечение из-за возникновения побочных эффектов. Сообщалось о низкой частоте нежелательных явлений, связанных с лечением (10%). Наиболее распространенными побочными явлениями 3 степени и выше были усталость, повышение уровня щелочной фосфатазы, колит и мышечная слабость.
У небольшой доли пациентов (17%) возникали иммунно-опосредованные нежелательные явления, такие как гипотиреоидизм, колит, пневмония, надпочечниковая недостаточность, гепатит, диабетический кетоацидоз, диабет 1 типа и тиреоидит. Большинство из них купировались введением кортикостероидов и протекали без осложнений. Притом что в исследовании KEYNOTE‑052 приняло участие большее количество пациентов пожилого возраста и с худшим функциональным статусом, чем в других исследованиях, посвященных пембролизумабу, профиль безопасности в исследовании согласуется с ранее полученными данными.
Несмотря на то что медиана наблюдения в текущем исследовании была достаточно короткой (9 мес), ответ на пембролизумаб, по всей видимости, является длительным, а препарат переносится лучше по сравнению с цитотоксической ХТ. Например, у 15% пациентов с прогрессирующим уротелиальным раком и противопоказаниями к терапии цисплатином, получавших ХТ на основе карбоплатина (гемцитабин/карбоплатин или метотрексат/карбоплатин/винбластин), возникала выраженная токсичность, включая смертельные случаи.
Схемы лечения на основе карбоплатина были особенно токсичны для пациентов с нарушением функции почек. Таким образом, пембролизумаб может быть применен независимо от функционального статуса почек, в том числе у тех пациентов, которые в противном случае будут получать наилучшую поддерживающую терапию. Этот вывод подтверждается и тем, что в исследовании KEYNOTE‑052 приняло участие большое количество пациентов с нарушением функции почек (59%) и старше 80 лет (29%).
Результаты исследования II фазы IMvigor210 по изучению эффективности атезолизумаба у пациентов с прогрессирующим уротелиальным раком подтвердили целесообразность иммунотерапии у этой популяции пациентов. Однако были некоторые различия между исследованиями IMvigor210 и KEYNOTE‑052. Пациенты в KEYNOTE‑052 были немного старше (21 против 29% больных ≥80 лет) и имели худший соматический статус (висцеральное поражение – 66 против 85%, ECOG 2 – 27 против 41%). В исследовании KEYNOTE‑052 приняло участие большее количество пациентов (374 против 123), что позволило повысить точность оценки объективного ответа и провести более обширную оценку безопасности.
Данные также свидетельствуют о том, что экспрессия PD-L1 служит ценным прогностическим маркером, пациенты с распространенным уротелиальным раком чаще отвечают на анти-PD‑1 или анти-PD-L1 терапию. Экспрессия PD-L1 по меньшей мере на 1% опухолевых или стромальных клеток была предпосылкой для участия пациентов в исследовании I фазы KEYNOTE‑012. При последующем анализе с помощью иммуногистохимического теста PD-L1 22C3 pharmDx экспрессия PD-L1 как на опухолевых, так и на иммунных клетках ассоциировалась с благоприятным ответом на терапию.
Анализ потенциальной значимости высокой экспрессии PD-L1 позволит определить пациентов, для которых терапия пембролизумабом будет наиболее эффективной. В KEYNOTE‑052 дополнительно была изучена взаимосвязь экспрессии PD-L1 (комбинированная положительная оценка) и ответа на терапию. У пациентов с комбинированной положительной оценкой ≥10% ответ на терапию был выше, однако он наблюдался вне зависимости от уровня экспрессии PD-L1. Требуется дальнейшее изучение экспрессии PD-L1 в качестве прогностического маркера. Кроме того, продолжается изучение потенциальных биомаркеров, включая подтипы экспрессии генов и мутационную нагрузку.
Отсутствие контрольной группы ограничивает сравнение пембролизумаба с альтернативными вариантами лечения, включая наилучшую поддерживающую терапию. Сравнение выживаемости также ограничено коротким периодом наблюдения в исследовании KEYNOTE‑052.
Данные подтверждают эффективность пембролизумаба в первой линии терапии пациентов с местнораспространенным и неоперабельным или метастатическим уротелиальным раком, которым противопоказана терапия цисплатином. На момент анализа данных у 82% пациентов ответ на терапию продолжался ≥6 месяцев. Последующее наблюдение позволит лучше понять влияние пембролизумаба в первой линии на ОВ и длительность ответа. Благодаря противоопухолевой активности и благоприятному профилю безопасности пембролизумаб стал новым вариантом лечения пациентов, которые не могут получать терапию цисплатином и не являются подходящими кандидатами для ХТ в целом [4].
Химиотерапия в первой линии лечения пациентов с уротелиальным раком не всегда может быть проведена в связи с плохим функциональным статусом или наличием сопутствующей патологии. Поэтому актуальным является поиск альтернативных вариантов терапии. В исследовании KEYNOTE‑052 пембролизумаб показал активность в отношении уротелиальной карциномы, благодаря чему в 2017 г. FDA США в ускоренном режиме одобрило пембролизумаб для больных местнораспространенным или метастатическим раком, которым не представляется возможным назначение цисплатинсодержащей ХТ. Согласно рекомендациям NCCN от 2018 г., пембролизумаб является одним из вариантов первой линии терапии пациентов с распространенной уротелиальной карциномой.
Литература
1. Bellmunt J. Treatment of metastatic urothelial cancer of the bladder and urinary tract, 2017.
2. NCCN guidelines: bladder cancer version 1.2018.
3. Bladder cancer: ESMO Practice Guidelines for diagnosis, treatment and follow-up, 2014.
4. Balar A.V. First-line pembrolizumab in cisplatin-ineligible patients with locally advanced and unresectable or metastatic urothelial cancer (KEYNOTE‑052): a multicentre, single-arm, phase 2 study, 2018.
5. O’Donnell P.H. Biomarker findings and mature clinical results from KEYNOTE‑052: First-line pembrolizumab (pembro) in cisplatin-ineligible advanced urothelial cancer (UC). ASCO, 2017.
Подготовила Екатерина Марушко
Тематичний номер «Онкологія» № 1 (52), лютий 2018 р.



