20 березня, 2018
Антиметаболиты в терапии рака
 Прошедший 2017 год можно считать юбилейным для метаболомики – науки, которая изучает обмен веществ раковой клетки с целью блокады ее метаболических путей, отвечающих за процессы пролиферации.
Прошедший 2017 год можно считать юбилейным для метаболомики – науки, которая изучает обмен веществ раковой клетки с целью блокады ее метаболических путей, отвечающих за процессы пролиферации.
70 лет назад (в 1947 г.) Сидни Фарбер начал применять антиметаболит аминоптерин, антифолат 1-го поколения, для лечения детей, больных лейкемией.
60 лет назад (в 1957 г.) Чарльз Гейдельберг опубликовал первую статью о новом антипиримидиновом антиметаболите 5-фторурациле.
50 лет назад (в 1967 г.) академик Академии наук Латвийской ССР С. Гиллер синтезировал антипиримидиновый антиметаболит тегафур.
Все эти антиметаболиты и их производные до сих пор остаются уникальными противоопухолевыми агентами и используются при лечении рака различных локализаций.
Аэробный гликолиз
Раковые клетки обладают высокой пролиферативной активностью. Для роста, удвоения ДНК и бесконечного деления им необходимо большое количество строительных материалов (макромолекул), а также энергии в виде аденозинтрифосфорной кислоты.
Чтобы обеспечить избыточные физиологические потребности, раковые клетки способны изменять свой метаболизм. Этот эффект был назван «метаболическим перепрограммированием». Он относится к 10 основным признакам опухолевого роста, описанным Douglas Hanahan и Robert Weinberg в журнале Cell (Hallmarks of Cancer: The Next Generation, Cell, 2011).
Первым обнаружил уникальные метаболические способности злокачественных клеток Отто Варбург (лауреат Нобелевской премии 1931 г.). Эффект, который он открыл, носит его имя и называется аэробным гликолизом. Варбург показал, что раковые клетки потребляют глюкозу в 10 раз больше, чем нормальные, и даже в аэробных условиях активно производят недоокисленный лактат. Такой способ расщепления глюкозы характерен только для злокачественных клеток. Это быстрый, но неэффективный путь производства энергии.
Сегодня блокада эффекта Варбурга в раковой клетке является одним из наиболее перспективных направлений экспериментальной онкологии, а сам аэробный гликолиз служит возможной терапевтической мишенью противоопухолевой терапии.
Нарушение биосинтеза макромолекул
Однако полностью объяснить механизм канцерогенеза нарушенным метаболизмом глюкозы невозможно. Аэробного гликолиза и повышения синтеза лактата недостаточно для построения цитоскелета быстро пролиферирующих клеток.
Метаболическое перепрограммирование в злокачественной клетке касается не только расщепления глюкозы, запасов аденозинтрифосфорной кислоты, но и нарушения биосинтеза всех четырех классов макромолекул (углеводов, белков, липидов и нуклеиновых кислот).
Одной из перспективных терапевтических противоопухолевых стратегий является блокирование синтеза внутриклеточных нуклеотидов.
Первыми противоопухолевыми антиметаболитами, направленными на ингибицию синтеза ДНК в раковой клетке, были антифолаты и антипиримидины.
Антифолаты аминоптерин, метотрексат, пеметрексед
В 40-х годах прошлого столетия в лаборатории Lederle (сегодня – лаборатория компании Pfizer) было обнаружено, что фолиевая кислота является активным метаболитом и резко ускоряет рост бактерий, выделенных из говяжьей печени.
Yellapragada Subbarow, индийский биохимик, работавший в этой лаборатории, был первым, кто вначале синтезировал фолиевую кислоту, затем – ее аналог аминоптерин (4-аминофолиевую кислоту), а впоследствии и метотрексат, антифолат 2-го поколения.
Это позволило Сидни Фарберу, основоположнику современной противоопухолевой терапии, совершить одно из первых революционных открытий в клинической онкологии.
 Фарбер показал, что антагонист фолиевой кислоты аминоптерин вызывает полную ремиссию заболевания у детей, страдающих острым лейкозом. Несколько позже Jane C. Wright изучила действие метотрексата на клетки рака молочной железы и доказала преимущества антифолатов 2-го поколения перед аминоптерином. Более 30 лет ушло на поиски нового препарата, который был бы лучше, чем метотрексат. В 2004 г. в лаборатории американской компании Eli Lilly Edward C. Taylor создал антифолат 3-го поколения – пеметрексед, который способен ингибировать три внутриклеточных фермента, участвующих в синтезе пуриновых и пиримидиновых оснований, – тимидилатсинтазу (TS), дигидрофолатредуктазу (DHFR) и формилтрансферазу (GARFT). Блокада этих ферментов в S-фазе клеточного цикла препятствует образованию ДНК и РНК и ведет к необратимой смерти раковой клетки.
Фарбер показал, что антагонист фолиевой кислоты аминоптерин вызывает полную ремиссию заболевания у детей, страдающих острым лейкозом. Несколько позже Jane C. Wright изучила действие метотрексата на клетки рака молочной железы и доказала преимущества антифолатов 2-го поколения перед аминоптерином. Более 30 лет ушло на поиски нового препарата, который был бы лучше, чем метотрексат. В 2004 г. в лаборатории американской компании Eli Lilly Edward C. Taylor создал антифолат 3-го поколения – пеметрексед, который способен ингибировать три внутриклеточных фермента, участвующих в синтезе пуриновых и пиримидиновых оснований, – тимидилатсинтазу (TS), дигидрофолатредуктазу (DHFR) и формилтрансферазу (GARFT). Блокада этих ферментов в S-фазе клеточного цикла препятствует образованию ДНК и РНК и ведет к необратимой смерти раковой клетки.
Поскольку фермент GARFT наиболее активен в опухолевых клетках, пеметрексед действует именно на них и значительно меньше влияет на метаболизм нормальных клеток. Можно считать, что пеметрексед действует как таргетный препарат.
Клиническое применение антифолатов
Несмотря на то что метотрексат был синтезирован в 1940-х годах, этот препарат и сегодня активно используется как в онкологии, так и при лечении некоторых аутоиммунных заболеваний.
Основными показаниями для использования метотрексата являются острый лимфолейкоз, рак вульвы и шейки матки, рак пищевода, рак головы и шеи, почечной лоханки, мочеточников, саркома Юинга, герминогенные опухоли, а также рак легкого и рак молочной железы.
Основными показаниями для применения пеметрекседа являются злокачественная нерезектабельная мезотелиома плевры и немелкоклеточный неплоскоклеточный рак легкого.
Согласно рекомендациям ESMO 2016 и NCCN 2017, пеметрексед может быть использован как у пациентов с удовлетворительным соматическим статусом (PS0-1) в комбинациях с бевацизумабом, карбоплатином, цисплатином, так и при PS2 в виде дуплета (карбоплатин/пеметрексед) или в режиме монотерапии.
Современные рекомендации расширяют показания к назначению пеметрекседа как в первой, так и во второй линии терапии немелкоклеточного рака легкого (НМРЛ). Основные тенденции применения препарата – лечение пациентов с заболеванием не только IV, но и I-IIIA (максимум IIIB) стадии. Использование пеметрекседа в первой линии терапии неметастатического рака легкого показало его максимальную эффективность наряду с удовлетворительной переносимостью в сравнении с таксан- и гемцитабинсодержащими схемами.
У больных НМРЛ IV стадии c EGFR- или ALK-негативными карциномами пеметрексед демонстрирует такую же эффективность, как эрлотиниб.
Важной положительной чертой пеметрекседа является его высокая эффективность в качестве поддерживающей терапии больных с местнораспространенным или метастатическим неплоскоклеточным НМРЛ, у которых не было прогрессирования заболевания после химиотерапии препаратами платины.
Сегодня активно изучаются показания к назначению пеметрекседа при внелегочных локализациях рака – в частности, при раке молочной железы.
Антипиримидины
Пиримидины – гетероциклические соединения, производные которых участвуют во многих важных биологических процессах и широко распространены в живой природе. Такие производные пиримидинов, как цитозин, тимин и урацил, входят в состав нуклеотидов, из которых состоят нуклеиновые кислоты.
Нуклеиновые кислоты (ДНК и РНК) присутствуют в клетках всех живых организмов и участвуют в хранении и передаче наследственной информации.
Пиримидиновое основание урацил (2,4-диоксопиримидин) является компонентом РНК и, как правило, отсутствует в ДНК. В составе нуклеиновых кислот урацил может связываться с аденином.
Название «урацил» придумал немецкий химик Robert Behrend в 1885 г., а итальянец Alberto Ascoli в 1900 г. выделил урацил путем гидролиза дрожжей.
Установлено, что на поверхности Титана, крупнейшего спутника планеты Сатурн, содержится урацил. Данные, полученные из метеорита Мерчисона и миссии «Кассини» на основании анализа соотношения углерода 12С/13С, позволяют сделать вывод, что урацил имеет внеземное происхождение.
В 1955 г. Abraham Cantarow и Karl E. Paschkis, экспериментируя с культурой клеток первичной гепатомы, установили, что клетки рака печени быстрее накапливают радиоактивный урацил, чем нормальные гепатоциты. Два года спустя в журнале Nature Чарльз Гейдельбергер и соавт. опубликовали статью о новом классе противоопухолевых препаратов – фторпиримидинах (C. Heidelberger, N.K. Chaudhuri, P. Danneberg et al., March 1957. Fluorinated pyrimidines, a new class of tumour-inhibitory compounds. Nature 179 (4561): 663-6).
Известно, что фторпиримидины, как и урацил, быстро проникают в клетку и ингибируют процесс деления путем блокирования синтеза ДНК (за счет угнетения фермента тимидилатсинтетазы) и образования структурно несовершенной РНК (за счет внедрения фторурацила в ее структуру).
Внутри клетки фторурацил превращается в несколько активных метаболитов: фтордезоксиуридина монофосфат (FdUMP), фтордезоксиуридина трифосфат (FdUTP) и фторуридина трифосфат (FUTP). Именно эти активные метаболиты нарушают синтез РНК и действие тимидилатсинтазы.
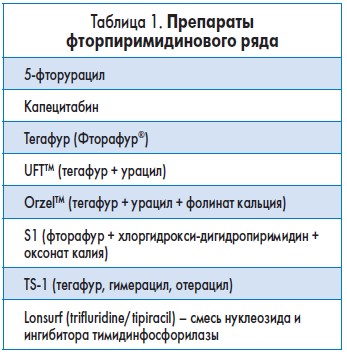
Сегодня препараты фторпиримидинового ряда широко представлены в клинической онкологии (табл. 1).
 Среди всех препаратов фторпиримидинового ряда особо следует выделить препарат тегафур, который был синтезирован С.А.
Среди всех препаратов фторпиримидинового ряда особо следует выделить препарат тегафур, который был синтезирован С.А.
Гиллером, академиком Академии наук Латвийской ССР в 1967 г.
Тегафур отличается от 5-фторурацила наличием тетрагидрофурановой группы, которая делает препарат липофильным водорастворимым соединением. Липофильная группа способствует проникновению тегафура через клеточные мембраны, включая гематоэнцефалический барьер.
Метаболический путь тегафура зависит от растворимых энзимов тимидин- и уридинфосфорилазы, концентрация которых в опухолях выше, чем в нормальных тканях. Высокий уровень тимидинфосфорилазы в раковых клетках обеспечивает образование 5-фторурацила непосредственно в опухоли.
Благодаря липофильной группе препарат избирательно накапливается в опухолевых тканях и не распространяется во внеклеточное пространство. Это способствует меньшему количеству побочных эффектов со стороны здоровых тканей.
Основные отличия 5-фторурацила и тегафура представлены в таблице 2.
Одним из основных клинических исследований по прямому сравнению эффективности длительной инфузии 5-фторурацила и перорального приема тегафура является исследование Is oral tegafur with leucovorin equivalent to intravenous 5-fluorouracil and leucovorin in colorectal cancer? (Friberg G., Schilsky R.L. Nat Clin Pract Oncol, 2006; 3(5): 240-1). Сегодня на ресурсе ClinicalTrials.gov есть информация о 90 продолжающихся клинических исследованиях по изучению эффективности тегафура и тегафурсодержащих комбинаций медикаментов при различных локализациях рака.
В Украине антиметаболит тегафур рекомендован для клинического применения при раке шейки матки (приказ МЗ Украины от 02.04.2014 № 236), колоректальном раке (приказ МЗ Украины от 12.07.2016 № 703), раке желудка, раке печени и раке анального канала (приказ МЗ Украины от 17.09.2007 № 554), а также раке молочной железы (приказ МЗ Украины от 29.04.2011 № 247).
Интерес к теме опухолевого метаболизма менялся на протяжении последнего столетия. На основе ранних исследований O. Варбурга было создано фундаментальное учение о различиях метаболизма в нормальной и раковой клетке. Тем не менее этих научных данных оказалось недостаточно, чтобы объяснить канцерогенез с позиций нарушения расщепления и утилизации глюкозы. Интерес к открытым протоонкогенам и генам-супрессорам надолго остановил научные исследования опухолевого метаболизма.
В последние годы снова появился интерес к этой проблеме. Стало ясно, что многие сигнальные пути управляют внутриклеточным обменом веществ, а генетические мутации в этих путях оказывают глубокое влияние на метаболизм макромолекул, изменяя его.
Изучение метаболизма рака и воздействие на метаболические пути раковой клетки являются наиболее актуальными и перспективными направлениями современной онкологии.
Справка ЗУ
В Украине тегафур представлен оригинальным лекарственным средством Фторафур® производства международного вертикально-интегрированного предприятия стран Балтии – АО «Гриндекс», Латвия. Фторафур® показан для лечения рака молочной железы, желудка, шейки матки, колоректального рака и кожных лимфом.
Применение препарата Фторафур® обосновано отраслевыми стандартами МЗ Украины и имеет фармакоэкономические выгоды
(K. Gerasimova et al., 2014).
Тематичний номер Онкологія № 1 (52) лютий 2018 р.