6 квітня, 2018
Резистентность к антибиотикам и противовирусным препаратам: пути ее преодоления
 Проблема антибиотикорезистентности уже вышла за рамки сугубо медицинской – сегодня к ней приковано внимание на самом высоком международном уровне: вопросы, связанные с угрожающими темпами распространенности устойчивости патогенных микроорганизмов к имеющимся на сегодняшний день антибактериальным средствам, регулярно обсуждаются на уровне глав ведущих мировых держав, Организации Объединенных Наций (ООН) и Всемирной организации здравоохранения (ВОЗ). Так, 21 сентября 2016 года вопрос глобальной антибиотикорезистентности был рассмотрен на Генеральной Ассамблее ООН в г. Нью-Йорке. Главы государств взяли обязательства скоординировать свои действия, направленные на преодоление устойчивости возбудителей к антимикробным препаратам.
Проблема антибиотикорезистентности уже вышла за рамки сугубо медицинской – сегодня к ней приковано внимание на самом высоком международном уровне: вопросы, связанные с угрожающими темпами распространенности устойчивости патогенных микроорганизмов к имеющимся на сегодняшний день антибактериальным средствам, регулярно обсуждаются на уровне глав ведущих мировых держав, Организации Объединенных Наций (ООН) и Всемирной организации здравоохранения (ВОЗ). Так, 21 сентября 2016 года вопрос глобальной антибиотикорезистентности был рассмотрен на Генеральной Ассамблее ООН в г. Нью-Йорке. Главы государств взяли обязательства скоординировать свои действия, направленные на преодоление устойчивости возбудителей к антимикробным препаратам.
Одними из ведущих причин роста антибиотикорезистентности, как известно, являются нерациональная антибиотикотерапия, а также назначение антибактериальных препаратов при отсутствии каких-либо показаний к их применению. О том, какой вклад в борьбу с распространением антибиотикорезистентности могут сделать практикующие врачи, в рамках научно-практической конференции «Современная педиатрия с позиций доказательной медицины» (8-9 ноября 2017 года, г. Львов) рассказал в своем выступлении заведующий кафедрой инфекционных болезней Национальной медицинской академии последипломного образования имени П.Л. Шупика, доктор медицинских наук, профессор Александр Константинович Дуда.
– Ключевой причиной развития резистентности служит бесконтрольное и чрезмерное использование антибиотиков в медицине, ветеринарии, сельском хозяйстве и животноводстве. По оценке Экспертной комиссии по борьбе с антибиотикорезистентностью (США), в мире ежегодно используется 73 млрд разовых доз, или 300 тыс. тонн антибиотиков.
Если мы не сумеем снизить растущие темпы распространения антибиотикорезистентности, то, согласно оценкам Комитета экспертов ВОЗ (2016), уже к 2050 г. именно по этой причине мир будет терять до 10 млн человек ежегодно. В первую очередь это связано с тем, что темпы приобретения антибиотикорезистентности возбудителями серьезных инфекций резко превышают темпы разработки принципиально новых антибактериальных средств. Что же касается сегодняшних реалий, то, согласно официальным оценкам, по причине резистентности к антибиотикам и невозможности вылечить различные инфекции в мире ежегодно умирает не менее 700 тыс. человек.
В странах Европейского союза от инфекций, вызванных антибиотикорезистентными бактериями, ежегодно погибают более 25 тыс. человек, а финансовые затраты на лечение таких инфекций превосходят 1,5 млрд евро в год. Особенно тревожной становится ситуация с заболеваемостью и смертностью от мультирезистентного туберкулеза: в настоящее время в 105 странах мира циркулируют возбудители этого заболевания, устойчивые сразу к нескольким противотуберкулезным препаратам. Согласно данным ВОЗ, в 2014 г. такие штаммы Mycobacterium tuberculosis были идентифицированы у 480 тыс. человек.
На переднем крае борьбы с распространением антибиотикорезистентности, безусловно, находятся врачи общей практики – семейные врачи, участковые терапевты и педиатры. Эксперты ВОЗ подчеркивают, что именно от врачей общей практики зависит, насколько разумной окажется политика применения антибиотиков в масштабах всей страны. Сдержать темпы распространения антибиотикорезистентности к существующим антибактериальным препаратам можно только путем строгого соблюдения принципов рациональной антибиотикотерапии.
Основными причинами возникновения резистентности патогенных бактерий к назначаемым антибактериальным препаратам являются:
- неумелое использование антибактериальных препаратов (несобюдение курса лечения, доз);
- назначение эмпирической антибактериальной терапии без адекватного выявления возбудителя;
- трудности своевременной и точной идентификации патогенных микроорганизмов.
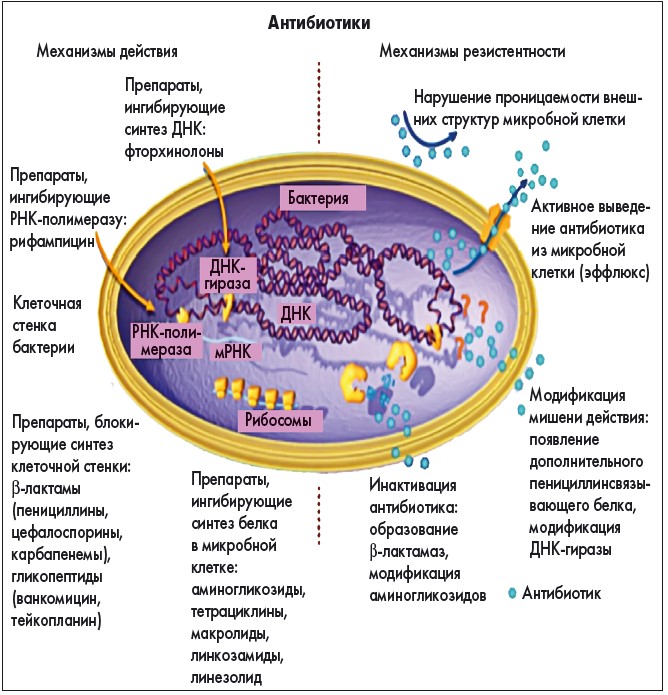
Благодаря усилиям ученых и фармацевтической индустрии в распоряжении врачей сегодня имеется несколько классов антибактериальных препаратов с различными механизмами действия. Однако патогенные бактерии, в свою очередь, уже успели выработать немалое количество механизмов резистентности к применяемым антибиотикам (рис.).
Рис. Механизмы действия антибиотиков
и механизмы формирования резистентности к ним
При этом известно, что бактерии, которые приобрели гены антибиотикорезистентности, способны передавать их другим штаммам.
Помимо передачи генов антибиотикорезистентности, огромной проблемой в настоящее время является формирование так называемых биопленок – симбиоза микроорганизмов, погруженных в выделяемый ими внеклеточный белково-полисахаридный матрикс.
Стадии развития бактериальных пленок:
1 – первоначальное закрепление бактерий на поверхности ткани;
2 – фиксация;
3 – созревание;
4 – образование взрослой биопленки в белково-полисахаридном каркасе;
5 – выброс бактерий/спор и образование новых колоний биопленок.
Следует отметить, что применение антибиотиков наиболее эффективно на первых трех стадиях формирования биопленок, в то время как воздействие на уже сформированную, зрелую биопленку и ее новые колонии представляет собой крайне сложную задачу, в особенности если речь идет о тяжелых гнойно-септических инфекциях.
Очень часто формирование биопленок связано с врачебными манипуляциями, процедурами и оперативными вмешательствами, такими как эндопротезирование тазобедренного сустава, операции на клапанах сердца, катетеризация центральных вен, установка мочевых катетеров. К числу патогенных микроорганизмов, наиболее часто образующих биопленки, относят Staphylococcus aureus, коагулазонегативные стафилококки, Enterococcus spp., Klebsiella pneumoniae и Pseudomonas aeruginosa.
В силу своей высокой распространенности в популяции очень значимой клинической проблемой остаются инфекции нижних дыхательных путей (ИНДП). В настоящее время установлено, что наряду с патогенными бактериями в их этиологической структуре весомую роль играют респираторные вирусы и вирусно-бактериальные ассоциации.
Наиболее распространенными вирусными возбудителями ИНДП являются коронавирусы, риновирусы, а также вирусы гриппа и парагриппа. На этапе первичного обследования пациента врачу необходимо принять решение о том, в каких условиях проводить лечение – амбулаторно или в стационаре. Амбулаторное ведение показано пациентам с сезонными острыми респираторно-вирусными инфекциями (ОРВИ) или гриппом (при продолжительности симптомов <48 ч) без признаков поражения нижних дыхательных путей (НДП) и тяжелой сопутствующей патологии. Госпитализации подлежат пациенты с подозрением на пандемический грипп и/или с наличием признаков поражения НДП, а также дыхательной недостаточности. Признаками, указывающими на тяжесть состояния, являются частота дыхательных движений 25 в 1 мин и тахикардия 100 уд./мин. Госпитализация также показана пациентам с сопутствующими заболеваниями, повышающими риск развития осложнений. На этапе стационарного лечения пациентам с гриппом рекомендовано назначение специфических противовирусных препаратов при длительности симптомов заболевания <48 ч.
Одним из весомых факторов развития антибиотикорезистентности при ОРВИ является нерациональное применение антибактериальных средств.
Среди этиотропных лекарственных средств, применяемых в лечении гриппа и ОРВИ, выделяют противовирусные препараты прямого действия (озельтамивир и занамивир), которые ингибируют процесс внедрения вирусов в клетки и их репликацию, а также препараты опосредованного действия, активирующие клеточные механизмы противовирусной защиты (интерферон и его индукторы).
Противовирусные препараты прямого действия имеют узкий спектр противовирусной активности и высокоэффективны в случае его точного соответствия возбудителю, поэтому они применяются только с целью лечения гриппа, вызванного вирусами гриппа А и В. Интерферон и его индукторы характеризуются широким спектром противовирусного действия, что дает возможность применять их при различных ОРВИ.
! В настоящее время все шире применяется препарат Циклоферон® – низкомолекулярный индуктор интерферона, обладающий широким спектром биологической активности: противовирусной, иммуномодулирующей, противовоспалительной.
Циклоферон® представляет собой оригинальный лекарственный препарат, химическая структура которого не имеет аналогов в мире. Он может применяться как парентерально (в форме раствора для инъекций), так и перорально (в форме таблеток). Циклоферон® индуцирует высокие титры α-, β- и γ-ИНФ в органах и тканях, которые содержат лимфоидные элементы (слизистой оболочке тонкого кишечника, селезенке, печени, легких), реализуя таким образом свое противовирусное действие.
Иммуномодулирующий эффект препарата Циклоферон® выражается в активации фагоцитоза, естественных киллерных клеток, цитотоксичных Т-лимфоцитов и коррекции иммунного статуса организма при иммунодефицитных состояниях различного происхождения. Противовоспалительное действие препарата обусловлено стимуляцией нейтрофилов периферической крови с увеличением их противовоспалительного потенциала.
Циклоферон® циркулирует в крови в свободном и/или связанном с белками состоянии и способен проникать через гематоэнцефалический барьер. Этот препарат может назначаться при различных вирусных и вирусно-бактериальных инфекциях, а также в комплексной терапии целого ряда острых и хронических бактериальных инфекций в качестве компонента иммунотерапии.
! Циклоферон® разрешен к применению у детей в возрасте старше 4 лет.
Безусловно, приоритетный интерес для врачей первичного звена здравоохранения представляют возможности профилактического применения препарата Циклоферон® в периоды сезонного подъема заболеваемости ОРВИ.
! Эффективность применения препарата Циклоферон® как средства экстренной профилактики в организованных коллективах в период повышенной заболеваемости ОРВИ и гриппом доказана в рамках многоцентровых рандомизированных контролируемых постмаркетинговых исследований, включая клинико-эпидемиологические исследования с участием 22 510 человек.
На фоне приема Циклоферона частота осложнений после перенесенного гриппа уменьшается в 20 раз (табл.).
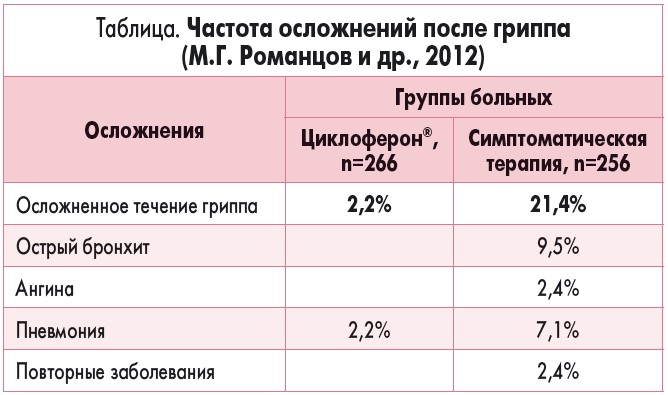 Для профилактики ОРВИ или гриппа Циклоферон® назначают внутрь по 2-4 таблетки на прием в 1, 2, 4, 6 и 8-е сутки приема. У больных со сниженной иммунной защитой с этой целью Циклоферон® рекомендуют принимать по 2 таблетки на прием в 1, 2, 4, 6, 8, 11, 14, 17, 20 и 23-и сутки. Детям Циклоферон® назначают в возрастной дозировке: от 4 до 6 лет – по 0,15 г (1 таблетка), от 7 до 11 лет – по 0,3-0,45 г (2-3 таблетки), старше 12 лет – по 0,45-0,6 г (3-4 таблетки) на прием в 1, 2, 4, 6, 8, 11, 14, 17, 20 и 23-и сутки.
Для профилактики ОРВИ или гриппа Циклоферон® назначают внутрь по 2-4 таблетки на прием в 1, 2, 4, 6 и 8-е сутки приема. У больных со сниженной иммунной защитой с этой целью Циклоферон® рекомендуют принимать по 2 таблетки на прием в 1, 2, 4, 6, 8, 11, 14, 17, 20 и 23-и сутки. Детям Циклоферон® назначают в возрастной дозировке: от 4 до 6 лет – по 0,15 г (1 таблетка), от 7 до 11 лет – по 0,3-0,45 г (2-3 таблетки), старше 12 лет – по 0,45-0,6 г (3-4 таблетки) на прием в 1, 2, 4, 6, 8, 11, 14, 17, 20 и 23-и сутки.
Таким образом, применение препарата Циклоферон® в профилактике и лечении целого ряда вирусных инфекций открывает новые возможности для того, чтобы снизить частоту необоснованного назначения антибиотиков.
Циклоферон® обладает высокой эффективностью и безопасностью, которая доказана в многочисленных клинических исследованиях – на сегодняшний день их насчитывается уже более 200. Циклоферон® производится в полном соответствии с требованиями Надлежащей производственной практики (GMP) и применяется в более чем 15 странах. Преимущества препарата Циклоферон® были по достоинству оценены и украинскими врачами – в нашей стране он успешно используется на протяжении уже более 18 лет.
Подготовили Елена Терещенко и Марина Титомир
Тематичний номер «Педіатрія» №1 (44), березень 2018 р.