14 травня, 2018
Гіперкаліємія в клінічній практиці. Індивідуалізація корекції гіперкаліємії: точка зору нефролога
 Калій є одним із найважливіших мікроелементів в людському організмі, при цьому більша його частина (приблизно 98%) міститься в клітинах. Калій задіяний у регуляції кислотно-лужної рівноваги крові, водного балансу міжклітинної і внутрішньоклітинної рідини, водно-сольового балансу, осмотичного тиску.
Калій є одним із найважливіших мікроелементів в людському організмі, при цьому більша його частина (приблизно 98%) міститься в клітинах. Калій задіяний у регуляції кислотно-лужної рівноваги крові, водного балансу міжклітинної і внутрішньоклітинної рідини, водно-сольового балансу, осмотичного тиску.
Калій також забезпечує створення мембранного потенціалу, необхідного для скорочення скелетних і серцевого м’язів, бере участь у передачі нервових імпульсів і в нервовій регуляції серцевих скорочень. Окрім того, він активує роботу деяких ферментів, вуглеводний і білковий обмін, є необхідним для синтезу білка, перетворення глюкози в глікоген, видільної функції нирок, до того ж покращує перистальтику кишечника [1-2].
Гіперкаліємія – тобто підвищення концентрації іонів калію в сироватці крові до ≥5,5 ммоль/л (норма 3,5-5,5 ммоль/л) – доволі поширена клінічна проблема, яка зазвичай є результатом порушення екскреції калію із сечею при гострій або хронічній хворобі нирок (ГХН, ХХН). Також на рівень калію в організмі людини може впливати прийом деяких лікарських засобів. В останні десятиліття ця проблема набула неабиякої актуальності внаслідок широкого і не завжди обґрунтованого застосування препаратів – інгібіторів ренін-ангіотензин-альдостеронової системи (іРААС) [3].
Гіперкаліємія класифікується за рівнем сироваткового калію (K+): м’яка (5,5-6,5 ммоль/л), помірна (6,5-7,5 ммоль/л) і тяжка (>7,5 ммоль/л). Частота випадків гіперкаліємії в загальній популяції невелика і становить 2,6-3,2%, тоді як у хворих зі зниженою швидкістю клубочкової фільтрації (ШКФ) – значно збільшується. Дослідження, яке тривало майже п’ять років (2005-2009), за участю 36 359 пацієнтів (м. Клівленд, штат Огайо, США) зі ШКФ <60 мл/хв/1,73 м2, показало, що в 11% хворих рівень калію перевищує 5,0 ммоль/л [4].
Диференційована оцінка частоти гіперкаліємії залежно від ШКФ виявила, що при ШКФ 37 мл/хв/1,73м2 вона спостерігалась у 9-10% хворих, при ШКФ 14,6 мл/хв/1,73 м2 частота випадків підвищення рівня калію сироватки крові до 5,0 та 5,5 ммоль/л склала 54 і 40% відповідно, тобто частота випадків розвитку гіперкаліємії зворотно пропорційна ШКФ [5].
На сьогодні доведено, що найвищому ризику гіперкаліємії піддаються хворі з низькими показниками ШКФ, яким призначена терапія за допомогою іРААС [4, 5]. У хворих з анурією, до яких застосовано діалізні методи, частота гіперкаліємії становить 12,5%, у пацієнтів з трансплантованою ниркою – від 34 до 73%, залежно від прийому інгібіторів кальциневрину.
У чому полягає небезпека підвищення рівня калію в сироватці крові для нефрологічного хворого? В багатьох дослід женнях продемонстровано, що як гіпо-, так і гіперкаліємія підвищують ризик смерті у хворих на ХХН (U-подібна крива на рис. 1) як на додіалізному, так і на діалізному етапах лікування [5, 6].
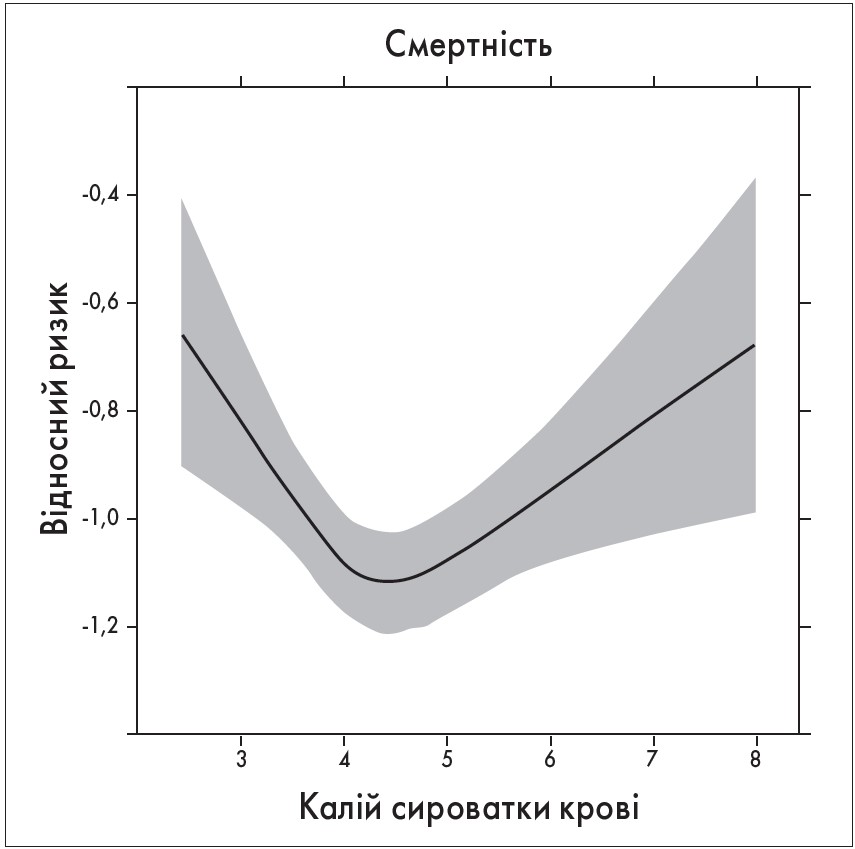 Рис. 1. Взаємозв’язок між калієм у сироватці крові (при безперервному визначенні) і смертю від усіх причин. Спостереження і аналіз результатів 36 359 пацієнтів (м. Клівленд, штат Огайо, США) зі ШКФ <60 мл/хв/1,73 м2 упродовж 2005-2009 років [4]
Рис. 1. Взаємозв’язок між калієм у сироватці крові (при безперервному визначенні) і смертю від усіх причин. Спостереження і аналіз результатів 36 359 пацієнтів (м. Клівленд, штат Огайо, США) зі ШКФ <60 мл/хв/1,73 м2 упродовж 2005-2009 років [4]
У ході багатофакторного регресійного аналізу було показано, що факторами ризику гіперкаліємії, у свою чергу, є: зниження рівня ШКФ, наявність цукрового діабету (ЦД) і використання іРААС. Проблема впливу гіперкаліємії на темпи прогресування ХХН поки ще є дискусійною (рис. 2).
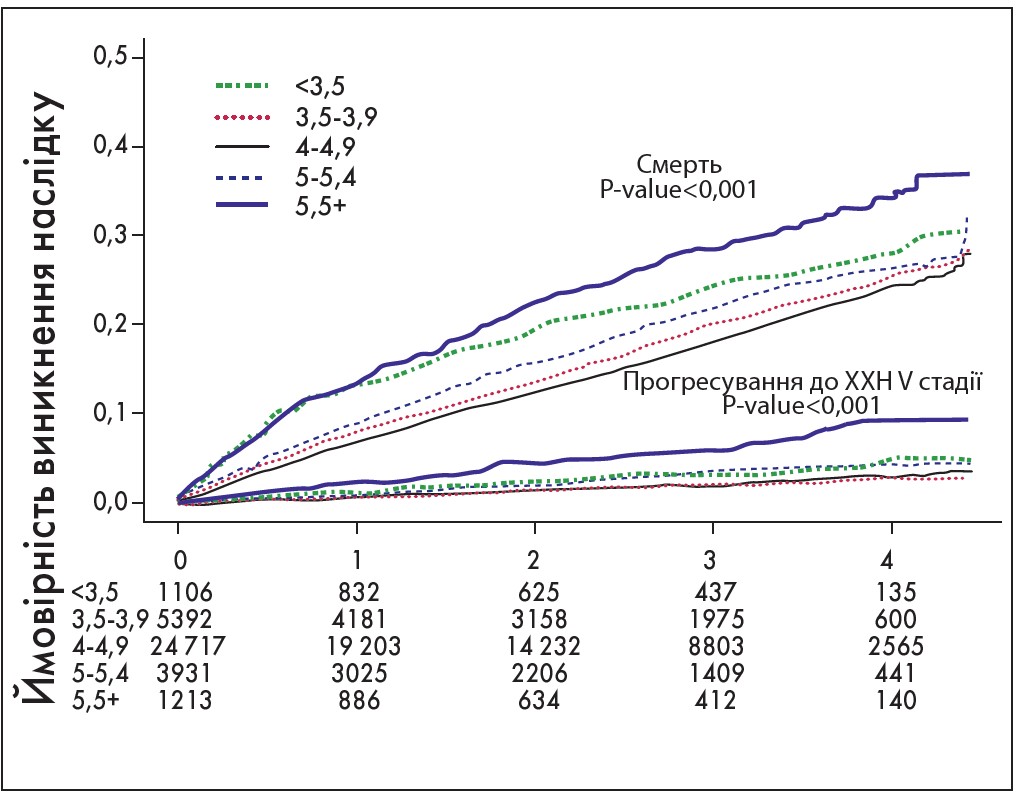
Рис. 2. Гіперкаліємія – предиктор несприятливого перебігу ХХН (хворі з рівнем калію >5,5 ммоль/л мають найбільший ризик виникнення ХХН V стадії та настання смерті) [4]
У пацієнтів, що перебувають на гемодіалізі, спостерігаються діаліз-зумовлені коливання рівня калію в сироватці крові, які призводять до частих тяжких аритмій незалежно від етіології ХХН. Автори численних досліджень пов’язують високий рівень смертності діалізних хворих із серцево-судинними подіями, частота яких збільшується на тлі гіперкаліємії та інших електролітних і кислотно-лужних порушень [1-4].
Отже, гіперкаліємія – це стан, що потенційно загрожує життю хворого, насамперед пацієнтів із ХХН, ЦД, серцевою недостатністю та комбінацією цих станів, які потребують лікування іРААС. За наявності гіперкаліємії обмежується можливість проведення ренопротекторної і гіпотензивної терапії; крім того, високий рівень калію в крові є предиктором прогресування серцево-судинних ускладнень.
Гіперкаліємія є безумовним показанням для якнайшвидшого початку лікування гемодіалізом у пацієнтів із ГХН або ХХН IV-V стадії; гіперкаліємію можна також розглядати як серйозний привід для передчасного призначення нирково-замісної терапії (НЗТ) у хворих на ХХН.
Найчастіші причини гіперкаліємії
- Надмірне надходження калію у пацієнтів зі зниженою видільною функцією нирок або з порушеним внутрішньоклітинним транспортом калію.
- Зниження виділення калію нирками – гостра або хронічна ниркова недостатність, недостатність альдостерону або глюкокортикоїдів (вроджена або набута), гіпореніновий гіпоальдостеронізм (у хворих з діабетичною, вовчаковою, аналгетичною або пов’язаною із ВІЛ-інфекцією нефропатією), резистентність ниркових канальців до альдостерону (псевдогіпоальдостеронізм).
- Медикаментозна гіперкаліємія, що спричинена прийомом наступних препаратів: інгібіторів ангіотензинперетворювального ферменту (іАПФ), блокаторів рецепторів ангіотензину ІІ (БРА II), інгібіторів реніну, які знижують синтез альдостерону, причому БРА II рідше сприяють гіперкаліємії, аніж іАПФ; БРА (спіронолактон, еплеренон) – блокують зв’язування альдостерону з рецепторами мінералокортикоїдів; препарати калію; нестероїдні протизапальні препарати (НПЗП) і селективні інгібітори циклооксигенази (ЦОГ) – пригнічують синтез простагландинів, що знижує кровоток аферентними артеріолами і перешкоджає синтезу реніну та альдостерону; амілорид, триамтерен, триметоприм – зменшують екскрецію калію; циклоспорин, такролімус – знижують продукцію реніну, що супроводжується зменшенням синтезу альдостерону і секреції калію в канальцях; гепарин, фториди – пригнічують синтез альдостерону; дигоксин – знижує активність Na+/K+-аденозинтрифосфатази (ATФази); протигрибкові препарати (флуконазол, ітраконазол, кетоконазол, міконазол) – зменшують синтез стероїдів у наднирниках, що супроводжується дефіцитом альдостерону; амінокислоти (лізин, аргінін, ε-амінокапронова кислота), які проникають у клітини в обмін на калій, також сприяють виникненню гіперкаліємії.
- Порушення внутрішньоклітинного транспорту калію – метаболічний ацидоз, блокада β2-адренергічного рецептора, дефіцит інсуліну і альдостерону, блокада ренін-ангіотензин-альдостеронової системи.
- Надмірне вивільнення калію з клітин – рабдоміоліз, синдром лізису пухлин, метаболічний ацидоз, сепсис, періодичний гіперкаліємічний параліч, занадто швидке виведення з гіпотермії, злоякісна гіпертермія; трансфузія еритромаси.
- Препарати, до складу яких входять глід, конвалія, сибірський женьшень, а також препарати з жаб’ячої шкіри, які діють подібно наперстянці, – знижують активність Na+/K+-ATФази, що супроводжується підвищенням позаклітинного рівня калію. Деякі рослинні та харчові добавки містять велику кількість калію (кульбаба, люцерна, хвощ, кропива).
- Псевдогіперкаліємія (позасистемне вивільнення калію з еритроцитів) – гемоліз проби крові, тромбоцитоз і лейкоцитоз [5, 6].
Фізіологія обміну калію в нормі
Здорові люди мають споживати приблизно 100-110 мкг калію на добу [34]. Кишечник поглинає практично увесь спожитий калій та регулює його рівень за допомогою двох механізмів. По-перше, калій, що надійшов в організм, спочатку одразу ж потрапляє в портальну венозну систему, стимулюючи виділення інсуліну підшлунковою залозою.
Гіперінсулінемія сприяє швидкому переміщенню калію з позаклітинного простору в клітини за допомогою Na+/K+-АТФази. По-друге, у відповідь на гіперкаліємію юкстагломерулярні клітини нирок починають виділяти ренін. Це посилює активацію ангіотензину І в печінці, який згодом перетворюється в ангіотензин ІІ в легенях.
Ангіотензин ІІ стимулює секрецію альдостерону наднирниками. У відповідь на підвищення рівня альдостерону в сироватці крові збірні канальці нирок виділяють у сечу калій і затримують натрій, так відбувається зниження рівня калію в сироватці крові. Отже, нирки виділяють надмірну кількість калію для підтримки загального гомеостазу в організмі: відбувається вільна фільтрація калію в клубочках, реабсорбція в проксимальному відділі канальців та секреції в дистальних звивистих канальцях і сегментах збірних канальців.
Альдостерон також підсилює виведення калію в дистальних відділах товстої кишки. Приблизно 10% вжитого з їжею калію евакуюється з калом. Цей шлях екскреції калію може бути надзвичайно важливим у хворих на ХХН.
Пасивна секреція калію відбувається в товстому кишечнику, що було продемонстровано у хворих, які лікуються за допомогою діалізних методів. Процес потенційно може бути активізовано за допомогою катіонообмінних смол, що може призвести до подальшого збільшення екскреції калію з калом [5, 6].
Встановлення етіології гіперкаліємії
Перший етап обстеження хворого з гіперкаліємією – виключення помилкового підвищення рівня калію (забір крові з вени або венозного катетера, через який виконується інфузія розчину калію, лабораторна похибка, псевдогіперкаліємія, гемоліз, лейкоцитоз, тромбоцитоз, багаторазове згинання кисті в кулак перед пункцією вени, травматична венепункція, рідкісні генетичні синдроми, сімейна псевдогіперкаліємія). Якщо рівень калію дійсно підвищений, наступним етапом є визначення причини:
- вплив медикаментів і надмірного надходження калію в організм;
- збій у розподілі калію між внутрішньоклітинним і позаклітинним простором (найчастіше трапляється при неконтрольованій гіперглікемії, наприклад діабетичний кетоацидоз або гіперосмолярний гіперглікемічний стан);
- порушення ниркової екскреції калію;
- наявність комбінованих причин.
Якщо гіперкаліємія є наслідком зменшення виведення калію нирками, лікування по суті має бути спрямоване на індукцію виведення калію. У разі коли гіперкаліємія спричинена виходом калію з клітин у позаклітинний простір, виникає перерозподільна гіперкаліємія.
Гіперосмолярність і дефіцит інсуліну насамперед відповідають за трансцелюлярне спрямування калію з клітин у позаклітинну рідину; змінити це можна шляхом введення рідин й інсуліну. В цілому в багатьох з таких пацієнтів спостерігається значний дефіцит калію в організмі, і необхідно уважно спостерігати за розвитком гіпокаліємії під час лікування.
Іноді причиною гіперкаліємії може бути зневоднення або надлишок калію, що надходить в організм хворого з їжею.
Діагностика
Встановлення діагнозу починається з вивчення анамнезу, лікарських засобів, які вживає пацієнт, і результатів фізикального обстеження. Ознаки і симптоми гіперкаліємії зазвичай є рідкісними, неспецифічними і розвиваються лише тоді, коли рівень калію у сироватці перевищує 7,0 ммоль/л: біль у м’язах, м’язова і загальна слабкість, шлуночкові аритмії, парестезії, нудота, блювання, серцебиття, депресія.
При фізикальному обстеженні треба звернути увагу на:
- показники життєдіяльності: нестабільність гемодинаміки і аритмію;
- кардіологічні зміни: екстрасистолія, блокада або брадикардія;
- неврологічний статус: зниження глибоких сухожильних рефлексів або зменшення м’язової сили; іноді спостерігаються в’ялий параліч м’язів і гіповентиляція;
- ознаки ниркової недостатності: набряки, суха шкіра, наявність артеріовенозної фістули, катетерів, у тому числі перитонеального;
- наявність травми, яка могла б спровокувати рабдоміоліз.
Виявити гіперкаліємію можна за допомогою електрокардіографії (ЕКГ), оскільки підвищений вміст калію проявляється передусім порушенням роботи міокарда: розширення, згладження, зникнення зубця Р; подовження інтервалу PQ; розширення комплексу QRS; високі загострені, «пікоподібні», зубці Т (рис. 3). Іноді широкий QRS зливається з високим «пікоподібним» зубцем Т. Можливий підйом сегмента ST. АВ-блокада високої градації. Шлуночкова тахікардія, фібриляція шлуночків, ідіовентрикулярний ритм.
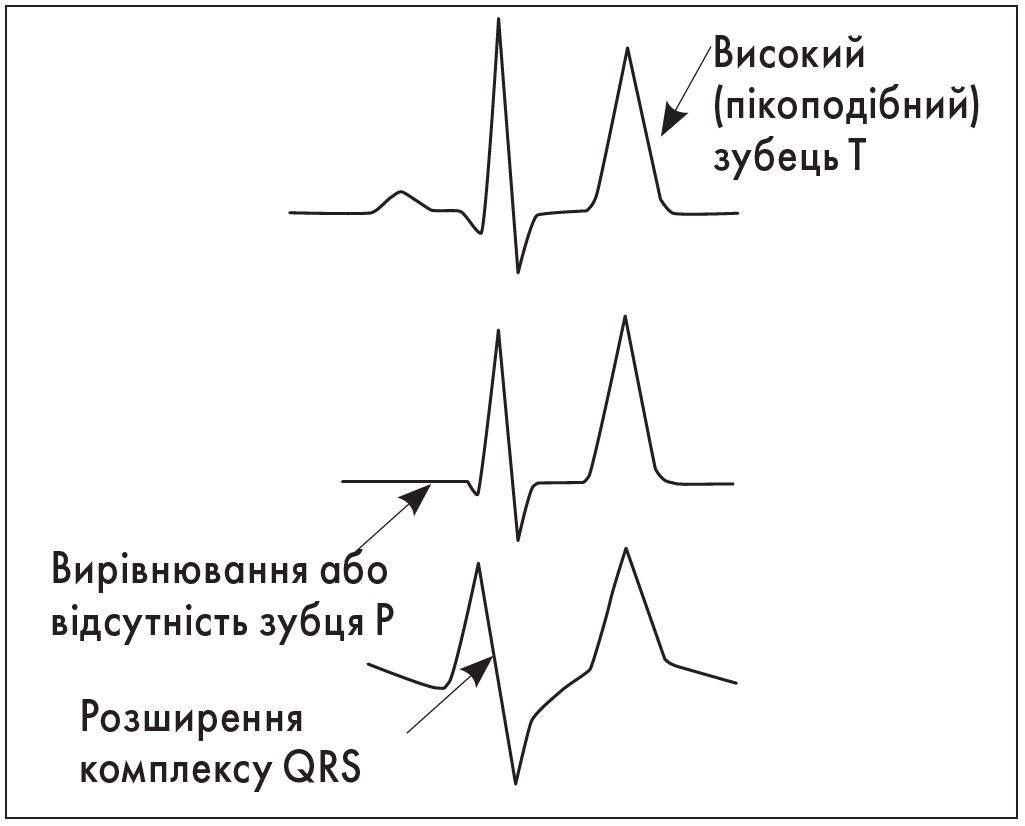 Рис. 3. Зміни ЕКГ при гіперкаліємії
Рис. 3. Зміни ЕКГ при гіперкаліємії
Лікування
Ургентна корекція гіперкаліємії показана при наявності змін на ЕКГ або вираженого ацидозу, швидкому підвищенні рівня калію в сироватці крові та зниженні функції нирок (рис. 4). У такому разі потрібні невідкладні лікувальні заходи ще до визначення етіології гіперкаліємії, проте рівень калію, креатиніну і осмолярність сечі бажано визначити першочергово.
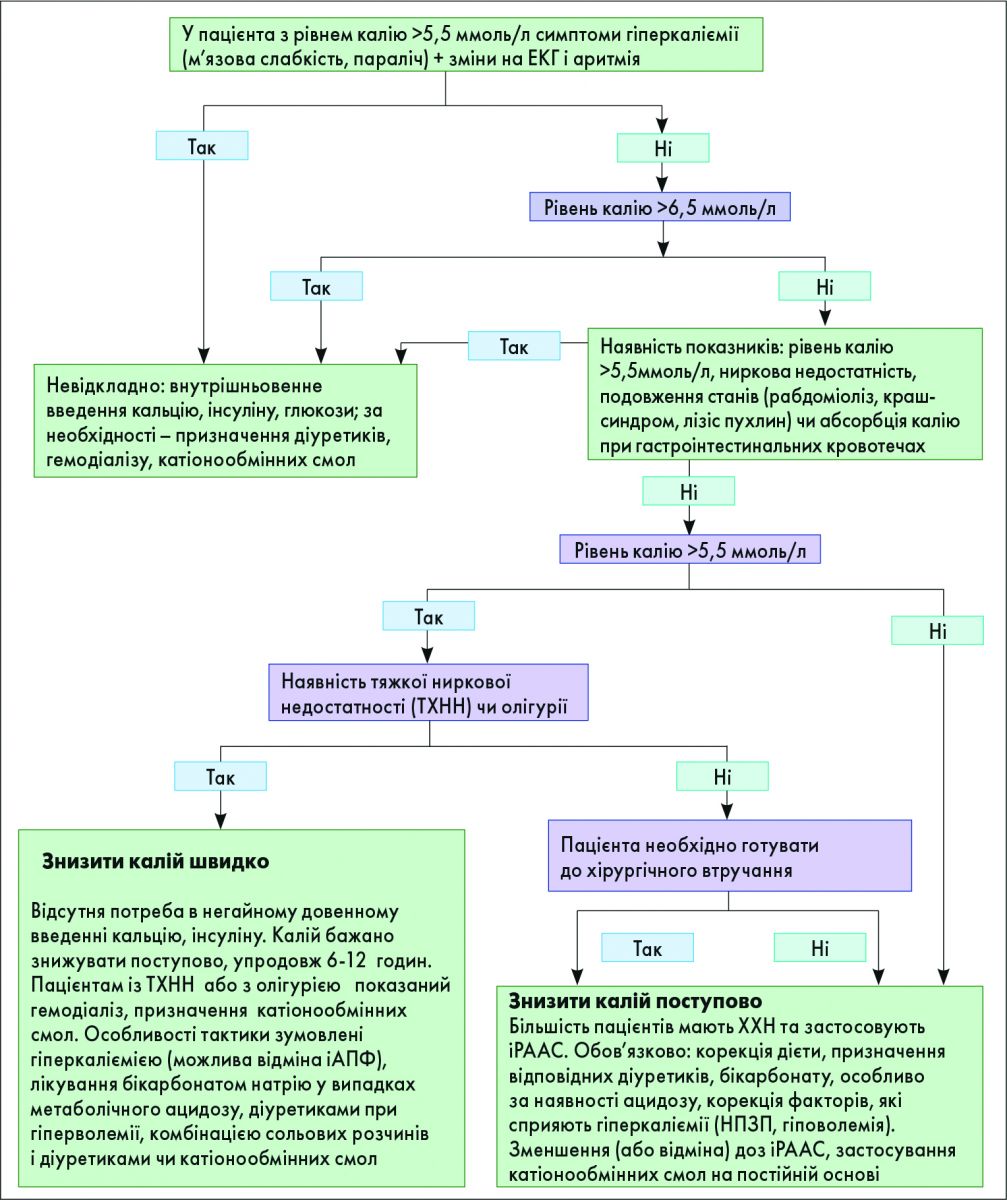 Рис. 4. Алгоритм дій лікаря при гіперкаліємії
Рис. 4. Алгоритм дій лікаря при гіперкаліємії
Хоча контрольовані дослідження не проводилися, клінічно значущою вважається концентрація калію >6,0 ммоль/л. Несприятливим передвісником потенційно смертельних аритмій у хворого з гіперкаліємією є зміни на ЕКГ. Однак гіперкаліємія може становити загрозу для життя навіть за відсутності змін на ЕКГ, приблизно у 50% пацієнтів з рівнем калію >6,0 ммоль/л дані ЕКГ нормальні.
Треба зазначити, що на сьогодні відсутні чіткі рекомендації щодо госпіталізації за наявності гіперкаліємії. У кожному разі вирішення питання доцільності госпіталізації для постійного ЕКГ-моніторингу залежить від клінічної картини. Хворим, у яких рівень калію підвищився за короткий термін, здебільшого рекомендовано лікування в стаціонарі, якщо ж гіперкаліємія розвивалася протягом декількох тижнів, лікування можна проводити амбулаторно під ретельним наглядом лікаря.
Невідкладні заходи
Екстрена допомога складається з трьох кроків:
- Стабілізація роботи міокарда завдяки введенню кальцію – функціонального антагоніста калію.
- Спрямування калію з позаклітинного простору в клітини за допомогою введення інсуліну і глюкози, β2-агоністів, розчину соди за наявності ацидозу.
- Призначення препаратів, спрямованих на виведення калію з організму: петльові та тіазидні діуретики – при збереженій функції нирок, а також катіонообмінні смоли (рис. 4). І водночас – заборона ліків, що сприяють затримці калію [10, 11]. Для захисту міокарда внутрішньовенно вводиться кальцій, який знижує поріг збудливості, протидіє токсичному впливу високої концентрації калію.
Кальцій можна вводити у вигляді глюконату або хлориду кальцію. Кальцію хлорид містить концентрацію елементарного кальцію, втричі вищу в порівнянні з глюконатом кальцію (13,6 проти 4,6 мекв у 10 мл 10% розчину). Проте глюконат кальцію є кращим вибором, оскільки ін’єкція кальцію хлориду може спричинити локальне подразнення. Хлорид кальцію вводять переважно у центральну або глибоку вену.
Глюконат кальцію можна вводити із застосуванням маленької голки або катетера у великій вені. Кальцій не рекомендується вводити в розчини, що містять бікарбонат, це може призвести до випадання карбонату кальцію в осад. Кальцій не впливає на рівень калію в сироватці крові. Через 2-3 хв після введення кальцію картина ЕКГ має змінитися. Через 5 хв, якщо зміни на ЕКГ зберігаються, інфузію розчину кальцію вводять вдруге.
Особливої уваги потребує дигоксин, а точніше – пацієнти, яким він призначений: у літературі є повідомлення про токсичний вплив дигоксину на міокард. Деякі експерти пропонують вводити кальцій хворим, які отримують глікозиди, методом повільної інфузії кальцію зі 100 мл 5% глюкози впродовж 20-30 хв, аби уникнути гострої гіперкальціємії [1] (як альтернативне лікування: для захисту міокарда замість кальцію вводять магній).
Зазвичай вводять 10 МО інсуліну із 50 мл 50% розчину глюкози для профілактики гіпоглікемії. Якщо рівень калію залишається підвищеним, можна вводити повторні дози інсуліну. Інгаляційні β2-агоністи характеризуються швидким початком дії. Вони доповнюють ефекти інсуліну, обидва препарати можна застосовувати одночасно. Інсулін і β2-агоністи сприяють переходу кальцію в клітини. Альбутерол, сальбутамол у дозі 10-20 мг використовуються в аерозолі. У разі розвитку метаболічного ацидозу для зниження явищ гіперкаліємії рекомендується призначення розчину натрію бікарбонату внутрішньовенно крапельно. Втрату калію нирками можна компенсувати введенням петльових діуретиків (наприклад, фуросеміду).
Моніторинг
Безперервний моніторинг роботи серця за допомогою запису серійних ЕКГ є підставою для корекції терапії. Калій у сироватці крові вимірюють через 1-2 год від початку лікування. Час подальших вимірювань визначається концентрацією калію в сироватці крові й реакцією на терапію. Пацієнтам, що отримують інсулін з декстрозою (глюкозою), необхідні погодинні вимірювання глюкози протягом 6 годин.
Зниження загального рівня калію в організмі
Лікувальні заходи, що сприяють переміщенню калію в клітини, не впливають на його загальний вміст в організмі. Калій виводиться за допомогою ниркової екскреції, діалізу або через шлунково-кишковий тракт. Препарати, що знижують загальний вміст калію, можуть впливати на результати тестів для встановлення етіології гіперкаліємії. Тому перед прийомом цих ліків необхідно визначити вміст калію й креатиніну в сечі та її осмолярність, проте не слід відкладати лікування в очікуванні результатів обстеження.
Екскреція калію зі шлунково-кишкового тракту досягається за допомогою полістирену сульфонату натрію, який зв’язує калій у товстій кишці в обмін на натрій. Препарат можна приймати перорально або вводити ректально за допомогою клізми. Введений ректально препарат починає діяти швидше; початок дії пероральної форми настає через 4-6 год – саме за цей час смола надходить у товсту кишку. Комбінація фуросеміду з полістиреном знижує ризик підвищення об’єму циркулюючої крові (ОЦК) завдяки натрію, що виділяється зі смоли в обмін на калій (табл.).
Втрату калію нирками можна посилити за допомогою сечогінних препаратів, особливо петльових діуретиків (зокрема, фуросеміду – 40 мг внутрішньовенно кожні 12 год або безперервна інфузія). За умови дефіциту ОЦК діуретики вводять під час інфузії фізіологічного розчину. Хворі зі зниженою функцією нирок можуть бути відносно резистентні до дії сечогінних. Якщо лікування медикаментозними препаратами виявилося неефективним, пацієнтів переводять на гемодіаліз або перитонеальний діаліз.
Довготривале лікування
Довготривале лікування призначають для усунення причини гіперкаліємії. З пацієнтом обговорюють дієту з включенням продуктів зі зниженим вмістом калію (обмежуються сухофрукти, морські водорості, горіхи, авокадо, крупи, пшеничні зародки, бобові, овочі: шпинат, томати, буряк, морква, цвітна капуста і капуста броколі, картопля; фрукти: диня, ківі, апельсини, манго; ковбасні вироби, яловичина, свинина, телятина, ягнятина). Необхідно також відмінити медикаментозні препарати, що здатні підвищити вміст калію у сироватці крові, для запобігання гіперкаліємії.
Хворим на гіпоренінемічний гіпоальдостеронізм за наявності рецидивуючої або хронічної гіперкаліємії доцільно призначити петльові діуретики або/та синтетичний кортикостероїд флудрокортизон у дозі 0,1 мг/ добу, деяким пацієнтам дозу можна підвищити. Тоді коли в одних пацієнтів гіпоренінемічний гіпоальдостеронізм має транзиторний характер і зникає після невідкладних заходів, інші хворі потребують тривалого лікування. У більшості пацієнтів тривалий прийом флудрокортизону протікає без будь-яких проблем.
Основні небажані явища – гіпертензія й затримка рідини, що зникають після додавання діуретика. Хоча наслідки тривалості лікування флудрокортизоном ніколи не досліджувалися, один з підходів до цієї проблеми полягає в поступовому зниженні дози в амбулаторних умовах, а на тлі підвищення рівня калію – в поновленні лікування.
Гіперкаліємія, зумовлена прийомом іАПФ та БРА II, насамперед при ХХН, потребує зменшення дози або навіть відміни цих препаратів – тимчасово або постійно. Якщо ж у пацієнтів констатовано метаболічний ацидоз, проблема гіперкаліємії може бути вирішена додаванням соди в дозі 2-5 г (1/2-1 чайна ложка харчової соди) на добу. Обов’язковим є призначення катіонообмінних полімерів.
Як вже було відзначено вище, катіонообмінна смола полістирену сульфонат натрію (sodium polystyrene sulfonate – SPS) обмінює в шлунково-кишковому тракті калій на натрій: 1 г препарату зв’язує 1 ммоль калію, в результаті вивільняється 2-3 ммоль натрію. Дія настає через 1-2 год і триває 4-6 годин. Концентрація калію в плазмі знижується на 0,5-1 ммоль/л. Полістирену сульфонат натрію вводять у вигляді клізми (для дорослих разова доза складає 30-50 г препарату, розведеного в 150-200 мл води).
SPS може застосовуватися в разі помірно-тяжкої гіперкаліємії з незначними змінами ЕКГ (наприклад, збільшення зубця Т), а також хронічної гіперкаліємії легкого і середнього ступеня [12, 14]. У ході ретроспективного неконтрольованого дослідження [13] 501 хворому з гострою гіперкаліємією призначали SPS у дозі 15-60 г у середньому впродовж 24 год, доки знову не був виміряний рівень калію в сироватці крові. Він знизився у середньому на 0,93 мекв/л [13].
Однак у деяких учасників дослідження виникли поширені побічні ефекти, а в двох пацієнтів розвинувся некроз кишечника, дане ускладнення від прийому SPS описане у багатьох дослідженнях [15-19].
SPS рекомендований пацієнтам у поєднанні із швидкодіючою короткотривалою терапією, про яку згадувалося вище (рис. 4), але за наявності певних ознак: у пацієнтів виникла потенційно небезпечна для життя гіперкаліємія, а діаліз для нього недоступний; інші терапевтичні заходи для зниження рівня калію (діуретики, швидке відновлення функції нирок) виявилися неефективними. Слід зауважити, що в разі застосування SPS інші призначені пацієнту препарати мають прийматися щонайменше за/через 3 год [20, 21], оскільки SPS може перешкоджати всмоктуванню багатьох поширених ліків.
2015 року в США до застосування для лікування гіперкаліємії було схвалено катіонообмінну смолу полістирол сульфонат кальцію – патіромер (Veltassa, Калімейт, Kowa Company Ltd, Японія). Шлунково-кишкові катіони – патіромер і поки ще не схвалений препарат ZS‑9 – це сполуки, які обмінюються кальцієм або натрієм та воднем відповідно на калій у кишечнику.
Патіромер – це сферичний неабсорбуючий органічний полімер, сформований у вигляді порошку для суспензії, який зв’язує калій у товстій кишці в обмін на кальцій [22, 23].
Патіромером у ІІ фазі відкритого дослідження (Effect of Patiromer on Serum Potassium Level in Patients With Hyperkalemia and Diabetic Kidney Disease: The AMETHYST-DN Randomized Clinical Trial) лікували 306 хворих на ЦД зі ШКФ 15-59 мл/хв/1,73 м2 і легкою або помірною гіперкаліємією (рівень калію в сироватці крові 5,1-5,5 і 5,6-5,9 мекв/л відповідно) в початкових дозах із поступовим збільшенням (від 4,2 до 16,8 г 2 р/день) упродовж 52 тиж [24].
Усі пацієнти продовжували отримувати стабільні дози іАПФ, або БРА II, або обидва, часто – у комбінації із спіронолактоном. Через чотири тижні динаміка рівня калію в сироватці крові в порівнянні з вихідними показниками становила: від -0,35 до -0,55 мекв/л із початковими дозами від 4,2 до 12,6 г 2 р/ день у хворих із легкою гіперкаліємією і від -0,87 до -0,97 мекв/л із початковими дозами від 8,4 до 12,6 г 2 р/день – у пацієнтів із помірною гіперкаліємію.
Приблизно 30% пацієнтів знадобилося корегування дози препарату. Після 52 тиж концентрація калію в сироватці крові залишалася в нормальному діапазоні з продовженням лікування патіромером. Припинення застосування патіромеру супроводжувалося збільшенням вмісту калію в сироватці протягом 3 днів.
У ході аналізу результатів дослідження AMETHYST-DN не було виявлено серйозних побічних ефектів, пов’язаних із лікуванням. Найчастіше спостерігалися такі небажані явища, як запор (6,3% пацієнтів) і гіпомагніємія (7,2% пацієнтів), остання розвивалася переважно у тих, кому призначали більші дози патіромеру (16,7% при дозі 33,6 г/день у порівнянні з 5,4% при дозі 8,4 г/день). У 13 хворих (4,3%) констатовано гіпомагніємію з рівнем магнію в сироватці <1,2 мг/дл.
У ході III фази рандомізованого плацебо-контрольованого дослідження OPAL-HK [25] вивчалась ефективність патіромеру в амбулаторних пацієнтів з ХХН і гіперкаліємією. У дослідженні OPAL-HK 237 пацієнтам із ШКФ 15- 59 мл/ хв/1,73 м2 і рівнем калію в сироватці крові 5,1-6,5 ммоль/л одночасно із стабільною дозою іАПФ або БРА II призначали 4,2 або 8,4 г патіромеру 2 р/день протягом 4 тиж залежно від рівнів калію.
Середнє зниження вмісту калію в сироватці крові за цей час становило 1,01±0,03 ммоль/л (р<0,001). Приблизно у 76% пацієнтів був досягнутий цільовий рівень калію сироватки, який знаходився в межах від 3,8 до 5,1 ммоль/л. Довільно призначали патіромер або плацебо ще на 8 тиж 107 пацієнтам з рівнем сироваткового калію ≥5,5 ммоль/л, які досягли цільового рівня калію в сироватці протягом 4-тижневого періоду лікування.
Рівень калію в сироватці крові залишався стабільним у пацієнтів, що продовжували лікування патіромером, і збільшувався на 0,72 ммоль/л у хворих, що приймали плацебо. Частота гіперкаліємії (≥5,5 ммоль/л) була значно вищою в групі плацебо (60 проти15%). Серйозні побічні ефекти були рідкісними і, ймовірно, не були пов’язані з патіромером; запор був найпоширенішим побічним явищем (11% пацієнтів).
Як і в дослідженні AMETHYST-DN, у деяких пацієнтів розвивалася гіпомагніємія – у 8 (3%) хворих рівень магнію в сироватці крові складав <1,4 мг/дл. Треба зазначити, що до сьогодні ефективність патіромеру в пацієнтів із гострою гіперкаліємією або кінцевою стадією ХХН не оцінювалася.
Окрім того, пацієнтам у дослідженнях OPAL-HK і AMETHYST-DN не була рекомендована планова гіпокалієва дієта; лише 50% пацієнтів, що брали участь у дослідженні OPAL-HK, отримували петльові або тіазидні діуретики; про кількість пацієнтів у дослідженні AMETHYST-DN, які отримували діуретики, не було повідомлено.
Як дієта з низьким вмістом калію, так і використання петльових або тіазидних діуретиків можуть бути довготривалими стратегіями для запобігання гіперкаліємії у багатьох пацієнтів із ХХН, що отримують іАПФ або БРА. До того ж патіромер може адсорбувати інші ліки в шлунково-кишковому тракті. Виявлено клінічно важливі взаємодії з ципрофлоксацином, тироксином і метформіном [26].
Циклосилікат цирконію натрію (ZS‑9) – це неорганічна кристалічна сполука, яка обмінює іони натрію і водню на калій протягом всього кишкового транзиту [27]. Сьогодні тривають дослідження цього препарату, але попередні висновки свідчать про його високу ефективність у лікуванні гіперкаліємії у хворих із ХХН, ЦД і серцевою недостатністю, які приймають іАПФ і БРА II. Треба також підкреслити, що на тлі застосування ZS‑9 найбільше зниження рівня калію в сироватці відбулося протягом перших 4 год терапії [27-29].
Це свідчить про безпосередній вплив на секрецію калію в кишечнику, а не просто про зниження всмоктування калію. Проте в жодному дослідженні дотепер не були оцінені довготривала ефективність та безпечність ZS‑9, а також не вивчені результати його застосування у пацієнтів із гострими гіперкалієміями і у хворих, що перебувають на діалізі.
Профілактика
Є кілька заходів для запобігання розвитку гіперкаліємії у пацієнтів із ХХН, особливо V стадії. Доповненням до дієти з низьким вмістом калію у стаціонарних хворих, насамперед діалізних, може стати наступне:
- необхідно утримуватися від епізодів голодування, щоб не спровокувати збільшення спрямованості калію в позаклітинний простір, принаймні частково, внаслідок зменшення секреції інсуліну [30]. У дослідженні 10 стабільних пацієнтів без ЦД, які перебували на програмному гемодіалізі, голодування впродовж 18 год привело до підвищення рівня калію в сироватці на 0,6 ммоль/л. Цьому можна було запобігти за допомогою повторного введення низьких доз інсуліну з декстрозою [30]. Отже, пацієнтам із недіабетичними захворюваннями, які лікуються діалізом і потребують планових операцій, показані парентеральні розчини, що містять глюкозу, під час голодування протягом ночі;
- слід уникати, якщо це можливо, лікарських засобів, здатних підвищувати концентрацію калію у пацієнтів із рівнем калію в сироватці крові ≥5,5 ммоль/л. Це іРААС (іАПФ, БРА II), прямі інгібітори реніну, антагоністи альдостерону і неселективні β-блокатори (наприклад, пропранолол та лабеталол) [31, 32]. β1-селективні блокатори (метопролол і атенолол) набагато рідше спричиняють гіперкаліємію [33].
Пацієнтам із ХХН або серцевою недостатністю часто призначають іРААС. Різні запобіжні заходи можуть зменшити ризик виникнення гіперкаліємії [31], як-от:
- постійний моніторинг концентрації калію в сироватці крові та ШКФ, особливо після змін у терапії іРААС;
- дієтичне обмеження калію;
- уникання або припинення використання препаратів, що погіршують екскрецію калію (наприклад, НПЗП);
- використання низьких початкових доз і доказових кінцевих доз іРААС для специфічних показань (зокрема, серцевої недостатності, протеїнурії, ХХН). Дозу необхідно зменшувати у разі помірної гіперкаліємії (калій у сироватці ≤5,5 ммоль/л) і терапію слід припинити, якщо рівень калію у сироватці крові перевищить 5,5 ммоль/л;
- застосування тіазидних або петльових діуретиків, катіонообмінних смол.
Недостатньо даних стосовно ефективності пероральної лужної терапії (бікарбонат натрію або цитрат натрію) для усунення стійкої гіперкаліємії [33]. Водночас існує безліч переваг лікування метаболічного ацидозу у таких хворих, і зазвичай рекомендується лужна терапія незалежно від будь-якого впливу на концентрацію калію в сироватці крові.
Отже, гіперкаліємія дійсно є серйозною проблемою, з якою стикаються лікарі у своїй рутинній клінічній практиці, передусім у лікуванні хворих на ХХН, ЦД, серцеву недостатність, особливо із застосуванням іРААС, калійзберігаючих діуретиків. Обидва – і пацієнт, і лікар – мусять дотримуватися заходів профілактики гіперкаліємії та постійно здійснювати моніторинг рівня калію.
Резюме і рекомендації
Актуальність лікування гіперкаліємії залежить від наявності або відсутності характерних для неї симптомів, ознак і причин. Лікування гіперкаліємії рекомендовано здійснювати згідно з алгоритмом.
Потребують негайних дій пацієнти:
- з клінічними ознаками або симптомами гіперкаліємії (зокрема, м’язова слабкість або параліч, порушення серцевої провідності, аритмії серця);
- з тяжкою (рівень сироваткового калію >6,5 ммоль/л) і помірною (рівень сироваткового калію >5,5 ммоль/л) гіперкаліємією та значними порушеннями функції нирок і тривалою травмою (розчавлення) тканин;
- що потребують невідкладного лікування. Деяким пацієнтам із помірною гіперкаліємією потрібна швидка корекція калію (протягом 6-12 год). Це пацієнти, які лікуються програмним гемодіалізом, однак перебувають у міждіалізному проміжку часу; пацієнти з низькою залишковою функцією нирок як за показниками ШКФ, так і за кількістю сечі; пацієнти з ХХН III-V стадії, яким передбачено проведення оперативного втручання;
- що потребують повільного зниження рівня калію. Більшість пацієнтів із гіперкаліємією мають хронічні, легкі (≤5,5 ммоль/л) або середні (5,5-6,5 ммоль/л) рівні підвищення калію в сироватці крові, передусім хворі на ХХН або пацієнти, які приймають іРААС. У таких пацієнтів відсутня необхідність у терміновому зниженні вмісту калію в сироватці крові.
Пацієнти з тяжкою гіперкаліємією мають отримувати:
- кальцій (внутрішньовенно) – функціональний антагоніст калію;
- інсулін (внутрішньовенно, зазвичай разом із глюкозою) – для спрямування позаклітинного калію в клітини;
- терапію, яка б сприяла швидкому видаленню надлишку калію з організму (петльові або тіазидні діуретики, якщо функція нирок не дуже порушена, або шлунково-кишкову катіонообмінну смолу, якщо ШКФ дорівнює <45 мл/ хв/1,73 м2. Якщо є можливість – діаліз (бажано гемодіаліз), насамперед на тлі ШКФ <15 мл/ хв/1,73 м2).
Окрім вищезазначеного треба вжити запобіжних заходів, таких як: усунення зворотних причин гіперкаліємії, таких як гіповолемії, і припинення прийому ліків, що підвищують вміст калію в сироватці крові (наприклад, НПЗП, іРААС). У ході лікування рекомендовано постійний моніторинг роботи серця, у тому числі контроль ЕКГ у динаміці.
Калій у сироватці крові вимірюють через 1-2 год після початку лікування. Час подальших вимірювань визначається концентрацією калію в сироватці крові та реакцією на терапію. У пацієнтів, які отримують інсулін з декстрозою або без нього, для контролю гіпоглікемії необхідно здійснювати погодинні вимірювання глюкози протягом 6 годин.
За відсутності тяжкої гіперкаліємії лікування залежить від того, як швидко необхідно знизити вміст калію в сироватці крові (рис. 4):
- пацієнтів, у яких виникла потреба у швидкому зниженні калію, здебільшого переводять на гемодіаліз (за наявності ХХН V стадії) із використанням шлунково-кишкового катіонного обмінника або без нього. Пацієнтам із нормальною функцією нирок або ХХН I-IV стадії додатково призначають інфузійну терапію і петльові діуретики; розчин бікарбонату натрію – за умови ацидозу; шлунково-кишковий катіон. Часто достатньо усунення причини гіперкаліємії (відміна препаратів, корекція гіповолемії);
- пацієнтам, які адаптовані до високих рівнів калію в сироватці крові, показано поступове його зниження за допомогою дієти з низьким вмістом калію, петльових або тіазидних діуретиків, зменшення доз або відміни ліків, здатних підвищити вміст калію в сироватці крові. Для хронічного контролю калію пацієнтам призначають шлунково-кишкові катіони.
Для профілактики гіперкаліємії або її погіршення на тлі ХХН, переважно V стадії, як додаток до дієти з низьким вмістом калію пацієнтам, що лікуються діалізними методами, рекомендовано:
- уникати епізодів голодування, які можуть призвести до збільшення рівня калію в позаклітинному просторі, принаймні частково, через скорочення секреції інсуліну;
- уникати (насамперед пацієнтам із помірною гіперкаліємією), якщо це можливо, препаратів, здатних підвищувати концентрацію калію в сироватці крові. Це іРААС, як-от іАПФ, БРА II, прямі інгібітори реніну, антагоністи альдостерону і неселективні β-блокатори (наприклад, пропранолол та лабеталол);
- уникати або відмовитися від прийому препаратів, які погіршують екскрецію калію (зокрема, НПЗП);
- використовувати тіазидні або петльові діуретики. Здійснювати корекцію ацидозу.
Список літератури знаходиться в редакції.