8 червня, 2018
Менеджмент преждевременной яичниковой недостаточности

В статье представлен современный взгляд на проблему преждевременной яичниковой недостаточности, которая негативно влияет на частоту развития сердечно-сосудистых и неврологических заболеваний, остеопороза, когнитивную функцию, половую жизнь и социальную реализацию женщин. Рассмотрены критерии диагностики иосновные принципы лечения этой патологии.
Под преждевременной яичниковой недостаточностью (ПЯН) подразумевают прекращение функции яичников у женщины в возрасте до 40 лет, что характеризуется нарушением менструальной функции (олиго-/аменорея), повышением уровней гонадотропинов и снижением – эстрадиола.
Клиническая значимость ПЯН состоит в том, что возникающая гипоэстрогения влияет на:
- продолжительность и качество жизни женщин;
- развитие сердечно-сосудистой и неврологической патологии;
- плотность костной ткани;
- когнитивные функции;
- социальную реализацию женщин.
Этиология первичной/спонтанной ПЯН включает инфекционные, генетические (25%), аутоиммунные (10%) факторы и обменные нарушения. В ряде случаев причина остается неустановленной, т.е. речь идет об идиопатической ПЯН.
Первичная ПЯН может быть как самостоятельным заболеванием (изолированные формы), так и частью комплексного фенотипа, включающего поражение других органов (синдромные формы) [1].
Среди синдромных форм ПЯН выделяют:
- нарушение карбогидратного обмена;
- псевдогипопаратиреоз, тип I;
- прогрессирующую наружную офтальмоплегию;
- синдром Демирхана;
- лейкодистрофию, сочетающуюся с поражением яичников;
- атаксию-телеангиэктазию (синдром Луи-Бар);
- аутоиммунный полигландулярный синдром, тип 1;
- редкие формы врожденной гиперплазии коры надпочечников.
Возникновение изолированных форм первичной ПЯН ассоциировано с количественными и структурными аномалиями Х-хромосомы; моногенными мутациями Х-хромосомы; мутациями в аутосомах [2, 3]. Одной из таких аномалий является синдром хрупкой/ломкой Х-хромосомы (fragile X-syndrome, синдром Мартина – Белл) – это сцепленное с полом доминантное заболевание, связанное с экспансией единичных тринуклеотидов в Х-хромосоме, что приводит к недостаточной экспрессии белка FMR1, который необходим для нормального развития нервной системы. Механизм развития ПЯН в связи с премутацией при данной патологии неясен. Возможно, избыточная транскрипция белка приводит к преждевременной деградации фолликулов (Bretherick K. L., 2005) [4]. Однако ни один из исследованных на сегодня генов не соответствует критериям генетического маркера ПЯН.
Несмотря на то что результат генетических исследований мало влияет на тактику и эффективность лечения, данные о наличии генетической аномалии в значительной мере определяют решение проблем фертильности,планирования беременности не только у пациентки, но и ее родственников (особенно при синдроме хрупкой X-хромосомы). Кроме того, определение наследственной причины заболевания способствует улучшению психологического состояния женщины, уменьшая чувство ущербности и сниженной самооценки.
В контексте ятрогенной ПЯН перед началом лечения онкологической патологии (в т.ч. у детей) следует сосредоточить внимание на методах сохранения фертильности. Современные подходы к профилактике ПЯН и сохранению фертильности у женщин, которым показана химио- или радиотерапия, предполагают:
- использование агонистов гонадотропин-рилизинг гормона;
- мобилизация яичников в необлучаемую зону;
- криопресервация яичниковой ткани и/или ооцитов;
- криопресервация эмбрионов.
Клиническая картина преждевременной яичниковой недостаточности
Обычно данная патология протекает бессимптомно. До прекращения менструаций основными и, как правило, единственными симптомами ПЯН могут быть субфертильность и олигоменорея. Вторичная аменорея (наиболее распространенный вариант) может наступить внезапно либо после периода олигоменореи. Также возможно отсутствие восстановления менструаций после приема гормональных контрацептивов или родов.
Вазомоторные симптомы встречаются редко у лиц с ПЯН в возрасте до 35 лет даже при длительной аменорее. По данным К. Масlаrаn, симптомы эстрогенного дефицита отсутствовали у 25% женщин с лабораторно подтвержденным диагнозом ПЯН.
Среди клинических проявлений могут встречаться сухость слизистой влагалища, снижение полового влечения, диспареуния, недержание мочи. К неспецифическим признакам относятся ухудшение памяти, способности сконцентрировать внимание, утомляемость, нарушение сна, сниженное настроение и депрессия, головокружение и головная боль, артралгии; ощущения, похожие на электрические импульсы; напряжение отдельных групп мышц, кожный зуд, дрожь конечностей, повышение артериального давления. Кроме того, у пациенток с ПЯН может наблюдаться прибавка в весе, выпадение волос, ломкость ногтей, изменение запаха тела.
Диагностика преждевременной яичниковой недостаточности
Согласно рекомендациям Европейского общества репродукции и эмбриологии (ESHRE, 2016), диагностическими критериями ПЯН являются: олигоменорея или отсутствие менструаций в течение четырех месяцев, уровень ФСГ > 25 МЕ/мл в двух исследованиях с интервалом не менее 4 нед.
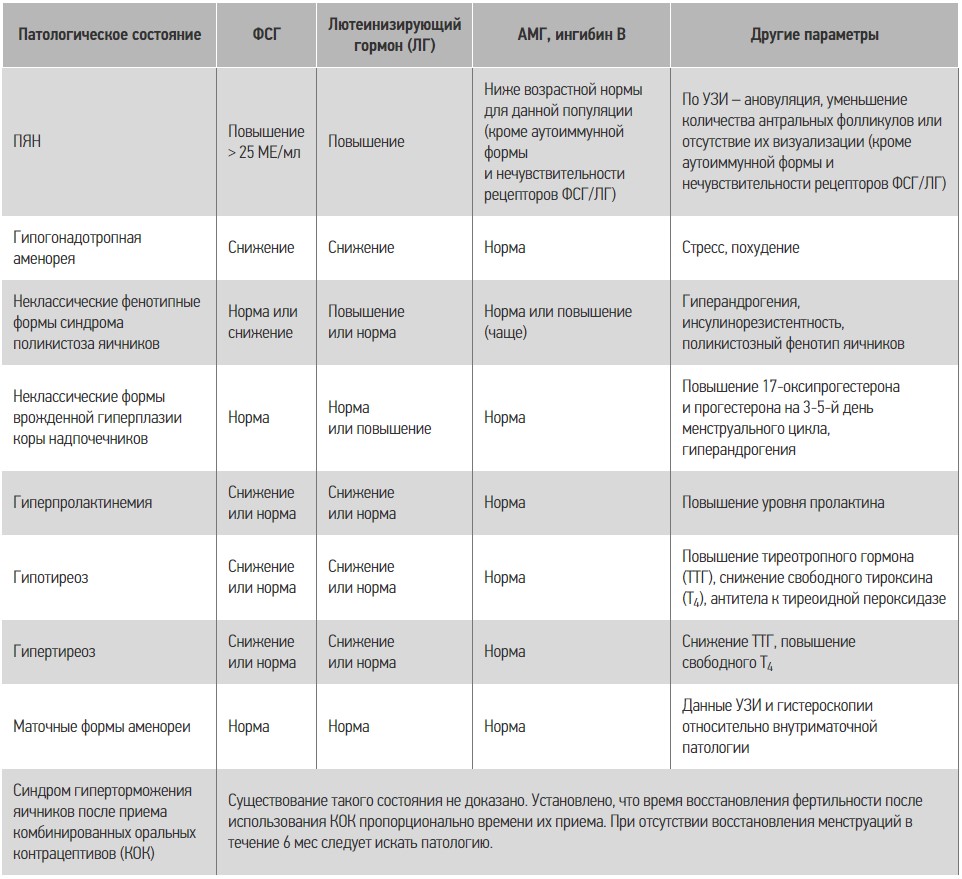
Лабораторные критерии дифференциальной диагностики ПЯН с другими эндокринными расстройствами представлены в таблице.
Таблица. Лабораторная диагностика гормональных нарушений
Для уточнения диагноза ПЯН рекомендовано определение концентрации фолликулостимулирующего гормона (ФСГ), эстрадиола, антимюллерова гормона (АМГ), ингибина В и подсчет антральных фолликулов.
Для ПЯН вследствие аутоиммунных причин характерны близкие к нормальным уровни АМГ и ингибина Б, при УЗИ – яичники нормальных размеров, фолликулярный аппарат представлен мелкими антральными фолликулами. Изолированные варианты аутоиммунной формы ПЯН встречаются редко, в большинстве случаев она сочетается с аутоиммнной патологией других органов.
Лечение преждевременной яичниковой недостаточности
Цели лечения пациенток с ПЯН:
- устранение дефицита эстрогенов независимо от наличия симптомов;
- решение репродуктивных задач;
- мониторинг и профилактика остеопороза;
- мониторинг и профилактика сердечно-сосудистых заболеваний;
- устранение и профилактика мочеполовых симптомов, сексуальной дисфункции.
Вне зависимости от наличия или отсутствия симптомов дефицита эстрогенов ПЯН является показанием для непрерывного применения заместительной эстроген-гестагенной терапии до возраста менопаузы, затем следует пересмотр доз. Исследования последних лет достаточно убедительно доказали отсутствие повышенного риска рака молочной железы на фоне приема заместительной гормональной терапии (ЗГТ) женщинами с ПЯН до возраста естественной менопаузы.
Для более молодых пациенток с ПЯН предпочтителен циклический режим назначения ЗГТ, который ассоциируется с большей вероятностью спонтанного восстановления функции яичников. В начале терапии обычно назначается 2 мг/сут эстрадиола per os или 100 мкг в виде трансдермальных форм. Выбор формы лекарственного средства зависит от индивидуальных особенностей и предпочтений пациентки. Согласно результатов исследований, при ПЯН 17β-эстрадиол является более предпочтительным вариантом эстрогенного компонента для ЗГТ, чем этинилэстрадиол или конъюгированные эстрогены.
Согласно рекомендациям Американской ассоциации клинических эндокринологов и Американского эндокринологического колледжа (2017) [5]:
- применение заместительной гормональной терапии у женщин должно проводиться с учетом всех факторов риска сердечно-сосудистых заболеваний, возраста и времени с момента наступления менопаузы;
- назначение трансдермальных эстрогенных препаратов (по сравнению с пероральными) связано с меньшей вероятностью развития тромботических осложнений и, возможно, с более низким риском развития инсульта и ишемической болезни сердца;
- в качестве гестагенного компонента более безопасной альтернативой является микронизированный прогестерон.
Применение трансдермальных форм эстрогенов (эстрожель) позволяет обеспечить более гибкий режим дозирования и индивидуальные потребности женщины. Концентрация, метаболизм и циркуляция в организме введенного 17β-эстрадиола идентичны эндогенному эстрогену. Устойчивая концентрация Е2 в крови устанавливается уже после 3 дней применения эстрожеля в дозе, соответствующей 1,5 мг эстрадиола.
Включение гестагенов в состав комбинированной ЗГТ необходимо не только для «защиты» эндометрия от пролиферативного действия эстрогенов. Прогестерон и его метаболиты играют важную роль в регуляции функций головного мозга, оказывая анксиолитический и снотворный эффекты путем взаимодействия с рецепторами ГАМК в ЦНС, а также нейропротективный и миелинизирующий эффект.
Для женщин с ПЯН жизненно важен контроль массы тела. Первостепенным подходом к оптимизации массы тела является соблюдение здорового питания и физической активности. В противоположность распространенному мнению, ЗГТ не ассоциирована с прибавкой массы тела и может предотвратить абдоминальное ожирение в перименопаузе [6].
Вопрос о длительности применения заместительной, а впоследствии менопаузальной гормонадльной терапии (МГТ) остается открытым. Согласно мнению экспертов Американского колледжа акушеров-гинекологов [7], некоторые женщины 65 лет и старше продолжают нуждаться в системной гормональной терапии для лечения вазомоторных симптомов. Поэтому у этой категории пациенток не рекомендуется рутинное прекращение МГТ. Как и у более молодых женщин, терапия должна быть индивидуальной и основываться на оценке риска и пользы в каждом конкретном случае.
Пациенткам с ПЯН и сопутствующими заболеваниями или отягощенным анамнезом (венозный тромбоэмбоэмболизм, ожирение, метаболический синдром) проведение ЗГТ не противопоказано. Необходимо учитывать, что перед началом таковой они должны быть проконсультированы гематологом, а также им необходимо выполнить допплерографию сосудов. У этой категории больных предпочтительным является трансдермальный путь введения эстрогенов.
Для повышения комплаенса гормональной терапии возможно ее сочетание с применением фитопрепаратов. Так, при наличии мастодинии/масталгии назначение Мастодинона, обладающего мягким дофаминергическим, противоотечным и аналгезирующим действием, способствует улучшению переносимости ЗГТ [8]. При выраженных вазомоторных и психосоматических симптомах сочетанное назначение гормональной терапии и фитоэстрогенов обусловливает потенцирование эффекта восполнения дефицита эстрогенов, быстрое достижение клинического эффекта. Возможно также применение препаратов, восполняющих дефицит ДГЕА, для улучшения функции яичников.
Для лечения и профилактики психовегетативных расстройств, нормализации сна, повышения стрессоустойчивости можно также рекомендовать средства седативного и анксиолитического действия.
Учитывая данные исследований последних лет (Giraldo H. et al., 2017) [9], показывающие, что применения стандартной дозы ЗГТ не всегда достаточно для предотвращения развития остеопении и остеопороза при ПЯН, дополнительной опцией может быть назначение препаратов антирезорбтивного действия, витамина D и кальция.
Решение проблем фертильности у женщин с ПЯН
В половине случаев ПЯН наблюдаются самопроизвольные флюктуации уровней гормонов и функции яичников. У 5-10% лиц, которым диагностирована ПЯН, возможно спонтанное восстановление функции яичников и наступление беременности.
В противном случае при наличии репродуктивных планов проводится экстракорпоральное оплодотворение, стимуляция овуляции. Однако эффективность последней процедуры недостаточна, что связано не только с небольшим количеством, но и с низким качеством ооцитов [10]. Вместе с тем в литературных источниках имеются сведения о том, что эстроген-гестагенная терапия в переходном периоде ПЯН повышает шансы наступления самостоятельной беременности и улучшает успех ВРТ за счет снижения ФСГ и увеличения чувствительности к нему клеток гранулезы, а также улучшения качества яйцеклеток [11].
В настоящее время разрабатываются новые перспективные методы лечения ПЯН – применение стволовых клеток, генная терапия.
Таким образом, диагноз преждевременной яичниковой недостаточности – не приговор, и одной из задач врача является разъяснение этого факта пациентке. Следует убедить женщину, что на современном этапе возможно подобрать индивидуализированную эффективную и безопасную терапию, способствующую поддержанию состояния ее здоровья и качества жизни, а иногда и восстановлению репродуктивной функции.
Список использованной литературы
1. Persani L., Rossetti R., Cacciatore C. Genes involved in human premature ovarian failure. J Mol Endocrinol. 2010; 45 (5): 257-79.
2. Arora P., Polson D. W. Diagnosis and management of premature ovarian failure. The Obstetrician & Gynaecologist 2011;13:67-72.
3. Maclaran K., Panay N. Premature ovarian failure. J Fam Plann Reprod Health Care. 2011; 37 (1): 35-42.
4. Bretherick K. L., Fluker M. R., Robinson W. P. FMR1 repeat sizes in the gray zone and high end of the normal range are associated with premature ovarian failure. Hum Genet. 2005;117 (4): 376-82.
5. Cobin R. H., Goodman N. F. Аmerican Аssociation of clinical endocrinologists and Аmerican Сollege of endocrinology position statement on menopause – 2017 update. Endocrine Practice. 2017; 23 (7): 869-880.
6. Baber R. J., Panay N., Fenton A.; IMS Writing Group. 2016 IMS Recommendations on women’s midlife health and menopause hormone therapy. Climacteric. 2016;19 (2): 109-150.
7. ACOG Committee opinion No 565. Hormone Therapy and Heart Disease (June 2013, Reaffirmed 2015 URL: https://www.acog.org/Clinical-Guidance-and-Publications/Committee-Opinions/Committee-on-Gynecologic-Practice/Hormone-Therapy-and-Heart-Disease.
8. Т. Ф. Татарчук, Н. В. Косей, О. А. Ефименко. Опыт применения Мастодинона для профилактики мастодинии при ЗГТ //Здоровье женщины № 3, 2001.
9. Giraldo H. et al. Standard hormone therapy is inadequate for bone density in premature ovarian insufficiency. Gynecological Endocrinology. 2017; 33 (4): 283-286.
10. Zeev Blumenfeld. Fertility treatment in women with premature ovarian failure. Expert Review of Obstetrics & Gynecology. 2011; 6 (3): 321330.
11. Pinelli S. et al. Estrogen treatment in infertile women with premature ovarian insufficiency in transitional phase: a retrospective analysis Journal of assisted reproduction and genetics (2017).
Журнал «Медичні аспекти здоров'я жінки» ‘ 2018. Спецвипуск «Гормональна терапія та контрацепція»