10 липня, 2018
Синдром хронической усталости: патогенез и диагностика
Синдром хронической усталости (СХУ) (Chronic fatigue syndrome – CFS), или миалгический энцефаломиелит, – заболевание, характеризующееся когнитивными и вегетативными расстройствами, миалгией, артралгией, головной болью, нарушением сна, который не восстановливает силы, болью в горле и лимфатических узлах, повышенной чувствительностью к шуму и свету, с длительностью симптомов как минимум 6 месяцев [1-3]. Наиболее частыми признаками СХУ являются бессонница, высокая тревожность, апатия, разнообразные фобии, быстрое утомление, склонность к рефлексии, диарея/запор, потеря мотивации и источников удовольствия, депрессия, раздражительность.
 Еще в 1984 г. впервые было отмечено, что СХУ может быть отдельном заболеванием, однако только в 1988 г. Центр по контролю и профилактике заболеваний, США (Centers for Disease Control and Prevention – CDC), выделил его как самостоятельное заболевание с отдельной нозолической единицей (код МКБ 10-10D.86.9). Распространенность СХУ колеблется от 0,2 до 6,41% среди взрослого населения (60-85% из которых женщины) и составляет 1-3 случая на 1 тыс. человек, что уступает лишь сердечно-сосудистым и онкологическим патологиям [4].
Еще в 1984 г. впервые было отмечено, что СХУ может быть отдельном заболеванием, однако только в 1988 г. Центр по контролю и профилактике заболеваний, США (Centers for Disease Control and Prevention – CDC), выделил его как самостоятельное заболевание с отдельной нозолической единицей (код МКБ 10-10D.86.9). Распространенность СХУ колеблется от 0,2 до 6,41% среди взрослого населения (60-85% из которых женщины) и составляет 1-3 случая на 1 тыс. человек, что уступает лишь сердечно-сосудистым и онкологическим патологиям [4].
Пик заболеваемости СХУ отмечается в возрасте 25-49 лет, т. е. приходится на наибоее активный, трудоспособный период жизнедеятельности человека. Поражения при этом синдроме характерны для людей, которые занимаются интеллектуальным трудом, где наобходим высокий уровень эмоциональной нагрузки, быстрота реагирования и сообразительность.
К группе риска относятся врачи, менеджеры среднего и высшего звена, учителя, журналисты, преподаватели, студенты, диспетчеры, спасатели и др.
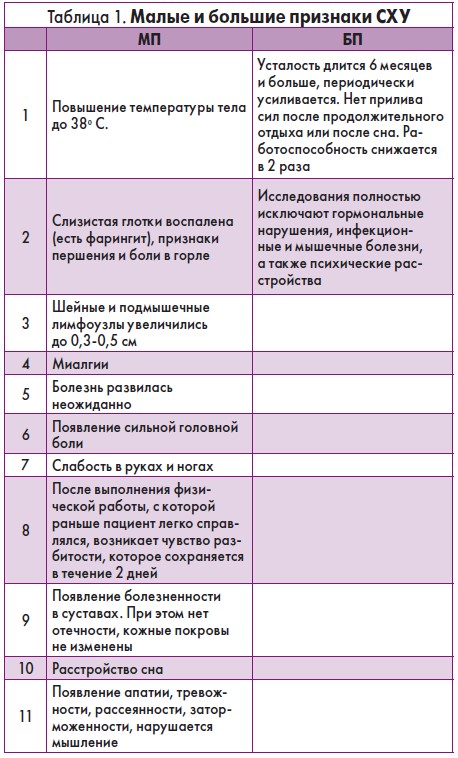
Диагноз СХУ ставится на основании малых (МП) и больших признаков (БП). Подтверждением этого синдрома является следующее: у пациента есть сочетание 6 МП и 2 БП или 8 МП и 2 БП, когда первых 3 МП отсутствуют либо есть всего 1 (табл. 1).
Патогенез СХУ
Причины возникновения данного синдрома до конца не изучены и носят дискуссионный характер. Предложено несколько различных теорий патогенеза СХУ: инфекционная, иммунная, эндокринная, неврологическая, психиатрическая.
1. Инфекционная, или вирусная, теория
 В середине 90-х годов XX века наиболее убедительной считалась инфекционная, или вирусная, теория, которая основывалась на том, что вирусы Эпштейна-Барр (EBV), герпеса (HHV I, II, IV типов), Коксаки, гепатита С, энтеровирус, ретровирус, цитомегаловирус (CMV) могут служить триггерными факторами СХУ.
В середине 90-х годов XX века наиболее убедительной считалась инфекционная, или вирусная, теория, которая основывалась на том, что вирусы Эпштейна-Барр (EBV), герпеса (HHV I, II, IV типов), Коксаки, гепатита С, энтеровирус, ретровирус, цитомегаловирус (CMV) могут служить триггерными факторами СХУ.
Последователи этой теории предполагали, что высокие титры IgG-антител, направленных против данных вирусов, отражают хроническую, активную инфекцию. Однако исследования случай-контроль выявили повышенные титры антител также и у здоровых индивидуумов через несколько лет после первоначальной инфекции.
Прямых доказательств хронической вирусной репликации и увеличения распространенности СХУ обнаружить не удалось. Полностью не исключается возможность существования еще не идентифицированного вируса (из группы вирусов герпеса), вызывающего СХУ.
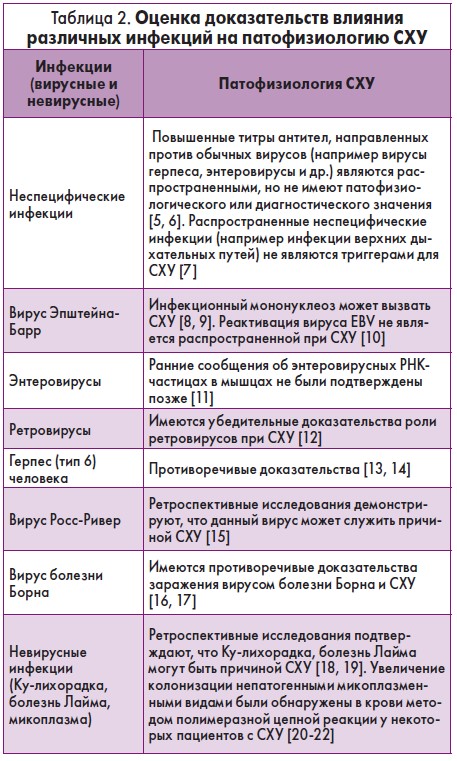
При этом другие известные вирусы (EBV, CMV, HHV‑6 и др.) могут играть вторичную роль, реактивируясь на фоне нарушений иммунного статуса. Результаты исследований влияния различных инфекционных факторов на патофизиологию СХУ представлены в табл. 2
2. Иммунная теория
При СХУ наблюдаются количественные и функциональные нарушения иммунной системы.
Отмечены повышение уровней эндорфина, интерлейкинов‑1, 2, 6, интерферона, фактора некроза опухоли (TNF) и снижение уровня IgG [24]. Обнаружено нарушение функции Т-лимфоцитов в виде уменьшения ответа на стимуляцию митогенами in vitro и снижение цитологической активности естественных киллеров [25].
В случае длительной персистенции в организме вируса Эпштейна-Барр происходит продуцирование фермента дезоксиуридин-трифосфат-нуклеотидгидролазы (dUTPase), что способствует активации продукции TNF, IL‑1β, IL‑6, IL‑8, IL‑10. При этом наблюдается постоянное повышение температуры, снижается вес и физическая активность, что характерно для СХУ [26].
Клеточная цитотоксичность
Наиболее последовательные выводы об изменениях в компонентах иммунной системы у пациентов с СХУ сделаны из исследований функции клеток натуральных киллеров (NК-клетки). NK-клетки являются отдельным типом цитотоксических лимфоцитов и важнейшим компонентом врожденной иммунной системы. NK-клетки играют ключевую роль на самых ранних стадиях распознавания инфицированных вирусом клеток и отторжения трасформированных клеток. NK-клетки могут также секретировать цитокины, которые влияют на другие клетки адаптивной иммунной системы. Снижение количества и активности NK-клеток может служить подтверждением СХУ.
Снижение количества и цитотоксической активности NK-клеток in vitro (CD16+CD56+) были зарегестрированы несколькими группами исследователей у пациентов с СХУ [27-29]. Tirelli и соавт. [31] обнаружили, что, хотя и происходит снижение NK-клеток, при этом повышаются уровни маркеров адгезии (CD11b, CD11c и CD54) и CD38. Это было подтверждено и в недавней публикации Е. Brenu и соавт. [32], где ученые зафиксировали значительное уменьшение уровня CD56 NK-клеток.
У пациентов с СХУ уровни перфорина (цитотоксический белок, содержащийся в гранулах NK-клеток) увеличены в NK-клетках и снижена экспрессия гранзимов А и К (индукторы запрограммированной клеточной смерти) по сравнению с популяцией NK-клеток в контроле. Интересно, что снижение уровней гранзима и перфорина обычно связано с герпевирусными инфекциями [33].
Цитокины
В настоящее время большая роль в патогенезе СХУ отводится нарушениям в системе цитокинов. Последние, являясь медиаторами иммунной системы, не только оказывают иммунотропное действие, но и влияют на многие функции организма, участвуя в процессах кроветворения, репарации, гемостазе, деятельности эндокринной и центральной нервной систем.
Цитокины представляют собой большую категорию маленьких белков, которые играют важную роль в передаче сигналов клетками, выступают как коммуникаторы между клетками иммунной системы и служат для модуляции баланса между гуморальным и прямым клеточно-опосредованным иммунными ответами.
Дисрегуляция цитокинов наблюдается во время и/или после иммуносупрессии, особенно связанной с воспалением. Хотя провоспалительные цитокины, такие как IL‑1, TNF, интерферон тип 1, способствуют системному воспалению, антивоспалительные цитокины, к которым относятся IL‑4, IL‑10 и трансформирующий фактор роста-β (TGF-β), могут ингибировать синтез провоспалительных цитокинов.
В последние годы несколько исследовательских групп изучали уровни цитокинов в сыворотке и спинномозговой жидкости у пациентов с СХУ и здоровых пациентов. Выяснилось, что исследования этих групп не согласуются друг с другом [34-38]. Вероятно, это связано с отличием в выборе методологических подходов в лабораториях, выборе пациентов и контрольной группы, фазы болезни, сроках отбора образцов.
Также недостаточное внимание уделено таким важным переменным, как влияние сна, суточные вариации, действие лекарственных препаратов и др. На сегодня согласованность данных при исследовании цитокинов отсутсвует, поэтому их трудно отнести к главным причинам развития СХУ.
Аллергические проявления
Отмечено, что у большинства пациентов с СХУ заболевание сопровождается аллергическими проявлениями, включая повышенную кожную реакцию к целому ряду аллергенов и увеличение уровня циркулирующего Ig E. Механизмы данной патологии пока не выявлены.
3. Эндокринная теория
В начале 2018 г. опубликовано исследование В. Ruiz-Núñez и соавт. [30], в котором продемонстрирована связь между СХУ и параметрами щитовидной железы (ЩЖ). У 98 пациентов с СХУ (21-69 лет, 21 мужчина) и 99 пациентов контрольной группы (19-65 лет, 23 мужчины) измеряли параметры функционирования ЩЖ, маркеры воспаления и питание, влияющее на эти параметры. У пациентов с СХУ наблюдался нормальный уровень тиреотропного гормона (TSH), но низкие уровни свободного трийодтиронина (FT3) (разница в среднем 0,1%), общего тироксина (ТТ4) (11,9%), общего трийодтиронина (ТТ3) (12,5%), общего трийодтиронина ТТ3 (4,7%).
FT3 ниже референтного интервала был обнаружен у 16 из 98 пациентов с СХУ и у 7 из 99 пациентов контрольной группы. FT3, TT3, ТТ4 и rT3 (reverse T3) положительно коррелировал с hsCRP (высокочувствительный С-реактивный белок) у пациентов с СХУ. Дополнительные анализы показали, что у больных с СХУ был низкий уровень йода в моче и неспецифическое воспаление, что отражает симптомы пациентов с гипотиреозом. У пациентов с СХУ были относительно более высокие уровни другого гормона ЩЖ, так называемого обратного трийодтиронина.
Это, по-видимому, связано с изменением выработки гормонов, когда организм превращает Т4 в rT3 вместо продуцирования Т3. Низкие уровни Т3, обнаруженные у пациентов с СХУ в сочетании с этим переключением на rT3, могут означать, что уровни Т3 сильно снижаются в тканях.
Возможно, что устранение этого гормонального дисбаланса поможет улучшить состояние пациентов с СХУ.
Лабораторные тесты
Исследования лабораторных тестов, которые бы указывали на наличие или отсутствие СХУ, имеют разнонаправленный характер. Так, например, по данным одних исследователей, у пациентов с СХУ наблюдается лейкоцитоз, а по другим – лейкопения. Это касается и таких показателей, как измение формулы крови (лимфоцитоз и лимфопения), а также повышение и снижение иммуноглобулинов классов G, A, M и D. Так как на сегодняшний день нет лабораторных тестов для подтверждения СХУ, оценки его тяжести и течения, используют рекомендуемые тесты только с целью исключения других причин усталости. Центр по контролю и профилактике заболеваний (США) предлагает минимальный набор тестов для пациентов с СХУ [40].
Рекомендуемые лабораторные тесты при СХУ:
- общий анализ крови и скорость оседания эритроцитов;
- уровни электролитов в сыворотке (калий, натрий, магний, кальций, фосфор);
- биохимические тесты для диагностики функционирования печени;
- тесты для оценки функции ЩЗ (Т3, Т4, FT3, FT4, TSH);
- мочевина, креатинин;
- С-реактивный белок;
- общий анализ мочи.
Нерекомендуемые лабораторные тесты при СХУ:
- серологические тесты (вирус Эпштейна-Барр, энтеровирусы, болезнь Лайма);
- рутинный анализ функционирования иммунной системы (субтипы лимфоцитов, уровни иммуноглобулинов и др.);
- токсины;
- метаболиты белков мочи.
Дополнительные исследования выполняют в том случае, когда история болезни достоверно указывет на другой диагноз (например аутоиммунная болезнь соединительной ткани, целлиакия) или патологию, обнаруженную при скрининговом исследовании.
Нерекомендуемые диагностические тесты должны выполняться только в контексте с надлежащим образом разработанными и одобренными с этической точки зрения клиническими исследованиями.
Активин В и СХУ
Активины идентифицированы в 1986 г. Они участвуют в биосинтезе и секреции фолликулостимулирующего гормона, регуляции менструального цикла. Имеют множество физиологических функций и играют роль в пролиферации и дифференциации клеток, апоптозе, метаболизме, гомеостазе, иммунном ответе и эндокринной системе. Обнаружены в экстрагонадных тканях, в том числе в трофобласте и децидуальной оболочке плаценты, яичках, надпочечниках, головном и спинном мозге, передней доле гипофиза. Активины являются димерами с массой ~25 кДа, которые состоят из 2 идентичных β-субъединиц и относятся к суперсемейству белков TGF-β. Димеризуются в следующие формы: активин А (βAβA) и активин В (βBβB) [41].
В 2017 г. было опубликовано исследование В. Lidbury и соавт. [42], в котором авторы изучали потенциал активина А, активина В и их связывающего белка фоллистатина как сывороточных маркеров при СХУ. В исследование включены 45 пациентов (40 женщин и 5 мужчин в возрасте 19-66 лет) с диагнозом СХУ при продолжительности болезни от 2 до 40 лет. Группа контроля состояла из 17 здоровых участников (13 женщин и 4 мужчин в возрасте 24-60 лет).
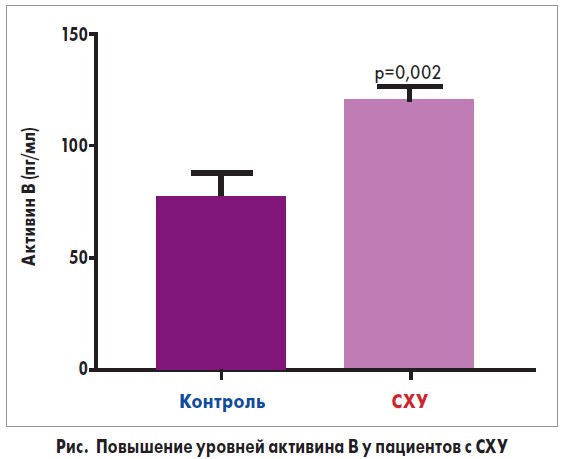 Концентрацию активина А и активина В в сыворотке определяли использованием иммуноферментного анализа [43, 44]. Было обнаружено значительное повышение (р=0,002) уровней активина В в отличие от активина А и фоллиститатина в образцах пациентов с СХУ по сранению с контрольной группой (рис.).
Концентрацию активина А и активина В в сыворотке определяли использованием иммуноферментного анализа [43, 44]. Было обнаружено значительное повышение (р=0,002) уровней активина В в отличие от активина А и фоллиститатина в образцах пациентов с СХУ по сранению с контрольной группой (рис.).
Повышение уровней активина В при СХУ является уникальным по сравнению с Активином А и другими цитокинами, такими как IL‑2 IL‑4, IL‑6, IL‑10, IL‑17A, TNF, IFN-γ, которые не были статистически значимыми.
Результаты данного исследования позволяют сделать вывод о том, что у пациентов с симптомами СХУ уровни активина В в сыворотке значительно повышены по сравнению с референтными интервалами.
Выводы
- СХУ является достаточно распространенной патологией, развитие которой связано с санитарно-экологическими особенностями проживания населения, частыми и длительными стрессами, гиподинамией, монотонной и напряженной работой, эмоциональной и психической нагрузкой, отсутствием жизненных перспектив.
- Для установления диагноза СХУ врач-клиницист должен исключить инфекционные, вирусные, паразитарные заболевания, дисфункцию ЩЖ, аутоиммунные, онкологические, гематологические, неврологические, психические заболевания, отравление тяжелыми металлами, лекарственными препаратами.
- Диагноз СХУ подтверждается, когда исключены другие болезни и не найдены другие причины систематической усталости.
- При СХУ не отмечается изменений в стандартных лабораторных тестах.
- Одним из объективных лабораторных показателей, который применяется в последнее время для подтверждения СХУ, является исследование гормонов ЩЖ. Отмечено снижение FT3, TT3 и TT4 при нормальном TSH.
- Считается, что перспективным биомаркером может стать определение сывороточной концентрации активина В, который увеличивается у пациентов с СХУ.
- СХУ отличается доброкачественным течением и полностью обратим.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 11-12 (432-433), червень 2018 р.


