17 вересня, 2018
Преэклампсия как проблема современного акушерства
С какими трудностями сталкивается врач при выборе тактики у пациенток с преэклампсией в условиях реформирования отечественного здравоохранения?
Продолжение. Начало в № 1 (29), стр. 18-19.
 Беременным с умеренным и высоким риском развития преэклампсии, особенно с низким потреблением кальция в рационе, следует предлагать прием этого макроэлемента до 1-2 г в сутки. Кальций в организме преимущественно содержится в костях, частично в плазме крови.
Беременным с умеренным и высоким риском развития преэклампсии, особенно с низким потреблением кальция в рационе, следует предлагать прием этого макроэлемента до 1-2 г в сутки. Кальций в организме преимущественно содержится в костях, частично в плазме крови.
Если беременная употребляет в пищу недостаточное количество кисломолочных продуктов, овощей и фруктов, если в рационе преобладают вещества, способствующие выведению кальция из организма (поваренная соль, газированные напитки, кофе), возможен дефицит кальция. Известные сегодня кальциевые калькуляторы позволяют рассчитать необходимое количество кальция в рационе.
Недостаток кальция при его низком потреблении может вызвать повышение кровяного давления, поскольку стимулируется выброс паратиреоидного гормона или ренина, которые, в свою очередь, увеличивают содержание внутриклеточного кальция в гладкомышечных стенках сосудов, что приводит к вазоконстрикции. Предполагают, что при повышении уровня кальция в крови уменьшается выработка паратиреоидного гормона, снижается количество внутриклеточного кальция, таким образом проявляется эффект вазодилатации.
Возможно, кальций опосредовано увеличивает уровень магния в крови и нормализует гладкомышечную функцию сосудов. Не исключено, что добавка кальция влияет на маточно-плацентарный кровоток, снижается индекс сопротивления в маточных и пупочных артериях.
Следует отметить, что прием кальция во второй половине беременности напрямую снижает АД, но не корректирует нарушение функции эндотелия или сосудов при преэклампсии.
Разделение суточной дозы препаратов кальция на несколько приемов может улучшать его усвоение. Рекомендуемая экспертами ВОЗ (2017 г.) схема приема кальция составляет 1,5-2 г/сутки перорально в три приема, предпочтительно во время еды. Существует мнение специалистов, что при одновременном приеме препаратов железа и кальция последний препятствует усвоению железа в желудочно-кишечном тракте, а железо способствует выведению кальция из организма, поэтому целесообразно принимать эти препараты с интервалом в несколько часов (не менее трех), а не одновременно.
Прием таблетки карбоната кальция сравнительно большого размера может вызвать дискомфорт у беременных, который усиливается при трехкратном суточном приеме этого препарата.
До настоящего времени отсутствуют четкие рекомендации об оптимальных сроках начала профилактического приема кальция, однако в мире осуществляются исследования в этом направлении. Кальций и магний во время беременности по рекомендации экспертов (руководство ВОЗ 2017 г.) могут назначаться для уменьшения судорог в ногах.
Единственным обязательным симптомом, наблюдаемым при преэклампсии, является гипертензия. Об особенностях измерения АД у беременных, интерпретации полученных результатов упоминалось ранее. Спорным остается вопрос об уровне АД, при котором следует начинать антигипертензивную терапию.
Большинство специалистов по вопросам гипертензивных расстройств при беременности согласны, что требуется срочное медикаментозное снижение АД, достигшего уровня 160-170/110 мм рт. ст., поскольку существует риск внутримозгового кровоизлияния и эклампсии. Эффекта от лечения повышенного уровня АД следует добиться в течение нескольких часов.
Считается, что такой уровень АД является суррогатным (заместительным) маркером риска развития инсульта, а также отражает тяжелое общее состояние женщины при преэклампсии. Для достижения целевого уровня АД во время беременности может быть использован ряд различных антигипертензивных средств. Ингибиторы ангиотензинпревращающего фермента и блокаторы рецепторов ангиотензина противопоказаны при беременности.
Использование этих препаратов в ІІІ триместре беременности приводит к неонатальной почечной недостаточности и гибели плода. При остром состоянии обычно используется нифедипин короткого действия перорально либо лабеталол или гидралазин внутривенно. Для повседневного контроля АД широко используемыми препаратами остаются пероральные метилдопа, нифедипин, окспренолол и гидралазин.
В опубликованной в 2016 г. FIGO монографии «Гипертензия у беременных. Рекомендации по мониторингу, профилактике и ведению» под редакцией Laura A. Magee и соавт. предложен выбор следующих гипотензивных препаратов.
При тяжелой гипертензии (АД ≥160/110 мм рт. ст.) следует использовать пероральные и парентеральные средства, прием которых при необходимости можно повторить через 30 мин, если АД остается на прежнем уровне:
- нифедипин в таблетках (10 мг перорально, до 30 мг);
- гидралазин (5 мг болюсно, если необходимо, 5-10 мг до 45 мг);
- лабеталол (20 мг, если необходимо, 40 мг, затем 80 мг до 300 мг).
Предлагается применение альтернативных пероральных гипотензивных средств, прием которых можно повторить через 1 ч:
- клонидин 0,1-0,2 мг;
- лабеталол 200 мг;
- каптоприл 6,25-12,5 мг (только в послеродовом периоде).
При нетяжелой артериальной гипертензии рекомендуется:
- метилдопа (500-2000 мг/сут 3-4 раза);
- лабеталол (300-2400 мг/сут 3-4 раза);
- нифедипин (20-120 мг/д один раз в день).
В настоящее время нет окончательного согласия в отношении уровня АД, который необходимо поддерживать, если антигипертензивные препараты при беременности назначаются не по ургентным показаниям. В ISSHP считают, что существующие данные не позволяют делать определенные заявления.
В частности, в руководстве Общества акушеров и гинекологов Канады обозначено придерживаться уровня АД 130-155/90-105 мм рт. ст. при отсутствии сопутствующих заболеваний, в то же время Национальный институт здравоохранения Великобритании рекомендует удерживать САД ниже 150 мм рт. ст., а ДАД – между 80 и 100 мм рт. ст. В ISSHP отмечают, что АД не следует снижать ниже упомянутых нижних уровней, так как это может ухудшить плацентарную перфузию, однако данное утверждение нуждается в дальнейших исследованиях. Разумным подходом является поддержание САД выше 110 мм рт. ст. и ДАД – выше 80 мм рт. ст. (табл. 1).
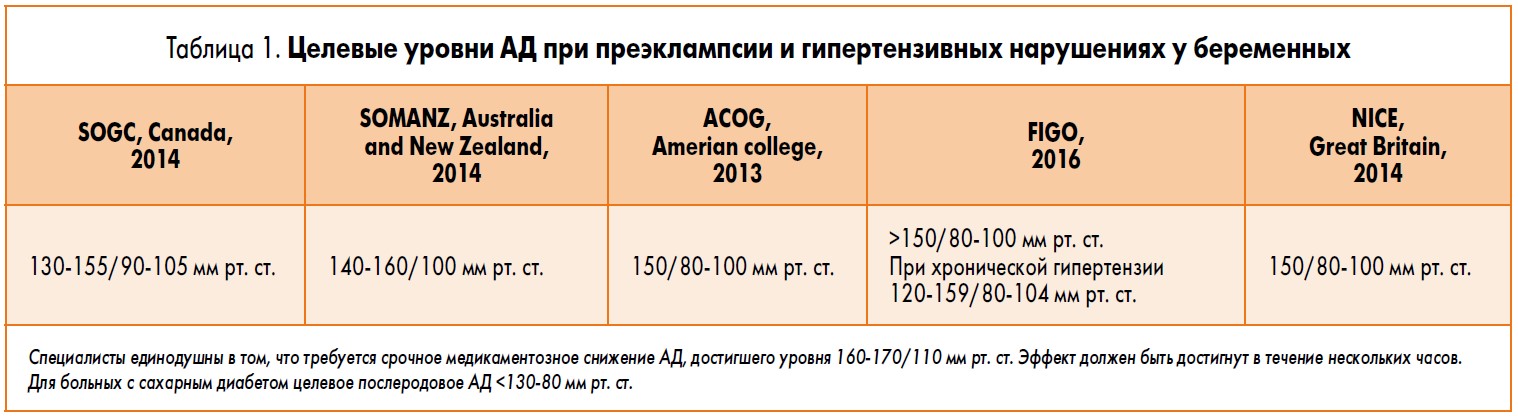
Каждое медицинское учреждение должно иметь клинический протокол (на основании национальных или международных рекомендаций), который регламентирует целевое АД и контроль ассоциированных материнских и перинатальных исходов беременности.
В послеродовом периоде повышение АД обычно достигает своего пика к концу первой недели, между 3-м и 6-м днем, поэтому требуется тщательное мониторирование АД с целью его возможной коррекции. Родильницы, как правило, уже выписаны из стационара, поэтому настоятельно рекомендуется инструктаж таких пациенток и консультирование относительно образа жизни в дальнейшем (WHO, 2012).
У женщин, имевших преэклампсию или гипертензивные нарушения при беременности, существует долгосрочный прогноз ранних кардиоваскулярных рисков, а также риска развития хронических заболеваний почек. Следует использовать идеальное окно возможностей устранения этих рисков в послеродовом периоде.
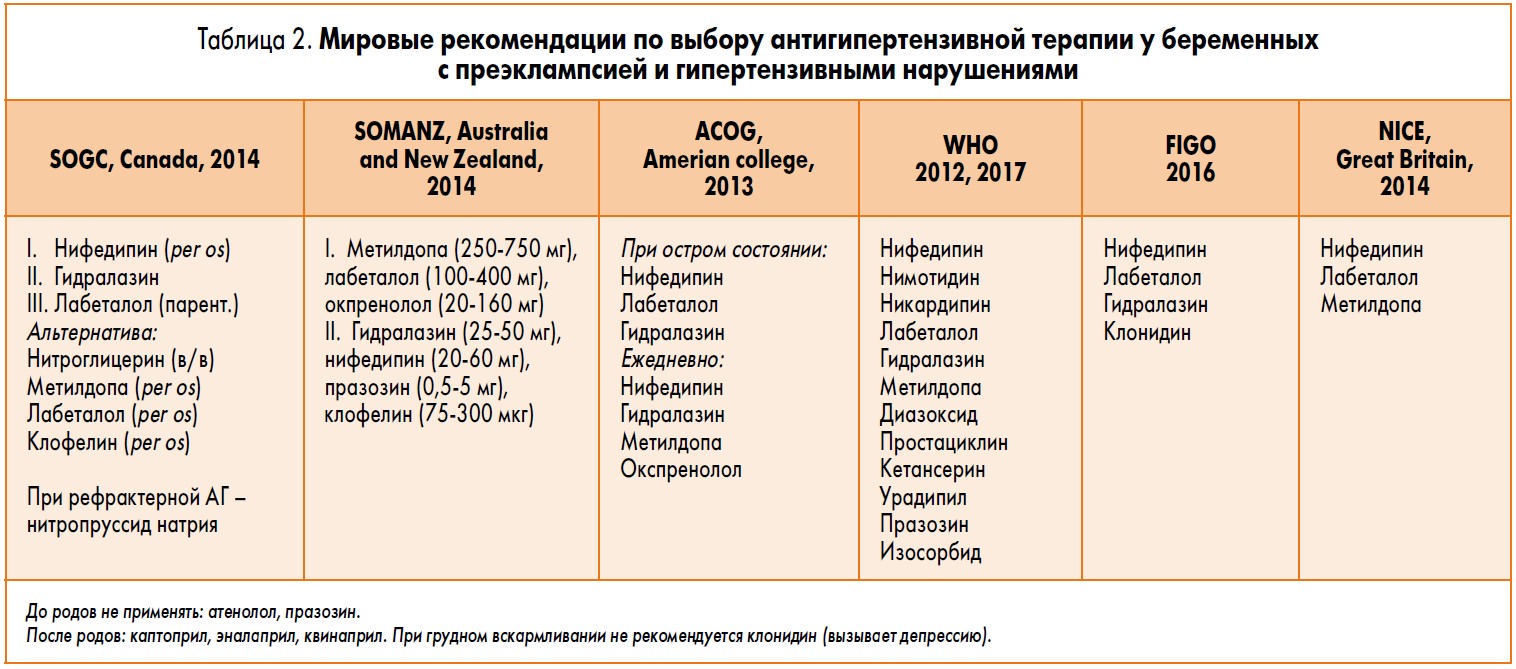
Наиболее важным моментом выбора и использования антигипертензивной терапии является знание практическим врачом особенностей и опыт применения антигипертензивного препарата в данной клинике. Практически у каждого антигипертензивного средства имеются как преимущества, так и побочные эффекты. В таблице 2 представлены антигипертензивные средства, рекомендуемые в известных мировых руководствах для применения при преэклампсии и гипертензивных расстройствах у беременных.
В рекомендациях междисциплинарной рабочей группы SOMANZ (2014) отмечена потенциальная роль применения прямых антикоагулянтов в профилактике преэклампсии у беременных с риском ее развития, особенно когда речь идет о неблагоприятных исходах беременности у женщин с наследственной тромбофилией. Некоторые авторы указывают на выраженный положительный эффект применения ежедневных инъекций дальтепарина (с подобранной дозой препарата в зависимости от массы тела женщины). Очевидно, для доказательных рекомендаций по этому вопросу требуются дальнейшие разработки.
Не менее важным остается вопрос об особенностях проведения антенатальной профилактики синдрома дыхательных расстройств (СДР) плода у беременных с преэклампсией. Антенатально кортикостероиды применяются с целью достижения фетальной легочной зрелости. SOGC в своем руководстве 2014 г. отмечает, что антенатальную профилактику СДР кортикостероидами следует рассматривать для всех женщин с преэклампсией на сроке ≤34 недель + 6 дней (IА), также следует принять решение об антенатальном применении кортикостероидов у беременных с преэклампсией, родоразрешение которых проводится посредством кесарева сечения на сроке ≤38 недель + 6 дней с целью снижения вероятности респираторных заболеваний новорожденных (IВ).
Члены междисциплинарной рабочей группы SOMANZ считают, что использование стероидной профилактики СДР у плода после 34 недель следует рассматривать индивидуально. Нет убедительных данных в пользу преимущества применения определенного вида кортикостероидов, в частности бетаметазона в сравнении с дексаметазоном.
До настоящего времени спорным остается вопрос о повторных курсах антенатальной профилактики СДР кортикостероидами, хотя в некоторых клиниках используется повторное проведение антенатальной профилактики СДР, если со дня завершения проведенного курса прошло более недели.
Для профилактики и лечения эклампсии рекомендуется полный курс внутримышечных и внутривенных инъекций сульфата магния. В качестве предпочтительного противосудорожного препарата для лечения эклампсии и профилактики эклампсии у женщин с тяжелой формой преэклампсии всеми экспертами рекомендуется сульфат магния (доказательства высокого качества, сильная рекомендация).
Первоначальная дозировка сульфата магния составляет 4 г (16 мл 25% раствора) болюсно с последующим введением 1-2 г в час продолжительностью до 12-24 ч. Сульфат магния применяется также в антенатальном периоде до 34 недель с целью нейропротекции и предотвращения развития детского церебрального паралича в постнатальном периоде. Допускается одновременное применение сульфата магния и нифедипина.
В монографии FIGO «Гипертензия у беременных. Рекомендации по мониторингу, профилактике и ведению» (2016) рекомендуется применение L-аргинина у женщин с уже диагностированной гестационной гипертензией (с протеинурией или без нее), которое может привести к улучшению АД матери и улучшению маточного кровообращения. Оптимальная доза должна быть определена и требуются большие рандомизированные исследования.
В медицинской литературе имеются сообщения о том, что для раннего прогнозирования развития преэклампсии разрабатывается метод анализа вариабельности сердечного ритма беременной (heart rate variability, HRV) и статистический метод анализа RR-интервалов по данным ЭКГ. Учитывая, что в организме человека симпатическая система ответственна за вазоконстрикцию, а парасимпатическая – за вазодилатацию, сбалансированная работа этих систем обеспечивает лабильный физиологический уровень артериального давления.
Анализ вариабельности ритма сердца беременной как важнейшего маркера функций автономной нервной системы позволяет определить резервы адаптации и сердечно-сосудистые риски, а с помощью частотного домена определить симпатовагальный баланс (соотношение низкочастотного компонента (LF) к высокочастотному компоненту (HF) автономной нервной системы).
Исследования показали, что вегетативный баланс LF/HF у беременных с преэклампсией значительно превышает аналогичный показатель нормотензивных беременных. Специфичность анализа вариабельности сердечного ритма в прогнозировании преэклампсии у беременных достигает 80%. Для повсеместного внедрения метода в рутинную медицинскую практику необходимы дальнейшие исследования.
Изменения уровня циркулирующих ангиогенных факторов (увеличеное содержание растворимых FMS, таких как тирозинкиназа‑1 (sFlt‑1) или растворимый эндоглин и уменьшенное – плацентарного фактора роста – PlGF) являются патофизиологически важными в развитии преэклампсии и могут иметь потенциальную роль в диагностике. Изменения уровня этих ангиогенных факторов обнаруживаются как до, так и во время возникновения гипертензии у женщин с преэклампсией.
Клиническая польза измерения PlGF самостоятельно или в сочетании с sFlt‑1 остается неясной (SOMANZ, 2014). Фонд медицины плода (Fetal Medicine Foundation, FMF) предлагает комплексную программу оценки риска развития преэклампсии в I триместре. Она включает в себя данные о беременной (вес, этническая принадлежность), наличие клинических факторов риска, УЗИ-признаков (индекса пульсации маточных артерий), средний уровень АД, показатели уровня PlGF и РАРРА, которые при наличии высокого риска значительно снижены.
Комплексная программа позволяет прогнозировать развитие ранней преэклампсии в 93% случаев при уровне ложноположительных результатов 5%. Скрининг должен быть проведен у всех беременных в I триместре в сроках 11-13 недель (оптимально).
В настоящее время существует стратегия двухэтапного скрининга прогнозирования преэклампсии: в I триместре в сроки 11-13 недель (оценка риска развития ранней преэклампсии) и в 30-33 недели для прогнозирования развития преэклампсии после 34 недель. В 2/3 всех случаев преэклампсия развивается после 34-й недели.
Низкие уровни PlGF или отношения растворимой FMS-подобной тирозинкиназы‑1 (sFlt‑1) к PlGF являются эффективными показателями развития преэклампсии в ближайшие 1-4 недели. При выявлении риска развития поздней преэклампсии необходимо обеспечить тщательный мониторинг клинических проявлений преэклампсии у матери и плода, определить алгоритм ведения таких пациенток, сроки родоразрешения, необходимость госпитализации, назначение корригирующей терапии для улучшения материнских и перинатальных исходов.
Для принятия решения об оптимальных сроках родоразрешения с целью минимизации перинатальных и материнских рисков при преэклампсии чрезвычайно важным является определение срока гестации. Рекомендации мировых экспертов относительно сроков родоразрешения у пациенток с преэклампсией и беременностью на фоне гипертензивных расстройств существенно не отличаются.
Сроки родоразрешения женщин с преэклампсией и гипертензивными расстройствами
I. Женщины с преэклампсией на сроке ≥37+0 недель беременности должны быть родоразрешены (ISSHP, 2013; ACOG, 2013; SOGC, 2014; SOMANZ, 2014; WHO, 2012). Выжидательная тактика по сравнению с преиндукцией и индукцией родов при доношенной беременности, осложненной преэклампсией, не имеет преимуществ, а наоборот, сопряжена со значительными осложнениями у матери и плода.
II. К женщинам с преэклампсией между 34 и 37 неделями беременности может применяться выжидательная тактика с консервативным подходом (ISSHP, 2013; WHO, 2012).
III. Женщин с преэклампсией на сроке менее 34 недели беременности следует вести консервативно (выжидательная тактика) в центре матери и медицины плода (ISSHP, 2013; ACOG, 2013; SOGC, 2014; SOMANZ, 2014; WHO, 2012).
Родоразрешение необходимо при следующих обстоятельствах:
- невозможности контролировать АД матери, несмотря на применение антигипертензивных средств;
- пульсоксиметрии матери <90% или имеющемся отеке легких и неэффективности начатой терапии диуретиками;
- прогрессирующем ухудшении функции печени, скорости клубочковой фильтрации, гемолизе или снижении уровня тромбоцитов;
- появлении неврологических симптомов или эклампсии;
- отслойке плаценты;
- реверсном диастолическом токе крови в пупочной артерии по данным доплерометрии, признаках дистресса при кардиотокографии или мертворождении.
Индукция родов рекомендуется женщинам с тяжелой преэклампсией в сроке беременности, при котором плод еще нежизнеспособен и не может достигнуть жизнеспособности в течение одной-двух недель (WHO, 2012).
По заключению канадских специалистов, для женщин с нетяжелой преэклампсией на сроке беременности <24+0 недель врачебное консультирование должно включать информирование о необходимости родов в течение нескольких дней. Для женщин с нетяжелой преэклампсией на сроке беременности от 24+0 до 33+6 недель следует рассмотреть целесообразность выжидательной тактики, но только в условиях медучреждений, способных обеспечить уход за глубоко недоношенными детьми (SOGC, 2014).
Члены группы WHO (2012) и эксперты SOMANZ, составившие руководство (2014), пришли к выводу о том, что доказательства недостаточны и не позволяют подготовить однозначную рекомендацию для пациенток с тяжелой преэклампсией на сроке 34-36 недель беременности (+6 дней). Но, принимая во внимание долгосрочные негативные последствия поздних преждевременных родов, было заявлено, что выжидательная тактика является более предпочтительной, чем раннее родоразрешение.
Эксперты ISSHP отмечают, что в качестве показания для родоразрешения не следует использовать ни уровень мочевой кислоты в сыворотке крови, ни степень протеинурии. Женщины с хронической, гестационной гипертензией и гипертензией «белых халатов» должны быть родоразрешены не позднее 40 недель либо раньше, если имеются перечисленные выше признаки материнских и перинатальных осложнений преэклампсии.
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 2 (30), червень 2018 р.