23 жовтня, 2018
Системний червоний вовчак у дітей
 Системний червоний вовчак – одне з найскладніших аутоімунних захворювань, воно виникає внаслідок генетично зумовленої недосконалості імунорегуляторних процесів. При ньому в організмі з’являються антитіла до власної ДНК, у системний запальний процес залучаються будь-які тканини організму, у результаті чого утворюються циркулювальні імунні комплекси, які відкладаються в субендотеліальному шарі базальної мембрани судин органів, спричиняють запальну реакцію, активуючи комплемент, міграцію нейтрофілів, вивільняючи кініни, простагландини й інші ушкоджувальні чинники [15, 17]. Відповідно до Міжнародної класифікації хвороб 10-го перегляду, системний червоний вовчак (СЧВ) внесений до блоку хвороб сполучної тканини (клас ХІІІ, код М32).
Системний червоний вовчак – одне з найскладніших аутоімунних захворювань, воно виникає внаслідок генетично зумовленої недосконалості імунорегуляторних процесів. При ньому в організмі з’являються антитіла до власної ДНК, у системний запальний процес залучаються будь-які тканини організму, у результаті чого утворюються циркулювальні імунні комплекси, які відкладаються в субендотеліальному шарі базальної мембрани судин органів, спричиняють запальну реакцію, активуючи комплемент, міграцію нейтрофілів, вивільняючи кініни, простагландини й інші ушкоджувальні чинники [15, 17]. Відповідно до Міжнародної класифікації хвороб 10-го перегляду, системний червоний вовчак (СЧВ) внесений до блоку хвороб сполучної тканини (клас ХІІІ, код М32).
Середній вік дебюту хвороби припадає на 6-11 років. Аналіз літератури свідчить, що захворюваність на СЧВ становить від 6 до 20 випадків на 100 тис. населення, хворіють переважно жінки [21, 22]. Останнє зумовлено різною дією статевих гормонів на імунну відповідь (естрогени сприяють підвищенню синтезу антитіл та Th2-цитокінів, натомість андрогени пригнічують клітинні реакції). СЧВ уражає населення усіх вікових груп.
В Україні, за даними медичної статистики, захворюваність на СЧВ серед дітей 0-17 років становила 0,4 на 100 тис. (О.П. Волосовець, 2017). Наявність НLA-DR2 або НLA-DR3 зумовлює підвищення ризику розвитку СЧВ у 2-3 рази, а носійство гаплотипу А1, В8, DR3 – у 10 разів [6, 22]. Окрім СЧВ виділяють інші форми вовчака: неонатальний, шкірний і медикаментозний [7, 14]. При шкірній формі у патологічний процес залучається тільки шкіра, системних проявів немає [5].
До цієї форми належать дискоїдний червоний вовчак і підгострий шкірний вовчак. Медикаментозна форма вовчака, спричинена застосуванням певних лікарських препаратів, за характером перебігу і клінічними ознаками подібна до СЧВ, але, на відміну від ідіопатичного вовчака, не потребує специфічного лікування, крім відміни препарату, який його зумовив [15].
З появою сучасних терапевтичних технологій виживаність хворих на СЧВ протягом 5, 10 і 15 років відповідно становить 96, 93 і 76%. Смертність від СЧВ значно варіює залежно від статі, належності до етнічної групи та країни проживання. Найтяжчий перебіг захворювання відзначають у чорношкірих чоловіків [16, 23].
Максимальна кількість дебютів СЧВ у дітей спостерігається після 10 років, переважно у дівчаток, але хвороба може розвинутися й у хлопчиків. Останніми роками реєструються випадки початку СЧВ у дітей раннього віку [3].
Патогенез. Пусковим механізмом розвитку СЧВ слід вважати дію деяких екзогенних факторів [6, 12]:
- ультрафіолетове опромінення стимулює апоптоз клітин шкіри, що призводить до появи деяких внутрішньоклітинних аутоантигенів на мембрані апоптозних клітин, індукуючи цим розвиток аутоімунного процесу у генетично схильних дітей. Ультрафіолетове опромінення також посилює вивільнення прозапальних цитокінів, що сприяє розвитку локального запалення;
- вплив поліклональних В-клітинних активаторів (інфекційні агенти стимулюють загальну високу імунну відповідь, головним чином, продукцію лімфоцитарних антитіл або антинуклеарного фактора);
- імунізація нуклеарними антигенами; залежно від генетичної схильності хворих це можуть бути бактеріальні чи вірусні інфекції, лікарські препарати, ультрафіолетове опромінення, щеплення тощо.
Морфологічна картина при СЧВ характеризується ураженням клітинних елементів і міжклітинних структур сполучної тканини із розвитком імунокомплексного запалення (мукоїдне набухання, фібриноїдні та проліферативно-склеротичні процеси), генералізованого ураження судин в основному мікроциркуляторного русла (продуктивний і продуктивно-деструктивний васкуліт) [21].
Серед хімічних медіаторів запалення, що забезпечують місцеві судинні реакції (вазоспазм, вазодилатацію), мають значення гістамін і серотонін, які виділяються у вогнищі запалення із тучних клітин, базофілів, тромбоцитів [21]. Неврогенний вплив на тонус і просвіт судин зумовлений аксон-рефлексом і продукуванням у нервових закінченнях під дією різноманітних подразників речовин, що підтримують запальний процес [19]. Перша безпосередня ушкоджувальна дія на тканини викликає короткочасне скорочення гладеньком’язових волокон у стінці артеріол і, як наслідок, їх звуження, що швидко змінюється стійкою вазодилатацією.
 Місцевий кровообіг сповільнюється, можливий розвиток стазу, мікротромбів. Сповільненню мікроциркуляції сприяють також підвищена в’язкість крові внаслідок ексудації плазми з судин і зростання екстраваскулярного тиску. Кровообіг, який у нормі є ламінарним (формені елементи займають центральну частину кровотоку, плазма – периферичну), у зоні запалення стає турбулентним.
Місцевий кровообіг сповільнюється, можливий розвиток стазу, мікротромбів. Сповільненню мікроциркуляції сприяють також підвищена в’язкість крові внаслідок ексудації плазми з судин і зростання екстраваскулярного тиску. Кровообіг, який у нормі є ламінарним (формені елементи займають центральну частину кровотоку, плазма – периферичну), у зоні запалення стає турбулентним.
Клітини та плазма крові змішуються – і за рахунок цього збільшується можливість контакту клітин з ендотелієм. Спостерігається також посилений вихід плазми крові із судин та, як наслідок, підвищення внутрішньотканинного тиску. Глибина морфофункціональних розладів залежить від ступеня активності процесу, тяжкості васкуліту [13].
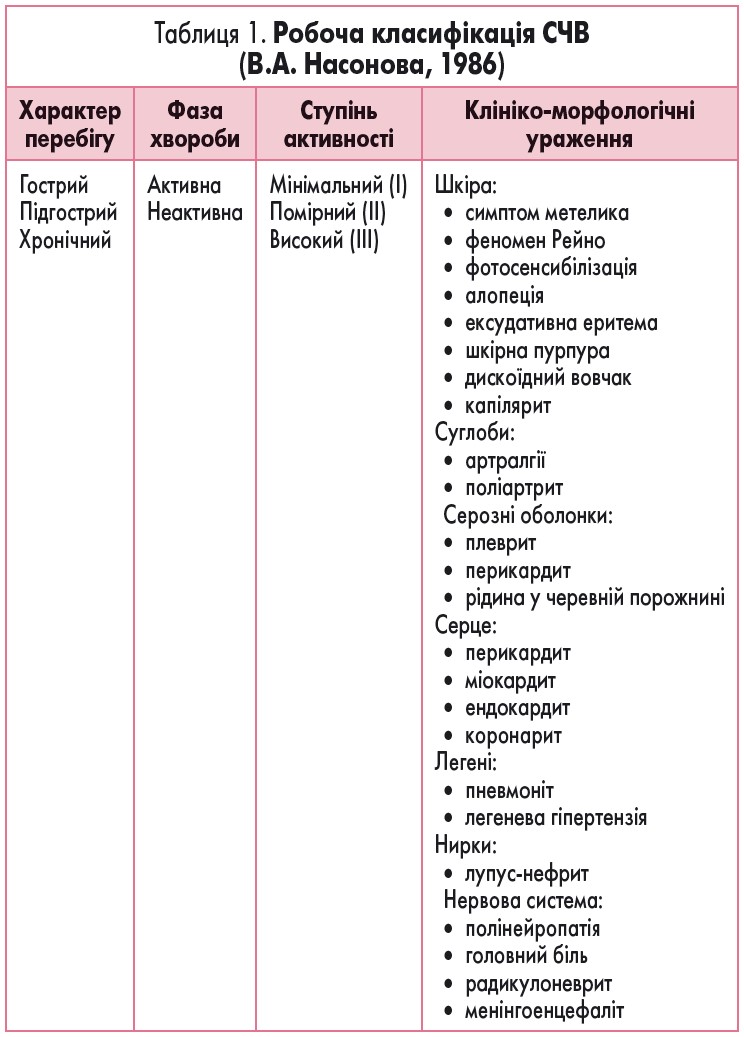
Клінічна класифікація СЧВ представлена у таблиці 1.
Клінічна картина СЧВ. Захворювання на початку може мати різноманітні прояви, воно може одягати «маски» будь-якого патологічного стану. Не випадково СЧВ називають багатоликим. Дебют СЧВ у дітей включає переважне ураження окремих органів і систем, а тяжкість перебігу залежить від активності загального запального процесу [20, 21]. Для загального стану характерна лихоманка на фоні слабкості та порушення самопочуття (зниження апетиту, зменшення маси тіла).
Ураження шкіри та її придатків виявляють у 70-90% пацієнтів, із них у 40% – вже в дебюті захворювання. Вони можуть бути різними: від локального ураження (еритематозна пляма) до тяжких бульозних висипань [16]. Найбільш характерною для перебігу СЧВ є наявність на шкірі обличчя еритематозних плям, що розташовані на щоках і крилах носа (симптом метелика).
Окрім шкіри обличчя еритематозні плями спостерігають на шиї, грудях, над колінними та надп’ятково-гомілковими суглобами. Поверхня еритематозних плям вкрита лусочками, плями мають темно-червоний колір, що може змінюватися відповідно до дії сонця та пори доби (ввечері стає менш інтенсивним). Окрім еритематозних плям на шкірі обличчя, шиї, грудей, кінцівок можуть розташовуватись кільцеподібні висипання з телеангіектазіями та депігментацією у центрі кільця.
Висипання можуть також мати вигляд геморагій та ерозій. Характерна фотосенсибілізація – підвищена чутливість шкіри до впливу сонячного опромінення, посилення інтенсивності еритематозних висипань після перебування під прямими сонячними променями. У ділянці дистальних фаланг і подушечок пальців виявляють капілярит, що проявляється набряковою еритемою з телеангіектазіями, атрофією подушечок пальців, долоні, поверхні стоп.
Стан погіршується після перебування на сонці, під час стресових ситуацій, соматичних захворювань. У результаті ураження капілярів кистей і стоп розвивається ішемія пальців (синдром Рейно), яка має стійкий характер. У зв’язку із порушенням трофіки шкіри спостерігаються її сухість, деформація та підвищена ламкість нігтів. У деяких хворих виникає алопеція – стоншення та підвищення випадіння волосся, в результаті чого відбувається гніздове або дифузне облисіння. Можливе також випадіння брів і вій.
Ураження лімфатичних вузлів проявляється полілімфаденопатією зі збільшенням лімфатичних вузлів до 1,5 см. Останні мають м’яку або еластичну консистенцію.
Ураження слизових оболонок відбувається у 30% хворих у вигляді енантеми слизової оболонки ротової порожнини, почервоніння, тріщин губів із сіруватими лусочками (хейліт), ерозіями, виразками [22]. У носі спостерігаються вогнища ерозій, які можуть стати причинами носових кровотеч.
Ураження суглобів проявляються артралгіями в одному або декількох суглобах, артритом міжфалангових, фалангово-п’ясткових, колінних, надп’ятково-гомілкових суглобів, тендинітами і тендовагінітами [5]. У результаті ішемізації кісткових структур може розвинутися асептичний некроз кісток. Ураження найчастіше симетричне.
Можуть спостерігатися ранкова скутість, минущі згинальні контрактури дрібних суглобів, але без деформації самих суглобів. Значного порушення функції суглобів, як при ювенільному ревматоїдному артриті, не відбувається.
Ураження серцево-судинної системи спостерігається при високому ступені запального процесу [22]. Виявляють розвиток перикардиту, міокардиту.
Перикардит при СЧВ може бути сухим або ексудативним. За даними багатьох досліджень, клінічно виражений перикардит нині виявляють у 25% дорослих із СЧВ. Цей діагноз підтверджувався за наявністю скарг (біль у ділянці серця, який посилюється у горизонтальному положенні, задишка), розширенням при перкусії меж відносної серцевої тупості, аускультативно – приглушенням тонів серця або шумом тертя перикарда, на електрокардіограмі (ЕКГ) – елевацією сегмента ST та зниженням вольтажу у всіх відведеннях, даними рентгенографічного дослідження – збільшенням кардіоторакального індексу.
При ехокардіографічному обстеженні перикардит виявляли у 37% випадків, він проявлявся патологічним випотом у порожнині перикарда, що відповідає діастолічній сепарації його листків, та їх потовщенням. При високій активності захворювання спостерігається скупчення великої кількості ексудату, що загрожує тампонадою серця.
Ураження міокарда може проявлятися ознаками серцевої недостатності, аритміями та порушенням провідності у вигляді серцевих блокад, зниженням скоротливої функції міокарда. Гістологічні зміни в міокарді при біопсії представлені периваскулярною та/або інтерстиціальною інфільтрацією макрофагами та лімфоцитами.
Можливі також дегенерація кардіоміоцитів, вогнищева інфільтрація міокарда імунними клітинами та поява дифузного або вогнищевого склерозу чи фіброзу. Часто єдиним клінічним проявом міокардиту при СЧВ є тахікардія, яку виявляють при об’єктивному обстеженні хворого та проведенні електрокардіографії. За відсутності лікування через невиражену клінічну картину міокардит врешті-решт може призвести до розвитку серцевої недостатності, що ускладнює перебіг основного захворювання.
Привертають увагу і дистрофічні процеси в міокарді при СЧВ. Вони виникають за рахунок порушення трофіки кардіоміоцитів через оклюзію дрібних інтраміокардіальних судин на фоні васкуліту. Це може призводити до порушення систолічної та діастолічної функції шлуночків, структурно-функціональної перебудови серця.
Ураження ендокарда спостерігається при панкардиті і призводить до ушкодження клапанного апарату серця, в результаті чого з часом формується набута вада серця (переважно мітральна або аортальна недостатність), недостатність кровообігу. Атиповий бородавчастий ендокардит (ендокардит Лібмана – Сакса) характеризується відкладенням тромботичних мас у вигляді бородавчастих структур (розміром 1-3 мм) на клапанах і хордах та ділянках ерозій ендокарда, які виявляють під час ехокардіографії (бородавчасті відкладення, клапанні вегетації). Нині ознаки ендокардиту та розвиток набутих вад при СЧВ у дітей спостерігаються дуже рідко. Окрім серця уражаються судини дрібного та середнього калібру (ураження коронарних судин може призвести до ішемії міокарда та навіть інфаркту міокарда).
Ураження нирок (лупус-нефрит) є найбільш характерним проявом вісцеральної агресії при СЧВ, коли розвивається імунокомплексний гломерулонефрит. Діагностується у 70% дітей з СЧВ, розвивається протягом перших 2 років від початку захворювання [16].
Залежно від тяжкості клінічної картини, перебігу СЧВ та прогнозу виділяють такі клінічні варіанти вовчакового нефриту (ВН; І.Є. Тареєва, 1985):
1) ВН, що швидко прогресує;
2) активний ВН із нефротичним синдромом;
3) активний ВН із вираженим сечовим синдромом;
4) латентний ВН (нефрит із мінімальним сечовим синдромом).
ВН, що швидко прогресує, становить 10-12% у структурі уражень нирок при СЧВ. Захворювання характеризується нефротичним синдромом, гіпертензією, раннім (у перші місяці) розвитком ниркової недостатності та вкрай несприятливим прогнозом. Морфологічно зазвичай виявляють дифузний проліферативний нефрит. Більшість хворих досить швидко (через 2-3 роки) помирають, проте сучасна терапія може сповільнити прогресування хвороби [16, 24].
Нефрит із нефротичним синдромом розвивається у 30-40% хворих на СЧВ. Особливості вовчакового нефротичного синдрому: різко виражена протеїнурія відзначається рідко, часто поєднується з гіпертензією, гематурією, диспротеїнемія виражена менше.
Активний ВН із вираженим сечовим синдромом спостерігається приблизно у 30% хворих. Клінічна картина характеризується протеїнурією вище 0,5 г на добу, постійною еритроцитурією та лейкоцитурією.
Як окремий варіант виділяють нефрит із мінімальним сечовим синдромом: протеїнурія нижче 0,5 г на добу, іноді незначна лейкоцитурія та еритроцитурія (поодинокі елементи в полі зору), артеріальний тиск нормальний, функція нирок збережена.
Для активного ураження нирок характерні: наростання протеїнурії, нефротичний синдром, артеріальна гіпертензія, еритроцитурія, швидке погіршення функції нирок, високий титр антитіл до нативної ДНК, а також тромбоцитопенія, анемія, високий рівень циркулювальних імунних комплексів.
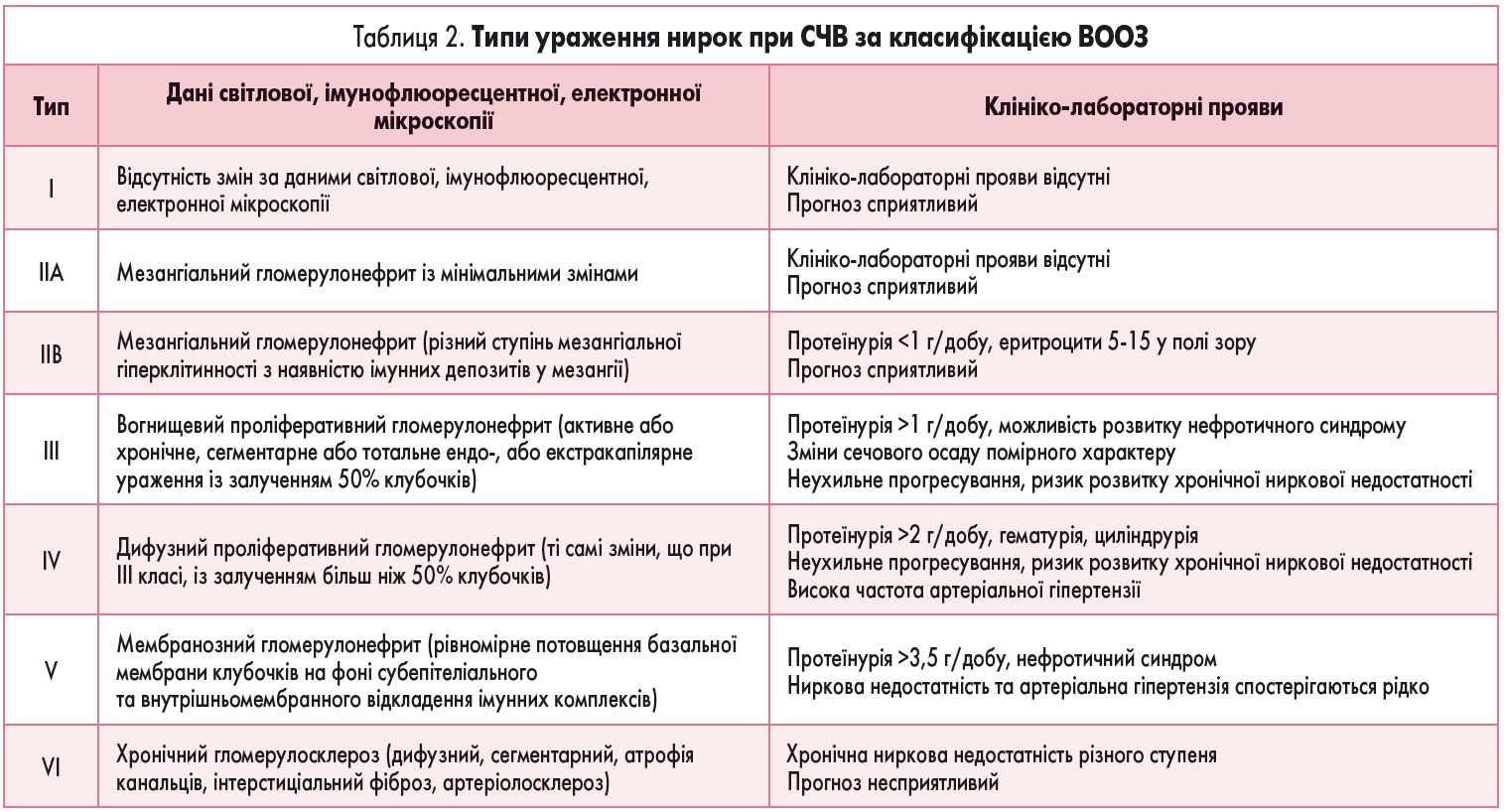
Згідно з класифікацією Всесвітньої організації охорони здоров’я (ВООЗ), при СЧВ виділяють шість типів ураження нирок за результатами біопсії та даними світлової імунофлюоресцентної електронної мікроскопії (табл. 2).
Ураження м’язів при СЧВ відбувається у 30-40% дітей. Воно характеризується запальним ураженням (міозит), ішемією, у результаті чого виникає біль у м’язах, але вираженої слабкості не спостерігається. Найчастіше симетрично уражаються проксимальні м’язи кінцівок [4].
Ураження легенів проявляється легеневим васкулітом, який провокує розвиток лупус-пневмоніту (спостерігаються кашель, задишка, акроціаноз, ослаблення дихання, хрипи у легенях, інфільтративні тіні на рентгенограмі). Можливий розвиток двобічного ексудативного плевриту. При ураженні судин легенів розвивається легенева гіпертензія, під час рентгенологічного дослідження виявляють посилений легеневий малюнок, можливе формування ателектазів у нижніх відділах.
Ураження нервової системи спостерігається майже у всіх хворих і проявляється головним болем, психічною неврівноваженістю, порушенням функції черепних нервів, полінейропатією, ураженням органа зору. Хвору на СЧВ дитину регулярно має оглядати невролог для своєчасного виявлення уражень нервової системи [19, 20].
Ураження шлунково-кишкового тракту зумовлено ступенем ураження його судин. У результаті відносного звуження спостерігають порушення трофіки стінки та слизової оболонки, формуються ерозії та виразки слизової оболонки, розвивається абдомінальний синдром, що проявляється болем у животі [16].
Ураження печінки включає прояви вовчакового гепатиту, при цьому спостерігаються збільшення печінки, жовтяниця, підвищення вмісту печінкових ферментів.
Ураження селезінки розвивається внаслідок периваскулярного набряку або склерозу судин селезінки, проявляється збільшенням органа, яке виявляють пальпаторно.
Антифосфоліпідний синдром (АФС) – це симптомокомплекс, який характеризується венозними або артеріальними тромбозами, рідше тромбоцитопенією та розвитком вторинних проявів тромбофілії (ураження серцево-судинної, нервової систем, шкіри). Може супроводжувати перебіг СЧВ у 10-20% хворих дітей.
Клінічною ознакою АФС при СЧВ є наявність тромбозу дрібних судин у будь-якому органі (на підставі клінічного й інструментального обстеження): некротичні вогнища на кінцівках, ішемічні зміни м’язів, ішемічний інсульт, прояви інфаркту міокарда [4].
До загрозливих для життя станів при СЧВ належить синдром активації макрофагів (САМ), частота якого може становити до 4%. САМ може розвинутися на початку хвороби, ускладнюючи її діагностику та призначення адекватної терапії [20]. Критерії САМ були визначені групою експертів (2009).
Клінічні критерії:
- лихоманка (>38 °C);
- гепатомегалія (≥3 см від ребрового краю);
- спленомегалія (≥3 см від ребрового краю);
- геморагічні прояви (підвищена кровоточивість, пурпура, екхімози);
- ураження центральної нервової системи (збудливість, сонливість, головний біль, судоми).
Лабораторні критерії:
- цитопенія за двома або трьома показниками (лейкоцити <4,0×109/л, гемоглобін <90 г/л, тромбоцити <150,0×109/л);
- підвищення рівня аспартатамінотрансферази (>40 од/л);
- підвищення рівня лактатдегідрогенази (>567 од/л);
- гіпофібриногенемія (<1,5 г/л);
- гіпертригліцеридемія (>150 мг/дл);
- гіперферитинемія (>400 мкг/л).
Дані патогістологічного дослідження: наявність гемофагоцитозу в пунктаті кісткового мозку.
Для встановлення діагнозу необхідна наявність не менше ніж одного клінічного і двох лабораторних критеріїв. Патогістологічне дослідження кісткового мозку показане тільки в сумнівних випадках.
Особливості лабораторних досліджень. У загальному аналізі крові спостерігають підвищення швидкості осідання еритроцитів (ШОЕ), лейкопенію зі зсувом лейкоцитарної формули ліворуч, лімфопенію, гіпохромну анемію, тромбоцитопенію [1].
Під час біохімічного дослідження крові виявляють гіперпротеїнемію, диспротеїнемію, підвищення вмісту серомукоїду, наявність С-реактивного протеїну, підвищення вмісту циркулювальних імунних комплексів.
Імунологічне дослідження крові: наявність кріопреципітатів, антитіл до двоспіральної ДНК, до нуклеосом, антифосфоліпідних антитіл.
У загальному аналізі сечі можлива наявність протеїнурії, гематурії, лейкоцитурії, циліндурії. Пацієнтам із СЧВ рекомендується визначення швидкості клубочкової фільтрації нирок за формулою Шварца для виявлення уражень нирок. Зниження швидкості клубочкової фільтрації свідчить про розвиток ниркової недостатності.
Діагноз АФС підтверджується за наявності вовчакового антикоагулянту в плазмі крові, який виявляють у двох та більше дослідженнях із проміжком 12 тижнів, наявності антикардіоліпінових антитіл (IgM або IgG) у сироватці або плазмі крові у високих титрах, які визначають у двох та більше дослідженнях з інтервалом більше ніж 12 місяців, антитіл до β-глікопротеїну І (IgM або IgG) у сироватці або плазмі крові, які виявляються у двох та більше дослідженнях з інтервалом більше ніж 12 місяців. Діагноз АФС може бути встановлений у хворого за наявності 1 клінічного та 1 серологічного критерію.
Гострий перебіг АФС характеризується високим ступенем запальної активності з боку крові (різко підвищена ШОЕ, лейкоцитопенія, підвищення рівня С-реактивного протеїну, серомукоїду, високі титри антинуклеарного фактора та антитіл до двоспіральної ДНК, нуклеосом), швидким розвитком органних уражень, залученням у патологічний процес нирок. Початок хвороби при цьому раптовий із високою лихоманкою, шкірними висипаннями, артралгіями або артритом, ураженням нирок і внутрішніх органів, трофічними порушеннями [4].
Підгострий перебіг – поступовий розвиток хвороби із субфебрильною та періодично фебрильною температурою тіла, артритом або артралгіями, еритемними висипаннями на шкірі; періодичні загострення з помірним або мінімальним ступенем запальної активності, залученням у патологічний процес нирок та інших внутрішніх органів переважно на першому році захворювання.
Хронічний перебіг – тривалий час домінує один або кілька симптомів (феномен Рейно, дискоїдне ураження шкіри, артрит, незначна протеїнурія тощо) протягом кількох років. Процес повільно прогресує, упродовж декількох років у нього залучаються інші органи та системи.
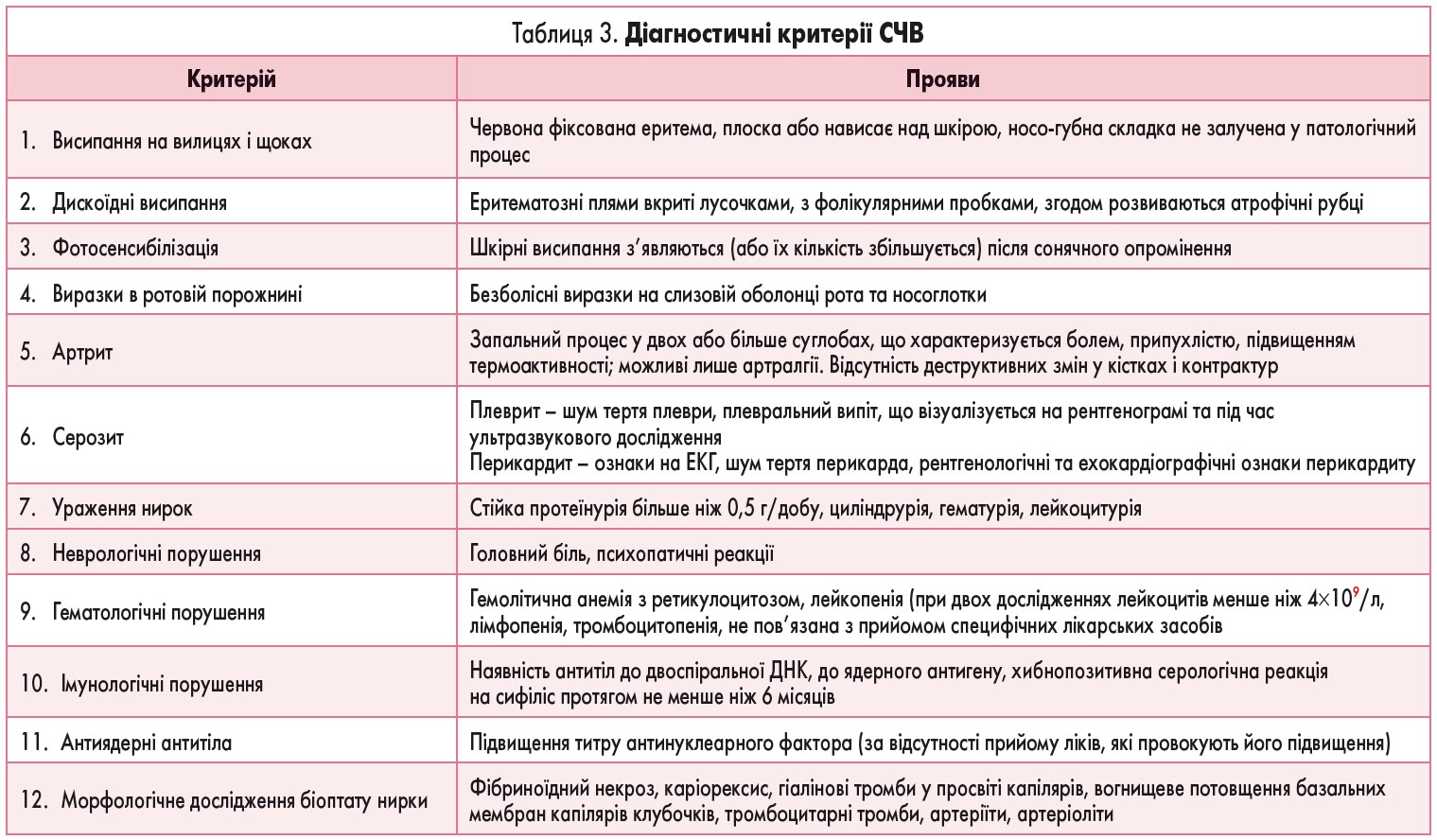
Діагностика СЧВ. Діагностичні критерії СЧВ запропоновані та доповнені Американською асоціацією ревматологів (1982, 1997; табл. 3).
За наявності 4 критеріїв та більше встановлюють діагноз СЧВ. Чутливість діагностичних критеріїв становить 80-90%, специфічність – 90-96%.
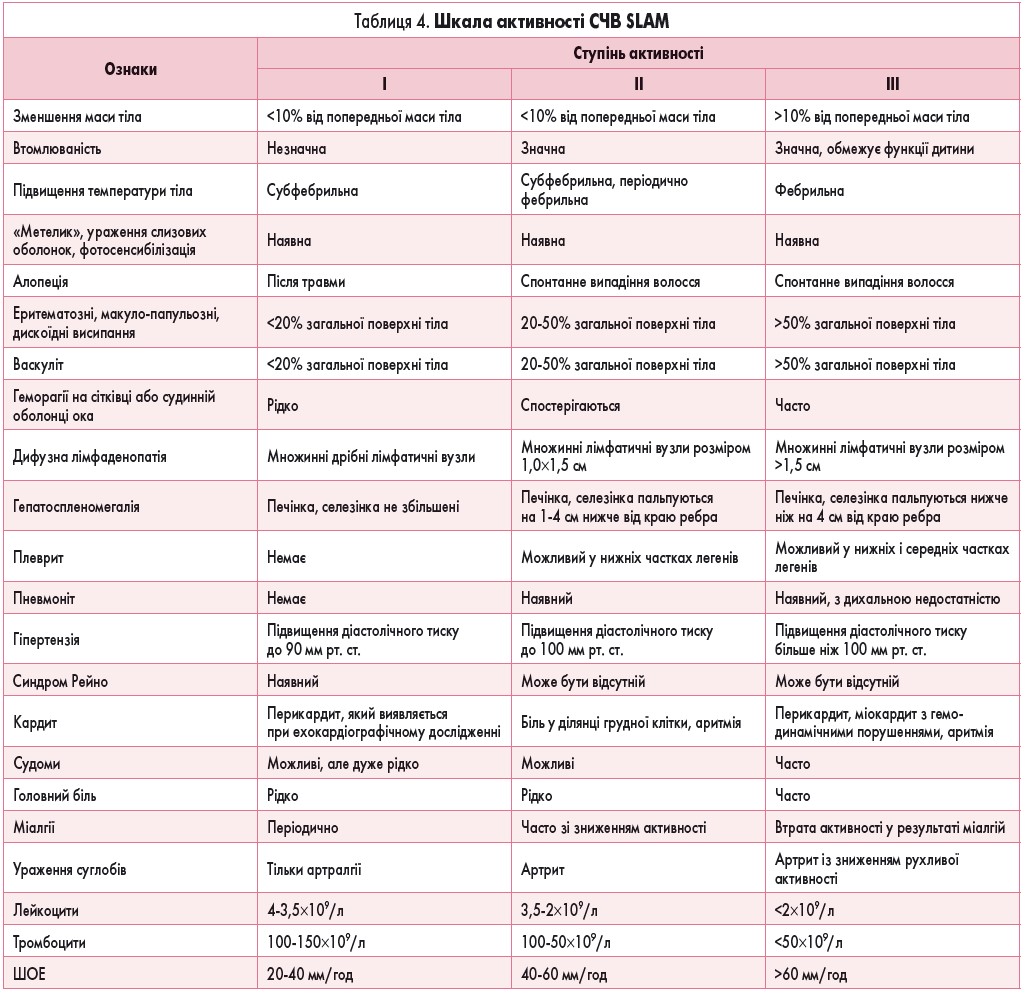
Для оцінювання загальної активності захворювання доцільно використовувати шкалу SLAM, розроблену американськими ревматологами (Systemic lupus activity measure, 2007; табл. 4).
Під час встановлення діагнозу СЧВ необхідна диференційна діагностика від інших дифузних захворювань сполучної тканини: ревматоїдного артриту, дерматоміозиту, системних васкулітів, онкогематологічних захворювань, ревматичної лихоманки, первинного антифосфоліпідного синдрому, захворювань нирок (гломерулонефриту). Основою диференційної діагностики залишаються діагностичні критерії СЧВ, які допомагають своєчасно встановити діагноз [21].
Лікування з приводу СЧВ кожній дитині підбирають індивідуально залежно від характеру перебігу, активності запального процесу та клініко-морфологічних уражень органів і систем [24]. На початку лікар має налагодити тісний контакт із пацієнтом та його батьками, тому що лікування при СЧВ тривале, потребує ретельного моніторингу, своєчасного виявлення побічних дій базових препаратів, загострення запального процесу. Батьки хворого мають усвідомити той факт, що будь-яке питання, пов’язане із призначенням або корекцією лікування їхньої дитини, необхідно вирішувати тільки разом із лікуючим кардіоревматологом.
Алгоритм лікування пацієнта рекомендується складати за результатами аналізу активності захворювання, оцінювання ступеня ураження органів, наявністю супутніх захворювань. Метою лікування дітей з СЧВ є вплив на основні клінічні прояви хвороби, запобігання загостренню аутоімунного запалення, залученню у запальний аутоімунний процес життєво важливих органів і систем (центральної нервової системи, серця, нирок), досягнення клініко-лабораторної ремісії захворювання.
Стартове лікування має проводитися в умовах стаціонару для контролю його ефективності та клінічного стану дитини. Слід здійснювати моніторинг артеріального тиску (2-3 рази на день), систематично проводити контрольні аналізи крові та сечі.
Режим дня дитини має повністю виключати психоемоційні навантаження, фізичну втому. Дієта дитини повинна бути повноцінною, із достатньою кількістю поліненасичених жирних кислот, кальцію, калію, вітамінів, але із низьким вмістом жирів, солі.
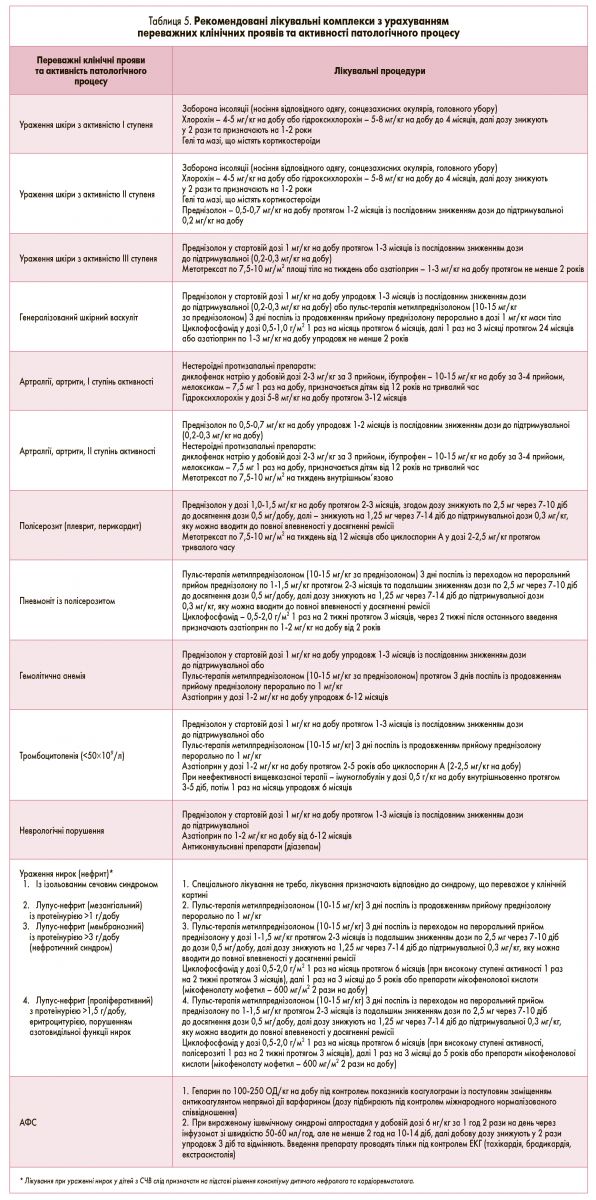 Для оптимізації лікування лікар має виділити основні клінічні прояви СЧВ, оцінити активність запального процесу та відповідно до цього призначити основне лікування (табл. 5).
Для оптимізації лікування лікар має виділити основні клінічні прояви СЧВ, оцінити активність запального процесу та відповідно до цього призначити основне лікування (табл. 5).
Пацієнтам із СЧВ рекомендується призначення препаратів мікофенолової кислоти у таких випадках:
- при неможливості проводити лікування циклофосфамідом у зв’язку з розвитком побічних ефектів або небажанні батьків пацієнта;
- для підтримання ремісії вовчакового нефриту, індукованої введенням циклофосфаміду;
- для індукції ремісії та забезпечення стероїдзберігального ефекту при неефективності циклофосфаміду, метотрексату, азатіоприну.
Мікофенолату мофетил призначають у дозі 600 мг/м2 2 рази на добу, мікофенолову кислоту – у дозі 450 мг/м2 2 рази на добу.
У разі неефективності кортикостероїдів у поєднанні з циклофосфамідом або іншими імунодепресантами, розвитку геморагічного альвеоліту, пневмоніту, ураження центральної нервової системи, АФС, тромбоцитопенії, цитопенії, інфекційних ускладнень рекомендується застосування преднізолону (метилпреднізолону перорально, пульс-терапії метилпреднізолоном) та циклофосфаміду поєднувати з терапією імуноглобуліном людським нормальним. Імуноглобулін людський нормальний застосовують внутрішньовенно в дозі 1-2 г/кг на курс.
Дітям із тяжким, кризовим перебігом захворювання, тяжким ураженням нирок, АФС доцільно включати до комплексного лікування препарати біологічної терапії – антитіла до CD20 В-лімфоцитів – ритуксимаб у дозі 375 мг/м2 на тиждень протягом 4 тижнів, курс лікування можна повторити через 24 тижні.
Пацієнтам, які отримують ритуксимаб, при появі катаральних явищ, лихоманки й ознак пневмонії рекомендується призначити внутрішньовенне введення ко-тримоксазолу (сульфаметоксазол + триметоприм) у дозі 15 мг/кг на добу, кларитроміцину – 15 мг/кг на добу і цефтріаксону – 50-100 мг/кг. Прийом імунодепресанту, інфузії ритуксимабу треба пропустити до одужання, а введення кортикостероїдів продовжити. Прийом імунодепресанту, імунобіологічного препарату продовжують не раніше ніж через 1 тиждень після повного усунення клінічних і лабораторних ознак гострої опортуністичної інфекції.
Пацієнтам, які отримують циклофосфамід, для профілактики розвитку пневмоцистної пневмонії рекомендується призначення ко-тримоксазолу (сульфаметоксазол + триметоприм) перорально в дозі 5 мг/кг.
Більшість хворих потребують тривалого лікування препаратами базисного ряду (від 3 до 8 років).
При виявленні активної герпетичної інфекції рекомендується призначення ацикловіру по 5-10 мг/кг на введення внутрішньовенно через кожні 8 год або ганцикловіру (з 12 років) – 5 мг/кг на введення внутрішньовенно через кожні 12 год протягом 14-21 дня в поєднанні з людським нормальним внутрішньовенним імуноглобуліном по 0,2-0,5 г/кг на курс, пероральне застосування кортикостероїдів продовжують.
Окрім базисної терапії, при СЧВ показана посиндромна терапія:
- Антикоагулянти та антиагреганти: гепарин у середньотерапевтичній дозі 150 тис. ОД/кг на добу; дипіридамол по 5 мг/кг 2 рази на день, пентоксифілін – 20 мг на рік життя за 2 прийоми.
- Кардіометаболіти: АТФ-лонг у дозі 60-80 мг/добу; рибоксин – 10-15 мг/добу; триметазидин – 10-35 мг/добу; мельдоній – 50-75 мг/кг/добу.
- Гіпотензивні препарати (блокатори ангіотензинперетворювального ферменту): каптоприл по 0,3 мг/кг 1 раз на добу, еналаприл – 0,07-0,47 мг/кг за 1-2 прийоми, лізиноприл – 0,08 мг/кг.
- Діуретики: фуросемід по 1-2 мг/кг на введення, спіронолактон – 1-3 мг/кг на добу.
- Препарати кальцію: кальцій D3 – 500-1200 мг/добу ввечері.
- Вітаміни (А, Е, групи В, С, D).
При терапії САМ показані кортикостероїди у високих дозах у режимі пульс-терапії (метилпреднізолон до 30 мг/кг) протягом 3 днів, потім пероральне застосування кортикостероїдів (преднізолон з розрахунку 1-2 мг/кг). При недостатній ефективності до терапії додають інгібітори кальциневрину (циклоспорин А в дозі 4-5 мг/кг на добу), імуноглобулін внутрішньовенно (1 г/кг), а також блокатори інтерлейкіну (IL)-1 (анакінра). Супровідна терапія включає застосування антибіотиків широкого спектра дії, противірусних препаратів, замісне введення свіжозамороженої плазми крові, тромбоконцентрату.
Диспансерне спостереження за дітьми, які хворіють на СЧВ, здійснюють в умовах поліклініки. Однак на першому році дитину слід госпіталізувати через кожні 1-3 місяці, далі – через кожні 6 місяців для контролю перебігу захворювання, адекватності лікування, виявлення побічних дій лікарських препаратів та їх корекції. Обов’язково треба пояснити рідним та самому хворому, що невиконання рекомендацій, самостійна зміна терапії є незалежними факторами несприятливого перебігу захворювання.
Лікар, який спостерігає за дитиною, має підібрати раціональний режим дня, комплекс адекватної лікувальної фізкультури, аерорежим, виключити перебування на відкритих променях сонця (ультрафіолетове опромінення здатне змінювати антигенні властивості ДНК клітин шкіри, сприяє розвитку аутоімунних реакцій, а також підсилює вивільнення IL‑1, IL‑6, фактора некрозу пухлини, сприяючи розвитку локального запалення).
Протягом першого року захворювання дитина обов’язково має перебувати на домашньому режимі, займатися за шкільною програмою в домашніх умовах, далі питання вирішують з урахуванням її стану. Відпочинок треба проводити в звичній кліматичній зоні, від’їзд до моря може спровокувати загострення патологічного аутоімунного процесу.
Хворі на СЧВ можуть відвідувати школу, за винятком періодів активності патологічного процесу, тому профілактика інфекцій шляхом імунізації особливо важлива. Дітям з тяжким перебігом, активною формою СЧВ не вводять жодних вакцин, дітям, які отримують імуносупресивну терапію, кортикостероїди у високих дозах, біологічні препарати, не проводять щеплення з використанням живої вірусної вакцини.
Введення пероральної вакцини проти поліомієліту також протипоказане членам сім’ї, які проживають разом з дитиною, котра отримує імуносупресивну терапію. Хворим на СЧВ, які отримують кортикостероїди у високих дозах, імунодепресанти, рекомендоване проведення вакцинації пневмококовою, менінгококовою вакцинами і щорічні щеплення проти грипу. У підлітковому віці не протипоказана вакцинація проти вірусу папіломи людини.
Прогноз для хворих на СЧВ нині залежить від об’єму ураження внутрішніх органів (особливо нирок, серця, нервової системи), активності захворювання, адекватної та планової терапії. Виживаність хворих на СЧВ після 10 років хвороби досягає 80%. До факторів, з якими пов’язаний несприятливий перебіг хвороби, належать неадекватне лікування, ураження нирок, артеріальна гіпертензія, АФС, інфекції, ускладнення унаслідок призначеної терапії.
Список літератури знаходиться в редакції.