22 грудня, 2018
I Национальный конгресс пульмонологов Украины: современные тенденции в ведении пациента с хроническим обструктивным заболеванием легких
18-19 октября в Киеве состоялся I Национальный конгресс пульмонологов Украины с участием ведущих специалистов в этой области медицины. В прозвучавших в ходе программы мероприятия докладах освещались наиболее актуальные темы, яркие выступления авторитетных ученых были ориентированы на мировые тенденции доказательной медицины. Среди тем, касающихся современных аспектов диагностики и лечения пульмонологических патологий, особый интерес вызвала секция, посвященная хроническому обструктивному заболеванию легких (ХОЗЛ).
.jpg) Открыла заседание секции член-корреспондент НАМН Украины, доктор медицинских наук, профессор Т.А. Перцева с докладом на тему «Подходы к лечению пациентов с бронхообструктивной патологией».
Открыла заседание секции член-корреспондент НАМН Украины, доктор медицинских наук, профессор Т.А. Перцева с докладом на тему «Подходы к лечению пациентов с бронхообструктивной патологией».
– Тема взаимосвязи между бронхиальной астмой (БА) и ХОЗЛ много лет вызывает интерес не только у ученых, но и у практикующих врачей. С одной стороны, БА и ХОЗЛ – это два различных заболевания с собственными патогенетическими механизмами, с другой – БА и гиперреактивность бронхов предрасполагают к появлению ХОЗЛ в более позднем возрасте, что подтверждается общностью генетической основы, а также последовательностью развития данных состояний.
Об этом говорят и результаты ряда эпидемиологических исследований. Исследование американских ученых (n=5261), длившееся в течение 20 лет, показало, что астма повышает риск развития эмфиземы в 17 раз (95% ДИ 8,3-34,8), ХОЗЛ – в 12,5 раза (95% ДИ 6,8-22,8) и хронического бронхита – в 10 раз (Gracicla E. Silca et al., 2004). Шведское ретроспективное исследование (n=5468) влияния комбинации ингаляционного кортикостероида (ИКС) и β-агониста длительного действия (БАДД) на частоту обострений ХОЗЛ выявило, что среди всей когорты больных ХОЗЛ 39% имели БА (Larsson K. et al., 2013).
Метаанализ 19 исследований позволил выделить следующие признаки БА у больных ХОЗЛ (Alshabanat A. et al., 2015; 10 [9]):
- ухудшение симптомов ночью или ранним утром;
- частичная обратимость обструкции;
- история аллергических состояний.
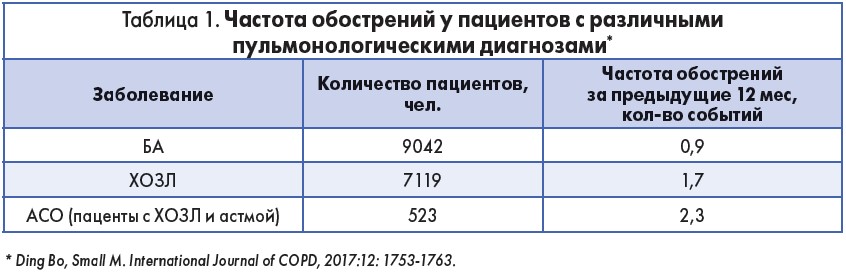
Также для сочетания ХОЗЛ и БА характерными являются более частые обострения. Для сравнения, частота обострений у пациентов с различной нозологией представлена в таблице 1.
Согласно результатам проспективного популяционного исследования Copenhagen City Heart Study, пациенты с ХОЗЛ и признаками астмы имеют наиболее неблагоприятный прогноз, что проявляется большим количеством госпитализаций и сокращением общей выживаемости на 12,8 года в сравнении со здоровыми некурящими пациентами. Кроме того, больные с подобной сочетанной патологией испытывают больше респираторных симптомов, что негативно влияет на качество жизни.
С учетом этой информации в GINA 2014 впервые были описаны особенности пациентов с сочетанием БА и ХОЗЛ (частые обострения, плохое качество жизни, более быстрое снижение функции легких, более высокая смертность, большее число обращений к медико-санитарной помощи), введен термин «ACOS» (Asthma-COPD overlap syndrome) и опубликован отдельный документ «Диагностика заболеваний с хроническим ограничением воздушного потока: астма, ХОЗЛ и ACOS». В GINA 2017 из термина «Asthma-COPD overlap syndrome» было удалено слово «syndrome», поскольку это не отдельное заболевание, а новое рекомендуемое понятие получило название «АСО».
Термин «Астма-ХОЗЛ» (АСО) необходим для осведомления о потребностях этой группы пациентов, поскольку большинство рекомендаций и клинических исследований посвящены только БА или только ХОЗЛ.
Доказательная база для лечения АСО крайне ограниченна из-за отсутствия исследований фармакотерапии в этой популяции, поэтому терапевтический подход остается неясным. Анализ результатов перекрестного опроса врачей и пациентов в рамках программы Adelphi Respiratory, проведенного в США, Франции, Германии, Италии, Испании и Великобритании и охватившего 9042 пациента с БА, 7119 пациентов с ХОЗЛ и 523 пациента с АСО, должен был дать оценку тенденций текущего лечения больных с сочетанием БА и ХОЗЛ в реальной когорте пациентов. Было выявлено, что:
- 18,2% пациентам с АСО не были назначены ИКС – нет базисной терапии БА;
- 41,7% пациентов с АСО курировали врачи первичного звена – не получали специализированной помощи;
- антагонисты лейкотриеновых рецепторов (АЛТР) чаще всего назначались пациентам с АСО в качестве базисной терапии.
Основные тенденции в лечении пациентов с БА, ХОЗЛ и АСО представлены на рисунке 1.
 Рис. 1. Препараты, чаще всего используемые в лечении распространенных заболеваний легких*
Рис. 1. Препараты, чаще всего используемые в лечении распространенных заболеваний легких*
Все вышеизложенное подтверждает необходимость формирования четких рекомендаций относительно базисной терапии у пациентов с АСО. Ретроспективный анализ корейской когорты пациентов с ХОЗЛ оценивал показатели функции внешнего дыхания после трехмесячной терапии ИКС/БАДД.
Результаты, приведенные на рисунке 2**, показали, что эта комбинация обеспечивает больший прирост объема форсированного выдоха за 1-ю секунду (ОФВ1) у пациентов с легким и умеренным ХОЗЛ в сочетании с БА по сравнению с больными только ХОЗЛ.
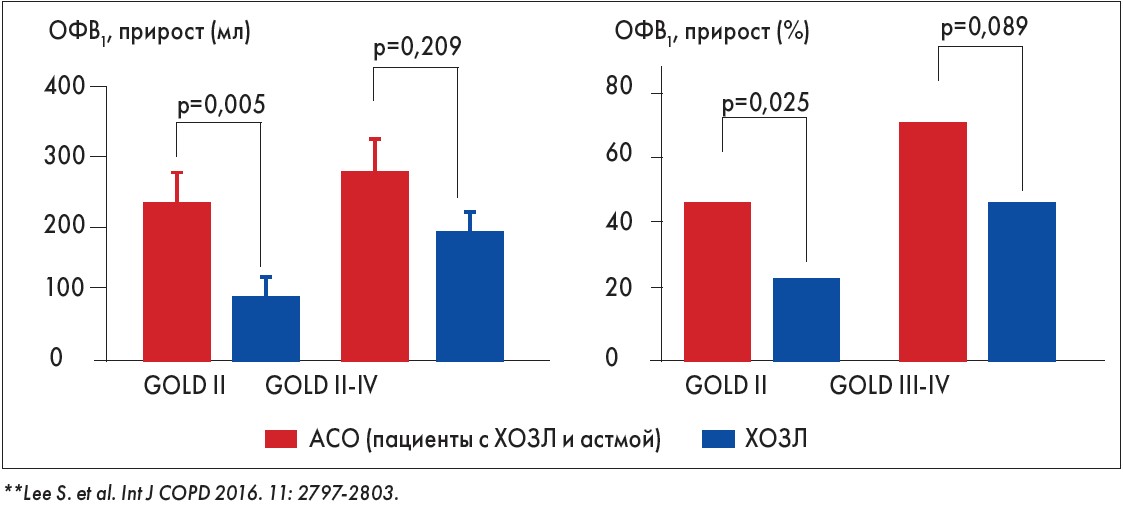 Рис. 2. Влияние ИКС/БАДД на ОФВ1 при ACO (пациенты с ХОЗЛ и астмой) против только ХОЗЛ после 3 мес лечения**
Рис. 2. Влияние ИКС/БАДД на ОФВ1 при ACO (пациенты с ХОЗЛ и астмой) против только ХОЗЛ после 3 мес лечения**
С позиции доказательной медицины пациенты с ХОЗЛ могут получить пользу от комбинации ИКС/БАДД (например, Симбикорт Турбухалер) в таких случаях:
- пациенты с частыми обострениями: ИКС/БАДД улучшают легочную функцию, статус здоровья и уменьшают количество обострений у пациентов с умеренным и тяжелым ХОЗЛ с частыми обострениями (GOLD 2018);
- пациенты с симптомами БА (с обострениями или без): с вариабельностью воздушного потока, положительным ответом на бронходилататор, повышенным количеством эозинофилов в мокроте или крови, с историей астмы (GINA/GOLD ACOS report);
- пациенты с признаками эозинофильного воспаления: эффект от лечения ИКС/БАДД в сравнении с БАДД при обострениях выше у пациентов с высоким уровнем эозинофилов в крови (GOLD 2018).
У больных БА Симбикорт Турбухалер снижает частоту тяжелых обострений, улучшает контроль астмы и обеспечивает быстрый регресс клинических симптомов, а у пациентов с ХОЗЛ предотвращает или снижает число обострений, приводящих к снижению функции легких и смертности, а также уменьшает симптоматику, особенно в утреннее время, что делает его назначение актуальным для этих категорий пациентов с бронхообструктивной патологией.
Обязательное лечение при сочетании БА и ХОЗЛ предполагает (GINA 2018):
- Отказ от курения, адекватная физическая активность, лечение сопутствующих заболеваний.
- Адекватную базисную терапию, включая ИКС (низкая или средняя доза в зависимости от симптомов), а не только монотерапию БАДД и МХДД.
- Симптоматическое лечение бронходилататорами или комбинацией ИКС/БАДД (МХДД), а не только ИКС в качестве монотерапии.
 Об изменениях в популяции больных ХОЗЛ рассказала в своем выступлении заведующая кафедрой профессиональных болезней и клинической иммунологии ГУ «Днепропетровская медицинская академия МЗ Украины» (г. Днепр), доктор медицинских наук, профессор Е.Ю. Гашинова.
Об изменениях в популяции больных ХОЗЛ рассказала в своем выступлении заведующая кафедрой профессиональных болезней и клинической иммунологии ГУ «Днепропетровская медицинская академия МЗ Украины» (г. Днепр), доктор медицинских наук, профессор Е.Ю. Гашинова.
– ХОЗЛ занимает одно из ведущих мест среди заболеваний, которые приводят к потере трудоспособности. По данным за 2016 год, оно является третьей по значимости причиной смерти в мире. У большинства клинических врачей сложилось устойчивое мнение, что типичный больной ХОЗЛ – это, как правило, мужчина старше 40 лет, заядлый курильщик, кашляющий и при этом считающий себя здоровым. Однако за последние годы тенденции существенно изменились. Чем же в настоящее время характеризируется популяция больных ХОЗЛ?
Сегодня болезнь поражает мужчин и женщин почти в равной степени. В странах с высоким уровнем дохода, например в США, вследствие возросшего уровня потребления табака среди женщин (а курение – главный установленный фактор риска развития ХОЗЛ) возрос также и процент женщин с таким диагнозом. У женщин при аналогичной табачной нагрузке ХОЗЛ развивается раньше и протекает тяжелее. В странах с низким уровнем дохода, учитывая дополнительный риск из-за воздействия загрязненного воздуха внутри помещений (в результате использования твердого топлива для приготовления пищи и обогрева), также наблюдается тенденция к нивелированию гендерных различий (GOLD 2018).
Еще одним заблуждением в отношении ХОЗЛ является возраст, в котором манифестирует заболевание. Как показали результаты когортного исследования, проведенного в Европе с участием 4636 пациентов в возрасте 20-44 года, частота ХОЗЛ варьировала от 1,85 до 2,88 случая на 1 тыс пациенто-лет (de Marco R. et al., 2011).
Важным моментом является также ассоциация курения с ХОЗЛ. Согласно данным популяционного исследования В. Lamprecht и соавт., из 4291 некурящего пациента с ХОЗЛ 6,6% имели ХОЗЛ I стадии (по классификации GOLD), а 5,6% – ХОЗЛ II-IV стадий (по классификации GOLD). Анализ факторов риска также показал, что никогда не курившие люди составляют 23,3% среди пациентов с ХОЗЛ II-IV стадий (по классификации GOLD).
Сегодня основными факторами риска развития ХОЗЛ являются:
- воздействие вредных веществ (особенно размером <5 мкм);
- табакокурение (в т. ч. пассивное);
- заменители сигарет;
- профессиональные вредности (органические и неорганические поллютанты: пыль, газы, дым, токсические аэрозоли) – 15-25% ХОЗЛ;
- грязный воздух в плохо вентилируемом помещении при отоплении и приготовлении пищи (группа риска – 3 млрд человек);
- загрязнение окружающей среды;
- БА;
- генетическая предрасположенность (дефицит α1-антитрипсина, полиморфизм гена матриксной металлопротеиназы‑12 – ММП12).
Актуальность проблемы профессиональных вредностей обусловлена тем, что экспозиция производственных аэрозолей в сочетании с курением сигарет способна в 6-8 раз увеличить риск развития ХОЗЛ. По результатам исследования Васильевой и соавт. профессиональные факторы увеличивают риск ежегодного снижения ОФВ1 приблизительно на 7-8 мл дополнительно к возрастному фактору и курению (рис. 3).
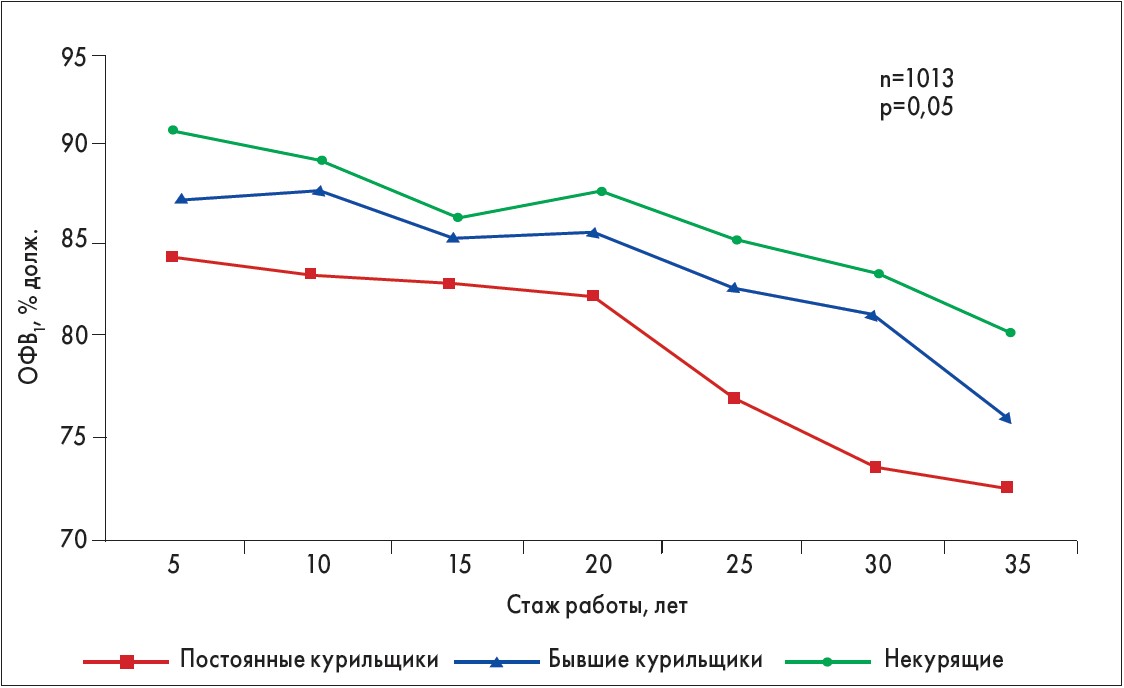 Рис. 3. Факторы, влияющие на снижение ОФВ1
Рис. 3. Факторы, влияющие на снижение ОФВ1
Профессиональные факторы риска развития ХОЗЛ перечислены в таблице 2.
Эти же факторы влияют на риск развития БА, что указывает на высокую вероятность развития АСО у этой категории пациентов.
Во всем мире подход к лечению ХОЗЛ осуществляется в соответствии с рекомендациями GOLD (рис. 4).
В них четко прослеживается указание об использовании ИКС у пациентов с ХОЗЛ, что часто является камнем преткновения в реальной клинической практике из-за боязни развития инфекционных осложнений.
Последние публикации в зарубежной научной литературе позволили разобраться с этим сложным вопросом, предоставив следующие выводы (Alvar A. et al., 2018):
- ИКС не следует использовать в качестве монотерапии при ХОЗЛ, нужно использовать комбинацию с БАДД.
- Преимущества от добавления ИКС к БАДД получают пациенты с историей частых или тяжелых обострений, при эозинофилии крови >300 кл/ мкл и с анамнезом и/или сопутствующей астмой.
- Риск пневмонии у пациентов с ХОЗЛ при использовании ИКС выше у пациентов старшего возраста, с низким индексом массы тела, при приеме высоких доз ИКС и эозинофилии крови <100 кл/мкл, что важно учитывать, решая вопрос о назначении и подборе дозы ИКС.
Исходя из вышесказанного, предпочтение нужно отдавать комбинированным препаратам ИКС с БАДД, так как они позволяют достичь максимального комплаенса. Когда речь заходит о выборе препарата, необходимо учитывать его способность обеспечить максимально быстрое уменьшение тяжести симптомов, особенно в утреннее время, что лучше всего достигается при использовании формотерола, начало действия которого приравнивается к сальбутамолу. Препаратом с солидной доказательной базой, в состав которого входит БАДД формотерол и ИКС будесонид, является Симбикорт Турбухалер, обладающий рядом преимуществ у пациентов с ХОЗЛ, нуждающихся в ИКС.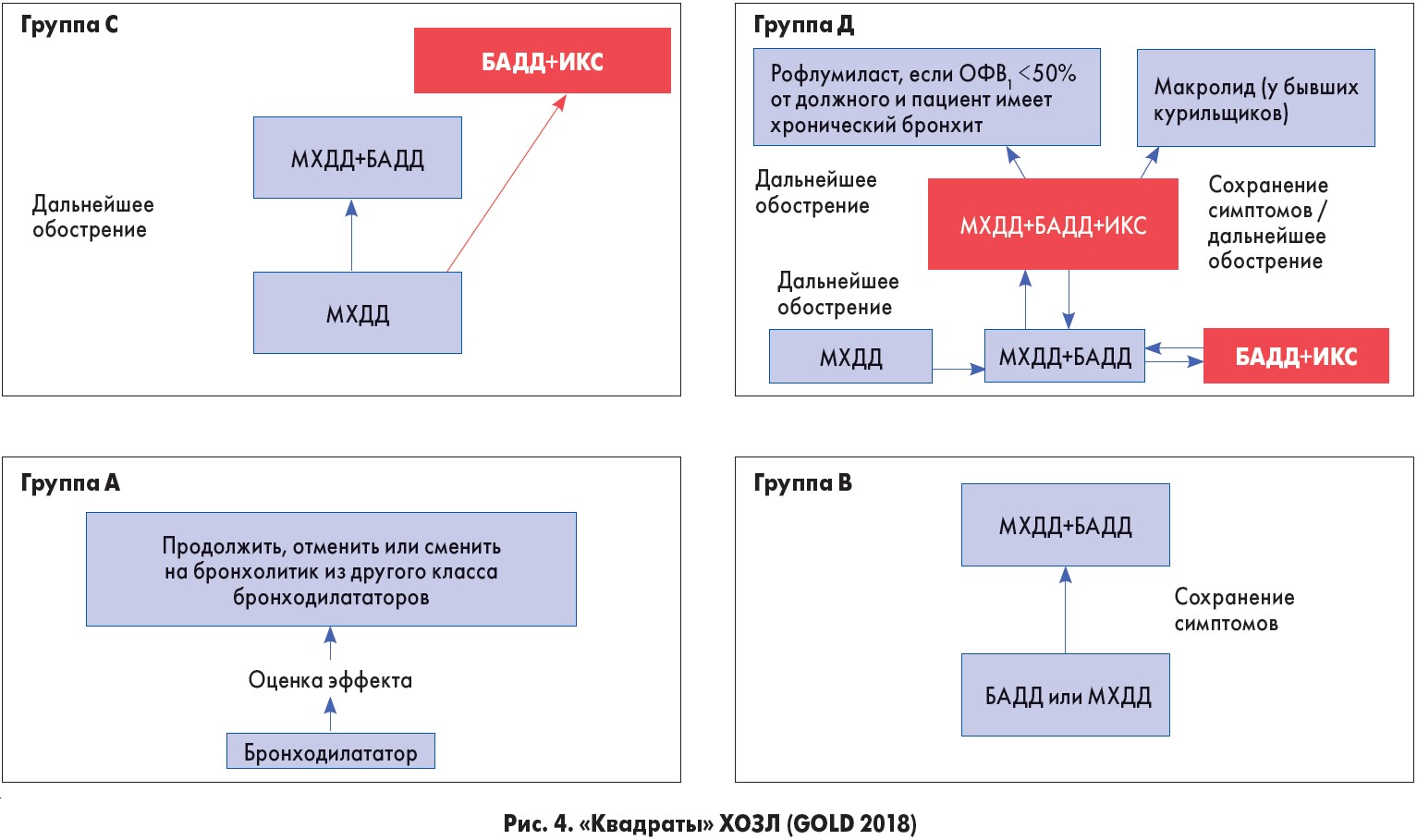
 В заключение работы секции был заслушан доклад ведущего научного сотрудника ГУ «Национальный институт фтизиатрии и пульмонологии им. Ф.Г. Яновского НАМН Украины» (г. Киев), доктора медицинских наук Я.А. Дзюблика, сделавшего акцент на использовании результатов клинических исследований в реальной клинической практике.
В заключение работы секции был заслушан доклад ведущего научного сотрудника ГУ «Национальный институт фтизиатрии и пульмонологии им. Ф.Г. Яновского НАМН Украины» (г. Киев), доктора медицинских наук Я.А. Дзюблика, сделавшего акцент на использовании результатов клинических исследований в реальной клинической практике.
– Известно, что рандомизированные клинические исследования (РКИ), в том числе слепые, являются золотым стандартом надлежащей клинической практики и считаются наивысшим уровнем медицинских доказательств. Большинство рекомендаций по поводу лечения ХОЗЛ основываются на данных, полученных в ходе РКИ и их систематических обзоров. Это объясняется тем, что рандомизация позволяет избежать двусмысленностей и гарантирует, что группы лечения и сравнения будут сопоставимыми по всем характеристикам, кроме схем терапии. Ослепление субъектов исследования и персонала позволяет избежать влияния на оценку результатов лечения знание о нем участников, исследователей или персонала.
Для минимизации влияния факторов, способных повлиять на результаты, к участию в РКИ привлекают тщательно подобранных пациентов с минимальными сопутствующими заболеваниями и мониторингом для обеспечения соблюдения режима лечения. Из РКИ часто исключают пожилых (≥65 лет) больных, пациентов с сопутствующими заболеваниями или принимающих другие препараты. Таким образом, иногда невозможно экстраполировать данные, полученные в РКИ, на рутинную клиническую практику в широкой популяции, где нет тщательного отбора, большее количество сопутствующих заболеваний и меньшая приверженность к лечению. В таких ситуациях необходимо помнить о возможности использования результатов, полученных в исследованиях реальной клинической практики (ИРКП). Согласно GOLD обострения являются ключевыми событиями при ХОЗЛ.
В ИРКП, проведенном в Италии и включившем 4680 пациентов с ХОЗЛ, подобранных по сопоставимым характеристикам, сравнивалась эффективность комбинаций будесонид/формотерол и флутиказон/сальметерол. Было выявлено, что у пациентов, получавших комбинацию будесонид/формотерол, было на 16% меньше госпитализаций по поводу обострения ХОЗЛ. Кроме того, наблюдалась тенденция к уменьшению потребности в системных глюкокортикоидах и антибиотиках (Perrone V. et al., 2016).
В еще одном ИРКП, осуществленном в Швеции в течение 11 лет с участием более чем 5 тыс пациентов, использование фиксированной комбинации будесонид/формотерол на 29% снижало частоту обострений, требующих госпитализации, по сравнению с больными, которым была назначена комбинация флутиказона с сальметеролом (Larsson K. et al., 2013).
Эти данные подтверждаются в том числе результатами канадского популяционного исследования (n=2262), проведенного в течение 1 года, в котором комбинация будесонид/формотерол против флютиказона/сальметерола на 39% снижала частоту обострений ХОЗЛ, требующих госпитализации (Blais L. et al., 2010).
Таким образом, и в РКИ, и в условиях реальной клинической практики комбинация будесонид/формотерол (Симбикорт Турбухалер) демонстрирует у пациентов с ХОЗЛ стабильно большее влияние на:
- утренние симптомы и активность;
- снижение частоты всех обострений в сравнении с комбинацией флутиказон/сальметерол;
- снижение потребности в назначении оральных кортикостероидов и антибиотиков;
- уменьшение частоты обращения за медицинской помощью.
Прозвучавшие в ходе работы секции доклады познакомили присутствующих с новыми тенденциями относительно ХОЗЛ, а также дали возможность практикующим врачам разобраться в проблемных вопросах, касающихся ведения наиболее сложных категорий пациентов – больных с АСО.
Подготовила Анна Кирпач
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 4 (45), листопад-грудень 2018 р.