17 березня, 2019
Противовирусная терапия при ОРВИ в сдерживании роста антибиотикорезистентности
 Зимне-весенний период – пиковое время для острой респираторной инфекции (ОРИ), когда распространенность заболеваний данной группы является наиболее высокой. Выбор стратегии лечения напрямую зависит от типа возбудителя. Поэтому перед врачом возникает дилемма: назначать противомикробные препараты или воздержаться от антибиотикотерапии. Как показывает практика, количество антибиотикорезистентных штаммов микроорганизмов непрерывно увеличивается, что свидетельствует о нерациональном использовании антибактериальных препаратов. Наиболее остро проблема роста антибиотикорезистентности стоит в педиатрии, что обусловливает необходимость применения радикальных мер и ограничения назначения антибиотиков пациентам с ОРИ при отсутствии конкретных показаний.
Зимне-весенний период – пиковое время для острой респираторной инфекции (ОРИ), когда распространенность заболеваний данной группы является наиболее высокой. Выбор стратегии лечения напрямую зависит от типа возбудителя. Поэтому перед врачом возникает дилемма: назначать противомикробные препараты или воздержаться от антибиотикотерапии. Как показывает практика, количество антибиотикорезистентных штаммов микроорганизмов непрерывно увеличивается, что свидетельствует о нерациональном использовании антибактериальных препаратов. Наиболее остро проблема роста антибиотикорезистентности стоит в педиатрии, что обусловливает необходимость применения радикальных мер и ограничения назначения антибиотиков пациентам с ОРИ при отсутствии конкретных показаний.
В структуре этиологических факторов ОРИ лидирующую позицию занимают вирусные возбудители, которые, по разным данным, вызывают от 80 до 95% случаев заболеваний данной группы. На сегодня насчитывается более 200 вирусных возбудителей ОРИ. Их классифицируют на типичные возбудители (вирус гриппа А, В и С), респираторно-синцитиальный вирус (РСВ А и В), вирус парагриппа (типа 1, 2, 3, 4А, 4В), аденовирусы (>51 серотипа), риновирусы (>100 типов), коронавирус (229Е, ОС43), вирус Коксаки, ЕСНО, герпес-вирусы (HSV 1, 2, 4, 5 и 6 типа A, B), новые и активируемые типичные возбудители (коронавирус ТОРС, NL63, HKU1, MERS-CoV), риновирус (тип С), аденовирус (тип 14), а также новые возбудители (метапневмовирус, бокавирус, мимивирус, полиомавирусы KI, WU и Merkel Cell, вирусы Мелака, гриппа A(H1N1)pdm09, Эбола (2014 г.), Зика (2015 г.); Е.И. Бурцева, 2015). Среди перечисленных вирусных возбудителей особый интерес представляют вирусы гриппа, которые характеризуются высокой степенью изменчивости, что приводит к появлению новых штаммов. Если в предыдущем сезоне 2017-2018 гг. доминировали вирусы гриппа A/Michigan/45/2015 (H1N1)pdm09, A/Hong Kong/4801/2014 (H3N2), B/Brisbane/60/2008, то в нынешнем (2018-2019 гг.) наблюдается другая эпидемиологическая картина: штамм вируса гриппа A/Michigan/45/2015 (H1N1)pdm09 по-прежнему доминирует, вторыми по частоте являются штаммы A/Singapore/ INFIMH/2016(HЗN2), B/Colorado/06/2017.
Несмотря на тот факт, что в этиологической структуре ОРИ как среди взрослых, так и детей преобладают вирусы, проблема нерационального использования антибиотиков не теряет своей актуальности. Так, по данным анализа, проведенного в 2000-2011 гг., 27,4% ОРИ были бактериального происхождения. При этом антибиотики получали 57% пациентов, что в 2,1 раза больше, чем необходимо. В половине случаев ОРИ препараты данной группы назначают при отсутствии показаний или неверно, что способствует росту антибиотикорезистентности. Что касается детей и подростков, то количество случаев необоснованного применения антибактериальных средств достигает 11,5 млн.
При инфекционном поражении дыхательных путей полностью исключить необходимость применения антибиотиков нельзя. Как известно, при отсутствии адекватного лечения острой респираторной вирусной инфекции (ОРВИ) вследствие снижения иммунной защиты есть вероятность присоединения бактериальной флоры. При наличии данных, подтверждающих такой вариант развития событий, рассматривается возможность применения антибиотиков у конкретного пациента.
В последнее время много внимания уделяется методам профилактики гриппа. Согласно рекомендациям Центра по контролю и профилактике заболеваний (CDC, 2018), ингибиторы нейраминидазы (осельтамивир, занамивир, перамивир) показаны к применению как для лечения инфекции, вызванной вирусом гриппа А и В, так и в качестве профилактики (более длительным курсом). Однако эта терапия имеет возрастные ограничения, а также высокую частоту побочных эффектов: при лечении осельтамивиром – тошнота, рвота, головная боль; занамивиром – аллергические реакции, риск развития бронхоспазма (особенно при наличии сопутствующей патологии органов дыхания), синуситы, головокружение, инфекции лор‑органов; перамивиром – диарея. Относительно всех трех препаратов имеются постмаркетинговые данные о серьезных кожных реакциях и спорадических транзиторных нейропсихических событиях. Исходя из вышеизложенного, применение ингибиторов нейраминидазы ввиду широкого спектра побочных эффектов, прежде всего в педиатрической практике, требует особой осторожности.
Выделяют такие факторы риска развития бактериальных осложнений: возраст <2 лет, длительное пребывание в стационаре для детей первых 2 лет жизни (в реанимационных отделениях для детей старшего возраста), частые детские инфекции, наличие очагов хронической инфекции, отягощенная наследственность, нарушение питания (искусственное вскармливание), ожирение, аллергия (экссудативный диатез), недостаточность иммунитета, патология бронхолегочной системы, нейропсихические расстройства, частое посещение детских коллективов, аномалии развития.
О присоединении вторичной бактериальной инфекции на фоне ОРВИ свидетельствует продолжительность симптомов заболевания, в частности лихорадки, более 4-5 дней. Если у ребенка наблюдается выраженная боль в горле, следует заподозрить стрептококковую ангину, увеличение лимфатических узлов – лимфаденит, боль в ухе – отит, заложенность носа длительностью более 2 недель – риносинусит. К бактериальным осложнениям ОРВИ также относятся пневмония (при появлении одышки, выраженном токсикозе, изменении перкуторного звука над легкими, наличии хрипов при аускультации), инфекция мочевыводящих путей, пиелонефрит (диспептические и дизурические расстройства, отеки), миокардит (появление одышки при физической нагрузке, боль в области сердца, слабость, сердцебиение, артралгии), гастродуоденит, панкреатит, холецистохолангит (абдоминальная боль, диспептические явления, изменение дефекации). При наличии у пациента симптомов, которые указывают на участие в патологическом процессе бактериального возбудителя, следует рассматривать как эффективный вариант лечения антибиотикотерапию.
Подбор адекватной терапии при ОРВИ осуществляется с учетом патогенетического механизма заболевания. Вирус как этиологический фактор является индуктором воспаления в первые часы заболевания, поэтому противовирусные препараты более эффективны на протяжении первых 24‑48 ч. При отсутствии адекватного лечения после 4-го дня заболевания риск присоединения вторичной бактериальной инфекции существенно увеличивается. Если это происходит, врач имеет дело уже с осложнениями ОРВИ или гриппа (отитом, риносинуситом, бронхитом, пневмонией, миозитом, острым нарушением функции почек, острым поперечным миелитом, миокардитом, перикардитом, менингитом, энцефалитом, остеомиелитом, обострением хронической патологии), которые трудно поддаются лечению.
С целью предотвращения роста антибиотикорезистентности сегодня активно внедряется стратегия SMART, предусматривающая рациональное, адекватное, своевременное использование антибиотиков, которые рекомендованы в соответствии с международными стандартами и разработаны с учетом резистентности микроорганизмов к антибиотикам. При ОРИ выделяют следующие основные показания к немедленному назначению антибактериальных средств:
- тяжелое состояние пациента;
- наличие угрожающих симптомов заболевания/осложнений (пневмония, мастоидит, перитонзиллярный абсцесс/флегмона, внутричерепные осложнения);
- группа высокого риска развития тяжелых осложнений (при сопутствующей патологии сердца, почек, печени, иммуносупрессии, муковисцидозе, недоношенности);
- двусторонний средний отит у детей до 2 лет, оторея у детей;
- острый тонзиллит (острая боль в горле) при наличии ≥3 критериев Сентора (отечность и наличие экссудата на миндалинах, увеличенные и болезненные передние шейные лимфатические узлы, лихорадка >38 °C в анамнезе, отсутствие кашля).
Несмотря на наличие четких показаний для проведения антибиотикотерапии пациентам с ОРИ, сегодня наблюдается тенденция к злоупотреблению этими препаратами. Нерациональное использование антибиотиков представляет наибольшую опасность для детей, поскольку может привести к ухудшению состояния ребенка, развитию различных патологических процессов, а также способствует дальнейшему распространению антибиотикорезистентности. Согласно результатам экспертизы наиболее частых причин смерти детей с ОРИ (n=398) было установлено, что в 68 случаях летальный исход был следствием нерациональной антибиотикотерапии (З.Х. Сорокина, 2011).
С одной стороны, антибиотики – это лекарственные средства, с помощью которых были спасены миллионы жизней во всем мире, с другой – бактерии, вызывающие ОРИ, на протяжении нескольких десятилетий развивали резистентность к каждому новому антибиотику. Как результат, по данным CDC США, в последние годы от инфекций, вызванных резистентными к антибиотикам возбудителями, ежедневно умирает не менее 23 тыс. человек. Эксперты прогнозируют, что в недалеком будущем смертность, связанная с антибиотикорезистентностью, может превысить показатель при онкологической патологии.
В 2015 г. была создана Глобальная система эпиднадзора за антибактериальной резистентностью (Global Antimicrobial Resistance Surveillance System, GLASS). Ее целью которой является постоянное обновление базы данных о резистентности микроорганизмов к антибиотикам, которая в дальнейшем может быть использована для реализации региональных и глобальных мероприятий. Украина не входит в систему GLASS. При этом благодаря последним исследованиям отечественных детских инфекционистов, микробиологов (Л.И. Чернышова, А.М. Гильфанова, А.В. Бондаренко, В.В. Яновская, Т.Г. Глушкевич, С.А. Якимович) установлены показатели резистентности микроорганизмов к антибиотикам, которые применяют наиболее часто: высокая чувствительность сохранилась к пенициллинам, цефалоспоринам (цефуроксиму, цефотаксиму), ванкомицину, меропенему.
Таким образом, нынешняя ситуация с глобализацией антибиотикорезистентности во всем мире обусловливает необходимость реализации простой, но очень действенной стратегии Antibiotic SMART Use, основной принцип которой заключается в том, что антибиотики не следует применять для лечения небактериальных инфекций, прежде всего это касается ОРИ.
Среди ОРВИ одной из наиболее распространенных нозологий является острый риносинусит, который входит в десятку основных амбулаторных диагнозов. Данная патология чаще диагностируется у детей и занимает 5-е место среди заболеваний, по поводу которых назначается антибиотикотерапия, несмотря на то что риносинусит в 90% случаев имеет вирусную этиологию (В.И. Попович, 2016). Для острого риносинусита характерны большие (гнойные выделения из передних носовых ходов, гнойные или бесцветные выделения из задних носовых ходов, заложенность или обструкция носа, отечность лица, боль при надавливании, гипо- или аносмия, лихорадка при остром синусите) и малые (головная боль, спонтанная или спровоцированная боль в ухе, галитоз, зубная боль, кашель, лихорадка при подостром или хроническом синусите, слабость) клинические признаки (Brook, 2013).
Согласно Европейским рекомендациям по лечению острых риносинуситов и назальных полипов (EPOS) в первые 5 дней заболевания имеет место вирусная инфекция. В случае усиления симптомов через 5-10 дней от начала заболевания следует заподозрить участие бактериального возбудителя в патологическом процессе и рассмотреть возможность назначения антибиотиков (W. Fokkens et al., 2012).
Острый средний отит (ОСО) является наиболее частой лор-патологией и обусловливает 50% всех лор-назначений антибиотиков. Для заболевания характерны такие симптомы: заложенность ушей (снижение слуха), выделения из ушей, отказ от пищи, апатия, беспокойство, приступы крика, гипертермия, нарушение сна, диарея/рвота. Следует отметить, что в этиологической структуре ОСО на долю вирусных возбудителей приходится 43,5% (A. Arrieta et al., 2003). Поэтому назначение антибактериальных средств таким пациентам требует дифференцированного подхода.
В этиологии острого тонзиллофарингита (ОТФ) значительно преобладают вирусные возбудители (аденовирус, вирус парагриппа, респираторно-синцитиальный вирус, риновирусы, энтеровирусы и др.). Характерными симптомами вирусного ОТФ являются конъюнктивит, острый ринит, кашель, диарея, осиплость, единичные афты в ротовой полости, вирусная экзантема (С.В. Рязанцев, 2014). Согласно действующему украинскому протоколу при ОТФ антибиотики следует назначать при наличии ≥3 критериев Сентора. Кроме признаков, которые входят в перечень этих критериев, о бактериальной этиологии ОТФ также свидетельствуют отсутствие расширенной сосудистой сетки, бугристости поверхности слизистой оболочки, ринита, конъюнктивита, а также продолжительность симптомов заболевания более 3 дней.
Обоснование назначения антибиотиков имеет важное значение также при остром бронхите (ОБ), при котором вероятность вирусной этиологии заболевания составляет более 90%. Перечень показаний к проведению антибиотикотерапии при ОБ у детей ограничен и представлен несколькими позициями: подозрение на ОБ микоплазменной или хламидийной этиологии у детей старше 5 лет, гипертермия (>39 °C) продолжительностью более 3-5 дней от начала заболевания или повторная гипертермия после периода нормальной температуры, наличие отягощенного преморбидного фона, а также активных очагов хронической инфекции.
Единственным абсолютным показанием к назначению антибиотиков является внебольничная пневмония. Следует также учитывать возможную роль вирусных возбудителей (у детей – респираторно-синцитиального вируса, риновируса, метапневмовируса, вируса парагриппа, бокавируса) в развитии заболевания. Это обосновывает целесообразность сопроводительной противовирусной терапии у детей с пневмонией.
Основная угроза здоровью пациента, которую представляют респираторные вирусы, состоит в том, что они подавляют функциональную активность различных звеньев иммунной системы и приводят к обострению хронических заболеваний, развитию вторичных бактериальных осложнений, а также способны индуцировать аллергические реакции (Л.А. Степанищева, 2012, И.В. Николаева, 2014).
! Проведение противовирусной терапии педиатрическим пациентам с ОРВИ позволяет предупредить развитие бактериальных осложнений. Современный противовирусный препарат должен иметь активность относительно широкого спектра вирусных возбудителей, способность подавлять сенсибилизацию слизистых оболочек вирусом, обладать иммуномодулирующим действием. Важными критериями выбора лекарственного средства для этой терапии также являются отсутствие резистентности (возможность многократного применения препарата), низкая токсичность и высокая эффективность.
Лечение с использованием оптимального препарата позволяет предупредить развитие осложнений и обострение хронической инфекции.
Всем перечисленным требованиям соответствует комбинированный противовирусный препарат Эргоферон. Благодаря комбинации усиленного противовирусного, противовоспалительного и антигистаминного эффектов Эргоферон может применяться в качестве этиотропной, патогенетической, симптоматической терапии при отсутствии риска развития резистентности, что было доказано в экспериментальных и клинических исследованиях (О.М. Охотнікова, 2017).
! Эргоферон обладает широким спектром противовирусной активности относительно основных возбудителей ОРВИ (риновирусов, вирусов гриппа, парагриппа, аденовирусов, герпес-вирусов, коронавирусов, ротавирусов, энтеровирусов, респираторно-синцитиального вируса), имеет выраженный противовоспалительный и антигистаминный эффекты, которые подтверждены результатами клинических исследований.
Включение противовирусного средства в комплексную терапию внебольничной пневмонии позволяет уменьшить продолжительность основных симптомов заболевания, сократить длительность антибактериальной терапии и сроки пребывания пациента в стационаре (А.Л. Заплатников и соавт., 2015).
В прошлом году завершилась реализация масштабной наблюдательной программы «ЭРМИТАЖ», целью которой было изучить эффективность и безопасность применения препарата Эргоферон у пациентов с ОРВИ в условиях клинической практики. Это подразумевало, что пациенты были включены в исследование независимо от дня заболевания, когда они обратились за медицинской помощью, и от наличия сопутствующих заболеваний (706 (8%) пациентов имели отягощенный аллергологический анамнез в виде аллергического ринита/риносинусита, атопического дерматита/экземы, бронхиальной астмы).
В исследовании «ЭРМИТАЖ» приняли участие врачи из 8 стран, 2069 пациентов в возрасте 18-90 лет и 6005 детей от 6 мес до 18 лет. В ходе исследования было установлено, что назначение препарата Эргоферон в 1-й день заболевания сокращает длительность симптомов до 4,7 дня, а на 4-й – до 5,09 дня. Разница в длительности всех симптомов заболевания у пациентов, которые начали лечение в 1-й и 4-й день, составила всего 0,39 суток (9,4 ч). Эргоферон нормализует температуру тела уже после 1-го дня лечения у 29% пациентов, после второго – у 78% (рис. 1).
! В исследовании «ЭРМИТАЖ» уже через два дня терапии средством Эргоферон у 65,7% пациентов наблюдалось исчезновение симптомов интоксикации, у 42,3% – боли/першения в горле, у 41% – заложенности/отделяемого из носа (рис. 2). 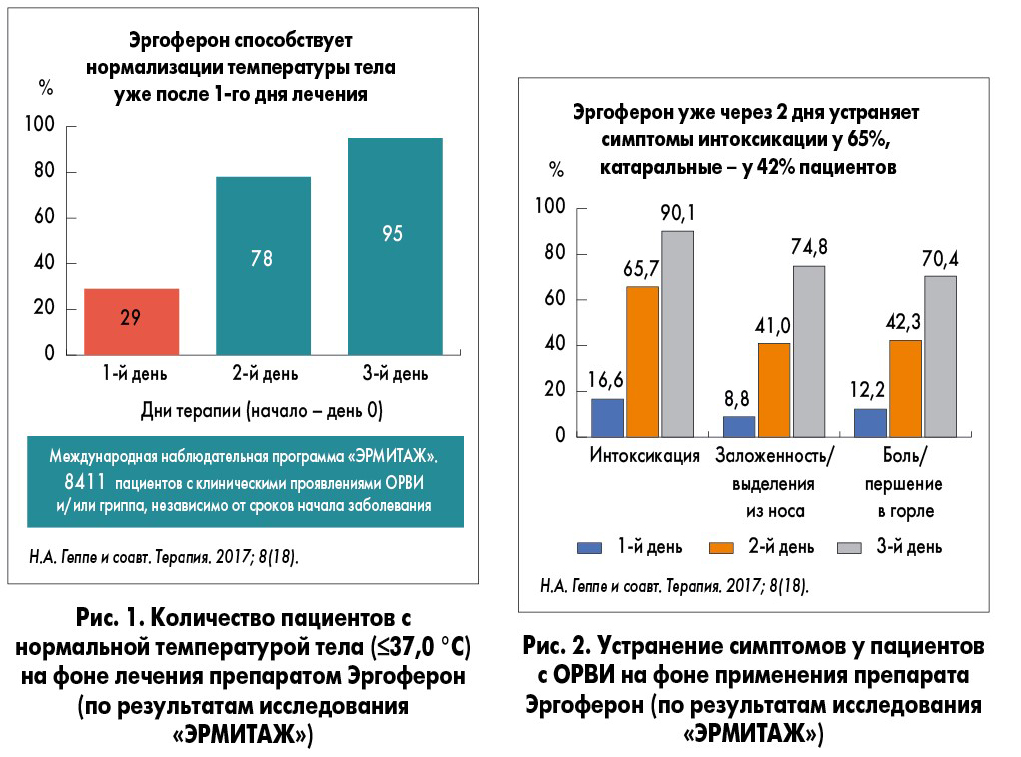
Следует отметить, что эффективность лечения препаратом Эргоферон была сопоставимой у пациентов с ОРВИ без сопутствующей патологии и с аллергическим заболеванием. Это стало подтверждением дополнительного противоаллергического эффекта лекарственного средства. Использование препарата Эргоферон в виде монотерапии позволяет исключить необходимость симптоматической терапии у 49% пациентов (Н.А. Геппе и соавт., 2017; рис. 3).
Одним из важнейших результатов исследования стало подтверждение того, что противовирусная терапия препаратом Эргоферон существенно снижает потребность в назначении антибиотиков: только 3,3% пациентов получали антибиотик на 2-й и в последующие дни курса лечения (Н.А. Геппе и соавт., 2017; рис. 4).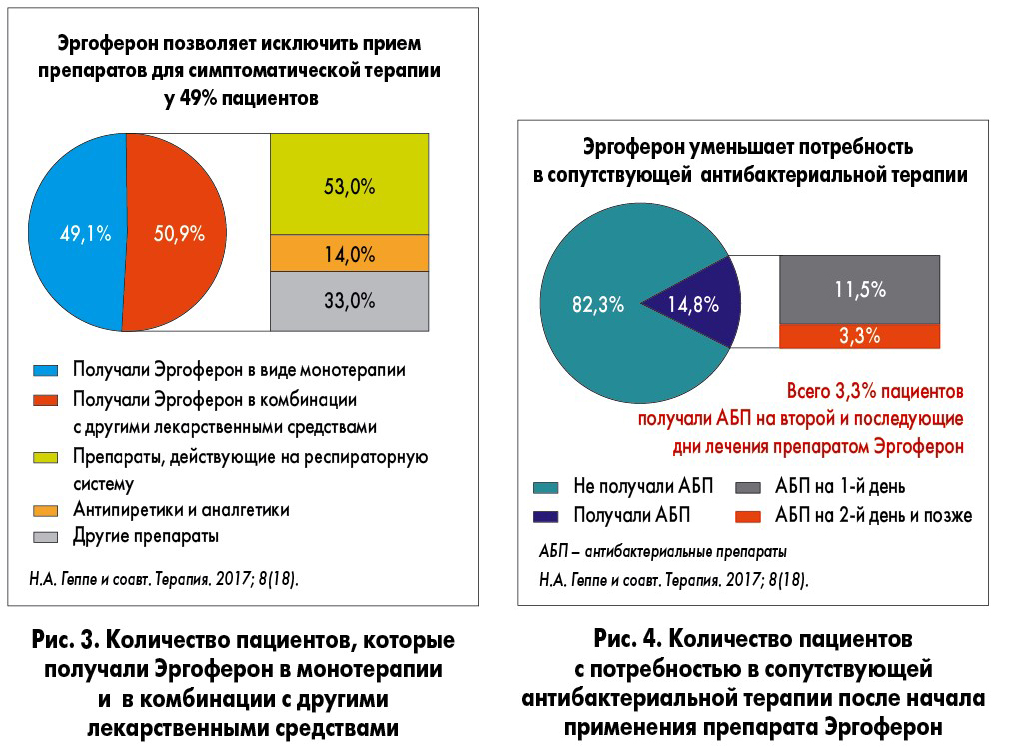
Доказано, что использование препарата Эргоферон у детей с исходно низким уровнем продукции интерферонов (IFN) позволяет восстановить уровень IFN‑γ и, тем самым, предупредить развитие вторичной бактериальной инфекции. В группе пациентов с исходно высоким уровнем IFN‑γ применение противовирусного средства не приводило к усилению индуцированной продукции IFN. Таким образом, Эргоферон оказывает иммуномодулирующее действие (С.А. Крамарев, 2014).
Есть данные, свидетельствующие о хороших результатах комплексного лечения пациентов с сопутствующими хроническими болезнями при включении препарата Эргоферон в схему терапии. Ввиду того, что лекарственное средство характеризуется благоприятным профилем переносимости, отсутствием гепатотоксичности, саморегулирующим имунномодулирущим действием, его применение может быть востребовано для лечения ОРВИ у пациентов онкологического профиля (А.В. Мордык и соавт., 2017; Е.В. Яковлева, 2016).
Противовирусная терапия – это мощный инструмент, правильное использование которого позволит приостановить распространение антибиотикорезистентности. Минимизация назначения антибиотикотерапии способствует сохранению нормальной микрофлоры, что обеспечивает стойкость иммунной защиты организма, а это является залогом долголетия человека. Украинские врачи имеют уникальную возможность применять препарат Эргоферон для высокоэффективной и безопасной противовирусной терапии. Преимущества и возможности использования препарата в лечении целого ряда заболеваний подтверждают результаты множества исследований, а также многолетняя клиническая практика.
Клинический случай 1
Пациенту А., подверженному частым простудным заболеваниям, была проведена иммунограмма, на которой обнаружено снижение уровня CD4-лимфоцитов.
Вопрос: Можно ли считать такие результаты иммунограммы показанием к назначению препарата Эргоферон?
Ответ: Да. CD4-лимфоциты – это ключевое звено иммунной защиты организма. У детей с исходно низким уровнем CD4‑лимфоцитов применение препарата Эргоферон позволяет нормализировать этот показатель. Таким пациентам противовирусное средство можно назначать более длительным курсом (1-3 мес). В случае нормального уровня CD4-лимфоцитов на фоне терапии препаратом Эргоферон он будет удерживаться.
Клинический случай 2
Пациент К., 16 лет. Год назад подростку была выполнена операция по пересадке костного мозга в связи с онкогематологическим заболеванием. Сейчас пациент каждые 2 недели принимает азитромицин в дозе 500 мг курсом по 3 дня.
Вопрос: Можно ли назначать пациенту противовирусную терапию при ОРВИ?
Ответ: Да. Назначение препарата Эргоферон вместе с антибиотиком позволит поддерживать оптимальный уровень интерферонов, и в последующем больше не будет потребности в рутинном назначении антибактериального средства.
Тематичний номер «Педіатрія» №1 (48), березень 2019 р.


