17 березня, 2019
Неінвазивне проспективне багатоцентрове дослідження з оцінки ефективності застосування рослинного лікарського засобу Канефрон® Н у амбулаторних педіатричних пацієнтів
Хвороби сечовидільної системи у педіатричній практиці включають широкий спектр патологічних порушень. Найбільш поширеним захворюванням сечовидільної системи у дітей та підлітків є інфекція сечовивідних шляхів (ІСВШ). Клінічні прояви ІСВШ варіативні – від загальних ознак (лихоманка, блювання, відмова від їжі, дратівливість тощо) до специфічних проявів з боку сечовивідних шляхів (часте сечовипускання, біль та печіння при сечовипусканні, нетримання сечі). ІСВШ, насамперед пієлонефрит, можуть призвести до ураження нирок, яке асоційоване з такими серйозними ускладненнями, як гіпертонія, порушення функції нирок і хронічні захворювання нирок кінцевої стадії. Своєчасна діагностика та ефективне лікування ІСВШ дозволяють запобігти розвитку тяжких розладів та серйозних ускладнень у пацієнтів із рецидивуючим перебігом захворювання.
Обґрунтування
У педіатричній практиці в Росії традиційне лікування ІСВШ передбачає використання протимікробних препаратів, а також цілої низки рослинних лікарських засобів (РЛЗ). Один із рослинних препаратів – Канефрон® Н (виробник – Bionorica SE, Німеччина), який містить у своєму складі траву золототисячнику (Centaurii herba), корінь любистку (Levistici radix) і листя розмарину (Rosmarini folia) (далі – РЛЗ). Протягом багатьох років РЛЗ широко застосовують для лікування та профілактики ІСВШ, а також інших захворювань сечовидільної системи. Він продемонстрував високу ефективність як у дорослих, так і у дітей.
Трава золототисячнику містить ксантони, які мають антибактеріальний та антихолінергічний ефекти. Її традиційно використовують для виведення каменів із нирок та нормалізації діурезу. Доведено, що фуранокумарини, які містить корінь любистку, чинять спазмолітичну та сечогінну дію, тому його використовують для діуретичної терапії при запаленні нижніх сечовивідних шляхів. Дитерпени, поліфеноли та феноли, які входять до складу листя розмарину, чинять антиоксидантну, антибактеріальну, антивірусну, протизапальну, спазмолітичну та протисудомну дію. Листя розмарину підтримує ниркову екскрецію та діурез. Показано, що діуретична активність РЛЗ підвищується за рахунок усіх його компонентів. Механізми протизапальної, знеболювальної та антиоксидантної дії активних фармацевтичних інгредієнтів (АФІ) препарату включають зменшення вивільнення простагландину Е2 (PGE2) та інгібування ферментів, які продукують PGE2. РЛЗ знижує концентрацію фізіологічно релевантних реакційноздатних кисневих та азотних видів, гідроксильних радикалів, пероксильних радикалів і пероксинітритів.
Спазмолітичні та антиноцицептивні властивості РЛЗ були вивчені на тваринній моделі циститу, спровокованого циклофосфамідом. Показано, що АФІ засобу знижують частоту скорочень сечового міхура, нормалізують його ємність та зменшити гіпералгезію, спровоковану циклофосфамідом. AФI засобу інгібували адгезію Escherichia coli до клітин слизової оболонки сечового міхура залежно від концентрації, що підтверджує його позитивний ефект при бактеріальних ІСВШ.
Отже, основні фармакодинамічні властивості препарату включають протизапальну/антиоксидантну, спазмолітичну, антиноцицептивну, антиадгезійну та діуретичну активність.
РЛЗ має сприятливий профіль безпеки та хорошу переносимість порівняно з іншими препаратами для лікування захворювань сечовивідних шляхів, наприклад, з антибіотиками, нітрофуранами [3]. Препарат доступний у вигляді таблеток, вкритих оболонкою (драже), та перорального розчину, що дозволяє точно дозувати лікарський засіб навіть для дуже маленьких дітей.
У ході цього неінвазивного дослідження (НІД) планувалося отримати унікальні дані щодо використання РЛЗ у рутинній клінічній практиці в амбулаторних педіатричних пацієнтів із захворюваннями сечовидільної системи в Росії, його ефективності та безпеки. Результати дослідження сприятимуть оптимізації лікування захворювань сечовидільної системи у дітей.
Методи
Дизайн та процедури дослідження
Мета цього неінвазивного проспективного багатоцентрового дослідження полягала у зборі даних про застосування РЛЗ у популяції амбулаторних педіатричних пацієнтів у Росії. НІД проводили відповідно до Гельсінської декларації, Керівництва з належної фармакоепідеміологічної практики, усіх чинних норм Належної клінічної практики (ICH-GCP) та національного стандарту GCP Росії.
Протокол НІД був затверджений місцевими комітетами з питань етики. НІД проведено з моніторингом на місці з боку контрактної дослідницької організації (КДО), уповноваженої спонсором дослідження. План моніторингу включав 100% перевірку вихідних даних для форм інформованої згоди, небажаних явищ (НЯ) та серйозних небажаних явищ (СНЯ). Крім того, було заплановано та здійснено 100% перевірку даних перших двох пацієнтів у кожному центрі для вирішення питань щодо документування та підготовки центру дослідження (за необхідності) для отримання точних і достовірних даних. Для забезпечення безпеки пацієнтів, а також для правильного їх відбору здійснювали перевірку критеріїв включення та виключення для перших 5 пацієнтів у кожному центрі.
НІД проводили у 26 поліклініках та амбулаторних закладах різних регіонів Росії. Усі лікарі були спеціалістами – педіатрами, дитячими нефрологами, дитячими урологами та ін. Учасники дослідження – амбулаторні педіатричні пацієнти віком від 1 до 17 років із підтвердженим діагнозом захворювання сечовидільної системи, яким призначали лікування РЛЗ. Критеріями виключення були протипоказання, вказані в інструкції для медичного застосування (підвищена чутливість до будь-яких компонентів РЛЗ, виразка шлунка та виразка дванадцятипалої кишки у гострій фазі), а також участь у клінічному дослідженні одночасно або за 3 місяці до його проведення. У НІД були включені лише ті пацієнти, чиї батьки та/або законні представники надали письмову інформовану згоду на участь. Пацієнти віком від 14 до 17 років також мали підписати письмову форму згоди на участь у дослідженні.
Закріплений лікар мав призначати РЛЗ у лікарській формі перорального розчину або таблеток пацієнтам за наявності показань відповідно до інформації про РЛЗ для Росії (інструкції для медичного застосування). Так, РЛЗ використовують для комплексної терапії хронічних інфекцій сечового міхура (циститу) і нирок (пієлонефриту), неінфекційного хронічного запалення нирок (гломерулонефриту, інтерстиціального нефриту), а також для профілактики утворення сечових каменів та після їх видалення. Рекомендації щодо дозування для дітей шкільного віку – 25 крапель або 1 таблетка 3 р/добу, для дітей дошкільного віку – 15 крапель 3 р/добу. Після зменшення симптомів захворювання рекомендується продовжити лікування препаратом протягом 2-4 тижнів. Повну інформацію про продукт, застереження, протипоказання тощо містить інструкція для медичного застосування РЛЗ, яка представлена в оглядовому плані дослідження. Відповідно до інформації про продукт немає жодних обмежень для застосування РЛЗ у комплексному лікуванні.
Тривалість терапії визначав закріплений лікар на власний розсуд залежно від клінічної картини захворювання у конкретного пацієнта. Вона становила від кількох днів до кількох тижнів або місяців. Пацієнтів можна було лікувати РЛЗ до їх включення у НІД. Їх включали для оцінки безпеки у вибірку, яку використовували для аналізу, лише у тому випадку, якщо вони приймали принаймні одну дозу РЛЗ протягом дослідження.
Період спостереження, який включав етапи лікування та подальшого спостереження, був обмежений максимальним терміном 6 тижнів. Збір даних проводили на початковому етапі, через 2 та 6 тижнів лікування методом опитування під час візитів пацієнта до лікаря або телефоном. У рамках цього дослідження будь-які спеціальні процедури збору даних не було передбачено.
У НІД здійснювали оцінку таких основних параметрів: показання для призначення РЛЗ, призначені лікарські форми засобу, встановлений режим лікування, призначена та фактична тривалість терапії, тип застосування РЛЗ (профілактика та/або лікування), використання супутніх препаратів, проведення немедикаментозної терапії. Схему лікування визначали як кількість і відсоток пацієнтів, які отримували різні добові дози та мали різну частоту введення РЛЗ. Кодування показань здійснював адміністратор даних КДО за допомогою Медичного словника для регуляторної діяльності (MedDRA, версія 19.0).
Супутніми препаратами були ЛЗ, прийом яких пацієнт не припиняв перед початком дослідження. Вони були закодовані з використанням Розширеного словника лікарських засобів ВООЗ (WHO DDE, версія від 01.06.2016). На основі даних про призначену та фактичну тривалість лікування підраховували частоту дотримання терапії пацієнтом у відсотках: дотримання терапії (%) = фактична тривалість (дні) / призначена тривалість (дні) × 100%.
Для оцінки загальної ефективності та переносимості РЛЗ лікарем та пацієнтом/батьками дитини використовували 5-бальну шкалу. Окрім цього, були задокументовані симптоми з боку сечовидільної системи та результати лікування захворювань сечовидільної системи (повне одужання, покращення перебігу, без змін, погіршення перебігу та рецидиви). Змінними у дослідженні були дані про лікування захворювань сечовидільної системи протягом 2 тижнів до початку дослідження, немедикаментозну терапію та основні фізіологічні показники.
Оцінка профілю безпеки РЛЗ включала дані про всі НЯ, що виникали на фоні терапії, небажані лікарські реакції (НЛР), НЛР, які виникали на фоні терапії, серйозні НЯ та серйозні НЛР. НЯ та НЛР кодували за допомогою словника MedDRA (версія 19.0).
Підгрупи пацієнтів
Аналіз по підгрупах проводили за віковою категорією, за використанням супутньої медикаментозної терапії (порівняльний аналіз ефективності монотерапії та комбінованої терапії) та за показаннями. Вікові категорії визначали таким чином: діти раннього віку (12-23 міс), дошкільного віку (2-5 років), раннього шкільного віку (6-11 років), підлітки (12-17 років). Підгрупа пацієнтів, які отримували монотерапію РЛЗ, включала усіх дітей та підлітків, які під час проведення НІД приймали тільки цей засіб без будь-яких додаткових супутніх медикаментів. Якщо пацієнт приймав для лікування захворювань сечовидільної системи будь-які лікарські засоби одночасно з РЛЗ, його включали у підгрупу комбінації ЛЗ. Для аналізу за показаннями планувалося групувати зареєстровані показання. Групи показань були визначені згідно з переліком найчастіших показань, задокументованих в індивідуальній реєстраційній картці (ІРК) пацієнта. У підсумку за показаннями сформували 6 груп.
Статистичний аналіз
Аналіз даних проводили за допомогою методів описової статистики. Статистичні дані представлені у зведених таблицях (безперервні змінні: n, середнє та стандартне відхилення, медіана, мінімальне та максимальне значення; категоріальні змінні: n, частота і відсоток). Пропорцію оцінювали разом з 95% довірчим інтервалом (у відповідних випадках).
Результати
За період з вересня 2015 року по червень 2016 року 636 дітей були включені у НІД в 26 центрах. Із них 620 пацієнтів завершили лікування за протоколом дослідження, 16 пацієнтів передчасно припинили участь через НЯ (n=8). Зареєстровано також випадки припинення спостереження через втрату зв’язку з пацієнтом (n=5) та з інших причин (n=3). Загалом 634 пацієнти (99,7% усіх включених у дослідження пацієнтів) отримали принаймні одну дозу РЛЗ і були включені у вибірку для оцінки безпеки, яку використовували для аналізу (наведені нижче відсотки стосуються вибірки для оцінки безпеки, якщо не зазначено інше). Підгрупу, яка розпочала лікування РЛЗ до включення у НІД, склали 37 пацієнтів. Характеристики пацієнтів наведено у таблиці 1.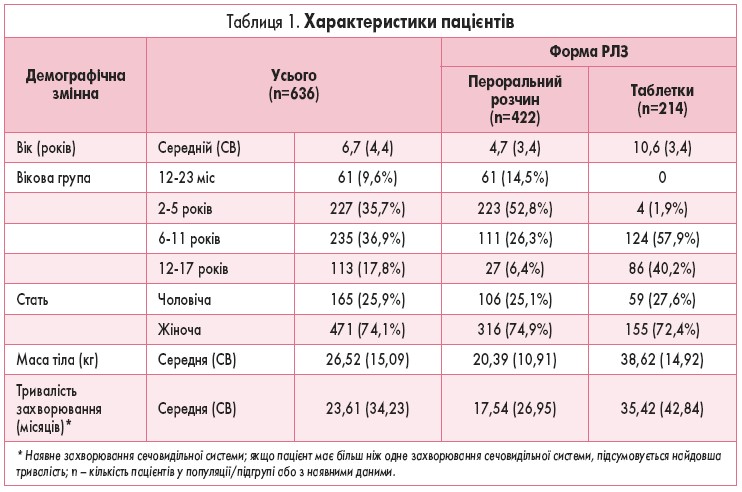
Пероральний розчин РЛЗ призначили 66,4% пацієнтів, включених у дослідження, таблетки – 33,6%. У більшості дітей віком до 6 років використовували розчин (табл. 1). Не встановлено жодної різниці в розподілі за статтю пацієнтів, яким призначили розчин або таблетки. Більшість пацієнтів (98,3%) приймали РЛЗ тричі на добу.
РЛЗ використовували для лікування гострого або хронічного захворювання – у 48% пацієнтів, для профілактики – у 25%, як для профілактики, так і для лікування – у 27%. Розподіл пацієнтів, які приймали розчин або таблетки, був аналогічним.
РЛЗ призначали 75,2% усіх пацієнтів за наявності показань, які кодують за системно-органним класом (СОК) «Інфекційні та паразитарні захворювання». Найбільш частими показаннями, які включені у цей СОК, були ІСВШ (34,1%) та пієлонефрит (30,0%). У 36% пацієнтів показання СОК «Порушення з боку нирок та сечовивідних шляхів» задокументовані як підстава для лікування РЛЗ (табл. 2).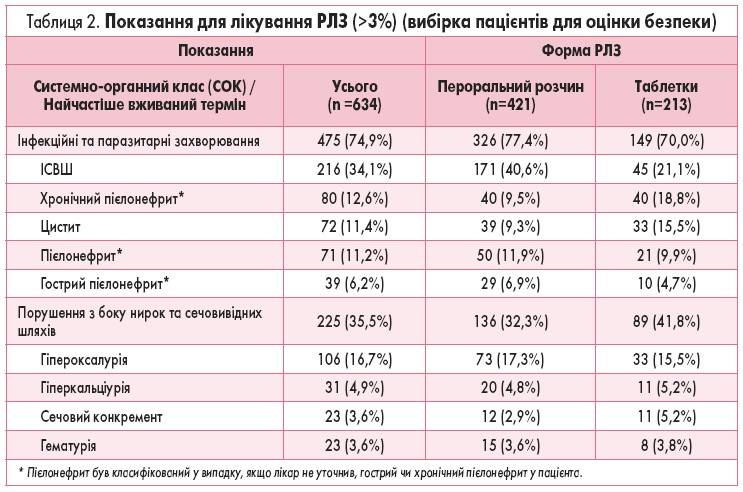
У деяких пацієнтів РЛЗ використовували поза зареєстрованими показаннями – у випадках нейрогенного сечового міхура, гіпотонічного сечового міхура і гідронефрозу. У рідкісних випадках (1,6%) засіб призначали за показаннями, які включені у СОК «Вроджені, сімейні та генетичні розлади».
Для подальшого аналізу за показаннями пацієнти були розподілені на 6 груп: неуточнених ІСВШ (216 пацієнтів), пієлонефриту (190 пацієнтів), дисметаболічної нефропатії/кристалурії (120 пацієнтів), циститу (73 пацієнти), сечокам’яної хвороби (26 пацієнтів), нефриту (23 пацієнти). Групи показань представлені у таблиці 3. Із 120 пацієнтів із дисметаболічною нефропатією/кристалурією 106 пацієнтів (88%) мали гіпероксалурію, 31 пацієнт (26%) – гіперкальціурію (у пацієнта могло бути більше одного діагнозу – 120 пацієнтів мали 150 діагнозів).
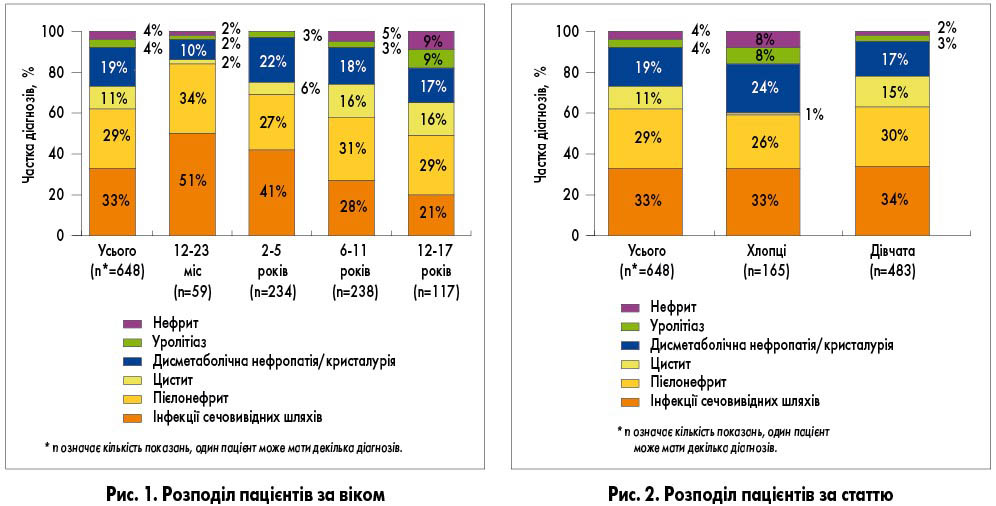
 Частота ІСВШ була найбільшою в наймолодшій віковій категорії (51%) і зменшилася у пацієнтів старшого віку, тоді як частота показань групи циститу збільшилася у пацієнтів віком старше 2 років. Показання групи сечокам’яної хвороби та групи нефриту мали лише пацієнти віком від 12 до 17 років (рис. 1). Показання групи циститу частіше зустрічалися у дівчат, ніж у хлопців (15% та 1% відповідно), а показання групи нефриту, сечокам’яної хвороби та дисметаболічної нефропатії/кристалурії частіше реєстрували у хлопців (рис. 2).
Частота ІСВШ була найбільшою в наймолодшій віковій категорії (51%) і зменшилася у пацієнтів старшого віку, тоді як частота показань групи циститу збільшилася у пацієнтів віком старше 2 років. Показання групи сечокам’яної хвороби та групи нефриту мали лише пацієнти віком від 12 до 17 років (рис. 1). Показання групи циститу частіше зустрічалися у дівчат, ніж у хлопців (15% та 1% відповідно), а показання групи нефриту, сечокам’яної хвороби та дисметаболічної нефропатії/кристалурії частіше реєстрували у хлопців (рис. 2).
Супутній препарат у будь-який момент періоду спостереження, тобто необов’язково одночасно з лікуванням РЛЗ, приймали 392 пацієнти (61,8%), 377 із них приймали додатковий препарат разом із РЛЗ, тому були класифіковані як пацієнти, що отримували комбіновану терапію. Монотерапію використовували у 257 пацієнтів. У групу пацієнтів, які отримували монотерапію, були включені також хворі, яким проведено супутнє медикаментозне лікування, але не одночасно з лікуванням РЛЗ.
Один додатковий препарат у складі комбінованої терапії отримували 22% пацієнтів, два додаткові препарати – 16%, три і/або більше додаткових препаратів – 9%. Частка пацієнтів, які отримували комбіновану терапію, була найбільшою у групі нефриту (65%). Показники використання монотерапії були найвищими у групах дисметаболічної нефропатії/кристалурії (61%), сечокам’яної хвороби (58%), ІСВШ та циститу (51%).
Тривалість терапії РЛЗ варіювала від 7 до 84 днів. Хворі приймали засіб у середньому на два дні довше, ніж призначив лікар, що зумовило частоту дотримання терапії пацієнтом – 106,3±23,6%, при цьому не встановлено значущих відмінностей залежно від лікарської форми та групи за показаннями. Середня тривалість лікування була найкоротшою для групи ІСВШ та найдовшою для групи нефриту (рис. 3). Фактична тривалість терапії РЛЗ становила 30,6 днів у пацієнтів, які отримували монотерапію, та 32,5 дні, якщо РЛЗ приймали у комбінації з іншою терапією. Тривалість лікування була однаковою для пацієнтів, які отримували його для лікування та/або профілактики.
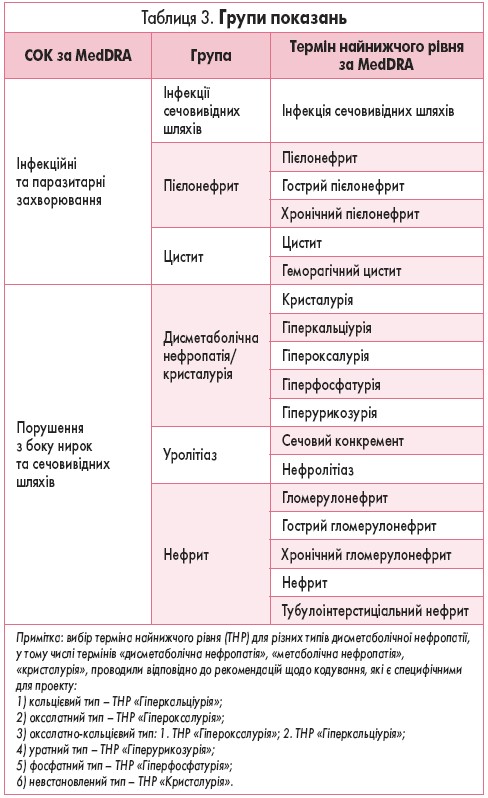
 Через 6 тижнів терапії у більшості пацієнтів зареєстровано зменшення симптомів з боку сечовивідних шляхів (частоти сечовипускання, змін у макроскопії сечі). Аналіз результатів лікування захворювань сечовидільної системи, який було проведено наприкінці періоду спостереження, показав, що захворювання залишилося невирішеним менш ніж у 4% пацієнтів, включених у дослідження. Згідно з отриманими даними, 20% пацієнтів повністю одужали, у 65% спостерігалося покращення перебігу, 13% повідомили про відсутність змін, тоді як по 1% – про погіршення перебігу або рецидив. Найвищий коефіцієнт відновлення показань був у групі ІСВШ (37,4%). Частка пацієнтів, стан яких оцінено як «одужання», була тільки на 10% більше після закінчення дослідження порівняно з показником під час візиту 2 і на 5% менше частки пацієнтів, які оцінили свій стан «без змін» наприкінці дослідження порівняно з візитом 2. При цьому кількість осіб із погіршенням перебігу або рецидивом захворювання не змінилася (рис. 4).
Через 6 тижнів терапії у більшості пацієнтів зареєстровано зменшення симптомів з боку сечовивідних шляхів (частоти сечовипускання, змін у макроскопії сечі). Аналіз результатів лікування захворювань сечовидільної системи, який було проведено наприкінці періоду спостереження, показав, що захворювання залишилося невирішеним менш ніж у 4% пацієнтів, включених у дослідження. Згідно з отриманими даними, 20% пацієнтів повністю одужали, у 65% спостерігалося покращення перебігу, 13% повідомили про відсутність змін, тоді як по 1% – про погіршення перебігу або рецидив. Найвищий коефіцієнт відновлення показань був у групі ІСВШ (37,4%). Частка пацієнтів, стан яких оцінено як «одужання», була тільки на 10% більше після закінчення дослідження порівняно з показником під час візиту 2 і на 5% менше частки пацієнтів, які оцінили свій стан «без змін» наприкінці дослідження порівняно з візитом 2. При цьому кількість осіб із погіршенням перебігу або рецидивом захворювання не змінилася (рис. 4).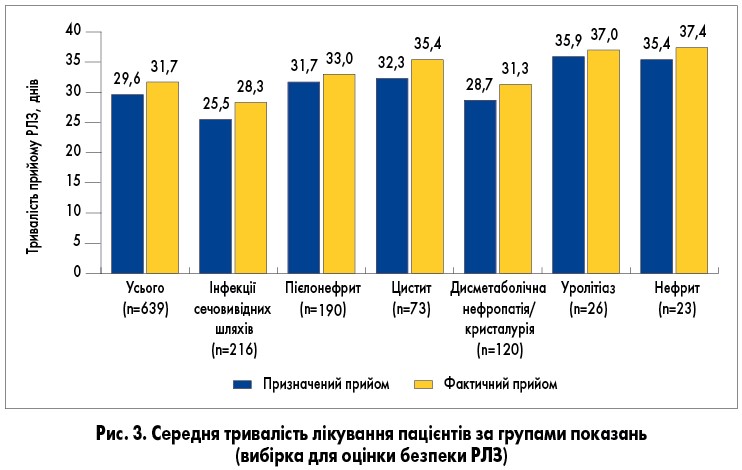
Для 88 і 91% усіх пацієнтів, які отримували монотерапію РЛЗ, дослідники оцінили ефективність лікування як «хорошу» або «дуже хорошу» під час візиту 2 (тиждень 2) і наприкінці дослідження відповідно. Частка пацієнтів, у яких ефективність монотерапії РЛЗ оцінили як «дуже хорошу», збільшувалася протягом періоду спостереження (рис. 5 і 6). Відмінностей в ефективності монотерапії РЛЗ та комбінованої терапії не встановлено. Оцінка ефективності лікування пацієнтами була аналогічною оцінці дослідників.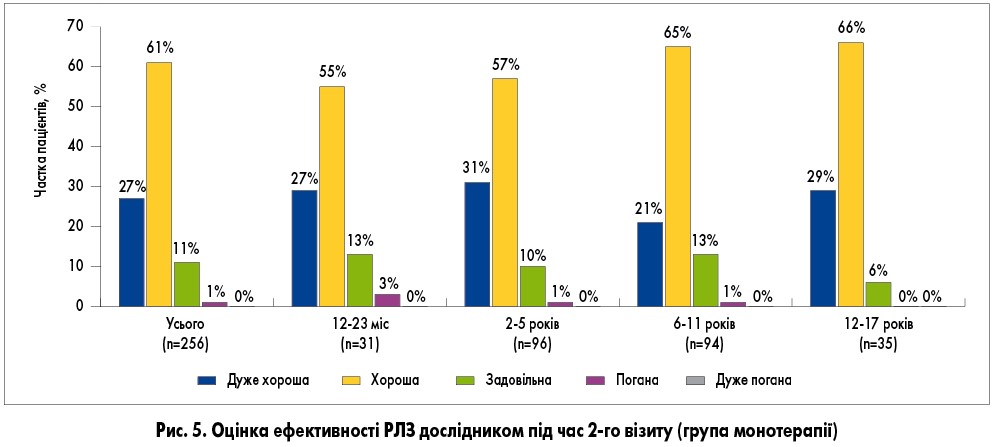

Переносимість РЛЗ наприкінці дослідження оцінили як «хорошу» або «дуже хорошу» 99% пацієнтів. У всіх вікових групах співвідношення оцінок «хороша» та «дуже хороша» переносимість було високим (рис. 7). Протягом періоду спостереження у 82 (12,9%) пацієнтів зареєстровано 96 НЯ, причому найчастішими задокументованими НЯ були «інфекційні та паразитарні захворювання» (у 55 пацієнтів) та «порушення функції нирок і сечовивідних шляхів» (в 11 хворих). Найбільш частими НЯ за найдовшою тривалістю були вірусна інфекція дихальних шляхів (15 пацієнтів), назофарингіт (7), цистит (5) та інфекція дихальних шляхів (5). Решту НЯ зареєстровано у ≤4 пацієнтів. Більшість НЯ були легкого ступеня (67 пацієнтів). Серйозних НЯ не спостерігалося.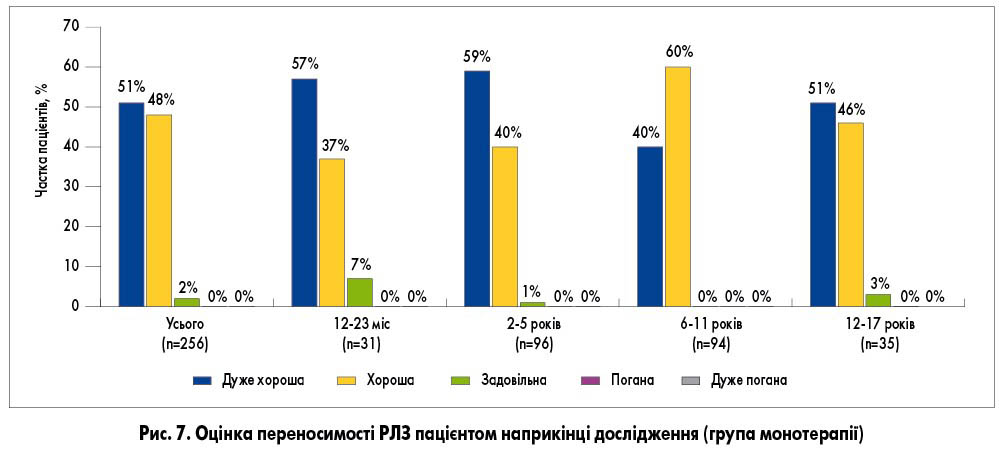
Про НЛР повідомлялося лише у 5 пацієнтів: 3 пацієнти мали алергічний дерматит, один пацієнт – диспепсію і ще один – ниркову коліку. Чотири з них належали до групи комбінованої терапії і лише один пацієнт (з алергічним дерматитом) – до групи монотерапії. Тільки одну НЛР (ниркову коліку) у групі комбінованої терапії оцінили як «серйозну». Ниркова коліка призвела до виведення конкременту з нирки.
Лише 8 (1,3%) пацієнтів передчасно припинили участь у НІД через НЯ/НЛР: 3 пацієнти, які отримували монотерапію, 5 – комбіновану терапію. Серед них – 3 пацієнти з дерматитом та один пацієнт із функціональними порушеннями ШКТ, блюванням, пієлонефритом, ІСВШ та нирковою колікою.
Обговорення
Фітотерапевтичні лікарські засоби, у тому числі РЛЗ, який був об’єктом цього дослідження, широко використовують у рутинній клінічній практиці для лікування та профілактики різних захворювань сечовидільної системи у популяції педіатричних пацієнтів у Росії. Проте плацебо-контрольовані дослідження з оцінки ефективності РЛЗ досі не проводили. Оскільки це дослідження було неінвазивним, закріплені лікарі мали призначити РЛЗ відповідно до інформації про продукт, схваленої в Російській Федерації. Однак застосування РЛЗ не обмежувалося будь-якими показаннями. Отже, представлені результати дослідження відображають клінічну практику його застосування у педіатричних пацієнтів. Вони можуть бути використані для оптимізації керування перебігом патології у дітей із захворюваннями сечовидільної системи та покращення результатів їх лікування.
Дітям віком до 6 років здебільшого призначали пероральний розчин відповідно до інструкції для медичного застосування РЛЗ, у якій вказано, що таблетки (драже) показані лише дітям віком старше 6 років. Переважання пацієнтів жіночої статі у спостережуваній популяції відображає гендерні відмінності у структурі ІСВШ. Частота захворюваності у дівчат, про яку повідомлялося, у 2-4 рази вища, ніж у хлопців. У більшості пацієнтів РЛЗ застосовували для лікування або профілактики ІСВШ, пієлонефриту та циститу. РЛЗ використовували у педіатричній практиці для широкого спектра показань, а також поза зареєстрованими показаннями. Нетипові показання, такі як нейрогенний сечовий міхур, гіпотонічний сечовий міхур та гідронефроз, демонструють можливості застосування РЛЗ. Дисметаболічна нефропатія, або кристалурія, була показанням для лікування РЛЗ у 120 випадках.
Переваги та хороша переносимість РЛЗ у лікуванні та профілактиці захворювань сечовивідних шляхів продемонстровано у дітей та підлітків віком від 1 до 17 років. Симптоми з боку сечовидільної системи зменшилися, більшість пацієнтів одужали або у них спостерігалося покращення перебігу захворювання.
Результати, отримані у цьому дослідженні, узгоджуються з даними попередніх досліджень за участю дорослих і дітей, які проаналізували Naber та співавт. (17 досліджень). Naber та співавт. дійшли висновку, що РЛЗ зменшує симптоми інфекції та запалення сечовивідних шляхів, сприяє виведенню невеликих каменів оксалату кальцію та запобігає літогенезу.
В іншому порівняльному дослідженні за участю 86 дітей з рецидивуючим пієлонефритом РЛЗ у комплексі зі стандартною антибіотикотерапією забезпечив повну ремісію у 61% пацієнтів. Дослідження показало, що курс протимікробних препаратів для запобігання рецидивам пієлонефриту може бути скорочений і таким чином можна зменшити побічні ефекти антибактеріальних препаратів. Комбінована терапія з включенням РЛЗ при пієлонефриті у дітей покращує мікроальбумінурію, яка є ранньою ознакою ураження паренхіми нирок [27].
Особливості використання РЛЗ дають можливість лікарю визначати тривалість терапії на власний розсуд. У цьому дослідженні тривалість лікування варіювала від декількох днів до декількох тижнів залежно від індивідуальних потреб пацієнта. Досягнуто 100% дотримання призначеної тривалості курсу як для обох лікарських форм, так і для усіх груп пацієнтів за показаннями, що підтверджує хорошу переносимість РЛЗ, 99% пацієнтів оцінювали переносимість як «хорошу» або «дуже хорошу», лише 8 пацієнтів припинили участь у дослідженні через НЯ. Про сприятливий профіль безпеки РЛЗ також повідомлялося у попередніх дослідженнях [3]. Найбільш поширені НЛР, перелік яких подано в інформації про продукт, включають порушення з боку ШКТ (нудоту, блювання, діарею, алергічні реакції).
Висновки
На підставі отриманих у дослідженні даних можна зробити висновок, що лікування дітей та підлітків віком від 1 до 17 років за допомогою препарату Канефрон® Н є безпечним і добре переноситься пацієнтами. Препарат є ефективним для лікування захворювань сечовидільної системи. Подальші клінічні випробування допоможуть краще зрозуміти користь від застосування РЛЗ в обраних популяціях пацієнтів щодо результатів терапії для відповідних показань.
Список літератури знаходиться в редакції.
Стаття друкується у скороченні.
Dlin et al. Clinical Phytoscience (2018) 4:31https://doi.org/10.1186/s40816-018-0092-9
Тематичний номер «Педіатрія» №1 (48), березень 2019 р.