21 березня, 2019
Эффективность микафунгина в лечении микозов
Повышение частоты грибковых заболеваний (в т. ч. микозов, ассоциированных с ВИЧ-инфекцией, онкогематологическими заболеваниями) наряду с развитием устойчивости возбудителей к лекарственным средствам ставит перед исследователями вопрос о поиске эффективных противогрибковых препаратов. Для лечения заболеваний, вызванных дрожжеподобными грибами, используют ряд лекарственных средств, различных по происхождению (природные или синтетические), спектру и механизму действия, оказываемому эффекту (фунгицидный или фунгистатический), показаниям (местные или системные инфекции) и способу применения (парентерально или перорально). Выбор препарата для терапии микозов зависит от вида возбудителя и его чувствительности к данному препарату, особенностей его фармакокинетики и фармакодинамики, токсичности, а также от клинического состояния пациента.
Среди доступных в настоящее время противогрибковых средств одними из наиболее мощных агентов против различных видов Candida и большинства видов Aspergillus являются эхинокандины. Эти препараты оказывают быстрый фунгицидный эффект и обладают хорошей переносимостью.
Эхинокандины представляют собой новый класс полусинтетических липопептидов, механизм действия которых связан с блокадой синтеза составного компонента клеточной стенки грибов, что приводит к нарушению ее образования. При этом эхинокандины, не теряя эффективности, имеют значительно меньше побочных эффектов, чем другие противогрибковые средства для системного применения. Они не метаболизируются цитохромами Р450 и не обладают большим количеством лекарственных взаимодействий. Это позволяет рассматривать этот класс в качестве препаратов выбора при системных микозах, особенно в ситуациях, когда другие противогрибковые средства неэффективны. Кроме того, из-за особого механизма действия эхинокандины имеют потенциал для комбинированной терапии с другими классами антимикотиков. Все препараты класса эхинокандинов назначают только внутривенно. Они обладают дозозависимой фармакокинетикой с периодом полувыведения 10-15 ч, что позволяет назначать их 1 раз в сутки. Все эхинокандины имеют высокую (>95%) степень связывания с белками и распределяются в основные ткани организма, включая головной мозг, однако концентрации в неинфицированной спинномозговой жидкости низкие.
Впервые препарат из группы эхинокандинов для системного применения у человека был одобрен почти 10 лет назад. С тех пор эффективность препаратов этого класса в лечении и профилактике кандидоза у детей и взрослых подтверждена многими учеными. В нескольких рандомизированных клинических исследованиях, в которых изучалась эффективность эхинокандинов в лечении инвазивного кандидоза в сравнении с другими противогрибковыми средствами, установлено, что эти препараты обладают стабильно высокой клинической и микологической активностью у пациентов с различными формами кандидоза, включая инвазивный кандидоз и кандидозный эзофагит. Учитывая благоприятные клинические результаты, эхинокандины стали препаратами первого выбора при большинстве форм инвазивного кандидоза у пациентов со среднетяжелым и тяжелым состоянием, у которых высок риск инфекции, вызванной Candida non-albicans spp., или недавно получавших лечение азолами.
Наиболее изученным на сегодняшний день препаратом класса эхинокандинов является микафунгин – препарат с высокой активностью in vitro против большинства видов Candida и Aspergillus. В клинических исследованиях показана высокая эффективность и безопасность данного препарата при парентеральном введении у большого числа пациентов с инвазивным кандидозом и кандидозным эзофагитом.
Микафунгин в лечении кандидемии и других форм инвазивного кандидоза
Проведено три крупных исследования микафунгина для лечения инвазивного кандидоза. В открытом мультицентровом исследовании (Ostrosky-Zeichner L. et al., 2005) микафунгин применялся в качестве препарата спасения у больных (n=148) с кандидемией. Участники получали микафунгин в виде монотерапии или в комбинации с другими противогрибковыми препаратами. В целом благоприятный исход был достигнут у 83% пациентов. Частота успешного лечения несущественно зависела от вида возбудителя, составив 85,1%, 93,8%, 86,4% и 83,3% у пациентов с C. albicans, C. glabrata, C. parapsilosis и C. tropicalis соответственно. Проанализировав полученные результаты, авторы пришли к выводу, что микафунгин в дозе 50-100 мг/сут безопасен и эффективен в лечении кандидемии.
В другом рандомизированном исследовании (Kuse E.R. et al., 2007) с участием 531 пациента сравнивали микафунгин 100 мг/сут и липосомальный амфотерицин B 3 мг/кг 1 раз в сутки для лечения кандидемии и инвазивного кандидоза. Исследуемые препараты применяли в течение не менее 14 дней, но не более 8 нед (для пациентов с осложнениями, включая хронический диссеминированный кандидоз, кандидозный остеомиелит и эндокардит). При отсутствии адекватного ответа на терапию допускалось повышение дозы на усмотрение исследователя (до 200 мг микафунгина и до 5 мг/кг липосомального амфотерицина B). В обеих группах подавляющее число выделенных штаммов составили Candida non-albicans. Всего в анализ были включены данные 494 пациентов (лица, получившие хотя бы одну дозу исследуемого препарата). Лечение было успешным у 74% больных в группе микафунгина и у 70% – в группе липосомального амфотерицина B. Авторами был сделан вывод, что микафунгин не менее эффективен, чем липосомальный амфотерицин B. В группе пациентов, получавших последний, отмечена более высокая частота инфузий-ассоциированных нежелательных реакций, в т. ч. нарушение функции почек и гипокалиемия. Согласно результатам данного исследования, микафунгин является безопасным и эффективным препаратом для лечения инвазивного кандидоза, в частности наиболее тяжелых форм этого заболевания, таких как хронический диссеминированный кандидоз, кандидозный остеомиелит и кандидозный эндокардит. Также было продемонстрировано, что микафунгин имеет более благоприятный профиль безопасности по сравнению с липосомальным амфотерицином B.
Целью еще одного исследования (Pappas P.G. et al., 2007) было сравнение эффективности микафунгина в двух разных дозах (100 и 150 мг/сут) и каспофунгина в стандартной дозе (50 мг/сут). Исследуемый препарат применяли не менее чем 10 дней, после чего при необходимости допускался переход на пероральный прием флуконазола. В общей сложности лечение продолжали в течение 14 дней после последнего положительного результата посева крови. В исследование включали только взрослых больных. Группы были сопоставимыми по демографическим характеристикам. По клиническим проявлениям заболевания участники распределились следующим образом: у 85% пациентов исходно диагностирована кандидемия, у остальных 15% – другие формы инвазивного кандидоза, кроме эндокардита и остеомиелита. Медиана продолжительности лечения в каждой группе равнялась 14 дням. Более половины выделенных штаммов составили Candida non-albicans c приблизительно равным представительством в группах. Частота успешного лечения составила 72; 76 и 71% при применении каспофунгина и микафунгина 100 и 150 мг/сут соответственно. Среднее время до получения отрицательных результатов посева составляло 2 дня в группе каспофунгина и при применении 100 мг микафунгина и 3 дня у пациентов, получавших 150 мг микафунгина. Существенных различий между исследуемыми группами в показателях смертности, частоты рецидивирования инфекции или развития побочных эффектов не обнаружено.
В этом же исследовании установлено, что у пациентов с C. parapsilosis и C. glabrata наблюдались более благоприятные исходы при любой дозе микафунгина (74 и 87% соответственно) по сравнению с каспофунгином (64 и 67% соответственно). В то же время у пациентов с C. tropicalis при лечении каспофунгином исходы были лучше, чем при лечении микафунгином (75 против 64%). Ни в одном из этих случаев разница не была статистически значимой и не могла быть обусловлена устойчивостью возбудителя к тому или иному препарату.
Таким образом, было доказано, что микафунгин в дозе 100 мг/сут эффективен у большинства больных инвазивным кандидозом. В большой выборке пациентов не обнаружено зависимости положительного результата лечения от дозы.
В обобщенном анализе (Horn D.L. et al., 2010) результатов двух крупных проспективных сравнительных исследований микафунгина у пациентов с кандидемией оценивались независимые факторы, влияющие на выживаемость пациентов и успех лечения. Были проанализированы показатели выживаемости в течение 42 дней от начала лечения и исходы в конце терапии. Исследователи обнаружили, что при кандидемии лечение было успешным значительно чаще, чем при инвазивном кандидозе без кандидемии. Кроме того, авторы выяснили, что факторами, отрицательно влияющими на выживаемость больных и эффективность лечения, были: наличие сосудистых катетеров, оценка тяжести состояния пациента по шкале APACHE II >20 баллов, возраст старше 70 лет, исходное лечение кортикостероидами, почечная недостаточность или упорная нейтропения.
С учетом результатов этих исследований есть основания считать микафунгин высокоэффективным средством лечения кандидемии и других форм инвазивного кандидоза. Установлено, что по своей активности этот препарат сопоставим с другими эхинокандинами и вызывает меньше побочных эффектов, чем липосомальный амфотерицин B. Кроме того, не выявлено значимой разницы в активности воздействия на разные виды Candida. Обобщенные данные свидетельствуют о том, что доза микафунгина 100 мг/сут достаточна для большинства пациентов с инвазивным кандидозом.
В руководстве (2009) Американского общества по борьбе с инфекционными болезнями (IDSA) по лечению инвазивного кандидоза уделено внимание менее частым формам кандидоза, однако в силу недостатка данных рекомендации по большей части основаны на мнении экспертов. Несмотря на ограниченное количество данных, полученных из описаний клинических случаев, единичных сообщений и ретроспективных наблюдений, все они свидетельствуют о целесообразности применения микафунгина при таких относительно редких формах инвазивного кандидоза, как инфекционный эндокардит, остеомиелит, гнойный артрит, менингит и эндофтальмит. Наиболее надежные данные касаются применения эхинокандинов при кандидозном эндокардите. В большинстве публикаций изложены результаты применения каспофунгина, а сведений относительно использования микафунгина при этом заболевании существенно меньше. В самом крупном на сегодня ретроспективном исследовании эхинокандины продемонстрировали значительное преимущество перед амфотерицином B в комбинации с флуцитозином или без такового в отношении общей эффективности у больных с кандидозным эндокардитом. Данных о применении микафунгина и других эхинокандинов в лечении остеомиелита и гнойного артрита опубликовано меньше. Сведения о применении эхинокандинов при кандидозном менингите и эндофтальмите крайне ограничены, и в целом эти препараты для первичного лечения таких заболеваний не рекомендуются.
Микафунгин в лечении кандидозного эзофагита
Кандидозный эзофагит – это СПИД-индикаторное заболевание, осложнение, возникающее на поздних стадиях ВИЧ-инфекции. Эффективность всех препаратов класса эхинокандинов в лечении кандидозного эзофагита изучена в рандомизированных многоцентровых исследованиях. В одном из них (Pettengell K. et al., 2004) оценивалась активность микафунгина в различных дозировках, еще в двух крупных рандомизированных двойных слепых исследованиях (de Wet N. et al., 2004; 2005) микафунгин сравнивался с флуконазолом.
В первом из упомянутых исследований 120 пациентов с эндоскопически подтвержденным диагнозом кандидозного эзофагита получали препарат в дозах от 12,5 до 100 мг/сут. Лечение продолжалось до 14 дней. В исследовании продемонстрирована прямая корреляция между клиническим и микологическим эффектом и дозой препарата: излечение было достигнуто у 33; 54; 87; 84 и 96% пациентов, получавших препарат в дозе 12,5; 25; 50; 75 и 100 мг/сут соответственно. Полученные результаты свидетельствовали о высокой результативности (минимальная эффективная доза составляла 12,5 мг), хорошей переносимости и безопасности микафунгина даже в высоких дозах (>100 мг/сут).
Сравнение эффективности микафунгина и флуконазола в лечении кандидозного эзофагита выполнено в исследованиях N. de Wet и соавт. В рандомизированном двойном слепом исследовании (2004) оценивались различные дозы (50, 100 и 150 мг/сут) микафунгина в сравнении с флуконазолом 200 мг/сут в течение 14-21 дня. В нем также была показана линейная зависимость частоты успешного лечения от дозы микафунгина: 69; 77 и 90% при дозе 50; 100 и 150 мг соответственно. Общая частота эндоскопически подтвержденного излечения при применении 100 и 150 мг/сут микафунгина составила 83,5% и была сопоставимой с таковой при применении 200 мг/ сут флуконазола (86,7%). В периоде наблюдения рецидивы заболевания развились у 9 (5%) пациентов, получавших микафунгин, в то время как у участников группы флуконазола рецидивирования не наблюдалось. Таким образом, можно сделать вывод о целесообразности применения более высоких доз микафунгина при кандидозном эзофагите. Вместе с тем авторами поднят вопрос об угрозе рецидива инфекции после отмены лечения.
Изучение сравнительной эффективности микафунгина (150 мг/сут) и флуконазола (200 мг/сут) продолжено этими авторами в рандомизированном двойном слепом исследовании (2005) с участием пациентов (n=523) с ВИЧ-ассоциированным кандидозным эзофагитом. Медиана продолжительности лечения составила 14 сут в каждой группе. Эндоскопически подтвержденное излечение было достигнуто у 87,7% пациентов, получавших микафунгин, и у 88% – флуконазол. Частота рецидивов в течение 4 нед наблюдения составила 15,2% в группе микафунгина и 11,3% в группе флуконазола.
Таким образом, в трех исследованиях подтверждена клиническая значимость микафунгина в лечении тяжелого кандидозного эзофагита. В последних рекомендациях IDSA по лечению кандидоза отмечается, что флуконазол высокоэффективен у большинства пациентов с кандидозным эзофагитом, поэтому эхинокандины рекомендованы как препараты резерва для больных с тяжелым или рефрактерным заболеванием или невозможностью перорального приема препаратов. У клиницистов может вызвать опасение частота рецидивов после лечения эхинокандинами. Однако следует отметить, что в самом крупном на сегодня исследовании, где сравнивали микафунгин 150 мг/сут и флуконазол 200 мг/сут, частота рецидивов в группах была сопоставимой (15 и 11% соответственно), поэтому опасения относительно рецидива на фоне лечения микафунгином могут быть преувеличены.
Чувствительность in vitro изолятов Aspergillus spp. к препаратам класса эхинокандинов
Грибы рода Aspergillus вызывают поражения, которые принято разделять на инвазивные, сапрофитные и аллергические. Инвазивные процессы, вызванные грибами рода Aspergillus, чаще всего поражают нижние дыхательные пути, пазухи носа, а также кожу и мягкие ткани. Головной мозг, сердечно-сосудистая система и другие органы и ткани могут инфицироваться вследствие гематогенной диссеминации из очагов первичного поражения или путем прямого проникновения из близко расположенных очагов. Сапрофитные поражения представлены отомикозом и легочным аспергиллезом. Аллергические формы включают аллергический аспергиллезный синусит и аллергический бронхолегочный аспергиллез.
Все препараты, относящиеся к группе эхинокандинов (анидулафунгин, каспофунгин и микафунгин), изучены в клинических исследованиях с участием больных инвазивным аспергиллезом. Тем не менее только каспофунгин был одобрен для применения у пациентов с рефрактерной формой заболевания или непереносимостью других противогрибковых средств. В то же время в исследованиях in vitro доказана активность всех трех препаратов против большинства видов Aspergillus. Вместе с тем отсутствуют данные касательно сравнения этих агентов между собой.
M.A. Pfaller и соавт. провели уникальное прямое сравнительное исследование in vitro активности представителей класса эхинокандинов против разных видов Aspergillus (A. flavus, A. fumigatus, A. niger, A. terreus). В общей сложности было исследовано 526 клинических изолятов Aspergillus spp., полученных из различных источников, включая образцы мокроты, материал бронхоскопии и биопсии тканей.
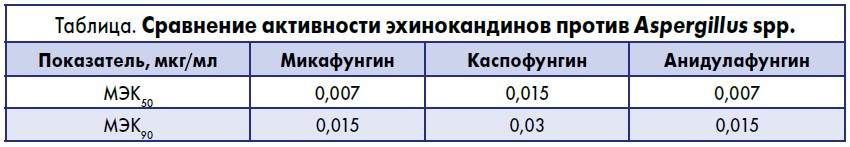
Методом микродилюции жидкой питательной среды (бульона) Института клинических и лабораторных стандартов (CLSI) определяли минимальную эффективную концентрацию (МЭК) препарата, при которой подавляется рост 50 и 90% микроорганизмов. В результате исследования была продемонстрирована высокая активность всех препаратов против грибов рода Aspergillus: от 99 до 100% изолятов были ингибированы при МЭК ≤0,06 мкг/мл. При сравнении значений МЭК каждого препарата было отмечено, что микафунгин и анидулафунгин более активны, чем каспофунгин (табл.).
Выводы
С учетом количества участников клинических исследований эффективности микафунгина можно сделать вывод о том, что указанный препарат не имеет себе равных среди доступных сегодня эхинокандинов по накопленному клиническому опыту. Три исследования охватывают в общей сложности более 1200 пациентов с кандидемией и составляют самую крупную базу данных по применению эхинокандинов в лечении этой и других форм инвазивного кандидоза. Кроме того, на основании анализа обширных данных, полученных при лечении почти 900 пациентов с ВИЧ-ассоциированным кандидозным эзофагитом, доказана эффективность и безопасность применения микафунгина у этой категории больных. В целом эти данные показывают, что микафунгин в рекомендованных дозах (100 мг/сут при кандидемии и 150 мг/сут при кандидозном эзофагите) у взрослых высокоэффективен, безопасен и способствует существенному снижению частоты осложнений и летальности при этих формах инфекции.
Результаты сравнения активности in vitro эхинокандинов в отношении Aspergillus spp. свидетельствуют о преимуществе микафунгина перед другими представителями этого класса притивогрибковых средств.
Подготовила Виктория Недвиженко
По материалам: P.G. Pappas. Micafungin for candidiasis. Mycoses. Vol. 55, Is. 1. Special Issue: Micafungin in Clinical Practice, 2012 и M. A. Pfaller, L. Boyken, R. J. Hollis et al. In Vitro Susceptibility of Clinical Isolates of Aspergillus spp. to Anidulafungin, Caspofungin, and Micafungin: a Head-to-Head Comparison Using the CLSI M38-A2 Broth Microdilution Method. Journal of clinical microbiology. 2009, Vol. 47, No. 10. Р. 3323-3325.