2 квітня, 2019
Современные мультидисциплинарные подходы в лечении гастроинтестинальных стромальных опухолей
 В структурном разнообразии неэпителиальных опухолей желудочно-кишечного тракта (ЖКТ) особую группу составляют гастроинтестинальные стромальные опухоли (gastrointestinal stromal tumors, GIST), обладающие индивидуальными гистологическими, иммуногистохимическими и молекулярно-генетическими признаками, а также особенностями клинического течения и прогноза. Отсутствие патогномоничных клинических проявлений GIST делает диагностику данных новообразований очень сложной задачей.
В структурном разнообразии неэпителиальных опухолей желудочно-кишечного тракта (ЖКТ) особую группу составляют гастроинтестинальные стромальные опухоли (gastrointestinal stromal tumors, GIST), обладающие индивидуальными гистологическими, иммуногистохимическими и молекулярно-генетическими признаками, а также особенностями клинического течения и прогноза. Отсутствие патогномоничных клинических проявлений GIST делает диагностику данных новообразований очень сложной задачей.
Актуальность проблемы
Термин GIST впервые был внедрен М.Т. Мazur и Н.В. Clark в 1983 г., когда они описали группу лейомиом и лейомиосарком, экспрессирующих маркеры, характерные для нейрогенных опухолей. До 85% гастроинтестинальных стромальных опухолей имеют мутации в гене KIT рецептора стволового фактора роста (экзоны 9, 11, 13, 17) и 3-18% – в гене PDGFRА (экзоны 12, 14, 18). В 10-15% случаев не выявляются мутации в генах KIT и PDGFRА – дикий тип, WT (Wild type). В 1998 г. японский ученый S. Hirota опубликовал результаты исследования, в котором было показано, что мутации в гене c-Kit с гиперэкспрессией тирозинкиназного рецептора KIT являлись ключевым событием при развитии гастроинтестинальных опухолей.
Частота встречаемости GIST составляет 10-20 случаев на 1 млн населения в год. Распространенность GIST одинакова в разных географических районах и этнических группах населения. Заболевание с одинаковой частотой встречается у мужчин и женщин. Наиболее часто GIST выявляется у пациентов старшей возрастной группы (55-60 лет), редко встречаясь у лиц моложе 40 лет. Гастроинтестинальные стромальные опухоли составляют 0,1-3% всех злокачественных новообразований ЖКТ, являясь при этом самыми частыми мезенхимальными опухолями вышеуказанной локализации. Чаще всего GIST локализуются в стенке желудка (60-70%), тонкой кишке (20-30%), реже – в толстой кишке (5%), пищеводе (<5%) и считаются потенциально злокачественными, а при диссеминации – безусловно злокачественными. В большинстве случаев метастазируют гематогенным путем – в печень и по брюшине, реже – в легкие и кости. Лимфогенный путь диссеминации менее характерен.
В связи с относительно благоприятным прогнозом при локализации опухоли в желудке все GIST разделены на две группы: желудочные и внежелудочные.
При стадировании заболевания должна использоваться система ТNM с последующей группировкой по стадиям (7-е изд., 2010). В окончательном гистологическом заключении указываются: размер опухоли, локализация, морфологический вид, митотический индекс. Иммуногистохимическое исследование опухоли с определением экспрессии CD117 и/или DOG1 является необходимым при подтверждении диагноза. Стадирование GIST также зависит и от митотического индекса опухоли. Митотический индекс для стромальных опухолей устанавливают по количеству митозов в 50 полях зрения (на общей площади 5 мм2) при большом увеличении микроскопа, используя объектив ×40. Низким митотическим индексом считается наличие не более 5 митозов в 50 полях зрения, высоким митотическим индексом – более 5 митозов. Помимо оценки митотического индекса значимыми прогностическими критериями являются наличие опухолевых клеток по линии резекции и разрыв капсулы опухоли. Наличие данных прогностических критериев оценивается как крайне неблагоприятные факторы прогноза, в основном для решения вопроса об использовании адъювантной терапии иматинибом.
Оптимальная тактика лечения пациентов с GIST представляет собой сложную проблему современной хирургической онкологии. Хирургическое лечение является основным методом лечения при GIST, которое может быть осуществлено путем применения открытых, лапароскопических и эндоскопических вмешательств либо с применением их комбинации, использование которых зависит от локализации, размеров и инвазии опухоли в соседние органы.
В 2000 г. в Хельсинки для лечения больного с метастатической формой GIST был впервые применен таргетный препарат иматиниб (Гливек), который избирательно блокирует передачу сигнала через рецептор гена c-Kit, что приводит к выраженному противоопухолевому эффекту.
Оптимальной для решения вопроса о применении адъювантной терапии иматинибом является схема, предложенная H. Joensuu в 2008 г. или M. Miettinen и J. Lasota. Риск прогрессирования по классификации H. Joensuu определяется характеристиками четырех основных прогностических факторов GIST: размера опухоли, митотического индекса, локализации и наличия разрыва капсулы опухоли.
Вместе с тем до сих пор не выработаны четкие алгоритмы хирургической тактики при GIST. Такие международные руководства, как ESMO и NCCN, представляют разнообразие тех или иных методик лечения, однако оптимальных критериев выбора не предлагают.
Целью данной работы является анализ результатов лечения больных с GIST.
Материалы и методы
Мы располагаем опытом лечения 10 больных, которые находились в клинике ГУ «Институт общей и неотложной хирургии им. В.Т. Зайцева НАМН Украины» в 2000-2018 гг. Женщин было 6, мужчин – 4. Возраст больных варьировал от 55 до 75 лет. Среди всех пациентов первичная локализация опухоли в желудке отмечена у 6 пациентов, в двенадцатиперстной кишке – у 2, в тонкой кишке – у 2. Размер опухоли варьировал от 1 до 25 см. Необходимо отметить, что один пациент был оперирован 4 раза по поводу диссеминации опухоли с локализацией метастазов в печени, забрюшинном пространстве и правой почке. Еще в одном наблюдении GIST была выявлена случайно при компьютерной томографии у пациентки с панкреонекрозом. Период наблюдения за пациентами составил от 2 до 120 мес.
Пациентам, поступающим в плановом порядке, в качестве предоперационной диагностики выполнялись стандартные лабораторные исследования, ультразвуковое и эндоскопическое исследования, спиральная компьютерная томография (СКТ), при необходимости – магнитно-резонансная томография (МРТ).
Все больные были оперированы открытым способом. Оперативные вмешательства разделили на две группы: радикальные – 9 больных и циторедуктивные – 1 пациент. Экономные резекции желудка были выполнены у 5 больных, гастрэктомия – у 1, резекция тонкой кишки с опухолью – у 2, иссечение опухоли двенадцатиперстной кишки с дуоденопластикой – у 2 пациентов. Лимфодиссекция не проводилась ввиду отсутствия видимых изменений регионарных лимфатических узлов по данным СКТ и интраоперационной ревизии, а также в связи с редкостью распространения GIST в регионарные лимфатические узлы.
После хирургического лечения 4 пациентам с высоким и промежуточным риском по H. Joensuu (2008) была проведена адъювантная терапия иматинибом. Осложнения в послеоперационном периоде развились у 2 больных. Летальный исход отмечен у 1 пациентки, у которой GIST сочетался с некротическим панкреатитом вследствие аррозивного кровотечения из панкреатических ветвей селезеночной артерии и вены на фоне тяжелой панкреатической инфекции через 45 дней после первичного хирургического вмешательства. Период наблюдения за пациентами составил от 2 до 120 мес; 7 пациентов наблюдались более 5 лет. При этом 5-летняя выживаемость составила 81%.
Необходимо отметить, что наличие GIST даже большого размера, а также диссеминация опухоли, в отличие от других злокачественных поражений ЖКТ, при агрессивном хирургическом подходе и адъювантной таргетной терапии позволяют рассчитывать на хорошие отдаленные результаты лечения, в связи с чем заслуживающими внимания представляются следующие клинические наблюдения.
Клинический случай 1
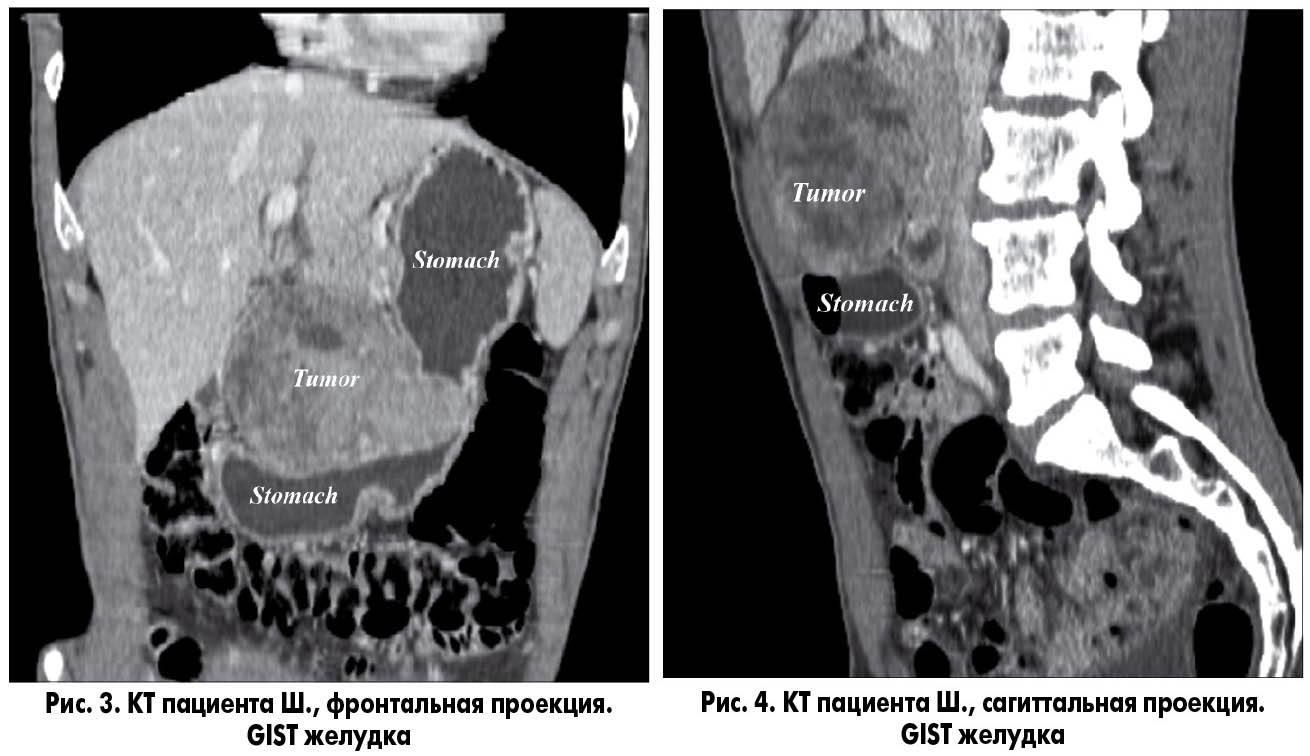
Пациент Ш., 53 лет, поступил в ГУ «Институт общей и неотложной хирургии им. В.Т. Зайцева НАМН Украины» с жалобами на тяжесть и периодическую боль в эпигастральной области, общую слабость, похудение на 5 кг за последние 6 мес. Из анамнеза известно, что пациент отметил появление вышеуказанных жалоб около полугода тому назад. За медицинской помощью в течение полугода не обращался. Для уточнения диагноза и возможного оперативного лечения обратился в клинику. Данные объективного исследования: правильного телосложения, удовлетворительного питания, дефицита массы тела нет. При эндоскопическом исследовании заподозрено наличие стромальной опухоли желудка. Взята биопсия: в одном из биоптатов выявлены фрагменты GIST. Для уточнения диагноза больному выполнена СКТ с контрастированием. По данным СКТ выявлено объемное образование желудка в области передней стенки тела и антрального отдела размерами 8,5×9×10 см, по виду напоминающее субсерозную GIST (рис. 1-4).
Лабораторные показатели – без существенных отклонений от нормы.
Произведена верхнесрединная лапаротомия, клиновидная резекция желудка с опухолью, гастропластика, дренирование брюшной полости. В послеоперационном периоде проводилось зондовое питание с 2-х по 5-е сутки, трансназальный зонд удален на 5-е сутки после операции. Послеоперационный период проходил без особенностей. Больной выписан на 8-е сутки после операции в удовлетворительном состоянии с рекомендациями по проведению дальнейшей адъювантной таргетной терапии иматинибом.
Клинический случай 2
Пациент Д., 67 лет. Впервые обратился в клинику в 2013 г. с жалобами на боль, тяжесть в правом подреберье, потерю массы тела, слабость. Из анамнеза известно, что в 1998 г. в одной из клиник г. Москвы перенес резекцию желудка по поводу GIST небольших размеров. Вышеуказанные жалобы беспокоят около 1 мес. Больному выполнена СКТ, по данным которой в правой доле печени, в сегментах 5-8, выявлено образование неоднородной структуры больших размеров, по структуре соответствующее GIST (рис. 5).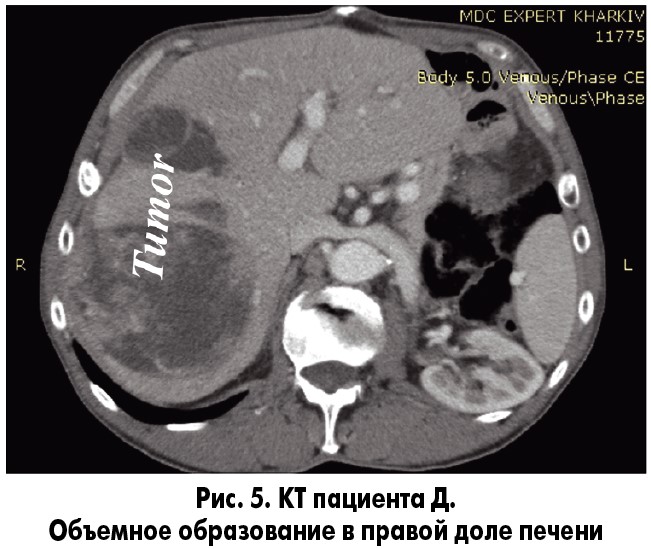
Клинико-лабораторные показатели в пределах нормы. С учетом данных анамнеза, дополнительных методов исследования больному установлен диагноз «метастаз GIST желудка в правую долю печени, состояние после резекции желудка с опухолью (1998 г.)». Больному выполнены лапаротомия, правосторонняя гемигепатэктомия, дренирование брюшной полости. Течение послеоперационного периода без осложнений. От проведения таргетной терапии отказался. Послеоперационное патоморфологическое, иммуногистохимическое исследование препарата подтвердило наличие метастаза GIST в правой доле печени.
При контрольном обследовании (2014 г.) по данным СКТ у пациента выявлено объемное образование 2-го сегмента печени на фоне значительной гипертрофии оставшейся левой доли. Ему выполнены лапаротомия, резекция 2-го сегмента печени с метастазом, дренирование брюшной полости. Послеоперационный период осложнился желчеистечением по дренажам брюшной полости, которое самостоятельно прекратилось на 10-е послеоперационные сутки.
Вновь обратился в клинику в марте 2018 г. с жалобами на боль в правой половине живота с иррадиацией в спину, слабость. Обследован. По данным КТ в забрюшинном пространстве справа определяется объемное образование до 12 см в наибольшем измерении с инвазией в диафрагму. Больному выполнены лапаротомия, удаление объемного образования справа с резекцией диафрагмы, дренирование забрюшинного пространства, брюшной полости, правой плевральной полости по Бюлау. Течение послеоперационного периода без осложнений. Пациент вновь отказался от таргетной терапии.
В декабре 2018 г. при скрининговом ультразвуковом исследовании выявлено образование в забрюшинном пространстве справа до 10 см в диаметре, инвазирующее в правую почку. Больному произведены лапаротомия, правосторонняя нефрэктомия с удалением забрюшинного опухолевидного образования. Выполнено дренирование брюшной полости, забрюшинного пространства. Течение послеоперационного периода без особенностей. Выписан под наблюдение онколога по месту жительства. Пациент согласился на проведение таргетной терапии иматинибом. Во всех случаях патоморфологическое и иммуногистохимическое исследование подтверждало GIST-характер удаленных опухолей. В настоящее время пациент находится под наблюдением. Данных в пользу пролонгации опухолевого процесса нет.
Данное клиническое наблюдение демонстрирует возможность успешного лечения пациентов с высоким риском прогрессирования GIST и длительную их выживаемость при агрессивном хирургическом подходе к лечению.
Клинический случай 3
Пациентка К., 62 лет, поступила в клинику с жалобами на боль в верхних отделах живота с иррадиацией в спину, тошноту, периодически – рвоту, повышение температуры тела до 38 °С, слабость.
Из анамнеза известно, что боль стала острой за 3 недели до поступления, после погрешности в диете. Также пациентка отмечает, что в течение года ее периодически беспокоила боль в правом подреберье, однако за медицинской помощью она не обращалась, лечилась по месту жительства по поводу острого панкреатита. В связи с нарастанием признаков эндогенной интоксикации больной произведена КТ, по данным которой у нее отмечаются признаки панкреонекроза с формированием острого некротического скопления сальниковой сумки, а также объемное образование на передней стенке антрального отдела желудка, по структуре соответствующее GIST, в связи с чем больная направлена в клинику Института.
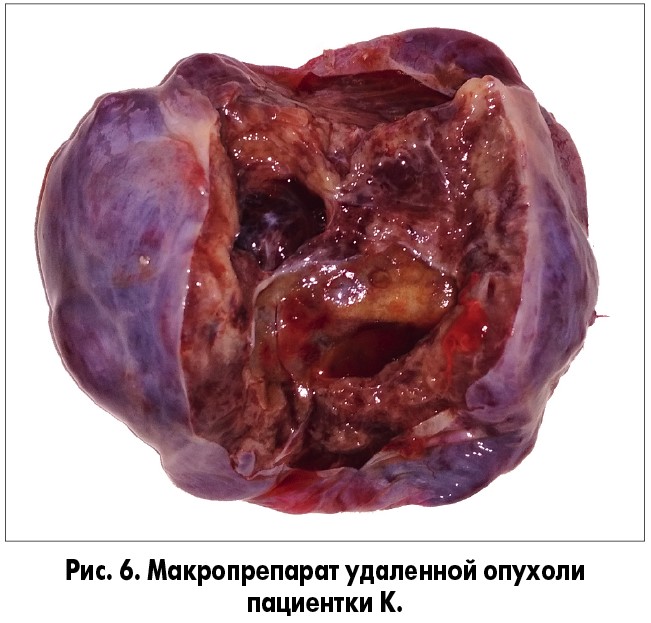 Обследована. Лабораторно обращало на себя внимание наличие лейкоцитоза со значительным нейтрофильным сдвигом. Больной установлен диагноз «GIST желудка T4N0M0. Панкреонекроз. Острое некротическое скопление сальниковой сумки. Синдром эндогенной интоксикации». В связи с признаками инфицирования острого некротического скопления больной выполнены лапаротомия, клиновидная резекция желудка с опухолью, гастропластика, вскрытие, санация и дренирование острого некротического скопления сальниковой сумки. При ревизии на передней стенке антрального отдела желудка выявлено объемное образование на ножке без признаков локального или отдаленного метастазирования. При макроскопическом исследовании удаленного препарата опухоль представляет собой кистозно-солидное образование до 18 см в наибольшем измерении, со слизистым и геморрагическим содержимым в кистах (рис. 6). Микроскопическое и иммуногистохимическое исследования показали GIST-характер удаленного образования.
Обследована. Лабораторно обращало на себя внимание наличие лейкоцитоза со значительным нейтрофильным сдвигом. Больной установлен диагноз «GIST желудка T4N0M0. Панкреонекроз. Острое некротическое скопление сальниковой сумки. Синдром эндогенной интоксикации». В связи с признаками инфицирования острого некротического скопления больной выполнены лапаротомия, клиновидная резекция желудка с опухолью, гастропластика, вскрытие, санация и дренирование острого некротического скопления сальниковой сумки. При ревизии на передней стенке антрального отдела желудка выявлено объемное образование на ножке без признаков локального или отдаленного метастазирования. При макроскопическом исследовании удаленного препарата опухоль представляет собой кистозно-солидное образование до 18 см в наибольшем измерении, со слизистым и геморрагическим содержимым в кистах (рис. 6). Микроскопическое и иммуногистохимическое исследования показали GIST-характер удаленного образования.
Течение послеоперационного периода тяжелое на фоне умеренно выраженных явлений эндогенной интоксикации. По дренажам из сальниковой сумки отмечалось длительное гноеистечение с примесью панкреатических секвестров. На 42-е сутки отмечены признаки аррозивного кровотечения, в связи с чем пациентке выполнена лапаротомия. При ревизии зона резекции желудка – без особенностей. После вскрытия сальниковой сумки и некрсеквестрэктомии выявлено субтотальное некротическое поражение поджелудочной железы. Источник кровотечения – панкреатические ветви селезеночных артерии и вены. Достигнут гемостаз. Пациентка скончалась на 3-и послеоперационные сутки (45-е сутки после первой операции) на фоне прогрессирования явлений полиорганной недостаточности.
Данное клиническое наблюдение демонстрирует возможность длительного бессимптомного существования GIST больших размеров, диагностика которых стала возможной в связи с развитием другого острого хирургического заболевания органов брюшной полости.
Результаты и их обсуждение
Диагностика и лечение GIST представляют собой сложную проблему, требующую тщательного планирования тактики лечения и правильного взаимодействия между онкологами, эндоскопистами и хирургами, что позволяет индивидуализировать выбор способа лечения.
Основное значение в выявлении GIST и их распространенности, а также в планировании лечения имеют инструментальные методы исследования, к которым относятся ультразвуковое исследование, СКТ, МРТ и эндоскопические исследования, включая эндоУЗИ.
Согласно рекомендациям ведущих онкологических сообществ (ESMO, NCCN, Canadian Advisory Committee on GISTs), диагноз GIST устанавливают на основании морфологического исследования биоптатов с обязательным проведением иммуногистохимического исследования. Также ESMO и NCCN рекомендуют обязательное удаление GIST размером ≥2 см, в то время как канадские эксперты считают, что все подозрительные на GIST опухоли должны быть удалены вне зависимости от их размеров, поскольку такие опухоли склонны к метастазированию.
Хирургический метод является основным в терапии GIST, он может быть применен путем открытых, лапароскопических и эндоскопических вмешательств либо их комбинаций, использование которых зависит от локализации, размеров и инвазии опухоли в соседние органы. Также данные факторы определяют степень резекции желудка в виде клиновидной резекции (Wedge-resection), резекции по Бильрот-I или Бильрот-II либо гастрэктомии. Основная цель хирургического лечения – радикальное удаление опухолевых очагов единым блоком с морфологически негативными краями резекции (R0). Большинство авторов не рекомендуют выполнять регионарную лимфаденэктомию, поскольку GIST редко распространяются в лимфатические узлы. Лимфодиссекция выполняется только при подозрении на метастазы в лимфатических узлах. Больным с GIST оправдано выполнение экономных резекций, с отступом от макроскопически видимого края опухоли не менее чем на 2 см.
В последние годы многочисленные клинические исследования посвящены сравнительному анализу роботизированных и лапароскопических и эндоскопических вмешательств при GIST желудочной локализации. M. Nakauchi и I. Uyama (2017) в своих работах указывают на наличие недостатков роботизированных резекций желудка в виде длительности оперативного вмешательства по сравнению с лапароскопическими вмешательствами.
На основе сравнительного анализа результатов хирургического лечения 406 больных с GIST желудка, проведенного в Корее за период с 1998 по 2012 г., которым были выполнены лапароскопические клиновидные резекции (у 38,4% пациентов) и открытые резекции (у 61,6%), была доказана эффективность лапароскопических вмешательств наряду с открытыми резекциями желудка. Численность рецидивов GIST составила 11 случаев (2,7%) в группе после открытых резекций желудка и ни одного рецидива – в группе после лапароскопических вмешательств. Средний размер опухоли составил 3,45 см в группе после лапароскопических вмешательств и 5,46 см после открытых резекций желудка соответственно. Данное исследование подтвердило возможность широкого использования лапароскопических вмешательств у больных с GIST.
Эндоскопические методы удаления (эндоскопические подслизистые диссекции, эндоскопические полнослойные резекции, подслизистые туннельные резекции) GIST желудка наряду с такими преимуществами, как снижение длительности пребывания в стационаре и минимизация стоимости вмешательства, имеют существенные недостатки, в частности возможность недостаточного радикализма вмешательства, риск перфорации и диссеминации.
T. Namikawa и соавт. (2015) была предложена новая миниинвазивная сочетанная методика оперативного вмешательства, так называемая лапароскопически-эндоскопическая (laparoscopic endoscopic cooperative surgery). Авторы доказали возможность использования этой методики при небольших размерах GIST желудка (<5 см), с результатами, аналогичными с лапароскопическими операциями (laparoscopic wedge resection).
Основным преимуществом предложенной T. Namikawa и соавт. (2017) методики является сокращение площади резекции стенки желудка по сравнению со стандартной лапароскопической клиновидной резекцией за счет использования линейного степлера. Авторы считают, что сочетанное использование эндоскопических и лапароскопических методик является альтернативой при неудачных попытках эндоскопической подслизистой диссекции GIST желудка.
В последние годы появились исследования, проведенные среди значительного количества пациентов с GIST, где показатель 5-летней выживаемости после хирургической резекции составил 83%.
На основании результатов исследований The American College of Surgeons Oncology Group, где оценивали показатель 5-летней выживаемости у 106 пациентов с высоким риском рецидива GIST желудка, которым наряду с R0- резекцией была проведена адъювантная терапия иматинибом по 400 мг/сут в течение 1 года, показатели 1-, 3- и 5-летней выживаемости составили 99, 97 и 83% соответственно. Таким образом, за последние годы диагностика, лечение и исход у пациентов с GIST претерпели значительные изменения благодаря открытию молекулярных механизмов, приводящих к развитию опухоли: активированные мутации KIT- и PDGFR-α-тирозиновой киназы. Эти открытия способствовали разработке ингибитора тирозиновой киназы – иматиниба, который показал существенное преимущество по срокам выживаемости пациентов.
Выводы
Лечение пациентов с GIST представляет собой сложную и окончательно не решенную проблему. Хирургический метод является основным в терапии данной патологии. Объем хирургического лечения зависит от локализации, размеров опухоли, наличия инвазии в соседние органы и метастазов. Агрессивный хирургический подход, даже при наличии метастатического поражения, оправдан в связи с особенностями молекулярной биологии таких опухолей, а также с их медленным ростом. Комбинированное лечение с применением адъювантной таргетной терапии позволяет добиться хороших результатов как общей, так и безрецидивной выживаемости больных.
Литература
- Bareck E., Ba-Ssalamah A., Brodowicz T. et al. Gastrointestinal stromal tumors: Diagnosis, therapy and follow-up care in Austria. Wien Med Wochenschr 2013; 163: 137-152.
- Bhalgami R., Manish K., Patil P. Clinicopathological study of 113 gastrointestinal stromal tumors. Indian J Gastroenterol 2013; 32: 1: 22-27.
- Blackstein M.E., Blay J.Y., Corless C. et al. Gastrointestinal stromal tumors: consensus statement on diagnosis and treatment. Can. J. Gastroenterol. 2006; 20: 157-163.
- Burkill G.J., Badran M., Al-Muderis O. et al. Malignant gastrointestinal stromal tumor: distribution, imaging feautures, and pattern of metastatic spread. Radiology. 2003; 226: 527-532.
- Casali P.G., Jost L., Reichardt P., Schlemmer M., Blay J.Y. ESMO Guidelines Working Group. Gastrointestinal stromal tumors: ESMO clinical recommendations for diagnosis, treatment and follow-up. Ann. Oncol. 2009; 20 (Suppl. 4): 64-67.
- DeMatteo R.P. et al. Two hundred gastrointestinal stromal tumors: recurrence patterns and prognostic factors for survival. Ann. Surg. 2000; 231: 51-58.
- DeMatteo R.P., Ballman K.V., Antonescu C.R. et al. Long-term results of adjuvant imatinib mesylate in localized, high-risk, primary gastrointestinal stromal tumor: ACOSOG Z9000 (Alliance) intergroup phase 2 trial. Ann Surg 2013; 258: 422-9.
- Demetri G.D., Antonescu C.R., DeMatteo R.P. et al. NCCN Task Force report: update on the management of patients with gastrointestinal stromal tumors J Natl Compr Netw 2010; 8 (2): 1-41.
- Demetri G.D., Benjamin R.S., Blanke C.D. et al. NCCN Task Forse report: managment of patients with gastrointestinal stromal tumors (GIST) – update of the NCCN clinical practice guidelines. J. Natl. Compr. Canc. Netw. 2007; 5 (Suppl. 2): 1-29.
- Eisenberg B.L., Judson I. Surgery and imatinib in the managment of GIST: emerging approaches to adjuvant and neoadjuvant therapy. Ann Surg Oncol 2004; 11: 465-475.
- Fletcher C.D., Berman J.J., Corless C. et al. Diagnosis of gastrointestinal stromal tumors: A consensus approach. Hum Pathol. 2002 May; 33 (5): 459-65.
- Gasali P.G., Blay J.Y., Bertuzzi A. et al. Gastrointestinal stromal tumors: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up Ann Oncol 2014; 25 (3): 21-26.
- Hassan I., You Y.N., Shyyan R. et al. Surgically managed gastrointestinal stromal tumors: a comparative and prognostic analysis. Ann. Surg. Oncol. 2008; 15: 52-59.
- Hirota S., Isozaki K., Moriyama Y., Hashimoto K., Nishida T., Ishiguro S. et al. Gain-of-function mutations of c-kit in human gastrointestinal stromal tumors. Science. 1998; 279 (5350): 577-580.
- Inoue H., Ikeda H., Hosoya T. et al. Submucosal endoscopic tumor resection for subepithelial tumors in the esophagus and cardia. Endoscopy 2012; 44: 225‑30.
- Joensuu H. Risk stratification of patients diagnosed with gastrointestinal stromal tumor. Human pathology. 2008; 39: 1411-1419.
- Joensuu H., Fletcher C., Dimitrijevic S., Silberman S., Roberts P., Demetri G. Management of malignant gastrointestinal stromal tumors. Lancet Oncol. 2002; 3 (11): 655-664.
- Joensuu H., Roberts P.J., Sarlomo-Rikala M., Andersson L.C., Tervahartiala P., Tuveson D. et al. Effect of the tyrosine kinase inhibitor ST1571 in a patient with a metastatic gastrointestinal stromal tumor. N. Engl. J. Med. 2001; 344: 1052-1056.
- Kim I.H., Kim I.H., Kwak S.G. et al. Gastrointestinal stromal tumors (GISTs) of the stomach: a multicenter, retrospective study of curatively resected gastric GISTs. Ann Surg Treat Res. 2014; 87: 298-303.
- Kurova N., Tanida N., Oonishi K. Significance of D2-40 expression in the diagnosis of gastrointestinal stromal tumor. Med Mol Morphol 2008; 41: 2: 109-112.
- Lasota J., Miettinen M. Clinical significance of oncogenic KIT And PDGFRA mutations in gastrointestinal stromal tumours. Histopathology. 2008; 53: 245‑266.
- Mazur M.T., Clark H.B. Gastric stromal tumors. Reapprasial of histogenesis. Am. J. Surg. Pathol. 1983; 7 (6): 507-519.
- Mietinen M., Majidi M., Lasota J. Pathology and diagnostic criteria of gastrointestinal stromal tumors (GISTs): a review. Eur. J. Cancer. 2002; 38: 39-51.
- Miettinen M., Lasota J. Gastrointestinal stromal tumors – definition, clinical, histological, immunohistochemical, and molecular genetic features and differential diagnosis. Virchows Arch. 2001; 438: 1-12.
- Nakauchi M., Uyama I., Suda K. et al. Robotic surgery for the upper gastrointestinal tract: Current status and future perspectives. Asian J Endosc Surg 2017; 10: 354-63.
- Namikawa T., Hanazaki K. Laparoscopic endoscopic cooperative surgery as a minimally invasive treatment for gastric submucosal tumor. World J Gastrointest Endosc 2015; 7: 1150-6.
- National Comprehensive Cancer Network. Clinical practice guidelines in oncology for soft tissue sarcoma. Version 2. Fort Washington, Pa: National Comprehensive Cancer Network; 2009.
- Nishida T., Hirota S. Biological and clinical review of stromal tumors in the gastrointestinal tract. Histol. Histopathol. 2000; 15: 1293-1301.
- Ntourakis D., Mavrogenis G. Cooperative laparoscopic endoscopic and hybrid laparoscopic surgery for upper gastrointestinal tumors: current status. World Journal of Gastroenterology. 2015; 21 (43): 1482-1497.
- Pidhorecky I., Cheney R.T., Kraybill W.G., Gibbs J.F. Gastrointestinal stromal tumors: current diagnosis, biologic behavior, and management. Ann. Surg. Oncol. 2000; 7: 705-712.
- Van Glabbeke M.M., Owzar K., Rankin C., Simes J., Crowley J. GIST Meta-Analysis Group (MetaGIST). Comparsion of 2 doses of imatinib for the treatment of unresrctable or metastatic gastrointestinal stromal tumors (GIST): a meta-analysis based on 1640 patients. J. Clin. Oncol. 2007; 25 (18, Suppl): abstr. 10004.
- Ye L.P., Zhang Y., Mao X.L. et al. Submucosal tunneling endoscopic resection for small upper gastrointestinal subepithelial tumors originating from the muscularis propria layer. Surg Endosc 2014; 28: 524-30.
- Архири П.П. Хирургическое лечение и факторы прогноза у больных стромальными опухолями желудочно-кишечного тракта: Автореф. дис. канд. мед. наук, 2010.
- Гастроинтестинальные стромальные опухоли (диагностика, лечение) / Практические рекомендации. – М., 2008. – 53 с.
- Карачун А.М., Орлова Р.В., Пелипась Ю.В. и др. Современные представления об особенностях хирургического лечения гастроинтестинальных стромальных опухолей. Клиническая больница 122, 2016, 16: 48-57.
- Стромальные опухоли желудочно-кишечного тракта (GIST); Клиническая монография. – Тверь: ООО «Издательство «Триада», 2006; 40 с.
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 1 (57), лютий 2019 р