2 квітня, 2019
44-й конгресс Европейской ассоциации трансплантации костного мозга
Обзор сессии, посвященной терапии лимфомы Ходжкина
 В марте 2018 года в Лиссабоне состоялся 44-й конгресс Европейского общества трансплантации костного мозга (EBMT). В этом самом авторитетном мировом форуме в данной области приняли участие более 4 тыс. клиницистов, иммунологов, фармацевтов, медицинских сестер, психологов, микробиологов и других специалистов со всех континентов. Отрывала программу конгресса сессия, посвященная лечению лимфомы Ходжкина.
В марте 2018 года в Лиссабоне состоялся 44-й конгресс Европейского общества трансплантации костного мозга (EBMT). В этом самом авторитетном мировом форуме в данной области приняли участие более 4 тыс. клиницистов, иммунологов, фармацевтов, медицинских сестер, психологов, микробиологов и других специалистов со всех континентов. Отрывала программу конгресса сессия, посвященная лечению лимфомы Ходжкина.
Участников сессии приветствовал президент ЕВМТ Мохамед Моти. Он кратко рассказал об истории изучения лимфомы Ходжкина. Первое упоминание о болезни, которую теперь мы знаем как лимфома Ходжкина, найдено в работе Мальпигия в 1666 году. Докладчик напомнил существующую классификацию лимфомы Ходжкина (ЛХ), привел статистические данные о ее распространенности на примере канцер-регистра США, где это заболевание регистрируется у 8500 пациентов в год и занимает 9-е место по частоте. Важной проблемой сегодня является оценка факторов риска развития ЛХ. Профессор Моти выделил три фактора: возраст, пол и связь с инфицированием вирусом Эпштейна – Барр (EBV).
ЛХ чаще развивается в возрасте 20 лет – 44 года (45,5% случаев), может возникать у пациентов старше 55 лет (29,7% случаев), является редким заболеванием у детей и подростков (10-15% случаев), а у детей в возрасте младше 5 лет встречается крайне редко. Мужчины болеют чаще женщин. Однако роль EBV в развитии ЛХ пока не ясна. Хотя инфицирование EBV и повышает риск развития заболевания, в целом риск очень невелик. EBV выявляют в клетках Рид – Штернберга у каждого третьего пациента.
 Мартин Хатчинс (Дания) выступил с докладом, посвященным оптимизации лечения пациентов с впервые выявленной ЛХ. Докладчик привел данные о результатах лечения больных с ЛХ поздних стадий, сравнив эффективность и токсичность схем ABVD и BEACOPPesc. Терапия в объеме 6 курсов ABVD позволяет излечить большую часть пациентов и характеризуется приемлемой токсичностью. Частота неудач терапии по этой схеме составляет 30‑35%; около половины этих пациентов могут быть излечены путем назначения противорецидивной высокодозовой химиотерапии (ВДХТ). Терапия по схеме ВЕАСОРРesc позволяет излечить большее количество пациентов. Однако такая терапия характеризуется более частыми ранними и отсроченными осложнениями (P. Borhmann, A. Engert, 2016).
Мартин Хатчинс (Дания) выступил с докладом, посвященным оптимизации лечения пациентов с впервые выявленной ЛХ. Докладчик привел данные о результатах лечения больных с ЛХ поздних стадий, сравнив эффективность и токсичность схем ABVD и BEACOPPesc. Терапия в объеме 6 курсов ABVD позволяет излечить большую часть пациентов и характеризуется приемлемой токсичностью. Частота неудач терапии по этой схеме составляет 30‑35%; около половины этих пациентов могут быть излечены путем назначения противорецидивной высокодозовой химиотерапии (ВДХТ). Терапия по схеме ВЕАСОРРesc позволяет излечить большее количество пациентов. Однако такая терапия характеризуется более частыми ранними и отсроченными осложнениями (P. Borhmann, A. Engert, 2016).
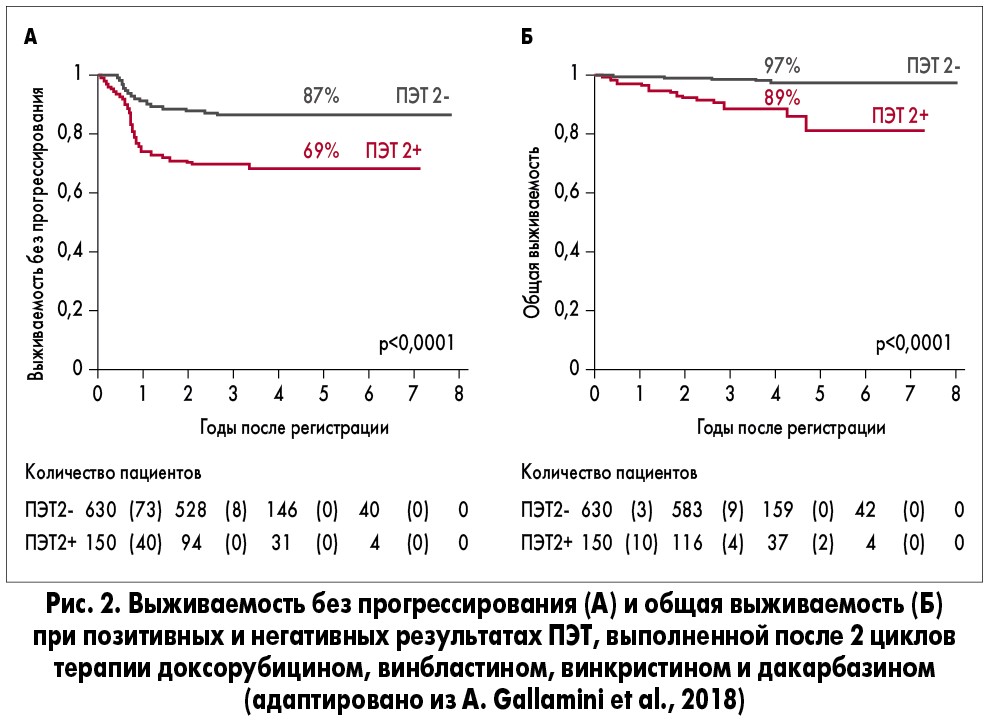
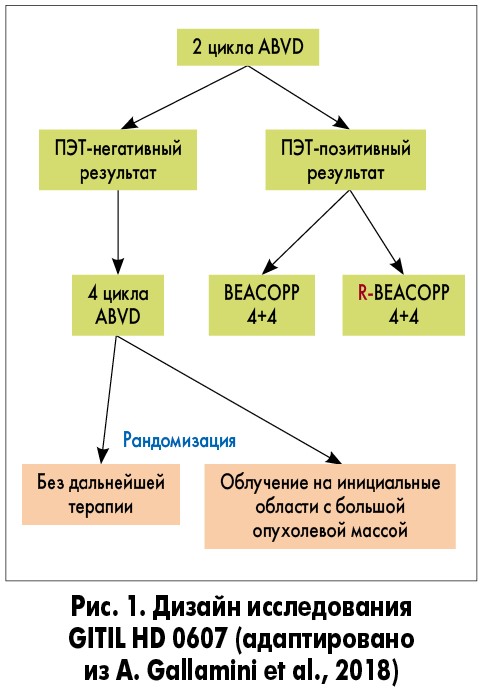
Докладчик сделал вывод, что при использовании схемы ABVD лечение около 1/3 пациентов недостаточное, а в случае применения схемы ВЕАСОРРesc около 2/3 пациентов получают избыточную терапию, ассоциированную с большей токсичностью. Для коррекции терапии сейчас активно изучается роль ранней оценки ответа с помощью позитронной эмиссионной томографии (ПЭТ). М. Хатчинс привел ряд исследований, в которых проводилась коррекция терапии после первых двух курсов на основании результатов ПЭТ. Так, в исследовании GITIL HD 0607 ответ оценивался после двух курсов лечения по схеме ABVD у пациентов с ЛХ IIВ-IV стадии (n=782). При ПЭТ-негативном статусе пациенты продолжали лечение по той же схеме, получив еще 4 курса. При ПЭТ-позитивных результатах схему меняли на ВЕАСОРР или R-ВЕАСОРР (рис. 1). В группе пациентов с ПЭТ-негативным статусом общая выживаемость и выживаемость без прогрессирования заболевания были статистически значимо выше, чем при ПЭТ-позитивном статусе, и составили 97 и 87% против 89 и 69% соответственно (рис. 2; A. Gallamini et al., 2018).
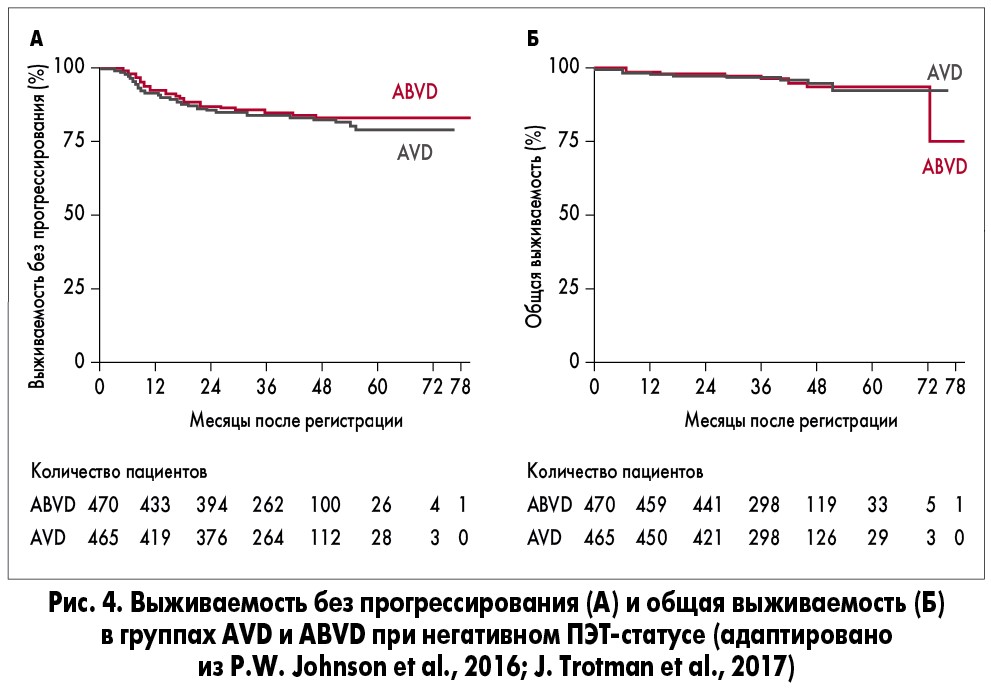
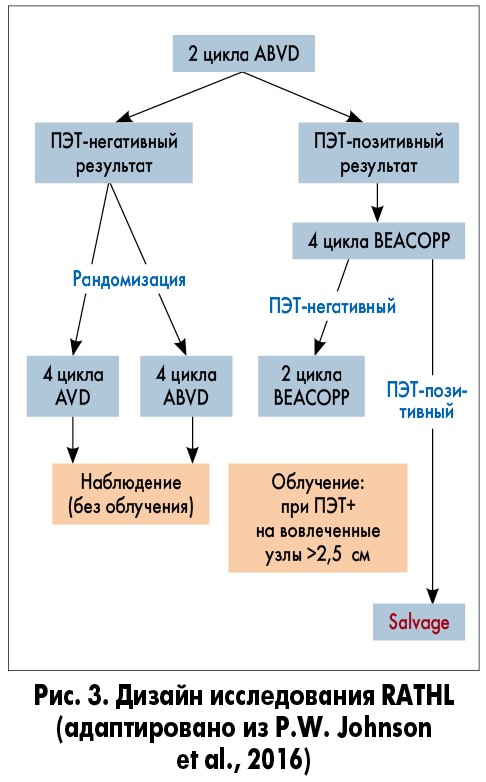 В исследовании RATHL 1202 пациента после проведения двух кусов лечения по схеме ABVD продолжали терапию в зависимости от результатов ПЭТ. Пациентов с ПЭТ-негативным статусом рандомизировали в группы ABVD (4 курса) и AVD (4 курса). При ПЭТ-позитивном статусе пациентам назначали ВЕАСОРР (4 курса), при ПЭТ-негативном статусе – еще два аналогичных курса, при сохраняющемся ПЭТ-позитивном статусе – переводили на сальвадж-терапию (рис. 3). При сравнении групп ABVD и AVD было отмечено существенное снижение легочной токсичности при минимальном влиянии на общую выживаемость и выживаемость без прогрессирования (рис. 4; P.W. Johnson et al., 2016; J. Trotman et al., 2017).
В исследовании RATHL 1202 пациента после проведения двух кусов лечения по схеме ABVD продолжали терапию в зависимости от результатов ПЭТ. Пациентов с ПЭТ-негативным статусом рандомизировали в группы ABVD (4 курса) и AVD (4 курса). При ПЭТ-позитивном статусе пациентам назначали ВЕАСОРР (4 курса), при ПЭТ-негативном статусе – еще два аналогичных курса, при сохраняющемся ПЭТ-позитивном статусе – переводили на сальвадж-терапию (рис. 3). При сравнении групп ABVD и AVD было отмечено существенное снижение легочной токсичности при минимальном влиянии на общую выживаемость и выживаемость без прогрессирования (рис. 4; P.W. Johnson et al., 2016; J. Trotman et al., 2017).
Говоря о роли консолидации путем проведения лучевой терапии, докладчик привел данные двух исследований – GHSG HD15 и BCCA, в которых пациенты проходили терапию по схемам ВЕАСОРР и ABVD соответственно. Были сделаны выводы, что большая опухолевая масса не влияет на выживаемость без прогрессирования у пациентов с ПЭТ-негативным статусом в случае отсутствия лучевой терапии (A. Engert et al., 2012; K.J. Savage et al., 2011).
Далее были представлены исследования, в которых изучали значение брентуксимаба ведотина (БВ) в первой линии терапии у пациентов пожилого возраста. Лечение больных старше 60 лет, которые составляют 15-35% от всех пациентов с ЛХ, имеет ряд проблем. Пятилетняя выживаемость без прогрессирования составляет 40-50%, общая выживаемость – 50-60%. Схема терапии АBVD используется часто, но не является стандартной. Смертность, связанная с легочной токсичностью, ассоциированной с введением блеомицина, составляет 18%. Смертность, ассоциированная с терапией, составляет 9% в сравнении с 0,3% у пациентов моложе 60 лет (D. Jagadeesh et al., 2013). Начато исследование GHSG B-CAP, в котором пациенты старше 60 лет в зависимости от статуса согласно шкале CIRS-G получают терапию по схеме B-CAP (БВ, циклофосфамид, доксорубицин, преднизолон) в группе go-go или монотерапию БВ в группе slow-go (ClinicalNrails.gov. N: NCT02191930).
 В ряде других исследований будет изучено применение ниволумаба у пациентов с впервые диагностированной ЛХ (R. Ramchandren et al., 2017; MSKCC Protocol 16-1536, 2018). Данные подходы находятся в разработке и не утверждены к применению в Украине.
В ряде других исследований будет изучено применение ниволумаба у пациентов с впервые диагностированной ЛХ (R. Ramchandren et al., 2017; MSKCC Protocol 16-1536, 2018). Данные подходы находятся в разработке и не утверждены к применению в Украине.
Далее Мохаммед Моти представил клинический опыт лечения пациентов с ЛХ по данным разных исследовательских групп. Так, зафиксировано повышение общей выживаемости с 1944 по 2004 год. Что касается роли ВДХТ, то обеспечиваемая этим лечением 3-летняя выживаемость без прогрессирования составляет 59%. Докладчик рассказал о риске повышения кардиоваскулярной токсичности и развития вторичных опухолей у пациентов с ЛХ после терапии и представил соответствующие клинические случаи.
Доклад профессора Андреа Галламини (Франция) был посвящен оптимизации лечения пациентов с рецидивом и рефрактерной ЛХ (Р/РЛХ). Для оценки предполагаемой эффективности терапии, в частности результатов ВДХТ, разработан ряд прогностических систем. Шкала RisPACT включает в себя следующие факторы риска: IV стадия, время до развития рецидива менее 3 мес, статус ECOG >1, опухоль >5 см и отсутствие как минимум частичного ответа на сальвадж-терапию. Пятилетняя общая выживаемость колеблется от 88% при 0 баллов до 47% при 3-5 баллах по указанной системе оценки риска (рис. 5; P.J. Brockelmann et al., 2017).
 Докладчик представил результаты метаанализа исследований, в которых изучалось значение ПЭТ в оценке ответа на сальвадж-терапию. Характеризуя новые опции для улучшения терапии пациентов с Р/РЛХ, профессор А. Галламини показал значение терапии анти-CD30-антителами и ингибиторами контрольных точек, а также важность оценки метаболического объема опухоли при ПЭТ (L.S. Poulou et al., 2010).
Докладчик представил результаты метаанализа исследований, в которых изучалось значение ПЭТ в оценке ответа на сальвадж-терапию. Характеризуя новые опции для улучшения терапии пациентов с Р/РЛХ, профессор А. Галламини показал значение терапии анти-CD30-антителами и ингибиторами контрольных точек, а также важность оценки метаболического объема опухоли при ПЭТ (L.S. Poulou et al., 2010).
В исследовании, проведенном A. Younes (2012), пациенты, у которых не был достигнут ответ на ВДХТ, получали БВ в дозе 1,8 мг/кг массы тела каждые 3 недели, максимально до 16 введений (n=102). Общий ответ на лечение составил 75%, при этом полный ответ зафиксирован у 34% пациентов (A. Younes et al., 2012).
В исследовании AETHERA (n=329) изучалась эффективность применения БВ в качестве консолидации после ВДХТ. В исследование включались пациенты группы высокого риска рецидива ЛХ, у которых была проведена ВДХТ с аутотрансплантацией стволовых клеток костного мозга. В группу риска входили пациенты с рефрактерностью к первой линии терапии, а также с рецидивом заболевания в течение 12 мес после первой линии терапии или рецидивом с экстранодальным поражением. Первое введение БВ осуществлялось на 30‑45‑й день после аутотрансплантации стволовых клеток. Медиана выживаемости без прогрессирования в группе БВ и плацебо составила соответственно 42,9 и 24,1 мес. Таким образом, консолидация БВ после ВДХТ с последующей аутотрансплантацией стволовых клеток костного мозга у пациентов группы высокого риска улучшает результаты терапии и снижает вероятность наступления события на 43% (рис. 6; C.H. Moskowitz et al., 2015).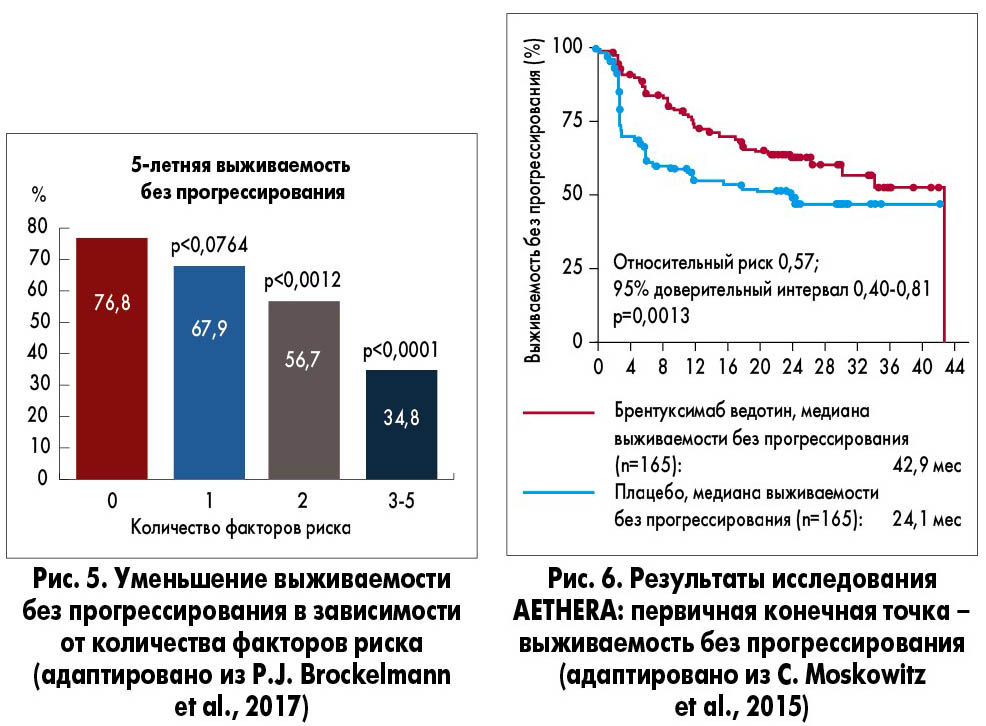
В завершение сессии состоялась интерактивная дискуссия между докладчиками и участниками.
Фото автора и с сайта https://www.ebmt.org/
Статья печатается при поддержке ООО «Такеда Украина».
UA/ADC/0219/0013
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 1 (57), лютий 2019 р