24 квітня, 2019
Инъекционная терапия сахарного диабета 2 типа: улучшение контроля гликемии, простота и безопасность
21-22 февраля в Киеве, под патронатом ГУ «Институт эндокринологии и обмена веществ им. В.П. Комиссаренко НАМН Украины» (г. Киев) (далее – Институт), в рамках ежегодного образовательного проекта «Школа эндокринолога» состоялась научно-практическая конференция. Основная часть прозвучавших здесь докладов была посвящена диагностике и лечению сахарного диабета (СД).
Темой одной из наиболее интересных секций, в которой принимали участие ведущие специалисты Института, стала инъекционная терапия СД 2 типа.
 Открыла работу секции заведующая отделением возрастной эндокринологии и клинической фармакологии Института, доктор медицинских наук Олеся Вадимовна Зиныч, которая в своем выступлении рассказала о необходимости индивидуализации сахароснижающей терапии в зависимости от коморбидной патологии.
Открыла работу секции заведующая отделением возрастной эндокринологии и клинической фармакологии Института, доктор медицинских наук Олеся Вадимовна Зиныч, которая в своем выступлении рассказала о необходимости индивидуализации сахароснижающей терапии в зависимости от коморбидной патологии.
– Выбор идеального препарата для конкретного пациента с СД 2 типа не всегда очевиден, несмотря на наличие шаблонов и пошаговых алгоритмов. Возьмем, например, агонисты рецепторов глюкагоноподобного пептида-1 (арГПП-1) и глифлозины, применяемые в лечении пациентов с превалирующими атеросклеротическими изменениями. Обе группы препаратов снижают общую смертность от сердечно-сосудистых заболеваний (ССЗ), причем глифлозины даже в большей степени, чем инкретиномиметики. Но при анализе причин смертности становится понятно, что эти лекарственные средства обладают разным протекторным эффектом. Например, риски смерти от нефатального инфаркта снижаются в равной степени в обеих группах препаратов. Но на риски смерти от нефатального инсульта глифлозины не оказывают существенного влияния. Кроме того, они потенциально повышают риски ампутации конечностей, что уже было доказано в многочисленных исследованиях. Поэтому целесообразность назначения глифлозинов пациентам с атеросклеротическим поражением периферических сосудов сомнительна.
В последнее время все чаще поднимается тема мультифокального атеросклероза, когда поражается несколько сосудистых областей. Так, по результатам международного исследования AGATA, у 25% пациентов с ишемической болезнью сердца (ИБС) выявляется атеросклеротическое поражение ≥2 фокусов – у 1/3 это дополнительно цереброваскулярные сосуды, а у 1/5 – периферические. И в этой ситуации возникает вопрос – какие препараты назначить: с изолированным протекторным действием только на коронарные сосуды или те, что защищают несколько локусов? Тем более учитывая тот факт, что пациенты с ИБС крайне редко дополнительно обследуются на предмет выявления атеросклеротического поражения других сосудистых бассейнов.
У пациентов с СД 2 типа и сердечной недостаточностью (СН) более предпочтительны глифлозины благодаря их кардиопротекторному действию, однако первопричина СН – это ИБС, метаболические нарушения и почечная недостаточность, поэтому, вероятно, более оправданна ее своевременная профилактика. Кроме этого, по данным Европейского общества кардиологов (ESC), частота СН у пациентов с СД 2 типа составляет 12%, из которых старше 70 лет – 16% мужчин и 22% женщин. А у этой категории больных эффективность и безопасность глифлозинов, потенциально ухудшающих клубочковую фильтрацию, которая снижается с возрастом, – весьма спорны. Также возникает вопрос: будут ли одинаково эффективны эти препараты при разной степени выраженности СН, ведь чем выше класс, тем хуже клубочковая фильтрация.
Очень важным критерием выбора препарата для лечения СД 2 типа является его безопасность с точки зрения развития гипогликемии. И хотя механизм действия арГПП-1 на сегодня достаточно хорошо изучен, было осуществлено крупное исследование с целью оценки рисков гипогликемии на фоне действия этих препаратов. У здоровых добровольцев был проведен гиперинсулинемический гипогликемический клэмп, результаты которого позволили сделать 3 важных вывода.
- Лираглутид (Виктоза®) стимулировал секрецию инсулина только тогда, когда уровень глюкозы в крови превышал 4,3 ммоль/л.
- Подавление секреции глюкагона на фоне приема арГПП-1 происходило только в состоянии эугликемии, т.е. >3,7 ммоль/л.
- арГПП-1 не нарушали общую контррегуляцию гипогликемии и не подавляли высвобождение катехоламинов, кортизола и глюкагона.
Другое исследование, которое оценивало секрецию инсулина на фоне введения арГПП-1 в зависимости от глюкозы крови, показало, что при уровне гликемии 2,8 ммоль/л не происходило выработки инсулина, но при 6,6 ммоль/л его секреция повышалась и продолжала нарастать даже при гликемии 16,7 ммоль/л.
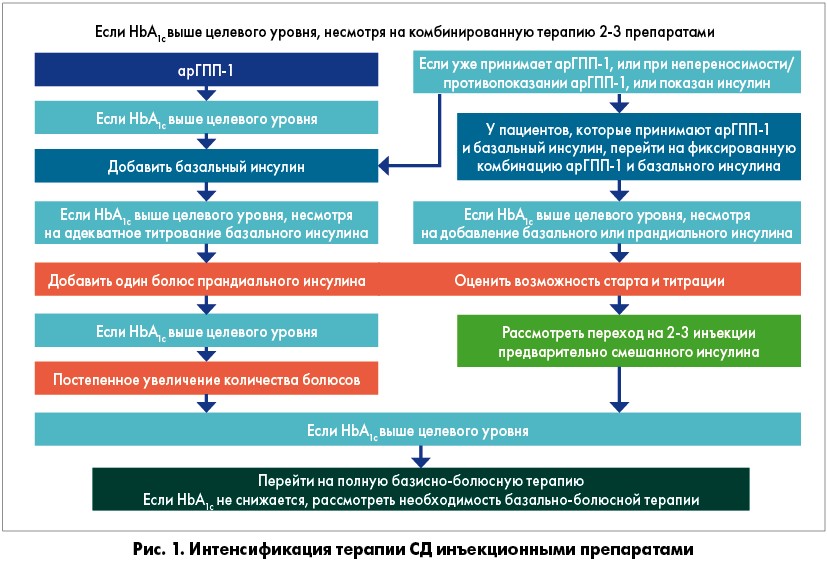
Рано или поздно у пациентов с СД 2 типа возникает необходимость перевода их с пероральных сахароснижающих препаратов (ПССП) на инсулинотерапию. Но сегодня, благодаря арГПП-1, есть возможность отсрочить этот момент. Согласно новым клиническим рекомендациям (октябрь, 2018) по интенсификации инсулинотерапии СД, перед переводом на базальный инсулин в случае неэффективности 2-3 ПССП должны быть назначены арГПП-1. На базальный инсулин переводят декомпенсированных пациентов или больных, не ответивших на терапию арГПП-1 (рис. 1).
Косвенным подтверждением перспективности применения арГПП-1 является большое количество исследований по этой группе препаратов. Например, в настоящее время продолжается исследование по применению лираглутида у пациентов с ожирением. В то время как по глифлозинам не отмечается такой тенденции.
Тем не менее, несмотря на все преимущества арГПП-1, они также могут оказаться неэффективными, поэтому перед их назначением имеет смысл оценить сохранность функциональной активности β-клеток поджелудочной железы. Маркерами их активности являются С-пептид и антитела к β-клеткам. Низкий уровень С-пептида и наличие антител – это предикторы недостаточной эффективности арГПП-1.
Таким образом, при существующих сегодня возможностях терапии СД выбор должен быть основан на клинических рекомендациях, но с обязательным учетом индивидуальных особенностей пациента и коморбидности.
 Тему персонификации лечения СД 2 типа продолжила в своем докладе старший научный сотрудник научно-консультативного отдела амбулаторно-профилактической помощи больным с эндокринной патологией Института, кандидат медицинских наук Светлана Викторовна Болгарская, уделив большое внимание рискам гипогликемии и поддержанию стабильного уровня глюкозы крови в течение дня.
Тему персонификации лечения СД 2 типа продолжила в своем докладе старший научный сотрудник научно-консультативного отдела амбулаторно-профилактической помощи больным с эндокринной патологией Института, кандидат медицинских наук Светлана Викторовна Болгарская, уделив большое внимание рискам гипогликемии и поддержанию стабильного уровня глюкозы крови в течение дня.
– Подход к выбору терапии СД должен быть индивидуальным, с учетом возможных побочных эффектов того или иного препарата у конкретного пациента.
При необходимости перевода больного на базальный инсулин основной фокус выбора должен быть направлен на безопасность – низкий риск гипогликемии. Наиболее предпочтительными с этой точки зрения являются инсулины деглюдек (представлен на отечественном рынке препаратом Тресиба® от компании Novo Nordisk А/S, Дания) и гларгин 300 ЕД. По данным различных исследований, эти инсулины показали наименьший риск гипогликемии в сравнении с аналогами инсулина 1-го поколения – детемир и гларгин 100 ЕД, не говоря уже об инсулине НПХ [нейтральный протамин Хагедорна], который Американская диабетическая ассоциация (ADA) не рекомендует применять у пациентов с СД 2 типа. Чтобы выбрать из наиболее предпочтительных лучший инсулин, необходимо сравнить их фармакокинетику, определить продолжительность действия, эффективность и профиль активности в течение суток по результатам исследований высокого качества.
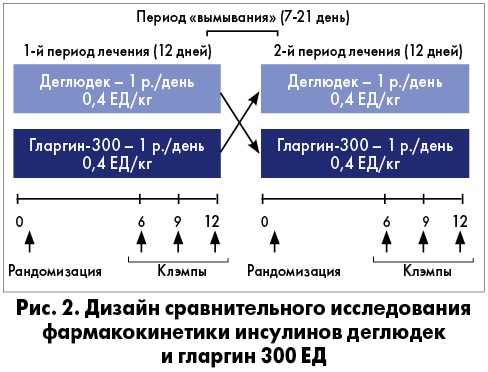 Одно из таких исследований (двойное слепое перекрестное) было проведено с участием 60 пациентов с СД 1 типа, рандомизированных на 2 группы. 1-й группе был назначен инсулин Тресиба® в первой части исследования с последующим переводом на инсулин гларгин 300 ЕД, а во 2-й группе, наоборот, пациентам вначале назначали гларгин 300 ЕД с последующим переводом на инсулин Тресиба® (рис. 2).
Одно из таких исследований (двойное слепое перекрестное) было проведено с участием 60 пациентов с СД 1 типа, рандомизированных на 2 группы. 1-й группе был назначен инсулин Тресиба® в первой части исследования с последующим переводом на инсулин гларгин 300 ЕД, а во 2-й группе, наоборот, пациентам вначале назначали гларгин 300 ЕД с последующим переводом на инсулин Тресиба® (рис. 2).
Целевыми точками исследования были: вариабельность гликемии у одного пациента, вариабельность гликемии в течение суток и общий гипогликемический эффект.
Было подтверждено, что деглюдек имеет более прогнозируемое и стабильное действие по сравнению с инсулином гларгин 300 ЕД, который продемонстрировал значительные колебания гликемии в промежутке 8-18 ч после введения. Вариабельность сахароснижающего эффекта инсулина деглюдек в течение суток оказалась на 40% ниже, чем у гларгина 300 ЕД, а у каждого отдельного пациента это выражается более стабильным уровнем гликемии в течение дня.
Дополнительно было обнаружено, что гипогликемический эффект инсулина Тресиба® на 30% выше, чем у гларгина 300 ЕД.
Важно, что результаты исследования фармакокинетики подтверждаются данными реальной клинической практики. В качестве иллюстрации можно привести пример одного из самых крупных сравнительных исследований CONFIRM, в ходе которого проводился ретроспективный анализ эффективности инсулина деглюдек и гларгина 300 ЕД у 4056 пациентов с СД 2 типа, ранее не получавших инсулин. Участники были отобраны из самой большой базы данных США, охватывающей все уровни медицинской помощи за последние 10 лет и включающей порядка 15% населения страны. Рандомизация была программной и идеальной – пациенты не отличались по возрасту, сопутствующей патологии, индексу массы тела и многим другим параметрам.
Целевыми точками были: эффективность; частота всех гипогликемий; количество пациентов, перенесших ≥1 эпизод гипогликемии; количество пациентов, отказавшихся от использования инсулина по тем или иным причинам.
Были получены такие результаты:
- Спустя 6 мес применения деглюдек продемонстрировал достоверно большее снижение уровня гликированного гемоглобина (HbA1c) по сравнению с гларгином 300 ЕД.
- Риск развития гипогликемии у пациентов, получавших деглюдек, снизился на 30% в сравнении с таковым у пациентов из группы гларгина 300 ЕД, а риск развития хотя бы одного эпизода гипогликемии – на 25%.
- Приверженность к инсулину деглюдек оказалась значимо выше, отказавшихся от его применения пациентов было на 27% меньше.
- Доза инсулина деглюдек, обеспечивающая лучший контроль гликемии, была на 9,3% ниже, чем у инсулина гларгин 300 ЕД.
Додолнительно безопасность применения инсулина деглюдек была доказана в исследовании DEVOTE с участием 7637 пациентов. В этом исследовании принимали участие пациенты с СД 2 типа, у которых имелись сопутствующие ССЗ. У этой тяжелой группы пациентов, при применении инсулина деглюдек:
- на 53% снизился риск ночной тяжелой гипогликемии;
- на 40% снизился риск тяжелой гликемии;
- на 27% меньше пациентов перенесли тяжелую гипогликемию.
Итак, согласно фармакологическим характеристикам, результатам многочисленных исследований и данным реальной клинической практики, применение инсулина Тресиба® более эффективно и безопасно по сравнению с инсулином гларгин 300 ЕД.
 Завершающим в работе секции стало выступление руководителя научно-консультативного отдела амбулаторно-профилактической помощи больным с эндокринной патологией Института, кандидата медицинских наук Валерии Леонидовны Орленко, которая представила инновационный инсулин Райзодег® ФлексТач® (компания Novo Nordisk А/S, Дания), значительно расширяющий возможности врача и пациента.
Завершающим в работе секции стало выступление руководителя научно-консультативного отдела амбулаторно-профилактической помощи больным с эндокринной патологией Института, кандидата медицинских наук Валерии Леонидовны Орленко, которая представила инновационный инсулин Райзодег® ФлексТач® (компания Novo Nordisk А/S, Дания), значительно расширяющий возможности врача и пациента.
– Часть больных, нуждающихся в инсулинотерапии, требует одновременной коррекции тощаковой и прандиальной гипергликемии. Но добавление прандиального инсулина к болюсному всегда ухудшает приверженность к терапии и усложняет ее. Многим пациентам и врачам известны «микст-инсулины», позволяющие сократить количество инъекций, однако они требуют четкого расчета пика действия и перекусов, чтобы избежать риска гипогликемии.
Сегодня в нашем распоряжении впервые появился базальный и болюсный инсулин в одной шприц-ручке – Райзодег®. Он сочетает в себе преимущества пролонгированного инсулина деглюдек (70%) и давно известного инсулина аспарт (30%). То есть это наиболее физиологичная комбинация из всех возможных. Этот инсулин объединил преимущество двух инсулинов – базального инсулина деглюдек и прандиального инсулина аспарт.
Деглюдек: действие >42 ч, низкий риск гипогликемии, вводится в удобное для пациента время (с минимальным интервалом в 8 ч и максимальным – 42 ч), разрешен у детей от 1 года, имеет опыт применения во всем мире >6 лет.
Аспарт – продолжительность действия в 2 раза быстрее и короче, чем у человеческого инсулина, меньше риск гипогликемии, введение – до, во время или после приема пищи, международный опыт применения – почти 20 лет.
Необходимость проведения базально-болюсной (Б-Б) терапии у пациентов с СД 2 типа продиктована наличием прандиальной гипергликемии, которая является следствием нарушения 1-й фазы секреции инсулина. А она, в свою очередь, не восстанавливается многими другими препаратами/инсулинами и является независимым фактором риска ССЗ. Кроме этого, отсутствие 1-й фазы секреции инсулина приводит к гиперглюкагонемии, глюконеогенезу, глюкогенолизу.
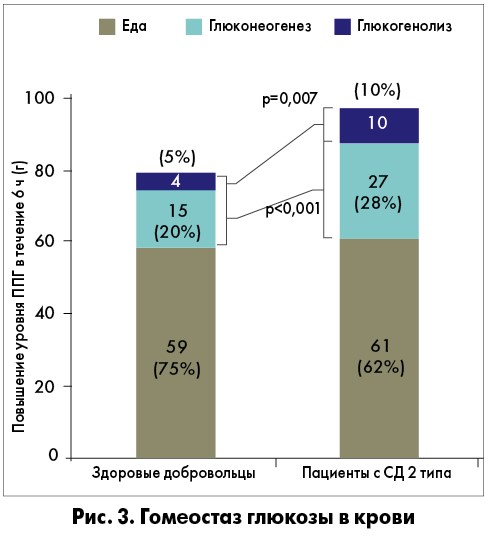 В отличие от здоровых людей у больных СД 2 типа вдвое увеличиваются глюконеогенез и глюкогенолиз (рис. 3). И именно это обстоятельство в большей степени, чем углеводная нагрузка, служит фактором, влияющим на повышение уровня постпрандиальной гликемии (ППГ). Вследствие потери 1-й фазы постпрандиальной секреции инсулина не подавляется продукция глюкагона. Поэтому независимо от употребления экзогенных углеводов продолжается образование эндогенной глюкозы (глюкогенез, глюконеогенез и гликолиз) с развитием выраженной ППГ, которая влияет на интегральные показатели компенсации.
В отличие от здоровых людей у больных СД 2 типа вдвое увеличиваются глюконеогенез и глюкогенолиз (рис. 3). И именно это обстоятельство в большей степени, чем углеводная нагрузка, служит фактором, влияющим на повышение уровня постпрандиальной гликемии (ППГ). Вследствие потери 1-й фазы постпрандиальной секреции инсулина не подавляется продукция глюкагона. Поэтому независимо от употребления экзогенных углеводов продолжается образование эндогенной глюкозы (глюкогенез, глюконеогенез и гликолиз) с развитием выраженной ППГ, которая влияет на интегральные показатели компенсации.
В исследовании DECODE, включившем >25 тыс пациентов с СД 2 типа, сравнивалась роль показателей гликемии натощак и 2-часовой ППГ в качестве предикторов смертности. В процессе исследования были получены уникальные данные, показавшие, что отсутствие контроля уровня ППГ (>8 ммоль/л) вдвое повышает риск сердечно-сосудистой смертности.
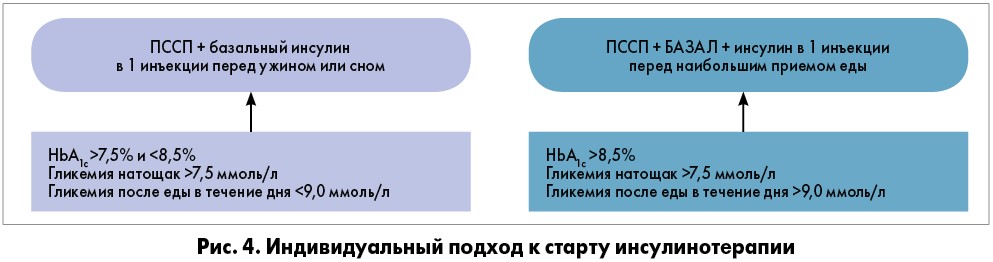
Доказано, что пациенты, контролирующие прандиальную гликемию с помощью болюсного инсулина, чаще достигают эффективного контроля HbA1c – 94 против 64%. Поэтому при целевых значениях гликемии натощак, но сохранении высоких показателей HbA1c следует оценить ППГ и использовать БАЗАЛ + инсулин перед наибольшим приемом углеводной пищи (рис. 4). Причем подстраивать прием еды под введение инсулина необязательно; напротив, время инъекции может быть изменено в зависимости от времени наибольшего приема пищи. При большей углеводной нагрузке – 2, а не 1 раз в день, суточная доза инсулина Райзодег® может быть разделена на 2 инъекции с интервалом не менее 4 ч (с учетом длительности действия инсулина аспарт).
Таким образом, выбор инсулина Райзодег® в качестве старта инсулинотерапии обеспечивает целый ряд преимуществ:
- одновременный контроль гликемии натощак и после приема пищи;
- простота применения – введение перед наибольшим приемом пищи;
- безопасность – снижение риска ночных эпизодов гипогликемии;
- более длительный контроль диабета с применением одного препарата.
Недостаточная эффективность базального инсулина требует добавления 1 болюса перед самым большим приемом пищи или перехода на 2 инъекции комбинированного инсулина (рекомендации ADA/EASD). Реализовать этот подход можно просто назначив БАЗАЛ + инсулин Райзодег®.
Важно отметить, что перевод с базального, двухфазного инсулинов или с Б-Б терапии на Райзодег® прост и безопасен – используются те же суточные дозы, даже если до этого не были достигнуты целевые значения гликемии, потому что чувствительность к деглюдеку в составе Райзодег® выше, чем к гларгину 300 ЕД.
Титруется доза инсулина Райзодег® 1 раз в неделю согласно среднему значению трехкратного определения глюкозы натощак. Если целевые значения гликемии не были достигнуты, добавляют 2 ЕД, при показателях ниже целевых доза снижается на 2 ЕД. Хлебные единицы не подсчитывают.
Преимущества перевода на инсулин Райзодег®:
- Улучшение контроля гликемии независимо от предыдущего режима инсулинотерапии.
- Простота применения – меньшее количество инъекций.
- Безопасность:
- снижение риска ночных гипогликемий;
- невозможность перепутать препараты инсулина.
- Достижение рекомендованного контроля диабета с меньшей дозой инсулина.
Инновационный инсулин Райзодег® значительно расширяет возможности старта и интенсификации инсулинотерапии, делает ее более удобной и эффективной.
Таким образом, сегодня есть все основания утверждать, что современная терапия СД позволяет сделать оптимальный выбор для каждого конкретного пациента, повысить его комплаенс к лечению и свести к минимуму риски.
Подготовила Ирина Чумак
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 1 (45) березень 2019 р.