25 квітня, 2019
Ішемічна хвороба серця та еозинофільний гранулематоз із поліангіїтом
Ішемічна хвороба серця (ІХС) займає провідне місце серед причин втрати працездатності та смертності у світі, особливо в економічно розвинених країнах. Так, за даними Американської асоціації серця (AHA) та Американської асоціації інсульту (ASA), ІХС є головною причиною смертності серед усіх серцево-судинних захворювань (ССЗ) у 43,8% випадків, інсульт – 16,8%, серцева недостатність (СН) – 9,0%, артеріальна гіпертензія (АГ) – 9,4% та інші ССЗ – 17,9%. ІХС призводить до 1 із 7 смертей у США [57]. Як відомо, основною причиною розвитку ІХС, зокрема гострого коронарного синдрому (ГКС), є атеросклероз коронарних артерій (КА). До інших рідших факторів, що зумовлюють розвиток ГКС, відносять коронароспазм, емболію, спонтанну дисекцію КА, системні васкуліти (СВ), зловживання кокаїном, травми, компресію КА міокардіальними містками тощо [132]. Ураження КА при ревматичних хворобах – провідна причина фатальних ускладнень, таких як інфаркт міокарда (ІМ), раптова серцева смерть, хронічна СН [2]. Коронарит є однією з рідкісних причин ІХС при СВ, системних захворюваннях сполучної тканини, ревматоїдному артриті та інших захворюваннях [2, 40, 58, 99, 109, 121, 141].
Серед первинних СВ ураження серця, зокрема КА, спостерігається і при еозинофільному гранулематозі з поліангіїтом (ЕГПА). Раніше це захворювання називали синдромом Черджа – Стросс, але 2012 р. було узгоджене поняття ЕГПА [64]. Ураження серця є поширеним при ЕГПА, являє собою несприятливий прогностичний чинник та потребує агресивнішої терапії [106, 135]. Раннє виявлення та своєчасне лікування порушення функції серцево-судинної системи (ССС) при ЕГПА важливі для запобігання подальшого ураження органів і систем, зокрема розвитку ІХС [28], що покращує прогноз таких хворих [30, 46, 100]. Складність діагностики цього захворювання полягає у мультисистемності порушень. Часто на ранніх стадіях відмічають неспецифічні симптоми, а також може спостерігатися асимптомний перебіг ураження ССС [13, 30, 65, 126]. Окрім того, ЕГПА може маскуватися під інші хвороби, такі як бронхіальна астма (БА), риніт, поліноз та ін. [99, 106, 123, 135].
Згідно з Міжнародною поєднавчою конференцією щодо номенклатури СВ (Чапел-Гілл, США, 2012), ЕГПА – еозинофільне й некротизуюче гранулематозне запалення респіраторного тракту та некротизуючий васкуліт дрібних і середніх судин, що асоціюється із БА та еозинофілією. Антинейтрофільні цитоплазматичні антитіла (АНЦА) частіше виявляють за наявності гломерулонефриту [64].
Епідеміологія
Щорічна захворюваність на ЕГПА складає 0,5-6,8 нових випадків на 1 млн населення, а поширеність – 10,7-14 випадків на 1 млн населення [81, 87, 142]. Середній вік пацієнтів становить 35-54 роки; хоча ця патологія може проявлятися у діапазоні від 7 до 74 років [8, 51, 115, 139] без гендерних відмінностей [92, 139], деякі дослідження виявили незначне переважання захворюваності серед осіб чоловічої статі [44].
Етіопатогенез
Етіопатогенез ЕГПА до кінця не з’ясований. Тригерними чинниками можуть бути алергени, інфекції, вакцинація, медикаменти [44, 78] та генетичні фактори [136]. Застосування деяких препаратів асоційоване з розвитком ЕГПА, серед яких антагоністи рецепторів лейкотрієну (монтелукаст, використання якого підвищує ризик ЕГПА у 4,5 рази) [55] та анти-IgE-моноклональні антитіла (омалізумаб) [101]. Слід підкреслити, що у пацієнтів з ЕГПА спостерігається висока поширеність HLADRB1, HLADRB4 [81]. Провідне значення для розвитку ЕГПА мають еозинофільна інфільтрація тканин і органів та АНЦА-опосередковане пошкодження ендотелію [4], хоча роль останніх у патогенезі ЕГПА до кінця не з’ясовано [6]. Вважається, що у АНЦА-негативних випадках ЕГПА активовані еозинофіли є основним фактором пошкодження тканин [123]. Еозинофільна інфільтрація міокарда з вивільненням токсичних медіаторів запалення, таких як еозинофільний катіонний і великий основний білок, еозинофільний нейротоксин та еозинофільна пероксидаза, є причиною пошкодження кардіоміоцитів [8, 107]. Гранулематозна еозинофільна інфільтрація міокарда та васкуліт КА зумовлюють ураження серця, що може призводити до розвитку застійної СН, ІХС і фатальних аритмій [33, 107]. Підтвердженням провідного значення еозинофілів при порушенні функції серця порівняно з АНЦА є те, що за даними гістологічного дослідження виявляють значну інфільтрацію еозинофілами серця [93]. Еозинофіл-опосередковане ураження серця може перебігати у трьох стадіях, як-то гостра некротична, проміжна тромботична і кінцева фіброзна [105].
У разі АНЦА-позитивного варіанта ЕГПА нейтрофіли відіграють основну роль у пошкодженні органів [135]. Існує декілька досліджень in vivo та in vitro, які доводять патогенетичне значення АНЦА для активації нейтрофілів, що веде до пошкодження ендотелію, некротизуючого васкуліту, і, зрештою, розвитку ішемії уражених органів [38]. Окрім того, є дані щодо важливості імунної системи для виникнення ЕГПА [4, 46, 51, 81]. Відзначено підвищення активності Тh1-, Th2-клітин, гіперпродукцію цитокінів, таких як інтерлейкіни (ІЛ) 3, 4, 5, 6, 9, 13, фактора некрозу пухлини α (ФНП-α), гранулоцитарно-колонієстимулювального фактора та хемокіну [46, 51], а також зменшення продукції ІЛ‑10 [6]. У деяких пацієнтів з ЕГПА виявляють гіпергаммаглобулінемію та позитивний ревматоїдний фактор, що може вказувати на роль гуморального імунітету в розвитку захворювання [6].
Основні гістопатологічні дані при ЕГПА [47]:
- еозинофільна інфільтрація тканин;
- великі ділянки некрозу;
- еозинофільний васкуліт;
- інтерстиційні/екстраваскулярні некротизуючі гранульоми.
Стратифікація ризику
У 2011 р. французька група з вивчення васкулітів (FVSG) переглянула п’ятифакторну шкалу (FFS) для проведення стратифікації ризику в осіб з ЕГПА. Згідно з цією шкалою чотири фактори ризику (ФР), а саме вік >65 років, ураження серця, шлунково-кишкового тракту (ШКТ), такі як кровотеча, інфаркт чи панкреатит, і підвищення креатиніну в крові >150 мкмоль/л (кожний із цих ФР оцінюється в 1 бал), пов’язують із несприятливим прогнозом, тоді як п’ятий ФР (ураження ЛОР-органів) асоціюється із кращим прогнозом (мінус 1 бал) [52]. Пацієнти без ФР (FFS=0) мають кращі показники виживаності порівняно з хворими із наявними ФР (FFS≥1), які відносяться до групи високого ризику [46]. Призначення цитостатиків рекомендоване пацієнтам групи високого ризику (FFS≥1) [48].
Клінічний перебіг
Клінічний перебіг ЕГПА характеризується трьома стадіями, які не завжди можна розрізнити [6, 31, 97]:
- Продромальна фаза відзначається наявністю алергічного риніту, синуситу та/або БА і може тривати місяці чи роки.
- Еозинофільна фаза, якій притаманна еозинофілія в периферичній крові та еозинофільна інфільтрація багатьох органів, зазвичай легенів.
- Васкулітна фаза проявляється неспецифічними конституційними симптомами та ознаками ураження декількох органів і може мати загрозливі для життя наслідки. Характерні ураження шкіри, периферичних нервів, ШКТ і серця [115]. Типовими клінічними ознаками ЕГПА є БА, синусити, транзиторні легеневі інфільтрати, периферична нейропатія, ураження шкіри тощо [13, 49, 71, 116, 124, 125, 139].
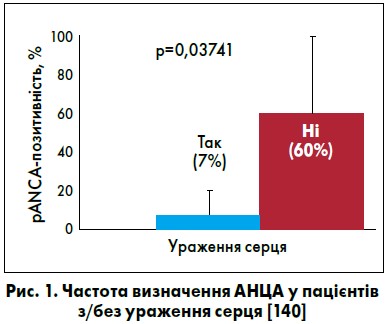 Ураження серця при ЕГПА відзначають достатньо часто: у 16-90% хворих (табл. 1) [13, 22, 30, 90, 116, 118, 126], яке є поширенішим у AНЦА-негативних пацієнтів (рис. 1) [13, 22, 45, 90, 108] та асоційоване зі значною еозинофілією [22, 30, 90, 109] й активністю захворювання [74]. За результатами роботи T. Neumann et al., усі особи з порушенням функції серця були АНЦА-негативними (р<0,05) [90], однак ці дані не підтверджені результатами іншого дослідження F. Moosig et al. [88]. Патологію серця зазвичай відзначають у еозинофільній та васкулітній стадіях хвороби [135]. Проте є відомості, що ураження серця може бути як раннім проявом ЕГПА, так і спостерігатися на пізніх стадіях захворювання [16, 125].
Ураження серця при ЕГПА відзначають достатньо часто: у 16-90% хворих (табл. 1) [13, 22, 30, 90, 116, 118, 126], яке є поширенішим у AНЦА-негативних пацієнтів (рис. 1) [13, 22, 45, 90, 108] та асоційоване зі значною еозинофілією [22, 30, 90, 109] й активністю захворювання [74]. За результатами роботи T. Neumann et al., усі особи з порушенням функції серця були АНЦА-негативними (р<0,05) [90], однак ці дані не підтверджені результатами іншого дослідження F. Moosig et al. [88]. Патологію серця зазвичай відзначають у еозинофільній та васкулітній стадіях хвороби [135]. Проте є відомості, що ураження серця може бути як раннім проявом ЕГПА, так і спостерігатися на пізніх стадіях захворювання [16, 125].
Ураження серця пов’язане з розвитком коронариту [8, 43]. Це може призводити до васкуліт-опосередкованої ішемії міокарда внаслідок пошкодження дрібних артерій міокарда та епікардіальних КА, значної інфільтрації еозинофілами та їхньою пошкоджувальною дією на тканини, дегрануляцією еозинофілів із виділенням білків, які чинять токсичний вплив на клітини з розвитком фіброзу та формуванням позасудинних гранульом [1, 8, 58, 90, 95, 113, 139, 140].
Залучення у патологічний процес ССС при ЕГПА асоціюється з несприятливим прогнозом і є провідною причиною захворюваності та смертності [45, 46, 50, 56, 88, 90, 92, 108, 116]. Це підтверджують дані досліджень, за якими патологія ССС є причиною смерті приблизно у 50% випадків ЕГПА [13, 29, 45, 50, 105, 109, 118, 135]. За результатами роботи G.C. Kane et al., ураження серця при ЕГПА асоціювалося з жіночою статтю, молодшим віком, значною периферичною еозинофілією та нижчою поширеністю АНЦА [67]. Пошкодження серця може характеризуватися як незначними змінами із мінімальними клінічними проявами, так і загрозливими для життя кардіоваскулярними подіями (зокрема, розвитком кардіогенного шоку внаслідок ГКС чи раптової смерті) [11, 111, 137]. Основними причинами летальних наслідків при ЕГПА були ІМ, СН, злоякісні шлуночкові аритмії та/або тампонада серця [10, 23]. За даними інших досліджень, захворюваність і смертність при ЕГПА переважно зумовлені міокардитом і коронаритом [50, 92], а приблизно у 50% випадків ці стани є причиною смерті внаслідок гіподіагностики [58].
Серцеві прояви при ЕГПА [118]
- Васкуліт епікардіальних артерій
- Васкуліт дрібних інтраміокардіальних судин (артеріол, капілярів і венул)
- Гранулематозна інфільтрація міокарда
- Еозинофільний міокардит
- Міокардіальний фіброз
- Ендоміокардіальний фіброз правого шлуночка
- Внутрішньопорожнинні тромби правого та/чи лівого шлуночка
- Рестриктивна кардіоміопатія
- Дилатаційна кардіоміопатія
- Недостатність мітрального клапана внаслідок дисфункції папілярних м’язів
- Гострий перикардит
- Тампонада серця
- Констриктивний перикардит
- Надшлуночкові та шлуночкові порушення ритму серця
- Атріовентрикулярні та внутрішньошлуночкові порушення провідності серця
- Раптова серцева смерть
При ЕГПА у патологічний процес можуть залучатися всі структури серця, зокрема епікардіальні та інтраміокардіальні судини, міокард, ендокард, перикард [13, 50, 53, 72, 92, 102, 108, 118, 125, 126, 140, 141].
Необхідно відзначити, що діагностика ураження ССС утруднена у зв’язку з частою відсутністю симптомів [13, 30, 65, 126]. Так, субклінічний перебіг патології серця при ЕГПА виявлений у 90% пацієнтів з ЕГПА у стадії клінічної ремісії з використанням мультимодального скринінгу – 24-годинного холтерівського моніторингу електрокардіограми (ЕКГ), ЕКГ-стрес-тесту, трансторакальної ехокардіографії (ЕхоКГ) та магнітно-резонансної томографії (МРТ) серця, що характеризувалося не тільки фіброзом, але й запаленням (за даними МРТ серця з пізнім підсиленням гадолінієм) [126]. ЕКГ-стрес-тест (у пацієнтів із незміненими епікардіальними КА за даними КГ) був позитивним у 20% хворих на ЕГПА, в яких спостерігався підвищений рівень еозинофілів. Зміни на ЕКГ при проведенні ЕКГ-стрес-тесту в осіб з ЕГПА, ймовірно, пояснюються інфільтрацією малих судин міокарда еозинофілами та/або васкулітом КА. Більш того, дослідники виявили, що вищий ступінь еозинофілії периферичної крові (до початку лікування) асоціювався з більшою поширеністю порушень ритму серця і зворотно корелював зі зниженням фракції викиду (ФВ) лівого шлуночка (ЛШ) (r=-0,65) [126]. За результатами роботи R.M. Dennert et al., клінічні симптоми, що свідчать про ураження серця, спостерігали у 26% пацієнтів, зміни на ЕКГ – у 66% та за даними ЕхоКГ – у 50%, МРТ – у 62% хворих на ЕГПА. Окрім того, патологію ССС за відсутності ознак чи змін на ЕКГ може бути виявлено у 38% осіб з ЕГПА за допомогою ЕхоКГ та МРТ серця [30]. У зв’язку з тим, що відсутність симптомів чи змін на ЕКГ у пацієнтів з ЕГПА не виключає ураження ССС, діагностика повинна охоплювати не тільки анамнез, фізикальне обстеження та реєстрацію ЕКГ, а й проведення ЕхоКГ чи МРТ серця [30, 65]. Результати роботи R.M. Dennert et al. також демонструють високу поширеність патології серця у хворих на ЕГПА. Систематична оцінка ССС, включно з методами обстеження із візуалізацією, необхідна для виявлення ураження серця, що підтверджують дані дослідження, проведеного A.F. Cereda et al. [30]. Так, у пацієнтів з ЕГПА у стадії клінічної ремісії порушення функції серця виявляли у 9-54,5% випадків: у 18,1% діагностували фібриляцію передсердь, перикардит – у 45,4%, кардіоміопатію із СН – у 27,2%, кардіогенний шок – у 9%, ІМ з елевацією сегмента ST – у 18,1% [16].
Автори дослідження P.R. Ames et al. дійшли висновку, що ЕГПА слід розглядати як захворювання з підвищеним ризиком тромбоутворення, який, можливо, пов’язаний із тромбогенним потенціалом еозинофілів на тлі пошкодження судин. Виникненню гіперкоагуляції при ЕГПА можуть сприяти складові еозинофільних гранул, окрім того, АНЦА іноді ушкоджують ендотелій із розвитком його проадгезивних та протромботичних властивостей [5]. За результатами цієї роботи, у пацієнтів з ЕГПА поширеність артеріального тромбозу складала 3,1-18,7%, венозного – 5,8-30% [5]. Згідно з даними літератури, при ЕГПА спостерігають утворення внутрішньоcерцевих тромбів [10, 68], тромбоз судин головного мозку [10], мезентеріальних артерій [94], вен нижніх кінцівок, тромбоемболію легеневої артерії тощо [86].
Атеросклероз і ЕГПА
При СВ відзначено прискорений і передчасний розвиток атеросклерозу [96]. Механізми виникнення атеросклерозу, асоціаційованого із СВ, включають атерогенний ефект традиційних серцево-судинних ФР, який потенційно посилюється у разі терапії глюкокортикоїдами (ГК), системного запалення [104]. Відомо, що лікування ГК може сприяти появі дисфункції серця внаслідок прискореного розвитку атеросклерозу та ІХС, а також підвищення частоти виникнення цукрового діабету й АГ [30]. Однак є дані, що системне запалення та імунні порушення можуть пришвидшувати ровиток атеросклерозу при ревматичних захворюваннях, зокрема СВ, незалежно від наявності класичних ФР ССЗ [27, 96], а також, ймовірно, терапії ГК [96].
Хронічне системне запалення при СВ може відігравати роль у розвитку раннього атеросклерозу як наслідок впливу C-реактивного білка (CРБ), деяких молекул адгезії та/або цитокінів, а також локального запалення, можливо, через локально секретований ФНП-α та/або дизрегуляції матричних металопротеїназ і оксидантного стресу. Окрім того, у пацієнтів із СВ виявлені ендотеліальна дисфункція та підвищена артеріальна жорсткість. На відміну від АНЦА, наявність яких не корелює з високим ризиком розвитку атеросклерозу або серцево-судинних подій, у патологічному процесі можуть брати участь автоантитіла до ендотеліальних клітин, білка теплового шоку або окислені ліпопротеїди низької щільності [96].
У літературі є дані, що при ЕГПА спостерігається підвищений ризик атеросклерозу. В дослідженні Grani C. et al. у хворого на ЕГПА виявлений стенозувальний атеросклероз КА з розвитком ІМ. Автори зазначають суперечливість опублікованих відомостей: хоча у пацієнта мало місце атеросклеротичне ураження КА, неясно, чи ІМ розвинувся внаслідок атеросклерозу чи поєднання васкуліту КА й атеросклерозу [44]. Згідно з даними ще одного дослідження, атеросклероз КА (стеноз >70%) виявлений у 15% осіб з ЕГПА за результатами коронарографії (КГ) [30]. Відомий випадок стенозу КА внаслідок атеросклеротичного ураження першої діагональної гілки лівої КА і спазму правої КА (ПКА). У роботі Р. Ungprasert et al. описано, як у 72-річного пацієнта зі встановленим діагнозом ЕГПА при проведенні КГ спостерігався атеросклероз трьох КА (проксимального відділу передньої міжшлуночкової артерії [ПМША], огинаючої КА та ПКА). У хворого наявні традиційні ФР ІХС, які включали чоловічу стать, вік, АГ і дисліпідемію. Пацієнту виконане аортокоронарне шунтування (АКШ) [135]. У дослідженні N. Kakouros et al. при проведенні КГ виявлені мінімальні зміни КА [66]. За даними патологоанатомічного дослідження, атеросклеротичні зміни (з виключно імунозапальними ураженнями судинної стінки) в одній чи більше магістральних артеріях мали місце у 57,1% випадків, однак слід відмітити дуже малу вибірку (n=4) [3]. Згідно з результатами мультиспіральної комп’ютерної томографії (КТ), рівень кальцієвого індексу, що відповідав помірному ризику розвитку ІХС, відмічали у 37,5% пацієнтів, а високому – у 25%. При проведенні перфузійної сцинтіграфії міокарда з технецієм‑99 у 48% осіб з ЕГПА діагностували переважно вогнищевий тип порушення перфузії міокарда, який відповідав зонам гіпокінезу за даними ЕхоКГ. У жінок з ЕГПА рівень загального холестерину позитивно корелював із розвитком серцево-судинних ускладнень (r=0,378; p<0,05) [3]. Однак є відомості щодо відсутності атеросклеротичного ураження КА у пацієнтів з ЕГПА, в яких відзначали розвиток ГКС [7, 42, 74, 106, 121, 130, 141].
Коронарит
Ураження КА може бути дифузним та небезпечним для життя станом [14]. Слід відмітити, що коронарит виявлений у 60% випадків ЕГПА за даними автопсій [17], однак прижиттєво діагностується рідко [58]. Стенокардія та ІМ є нечастими формами пошкодження ССС при ЕГПА [51, 73, 80, 130, 141], незважаючи на високу частоту розвитку коронариту [51], який може проявлятися у вигляді вазоспастичної стенокардії [35, 40, 99, 123, 140] та ГКС [15, 70, 74, 75, 122, 140, 141]. У літературі описано, що ураження КА спостерігається переважно у другій [135] і третій (стадія системного васкуліту) стадіях ЕГПА [29, 105]. У патологічний процес при ЕГПА можуть залучатися міокардіальні судини малого діаметра й епікардіальні КА, що нерідко призводять до ішемії міокарда, формуванню ектазій і аневризм КА внаслідок еозинофільної інфільтрації і прямої цитотоксичної дії еозинофільних білків.
Незважаючи на те що васкуліт є одним із основних механізмів ураження ССС, обструктивні зміни епікардіальних КА за даними КГ бувають відсутні, що може свідчити про переважне залучення у патологічний процес судин малого діаметра [139]. Часто це призводить до ішемії міокарда, пов’язаної з їхнім ураженням [118], що підтверджують дані, за якими зазвичай при ЕГПА спостерігають васкуліт дрібних артерій, рідко – середніх КА [34], а значуще пошкодження епікардіальних КА є рідкісним [68]. За результатами роботи K.W. Doo et al., васкуліт, ектазії та аневризми КА виявляються нечасто, оскільки при ЕГПА до патологічного процесу переважно залучаються дрібні артерії та рідко – середні [34]. Ураження епікардіальних КА при СВ, яке спостерігають із різною частотою залежно від СВ та досліджуваної групи пацієнтів, може проявлятися у вигляді різного ступеня стенозу, вазоспазму, тромбозу, дисекції, розвитку ектазій чи аневризм [30, 34, 95]. Так, у літературі описані випадки пошкодження КА великого діаметра при ЕГПА [35, 58, 74].
Коронарна хвороба серця значно частіше зустрічається в АНЦА-негативних пацієнтів і є провідною причиною смертності при ЕГПА [71, 108]. В осіб з ідіопатичним гіпереозинофільним синдромом та ЕГПА ураження серця спостерігали у вигляді стенокардії, ІМ, СН, раптової серцевої смерті. ЕГПА – не єдине захворювання, що може призводити до коронарної патології. Інші ревматичні хвороби також супроводжуються коронаритом і призводять до коронароспазму та/або тромбозу [18, 41]. Вважають, що системне запалення відіграє провідну роль у пошкодженні ендотелію, є основним чинником тромбозу КА і супроводжується активацією прозапальних цитокінів [39].
Коронароспазм
Серед інших проявів ураження ССС у пацієнтів з ЕГПА є коронароспазм, але як початковий вияв захворювання останній є надзвичайно рідкісним станом [24]. Цей прояв ЕГПА може спричиняти тотальну чи субтотальну оклюзію КА і призводити до стенокардії, ГКС, кардіогенного шоку та раптової серцевої смерті [26, 62]. Вищевказані серцево-судинні події спостерігають частіше в активній фазі хвороби, яка характеризується виразною еозинофілією, БА, парасинуситом, периферійною невропатією, інфільтратами в легенях та ураженням ШКТ [26, 100]. Слід відзначити, що коронарит при ЕГПА частіше асоціюється із коронароспазмом (артерій малого і середнього діаметра), ніж із коронаротромбозом [11, 42].
Необхідно відмітити, що куріння, порушення обміну електролітів (калію або магнію), вживання кокаїну, холод, гіпервентиляція та резистентність до інсуліну можуть сприяти розвитку коронароспазму [99] і бути причиною ендотеліальної дисфункції. Описано, що підвищений рівень серотоніну, гістаміну, тромбоксану й ендотеліну є біохімічними маркерами спазму судин [69, 99]. Для індукування коронарного вазоспазму, як правило, використовують ацетилхолін та ергометрин [99].
Як зазначено вище, еозинофіли відіграють провідну роль в ураженні серця при ЕГПА, у розвитку запалення і коронароспазму [99, 123, 130]. До кінця патофізіологію коронароспазму при ЕГПА не з’ясовано. Дані декількох робіт виявили зв›язок між еозинофілією та коронароспазмом [99, 123, 128]. Припускають, що еозинофільна інфільтрація артеріальної стінки призводить до сегментарної вазоконстрикції внаслідок вивільнення хемокінів та ейкозаноїдних прозапальних медіаторів [128]. Ці висновки підтверджують дані про те, що основною причиною коронароспазму є підвищення контрактильності гладеньких м›язів судин на тлі високої еозинофілії [24]. При активації/стимуляції еозинофіли можуть спричиняти вивільнення вазоактивних речовин, таких як гістамін, простагландин D2, лейкотрієни C4 і D4 із тучних клітин і базофілів із розвитком коронароспазму [99]. Роль біологічно активних речовин, що виділяються еозинофілами та мають важливе значення у коронароспазмі, підтверджено в експерименті. Так, лейкотрієн С4, який вивільняється з еозинофілів, викликає спазм КА у свиней [123].
Основні чинники, що можуть призвести до розвитку коронароспазму в пацієнтів з ЕГПА, окрім токсичного впливу еозинофілії на КА [37]:
- запалення з виділенням прозапальних цитокінів [61, 99], зокрема ФНП-α, що може сприяти функціональному репрограмуванню ендотеліальних клітин в осіб із хронічним запаленням судин [73];
- ендотеліальна дисфункція, зокрема, внаслідок порушення активності ендотеліальної синтази оксиду азоту та її зниженої біодоступності, зменшення концентрації оксиду азоту та підвищення схильності до спазму гладеньких м’язів КА [79, 114, 120].
Є відомості, що вазодилататори, такі як антагоністи кальцію та нітрати, ефективні при лікуванні коронароспазму [120]. Окрім того, зникнення ангінозних нападів і відсутність коронароспазму в пацієнтів на тлі прийому ГК можуть підтверджувати гіпотезу, що коронароспазм розвивається внаслідок гіперчутливості КА чи нез’ясованих автоімунних механізмів у результаті еозинофільної інфільтрації [123]. За даними A. Greco et al., Т-хелпери за допомогою цитокінів спричиняють активацію еозинофілів та підвищення IgE [46]. Із цього погляду зрозуміло, чому стандартне лікування коронароспазму може бути неефективним, тоді як терапія ГК та іншими імуносупресивними препаратами швидко й дієво приводить до усунення ангінозного болю [11, 123, 130]. Однак для оцінки зв’язку між коронароспазмом та еозинофілією потрібні наступні дослідження [123].
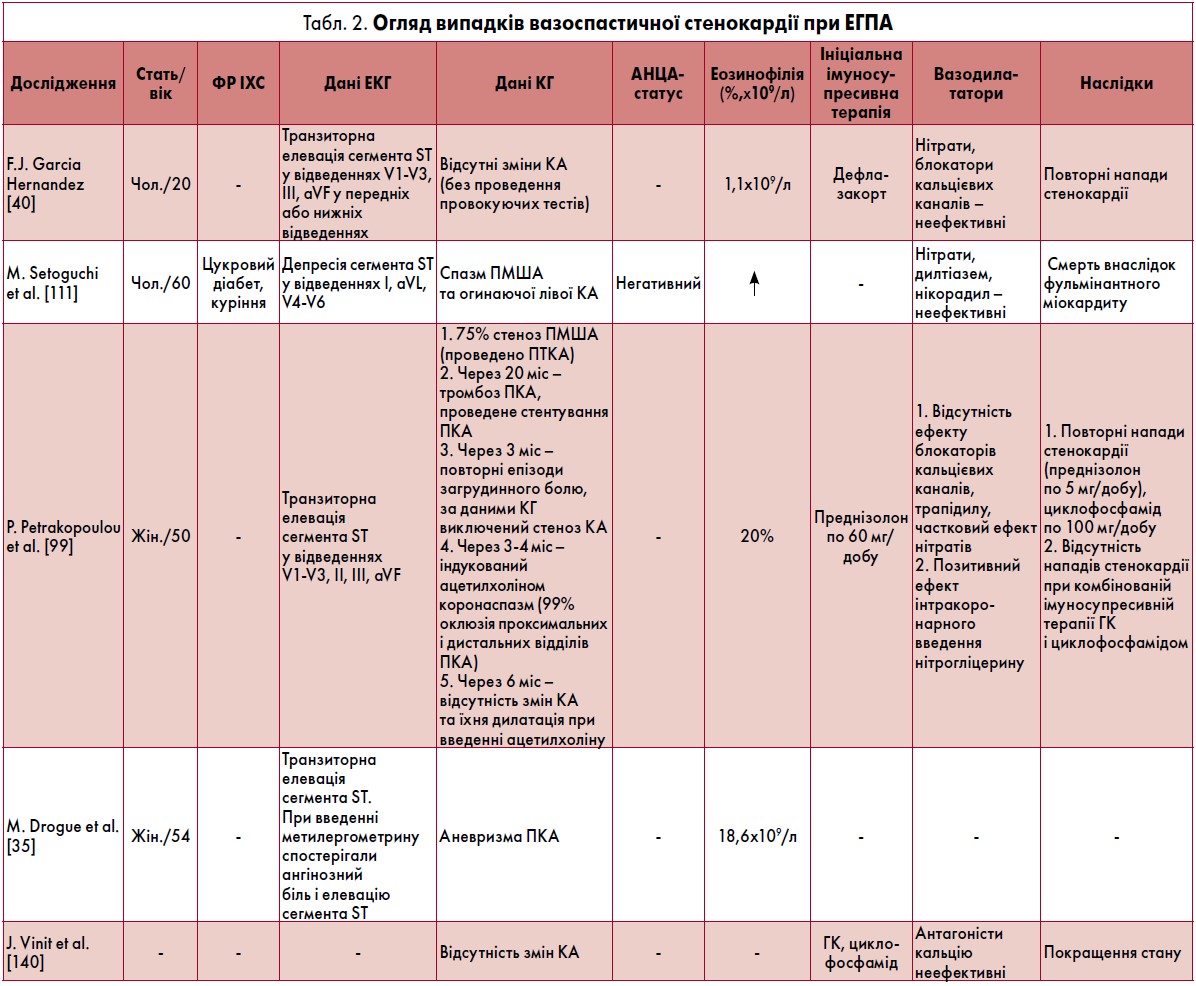
Коронароспазм може зумовити розвиток вазоспастичної стенокардії [99, 111], ГКС [42, 44, 99, 121, 123] і навіть ІМ, ускладненого кардіогенним шоком [37, 75], шлуночковою тахікардією, та раптової смерті [32]. Зазвичай коронароспазм спостерігають під час активної фази ЕГПА [99]. ІХС зустрічається приблизно у 20% пацієнтів з ЕГПА (при незмінених КА за даними КГ) [140], перикардит – 28,7%, аритмії – 22,7%, СН – 20,7%, стенокардія – 7,3%, коронарит (за даними КГ) – 2,7% [88]. За іншими відомостями, стенокардію відмічали у 12,2% хворих на ЕГПА, ІМ – 2% [3]. Патологія серця виявлена у 55% осіб з ЕГПА, коронарит – 30%, а СН – майже у 20%. ІМ діагностували у ранні строки захворювання, його розвиток асоційований із високою активністю імунозапального процесу та коронаритом [1]. Ішемія та ІМ у пацієнтів з ЕГПА поєднуються із запальним процесом та інфільтрацією еозинофілів. При проведенні КГ рідко виявляють зміни епікардіальних артерій [105]. За даними деяких досліджень коронароспазм, підтверджений ангіографічно, був причиною розвитку вазоспастичної стенокардії. Слід відзначити, що атеросклеротичні стенозувальні ураження КА не виявлені [15, 35, 40, 99, 111, 122, 141].
Як вже згадувалося, коронарит може призводити до появи вазоспастичної стенокардії внаслідок коронароспазму епікардіальних КА з розвитком субепікардіальної ішемії міокарда (табл. 2). На ЕКГ відмічають елевацію сегмента ST. Окрім того, можуть виникати шлуночкові тахіаритмії та навіть зупинка серця [99]. Описаний випадок розвитку рефрактерної стенокардії, пароксизмальної форми фібриляції передсердь, мітральної регургітації, систолічної дисфункції ЛШ (ФВ ЛШ 38%) із необструктивними, гемодинамічно незначущими ураженнями КА у 38-річного пацієнта з ЕГПА, якому проведено протезування мітрального клапана, радіочастотна абляція та денервація серця. Хворий виписаний із рекомендаціями прийому варфарину, аміодарону, спіронолактону, преднізолону та азатіоприну. Через три місяці у пацієнта не спостерігали нападів стенокардії. Причину її розвитку не з’ясовано, оскільки не проведене тестування на наявність коронароспазму [25].
ГКС може розвиватися внаслідок коронариту [74], коронароспазму, тромбозу КА [42, 129, 130]. За даними досліджень, виникнення ІМ відзначали у 9,4-18,1% пацієнтів з ЕГПА [16, 90], однак є дані про нижчу частоту його розвитку (2%) в осіб з ЕГПА [3]. Описані випадки розвитку ГКС як першого прояву ЕГПА [6, 99, 121], ГКС з елевацією сегмента ST [6, 9, 11, 15, 26, 32, 37, 94, 123, 141], ГКС без елевації сегмента ST [7, 29, 44, 130]. Огляд деяких випадків ГКС викладений у таблиці 3.
У літературі описані випадки розвитку ГКС внаслідок коронароспазму, що ускладнився кардіогенним шоком [6, 32], фібриляцією шлуночків (пацієнту проведено імплантацію кардіовертера-дефібрилятора) [9, 134], шлуночковою тахікардією [130]; ІМ і постінфарктної стенокардії [74]. Окрім того, відомий випадок появи ГКС при незмінених епікардіальних КА за даними КГ [6].
На додачу, описано клінічний випадок, коли у 35-річної пацієнтки, яка поступила до відділення невідкладної допомоги зі скаргами на біль у грудній клітці та задишку, за даними ЕхоКГ виявлений гіпокінез передньої стінки ЛШ; ФВ ЛШ дорівнювала 48%, діагностований мінімальний перикардіальний випіт. При проведенні КГ виявлено оклюзію (тромбоз) дистального відділу ПМША. Виконано ПТКА ПМША та інфузію тирофібану, після чого призначений метилпреднізолон по 80 мг/добу. Стан пацієнтки покращився, рівень еозинофілів знизився до норми, а за даними контрольної КГ, яку провели через тиждень, тромботичні ураження КА не виявлені. Через два тижні при повторній ЕхоКГ патологічні зміни не діагностовані (відсутні гіпокінез і перикардіальний випіт) [42].
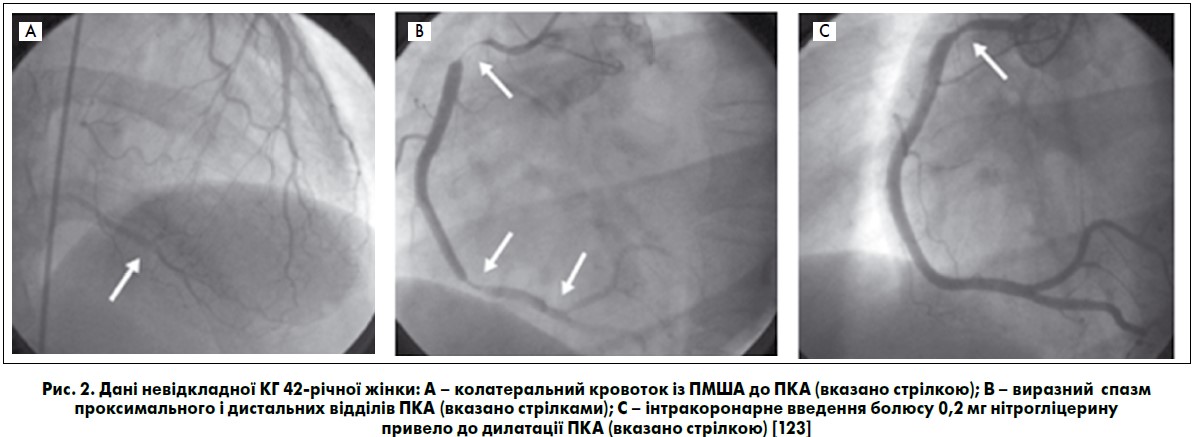
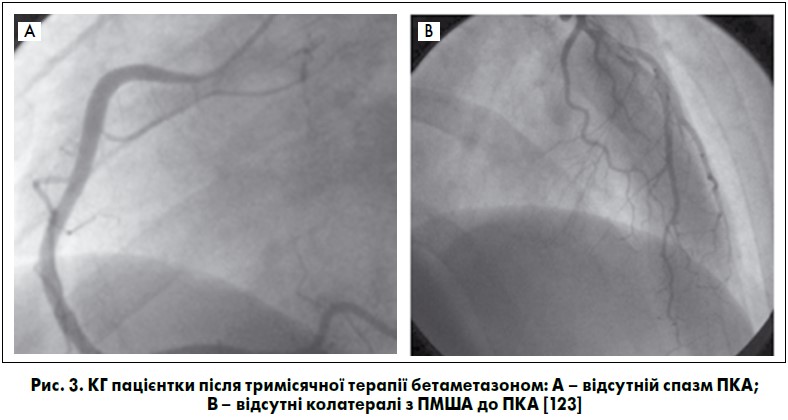
Також цікавим є випадок розвитку ГКС як наслідок спазму ПКА у 42-річної жінки з аспірин-індукованою астмою, що пройшов після інтракоронарного введення нітрогліцерину (рис. 2). На ЕКГ – елевація сегмента ST у відведеннях ІІ, ІІІ, aVF та дискордантна депресія сегмента ST у відведеннях V2-V5, підвищений рівень тропоніну Т, АНЦА не діагностовано. Після дообстеження (виявлено астму, синусити, пурпуру, поліпи носа, еозинофілію) встановлений діагноз ЕГПА. Ймовірно, у даному випадку коронароспазм пов’язаний з еозинофілією, оскільки інші можливі причини (куріння, вживання кокаїну, гіпервентиляція) виключені. За два місяці до госпіталізації у пацієнтки розвинувся біль у грудній клітці, через три тижні епізоди стали частішими. На тлі прийому пролонгованих нітратів та дилтіазему було відзначено ангінозні напади, однак після призначення бетаметазону стан хворої покращився. Ангінозний біль не спостерігали за відсутності прийому антиангінальних препаратів та через три місяці при проведенні КГ коронароспазм не відмічали (рис. 3) [123].
Як було зазначено вище, коронароспазм розвивається в активній фазі захворювання [99], однак появу коронароспазму спостерігали і в неактивній фазі ЕГПА [26]. G. D’Amico et al. описали випадок розвитку ІМ з елевацією сегмента ST передньобічної стінки ЛШ у 57-річної жінки (що приймала преднізолон) без ФР ІХС, яка поступила з типовим болем у грудній клітці. На ЕКГ виявлено елевацію сегмента ST у відведеннях I, aVL, V1-V6. Призначене лікування: прасугрель, аспірин, нефракціонований гепарин, морфін. При проведенні невідкладної КГ встановлено субоклюзію першої діагональної гілки, стеноз не зменшувався при інтракоронарному веденні нітратів. Стенозів ПКА не виявлено. Пацієнтці було проведене стентування першої діагональної гілки металевим стентом. Наприкінці процедури у хворої розвинувся рецидив болю у грудній клітці, на ЕКГ відзначали елевацію сегмента ST у відведеннях ІІ, ІІІ і aVF. За даними повторної КГ, виявлений множинний стеноз ПКА внаслідок коронароспазму, який пройшов після інтракоронарного введення нітратів і верапамілу [26].
Ще один випадок ураження КА у 58-річного пацієнта, при обстеженні якого встановлений діагноз ЕГПА. Крім того, хворий мав декілька ФР ССЗ: сімейний анамнез ССЗ, АГ, куріння, гіперхолестеринемію. В анамнезі – ішемічний та геморагічний інсульти, пролапс мітрального клапана з незначною регургітацією, атріовентрикулярна блокада 1-го ступеня. За допомогою КТ виявлено виразний кальциноз КА, а за даними КГ – дилатацію і дифузний кальциноз КА, оклюзію ПМША з розвиненим колатеральним кровотоком, критичний стеноз дистального відділу ПКА з субоклюзією задньої міжшлуночкової артерії та критичним стенозом задньо-бічної гілки. Пацієнту проведено коронарну ангіопластику шляхом імплантації металевого стента в задню мішлуночкову артерію із призначенням ГК [14].
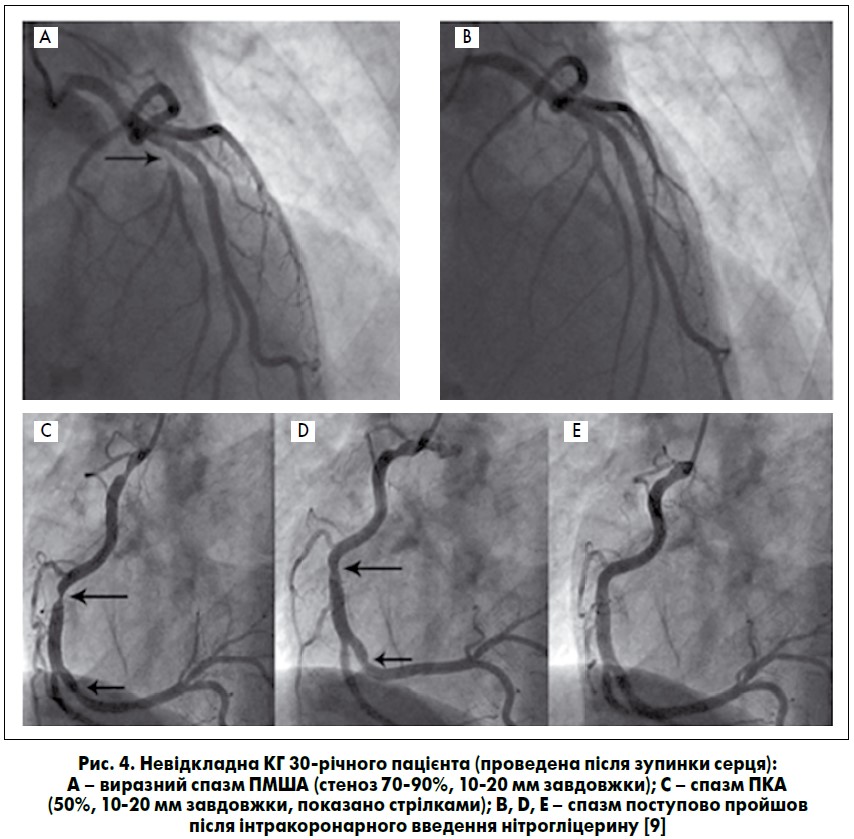
Необхідно відзначити, що прийом нестероїдних протизапальних препаратів (НПЗП) може посилити сегментарну вазоконстрикцію, опосередковану еозинофілами. Буває, що НПЗП сприяють розвитку коронароспазму внаслідок дегрануляції еозинофілів при ЕГПА. Окрім того, припинення прийому системних ГК може бути тригерним чинником маніфестації ЕГПА [50]. Так, описаний випадок коронароспазму з виникненням ангінозного болю, ІМ, фібриляції шлуночків і зупинки серця з успішною реанімацією у 30-річного пацієнта з ЕГПА після відміни ГК і через годину після введення НПЗП (кетопрофен). На ЕКГ відзначали елевацію сегмента ST у відведеннях V1-V6, І, aVL, реципрокну депресію сегмента ST у відведеннях II, III, aVF. За даними КГ, спостерігали спазм ПМША і ПКА, який пройшов після інтракоронарного введення нітрогліцерину (рис. 4). Через 15 днів хворому імплантований кардіовертер-дефібрилятор та призначені ГК, цитостатики. Упродовж 30 місяців на тлі щоденного прийому преднізолону й азатіоприну симптомів не виявлено [9]. Дані цього дослідження демонструють, що застосування НПЗП може призвести до коронароспазму внаслідок дегрануляції еозинофілів при ЕГПА. Більш того, для запобігання фатальних подій важлива прихильність до терапії ГК, особливо у пацієнтів з ЕГПА із високим серцево-судинним ризиком [9].
J.P. Smedema et al. описали розвиток серцебиття та атипового болю у грудній клітці в 53-річної жінки з ЕГПА (діагноз встановлений 7 років тому). На ЕКГ виявлено ішемію міокарда, при проведенні 24-годинного холтерівського моніторингу ЕКГ – часті шлуночкові ектрасистоли та нестійка мономорфна шлуночкова тахікардія, а при наступному обстеженні (перфузійна сцинтіграфія з талієм‑201 та дипіридамолом, кіно- та перфузійна МРТ серця) – зворотні/незворотні дефекти перфузії та фіброз у ділянці міжшлуночкової перегородки, дискінезія її сегмента. Таким чином, зазначені дефекти перфузії та рубцева тканина, які є вторинними відносно васкуліту дрібних судин міокарда та інфільтрації міокарда. За відсутності змін при проведенні КГ відзначені результати підтверджують ішемію, зумовлену васкулітом дрібних судин. До імуносупресивної терапії (низькі дози ГК та азатіоприн) були додані β-адреноблокатори й нітрати [118].
Описані випадки коронариту з розвитком ГКС з елевацією сегмента ST у ділянці передньої стінки ЛШ та периміокардиту [141], ГКС і міокардиту [109], як першого прояву ЕГПА, міокардиту та ГКС з елевацією сегмента SТ, що ускладнився кардіогенним шоком і клінічною смертю [37].
Ектазії та аневризми КА
Багато чинників можуть впливати на розвиток ектазій КА, зокрема, надмірна експресія матриксних металопротеїназ, асоційована з ремоделюванням артерій. При СВ виявлено підвищення рівня матриксних металопротеїназ (ММР‑2, ММР‑9) та зниження їхніх тканинних інгібіторів (TIMP‑1 і TIMP‑2) [29]. У таких пацієнтів ектазії КА можуть спричиняти розвиток різної симптоматики, часто їх виявляють несподівано або після появи атипового болю у грудній клітці, стенокардії чи ГКС [28]. Описаний випадок нестабільної стенокардії у 58-річного чоловіка, госпіталізованого з гострим болем у грудній клітці. За результатами КГ, у нього виявлені ектазії КА, хронічна оклюзія середнього відділу ПМША та стеноз (90%) проксимального відділу ПМША, проведено імплантацію металевого стенту. Встановлення діагнозу ЕГПА, дані про асоціацію ЕГПА з істотним ураженням КА (висока претестова ймовірність ІХС) і стійкий біль у грудній клітці були показаннями до проведення невідкладної КГ у хворого [29].
При ЕГПА виникнення аневризм КА є дуже рідкісним. Проте все ж описані випадки вазоспастичної стенокардії та аневризми ПКА [35], ІМ та гігантських аневризм ПКА і ЛКА за даними КГ [60]. Відомо про розвиток гігантської аневризми огинаючої лівої КА (діаметром 4 см із пристінковими тромбами) і аневризми ПКА, виявлені за допомогою КТ. Окрім того, у пацієнта на ЕКГ спостерігалися ознаки перенесеного ІМ, за даними ЕхоКГ – зниження скоротливості ЛШ (ФВ ЛШ 30%) [54]. Ще один клінічний випадок залучення до патологічного процесу КА при ЕГПА: при проведенні коронарної КТ-ангіографії у 69-річного чоловіка за відсутності симптомів зі сторони ССС виявлено ознаки васкуліту КА, потовщення судинної стінки, периваскулярну інфільтрацію. Наявні виразний стеноз проксимального відділу ПКА внаслідок сакулярної аневризми (6x10 мм) та стеноз проксимального відділу ПМША. Також діагностовано фузиформну аневризму низхідної грудної та черевної аорти. Хоча ураження великих КА не є частою знахідкою при ЕГПА, результати цього дослідження показали, що при ЕГПА ці артерії можуть залучатися у патологічний процес із розвитком васкуліту та аневризм [34].
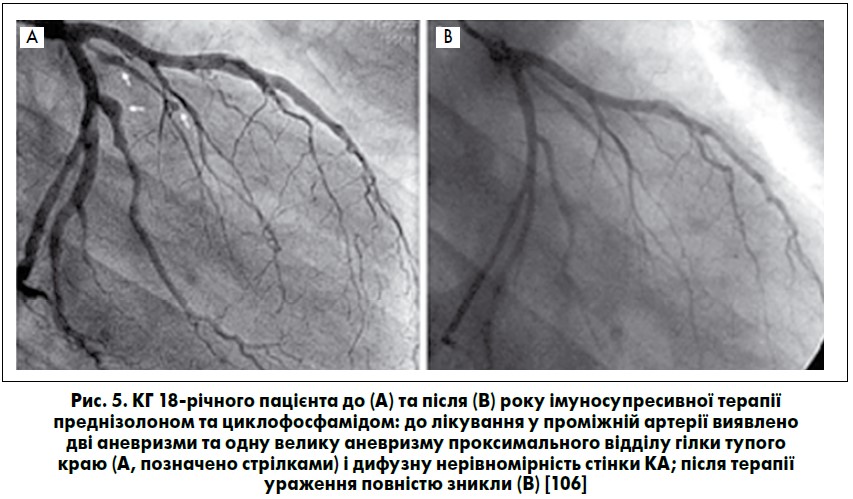
Клініцистами описаний розвиток болю у грудній клітці з дифузною елевацією сегмента ST на ЕКГ у 18-річного пацієнта. При проведенні КГ виявлений коронарит із розвитком стенозів та аневризм КА (рис. 5). За даними ЕхоКГ – помірний перикардіальний випіт. Через рік терапії преднізолоном та циклофосфамідом відмічали повний регрес васкуліту та змін КА [106].
У літературі є повідомлення про випадки раптової серцевої смерті у пацієнтів з ЕГПА [111, 137]. Описаний випадок раптової кардіальної смерті 49-річної пацієнтки з ЕГПА в активній васкулітній стадії за відсутності клінічних симптомів ураження серця та мультиорганним пошкодженням за даними автопсії з переважним залученням у патологічний процес серця. Гістологічне дослідження тканин шлуночків та міжшлуночкової перегородки виявило дифузну інфільтрацію еозинофілами, гранульоми та некротизуючий васкуліт з ушкодженням малих та епікардіальних КА (фібриноїдний некроз, трасмуральна еозинофільна інфільтрація, запалення, тромбоз та периваскулярна еозинофільна інфільтрація). У міокарді відмічали ділянки некрозу [137].
Слід відзначити, що у разі розвитку ГКС у пацієнтів із ЕГПА необхідно проводити ретельний диференційний діагноз, оскільки в літературі є дані щодо маніфестації еозинофільного міокардиту, який ускладнився кардіогенним шоком, замаскованим ІМ передньобічної стінки ЛШ [112], еозинофільного міоперикардиту (за даними біопсії) [135], міокардиту (був встановлений первинний діагноз ГКС) [133].
Діагностика базується на клінічних та гістологічних даних [51]. Діагноз ЕГПА встановлюють на основі критеріїв Американського коледжу ревматології (ACR) [84]. Дані лабораторного дослідження крові неспецифічні, тому їх діагностичне значення обмежене [8]. У загальному аналізі крові виявляють лейкоцитоз [66], еозинофілію – понад 10%, чи >1,5х109 [13, 51, 66, 96], анемію, підвищення швидкості осідання еритроцитів [8, 51]. Також відзначають збільшення СРБ, особливо в активній фазі васкуліту [8], у 75% випадків – зростання IgE у сироватці крові [8, 98]. При ураженні міокарда виявляють збільшення концентрації серцевих тропонінів, МВ-КФК, КФК [66, 82]. Додатковими діагностичними маркерами можуть бути вищі рівні розчинних форм рецепторів інтерлейкіну‑2, еозинофільного катіонного протеїну та розчинного тромбомодуліну, але вони не є широко доступними [110]. Окрім того, у літературі є дані щодо визначення рівня циркулюючих ендотеліальних мікрочастинок як маркера пошкодження ендотелію, у пацієнтки з ЕГПА та кардіоміопатією мало місце підвищення цього показника [76].
АНЦА виявляли у 30-77,8% осіб з ЕГПА [13, 22, 48, 70, 108, 116, 119], у 75-81% з яких спостерігалися антитіла з перинуклеарною імунофлюоресцентністю (pАНЦА), у більшості випадків – зі специфічністю до мієлопероксидази (у 92-100% пацієнтів) [13, 51, 98], які частіше визначали у хворих із гломерулонефритом, мононевритом чи пурпурою [116]. Однак, як зазначено вище, ураження серця частіше виявляють у АНЦА-негативних хворих [108].
Діагностику ураження ССС проводять за допомогою ЕКГ, ЕхоКГ [51, 105, 118, 135], МРТ/МРТ-ангіографії, КТ/КТ-ангіографії, позитронно-емісійної томографії, КГ [16, 37, 83, 118, 135], сцинтиграфії міокарда [140] та біопсії міокарда [118]. Раннє залучення ССС до патологічного процесу може бути субклінічним, і у більшості пацієнтів відсутні будь-які симптоми або зміни на ЕКГ. Тому ЕхоКГ та/або МРТ серця рекомендовані як частина обстеження хворих із підозрою на патологію серця [135]. Проведення ЕКГ, ЕхоКГ рекомендоване пацієнтам навіть за відсутності симптомів ураження ССС [139]. Так, за даними дослідження зміни на ЕхоКГ виявляли у 73% хворих із пошкодженням серця, ЕКГ – у 58% [140]. На ЕКГ діагностують ішемію міокарда, неспецифічні зміни сегмента ST, зміни зубця Т, порушення провідності (зокрема, блокади ніжок пучка Гіса, атріовентрикулярну блокаду ІІІ ступеня) і ритму серця, типові ЕКГ-ознаки перикардиту чи ГКС [29, 51, 105]. За допомогою доплерівської ЕхоКГ оцінюють розміри камер серця, порушення скоротливої здатності, ознаки діастолічної дисфункції ЛШ, виявляють тромби у порожнинах серця, перикардит тощо [51, 82, 109]. Найчастіші ЕхоКГ-знахідки включають зниження ФВ ЛШ, регіонарну чи дифузну гіпокінезію та перикардіальний випіт [30, 90].
МРТ серця є інформативним методом візуалізації не тільки для раннього виявлення ураження ССС, але й оцінки перебігу захворювання, прогнозу та ефективності лікування [83, 85, 118, 126]. Контрастна МРТ має суттєву діагностичну значущість при визначенні порушення функції серця, його структурних та морфологічних змін [118]. Відзначено цінність перфузійної МРТ для діагностики ураження малих судин міокарда. За допомогою МРТ серця з контрастуванням виявлений некроз міокарда у 3 із 8 пацієнтів із ЕГПА [85]. Окрім того, описаний транзиторний коронароспазм у хворих на ЕГПА, хоча за даними МРТ структурних змін КА не було [85, 141].
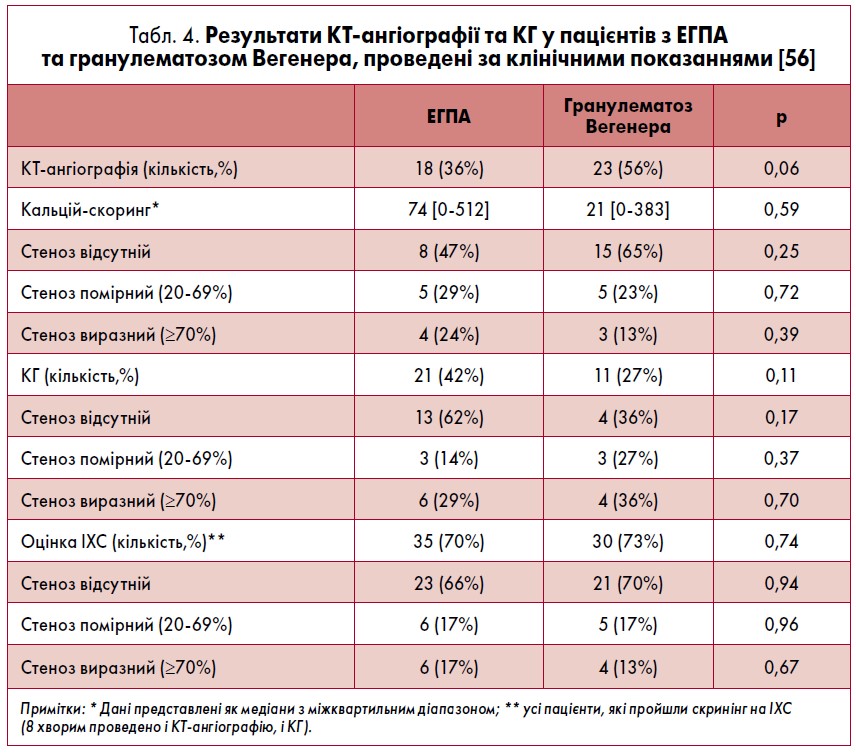
У дослідженні, проведеному M.R. Hazebroek et al., оцінювали стан КА за допомогою КТ-ангіографії та/або КГ у пацієнтів, у яких відзначали типовий біль у грудній клітці, дифузне чи регіонарне порушення скоротливої здатності ЛШ за даними ЕхоКГ або МРТ та/чи трансмуральний чи субендокардіальний інфаркт-асоційований фіброз міокарда (табл. 4) [56].
При проведенні КГ рідко виявляють зміни епікардіальних КА [68], однак є повідомлення про ангіографічно підтверджене їх пошкодження [58]. Слід відзначити, що відсутність змін за даними КГ не виключає ураження КА внаслідок ЕГПА, оскільки часто страждають дистальні (міокардіальні) відділи [138]. Пошкодження епікардіальних КА внаслідок васкуліту відзначають у вигляді коронароспазму [37, 99], стенозу і аневризм [106], тромбозу [42], дисекції КА [63]. Окрім того, за даними КГ відмічають васкуліт КА з нерівномірним просвітом судин, різкими обривами та аневризмами [35, 58, 85]. За результатами роботи T. Neumann et al., при проведенні КГ у пацієнтів із болем у грудній клітці та задишкою зміни КА були відсутні у 62% хворих, нерівномірність просвіту КА – у 23%, стеноз КА понад 70% – у 15% [90]. За даними дослідження R. Dennert et al., ІХС відповідно до КГ виявлено у 16% пацієнтів з ЕГПА проти 3% у контрольній групі [30].
Гістологічні дані
За даними біопсії уражених тканин (зазвичай шкіри, нервів чи м’язів) виявляють некротизуючий васкуліт, екстраваскулярні некротичні гранульоми, еозинофільну інфільтрацію [51, 139], хоча поєднання цих явищ рідкі [51, 115]. Найпоширенішими гістопатологічними знахідками при біопсії є еозинофільні інфільтрати тканин [139].
Принципи лікування
Використання ГК є наріжним каменем терапії пацієнтів з ЕГПА. Так, згідно з рекомендаціями щодо оцінки й лікування ЕГПА (2015), застосування ГК є доцільним для досягнення ремісії захворювання [48]. За наявності симптомів, що загрожують життю пацієнта, слід призначати пульс-терапію метилпреднізолоном. Як індукційне лікування рекомендоване застосування преднізолону по 1 мг/кг/добу упродовж 2-3 тижнів із поступовим зниженням до мінімальної ефективної дози або, за можливості, до відміни [48]. Пацієнтам із проявами, що загрожують життю, та/або ураженням життєво важливих органів (наприклад, серце, ШКТ, центральна нервова система, тяжка периферична невропатія, тяжке захворювання очей, альвеолярний крововилив та/або гломерулонефрит) для індукції ремісії доцільне призначення комбінації ГК та іншого імуносупресивного препарату, наприклад циклофосфаміду (рівень доказовості В). Монотерапія ГК показана за відсутності симптомів, що загрожують життю хворого, та/або ураження життєво важливих органів (рівень доказовості С) [48].
Згідно з рекомендаціями Європейської антиревматичної ліги, Європейської ниркової асоціації та Європейської асоціації діалізу і трансплантації (EULAR/ERA-EDTA, 2016), для індукції ремісії при АНЦА-СВ, зокрема ЕГПА, слід призначати комбінацію ГК (метилпреднізолон) та імуносупресивних засобів (циклофосфамід, мікофеналату мофетил, метотрексат) чи ритуксимабу [144]. Призначення ритуксимабу (химерні моноклональні антитіла, що мають специфічність до CD20-антигену, який виявляють на поверхні В-лімфоцитів) може розглядатися у деяких АНЦА-позитивних пацієнтів з ураженням нирок або рефрактерним захворюванням (рівень доказовості С) [48]. Застосування ГК та інших імуносупресивних препаратів (особливо циклофосфаміду) приводить до значного покращення прогнозу та виживаності осіб з ЕГПА [19, 97, 115]. Так, при використанні ГК як першої лінії терапії у пацієнтів за відсутності чинників несприятливого прогнозу індукцію ремісії спостерігали в 93% випадків [103].
Наявність патології ССС є несприятливим прогностичним чинником, що потребує агресивного лікування [135, 143]. ГК чинять протизапальну та імуносупресивну дію і використовуються у хворих на СВ з ураженням ССС. Застосування інших імуносупресантів, таких як циклофосфамід, азатіоприн, мікофенолату мофетил або циклоспорин, дозволяє знизити дозу ГК, тим самим зводячи до мінімуму побічні ефекти останніх [59]. Рання імуносупресивна терапія може мати протективний серцево-судинний ефект при ЕГПА [44] та приводити до регресу патології серця [7, 44, 118]. Так, відмічали позитивний вплив преднізолону та/або циклофосфаміду чи азатіоприну [32, 123, 130, 134] і нормалізацію рівня еозинофілів у крові [44, 130]. Рекомендоване призначення циклофосфаміду і високих доз ГК у випадках активного васкуліту з ураженням ССС [68, 141], антиангінальних препаратів [36] чи медикаментів для лікування СН (наприклад, інгібіторів ангіотензинперетворювального ферменту та β-адреноблокаторів) [68]. Така терапія знижує частоту серцево-судинних ускладнень [36]. За даними декількох досліджень, застосування преднізолону і циклофосфаміду упродовж року сприяло повному регресу змін КА та/або відсутності коронароспазму [36, 106, 109]. Окрім того, лікування ГК може спричинити підвищення скоротливої функції ЛШ і резолюції перикардіального випоту [42, 77, 118]. Т. Kubota et al. описали випадок ІМ, що ускладнився кардіогенним шоком у пацієнта із ЕГПА, який отримував пульс-терапію преднізолоном. При проведенні КГ виявлено оклюзію трьох КА. Стан хворого покращився після використання комбінації преднізолону та циклофосфаміду, а повторна КГ показала реканалізацію інфаркт-залежних артерій [75].
Вазодилататори є основою лікування при спазмі КА, але у пацієнтів із коронароспазмом при ЕГПА ці препарати не відіграють значної ролі. Такі хворі можуть краще реагувати на імуносупресивну терапію [145]. В осіб із коронароспазмом та еозинофілією часто виявляють резистентність до вазодилататорів, однак, за даними випробовувань, імуносупресивне лікування покращує симптоми при вазоспастичній стенокардії [99, 123, 143]. Це підтверджують дані інших досліджень, за якими відмічали резистентність стенокардії до вазодилататорів (антагоністів кальцію, нітратів), але позитивний ефект ГК (імуносупресивних засобів) [40, 111, 130]. Інші ж прояви ураження серця вимагали агресивнішого імуносупресивного лікування [92], оскільки затримка його призначення могла призвести до раптової смерті [143]. Тому рання діагностика ураження ССС важлива при ЕГПА [130]. Наприклад, коронароспазм був першим проявом у пацієнтки з розвитком ГКС, що ускладнився кардіогенним шоком на тлі незмінених епікардіальних КА. При застосуванні вазодилататорів у хворої спостерігали рецидивні епізоди коронарних подій, які не відмічали після початку імуносупресивної терапії [6]. Є дані щодо позитивного ефекту комбінованого лікування ГК, циклофосфамідом та вазодилататорами при вазоспастичній стенокардії, який полягав у зменшенні її симптомів та сприяв нормалізації функції ендотелію КА [99]. У літературі є повідомлення, що стенокардія може повторно з’являтися при зниженні дози ГК, у такому разі рекомендоване призначення інших імуносупресивних препаратів, таких як циклофосфамід, що, можливо, пригнічуватимуть вазоконстрикцію [130]. S. Tagaki et al. припустили, що коронароспазм може бути викликаний гіперреактивністю артерій, спровокованою локальним запаленням стінки КА, яку можливо зменшити протизапальним ефектом ГК [128]. Однак є дані щодо ефективності нітратів і антагоністів кальцію (верапаміл) [26], інтракоронарного введення нітратів [37]. T. Noguchi et al. при рефрактерному спазмі КА відмічали позитивний ефект інтракоронарного введення нікорандилу [91]. Проте рецидиви мають місце у 25% хворих на ЕГПА, тому подальше спостереження для оцінки довгострокових наслідків імуносупресивної терапії є необхідним [99].
У літературі є відомості про імплантацію металевих стентів [14, 26, 29], елютинг-стентів [11, 44, 99], кардіовертера-дефібрилятора [32] та проведення АКШ [135] пацієнтам з ЕГПА і ураженням КА. Описаний випадок ГКС у 68-річної жінки, що ускладнився кардіогенним шоком внаслідок рефрактерного множинного спазму КА: 90% середнього відділу ПМША і 70% проксимального відділу першої діагональної гілки, 90 та 70% стеноз проксимального і середнього відділів проміжної гілки відповідно та 70% стеноз гирла ПКА, 40% середнього відділу ПКА і 80% середнього відділу задньої міжшлуночкової артерії. Після інтракоронарного введення верапамілу та нітрогліцерину суттєво зменшився стеноз ПКА, а ПМША та її гілок – незначно. Тому, враховуючи рефрактерність коронароспазму до вазодилататорів і розвиток кардіогенного шоку, було імплантовано два елютинг-стенти у середній відділ ПМША та першу діагональну гілку ЛКА. Однак пацієнтку турбували напади стенокардії на тлі прийому антагоністів кальцію і нітратів тривалої дії. Після встановлення діагнозу ЕГПА та призначення ГК відзначали відсутність стенокардії, зниження периферичної еозинофілії, підвищення ФВ ЛШ до 42% (вихідна – 30%) [11].
Прогноз
До застосування ГК смертність при ЕГПА складала приблизно 50% упродовж трьох місяців після встановлення діагнозу [12, 100]. Використання ефективної імуносупресивної терапії та удосконалення діагностики ЕГПА привело до покращення виживаності пацієнтів [19, 30, 50, 100]. Прогноз при ЕГПА сприятливий, 10-річна виживаність становить 81-92% [50, 108, 119]. За даними досліджень, цей показник протягом року був 93-94%, 5 років – 60-97% [12, 50, 89, 119]. За результатами іншого випробування, 5- і 10-річна виживаність була 88,9% (95% довірчий інтервал [ДІ] 84,3-92,2) та 78,6% (95% ДІ 70,3-84,8) відповідно. Також 5- і 10-річна безрецидивна виживаність дорівнювала 64,8% (95% ДІ 58,6-70,4) і 54,4% (95% ДІ 45,8-61,6) відповідно [22]. Існують дані дослідження, згідно з якими 5-річна виживаність складала 97%, а 10-річна – 89%, що співставна зі смертністю у загальній популяції.
Тільки наявність СН асоціювалась із підвищенням смертності [88]. Ураження ССС є одним із важливих предикторів несприятливого прогнозу та причиною смерті у 50% випадків при ЕГПА [12, 50, 119]. У 83% осіб з ЕГПА упродовж року після початку імуносупресивного лікування розвиток летальних наслідків зумовило ураження ССС [12]. Згідно з результатами роботи A. Bourgarit et al., у пацієнтів, що померли у перший рік після початку імуносупресивного лікування, частіше спостерігали пошкодження ССС і ШКТ [12]. За даними випробування L. Guillevin et al. за участю 98 хворих, 78-місячна виживаність складала 90% за відсутності ураження ССС проти 30% у разі їхньої наявності [50]. Основними причинами смерті у пацієнтів з ЕГПА були СН, ІМ, аритмогенна раптова смерть, церебральна чи шлунково-кишкова кровотечі [50]. Шлуночкові аритмії та зупинка серця є небезпечними для життя ускладненнями, що потребують профілактичного лікування, поки протизапальна терапія не приведе до ремісії захворювання [50, 111, 137]. У подібних випадках необхідно розглядати доцільність імплантації кардіовертера-дефібрилятора [32].
Висновки
Таким чином, патологія ССС при ЕГПА є достатньо частою, гетерогенною та прогностично несприятливим чинником і провідною причиною смертності пацієнтів з ЕГПА. Рання діагностика ураження ССС та наступна ад’ювантна терапія можуть запобігти прогресуванню патології серця та поліпшити прогноз цих хворих. У випадках, що перебігають із болем у грудній клітці, в осіб із БА та іншими проявами (наприклад, еозинофілія) необхідно виключити діагноз ЕГПА. Ураження КА при ЕГПА часто є небезпечним для життя і потребує агресивного імуносупресивного лікування, тому рання діагностика, оптимальна терапія ГК та іншими імуносупресивними препаратами може запобігти прогресуванню патології серця та покращити прогноз хворих на ЕГПА. В умовах міждисциплінарного підходу ретельна оцінка ССС важлива при ЕГПА, навіть за відсутності симптомів з її боку, для поліпшення прогнозу пацієнтів з ураженням ССС.
Література
- Семенкова Е.Н., Моисеев С.В., Наместникова О.Г. Клинические аспекты синдрома гиперэозинофилии // Клин. медицина. – 2004. – № 2. – С. 28-31.
- Стрижаков Л.А. Коронарит при ревматических заболеваниях: обзор литературы // Фарматека. – 2012. – № 6. – С. 16-19.
- Стрижаков Л.А., Моисеев С.В., Семенкова Е.Н. и др. Клинико-патоморфологические варианты поражения сердца у больных системными васкулитами и возможности методов неинвазивной диагностики // Фарматека. – 2013. – № 9. – С. 65-71.
- Аbril A. Churg-Strauss Syndrome: An Update // Curr Rheumatol Rep. – 2011. – 13. – Р. 489-495.
- Ames P.R., Margaglione M., Mackie S., Alves J.D. Eosinophilia and thrombophilia in churg strauss syndrome: a clinical and pathogenetic overview // Clin Appl Thromb Hemost. – 2010. – 16 (6). – Р. 628-636.
- Apirami M., Pratheepan J.A., Kumanan T. et al. Cardiogenic Shock: An Unusual Initial Presentation of Churg-Strauss Syndrome // Hindawi Case Reports in Rheumatology, 2018, Article ID2076837, 3 рр.
- Asdonk T., Pabst S., Clauberg R. et al. Acute coronary syndrome as a first manifestation of Churg-Strauss syndrome // Dtsch Med Wochenschr. – 2012. – 1370. – Р. 671-674.
- Baldini C., Talarico R., Della Rossa A. et al. Clinical manifestation and treatment of Churg-Strauss syndrome // Rheum Dis Clin N Am. – 2010. – Vol. 36. – P. 527-543.
- Benallegue N., Lozach P., Belizna C. et al. Acute coronary vasospasm in a patient with eosinophilic granulomatosis with polyangiitis following NSAID administration: A case report // Medicine (Baltimore). – 2016. – 95 (47): e5259.
- Bhagirath K.M., Paulson K., Ahmadie R. et al. Clinical utility of cardiac magnetic resonance imaging in Churg-Strauss syndrome: case report and review of the literature // Rheumatol Int. – 2009. – 29 (4). – Р. 445-449.
- Bitar A.Y., Thompson C.D., Tanetal C.W. Coronary artery vasospasm and cardiogenic shock as the initial presentation for EGPA // Journal of Cardiology Cases. – 2016. – Vol. 13, № 4. – Р. 105-108.
- Bourgarit A., Le Toumelin P., Pagnoux C. et al. Deaths occurring during the first year after treatment onset for polyarteritis nodosa, microscopic polyangiitis, and Churg-Strauss syndrome: a retrospective analysis of causes and factors predictive of mortality based on 595 patients // Medicine (Baltimore). – 2005. – 84. – Р. 323-330.
- Brucato A., Maestroni S., Masciocco G. et al. Cardiac involvement in Churg-Strauss syndrome // G Ital Cardiol (Rome). – 2015. – 16 (9). – Р. 493-500.
- Buccheri D., Chirco P.R., Piraino D. et al. Coronary Arteries Involvement in Churg-Strauss Syndrome Simulating an Acute Coronary Syndrome: An Emblematic Case and Literature Review // J Thrombo Cir. – 2016. – 2. – Р. 102.
- Buhaescu I., Williams A., Yood R. Rare manifestations of Churg-Strauss syndrome: coronary artery vasospasm, temporal artery vasculitis and reversible monocular blindness-a case report // Clin Rheumatol. – 2009. – 28 (2). – Р. 231-233.
- Cereda A.F., Pedrotti P., De Capitani L. et al. Comprehensive evaluation of cardiac involvement in eosinophilic granulomatosis with polyangiitis (EGPA) with cardiac magnetic resonance // Eur J Intern Med. – 2017. – 39. – Р. 51-56.
- Churg J., Strauss L. Allergic granulomatosis. Allergic angiitis and periarteritis nodosa // Am J Pathol. – 1951. – 27. – Р. 277-301.
- Cocco G., Gasparyan A.Y. Myocardial ischemia in Wegener’s granulomatosis: coronary atherosclerosis versus vasculitis // Open Cardiovasc Med J. – 2010 . – 23; 4. – Р. 57-62.
- Cohen P., Pagnoux C., Mahr A. et al. Churg-Strauss syndrome with poor-prognosis factors: a prospective multicenter trial comparing glucocorticoids and six or twelve cyclophosphamide pulses in forty-eight patients // Arthritis Rheum. – 2007. – 57. – Р. 686-693.
- Cohen Tervaert J.W. Translational mini-review series on immunology of vascular disease: accelerated atherosclerosis in vasculitis // Clin Exp Immunol. – 2009. – 156. – Р. 377-385.
- Cohen Tervaert J.W. Cardiovascular disease due to accelerated atherosclerosis in systemic vasculitides //Best Pract Res Clin Rheumatol. – 2013. – 27 (1). – Р. 33-44.
- Comarmond C., Pagnoux C., Khellaf M. et al. Eosinophilic granulomatosis with polyangiitis (Churg-Strauss): clinical characteristics and long-term followup of the 383 patients enrolled in the French Vasculitis Study Group cohort // Arthritis Rheum. – 2013. – 65. – Р. 270-281.
- Correia A.S., Gonclves A., Arajo V. et al. Churg-Strauss syndrome presenting with eosinophilic myocarditis: A diagnostic challenge // Rev Port Cardiol. – 2013. – 32 (9). – Р. 707-771.
- Cui N., Su L., Wang H. et al. A case report of Churg-Strauss syndrome presenting with cardiogenic shock treated with extracorporeal membrane oxygenation // Medicine. – 2015. – Vol. 94, № 43: e1757.
- Cura L., Dayan V., Cristar F. et al. Cardiac denervation procedure to treat refractory angina in a patient with Churg-trauss syndrome and non-obstructive coronary lesions // Interactive CardioVascular and Thoracic Surgery. – 2012. – 15. Р. 166-168.
- D’Amico G., Nai Fovino L., Cucchini U. et al. Non-culprit coronary vasospasm in a woman affected by Churg-Strauss syndrome presenting with ST-elevation myocardial infarction // Int J Cardiol. – 2014. – 177: e10-e12.
- Del Rincon I., Williams K., Stern M.P., Freeman G.L., O’Leary D.H., Escalante A. Association between carotid atherosclerosis and markers of inflammation in rheumatoid arthritis patients and healthy subjects // Arthritis Rheum. – 2003. – 48. – Р. 1833-1840. Dendramis G., Paleologo C., Lo Presti A. et al. Coronary artery ectasia: etiopathogenesis, diagnosis and treatment // G Ital Cardiol (Rome). – 2014. – 15. – Р. 161-169.
- Dendramis G., Paleologo C., Piraino D. et al. Coronary involvement in Churg-Strauss syndrome // Indian heart Journal. 2015. – 67. – Р. 586-588.
- Dennert R., Paasen P. Cardiac involvement in Churg-Strauss syndrome // Arthritis Rheum 2010. – 62 (2). – Р. 627-634.
- d’Ersu E., Ribi C., Monney P. et al. Churg-Strauss Syndrome with cardiac involvement: case illustration and contribution of CMR in the diagnosis and clinical follow-up // International Journal of Cardiology. – 2018. – Vol. 258. – P. 321-324.
- Dimitriadis Z., Esdorn H., Horstkotte D. et al. Coronary spasms, cardiomyopathy, and Churg-Strauss syndrom // Herz. – 2013; DOI 10.1007/s00059-013-3899-7.
- Doherty L., Kumar P., Bexton R. et al. Aortic regurgitation and Churg-Strauss syndrome // QJM. – 2005. – 98 (10). – Р. 772-773.
- Doo K.W., Yong H.S., Kang E.Y. Coronary involvement in Churg-Strauss syndrome: a case report with CT findings // Jpn J Radiol. – 2013. – 31. – Р. 819-822.
- Drogue M., Vergnon J.M., Wintzer B. et al. Prinzmetal’s angina pectoris revealing aneurysm of the right coronary artery during evolution of Churg-Strauss syndrome // Chest. – 1993. – 103 (3). – Р. 978.
- Eleftheriadis D., Eleftheriadis N. Coronary Artery Disease and Systemic Vasculitis: Case Report and Review // Coronary Artery Diseases. – 2012. – P. 281-301.
- Estivals M., Pere M., Colombier D. et al. Churg-Strauss Syndrome Revealed by Acute Coronary Artery Disease: A Case Report // Open J Respiratory Diseases. – 2013. – Vol. 3. – P. 39-43.
Повний список літератури, що включає 145 пунктів, знаходиться у редакції.