9 вересня, 2019
Клінічні маски гіпереозинофільного синдрому: труднощі діагностики (клінічний випадок синдрому Лефлера)
Гіпереозинофільний синдром (ГЕС) зустрічається вкрай рідко і не завжди діагностується. Поширеність ГЕС на сьогодні не з’ясовано через відсутність статистичних даних. Відомо лише те, що чоловіки хворіють частіше за жінок – співвідношення становить 9:1, а їхній вік варіює від 20 до 50 років.
Сімейна гіпереозинофілія успадковується здебільшого за автосомно-домінантним типом. Відповідно до класифікації, розрізняють симптоматичний (СГЕС), або вторинний та ідіопатичний (ІГЕС).
Відтоді, коли 1879 р. P. Ehrlich вперше описав еозинофіл, майже через століття M.J. Chusid сформулював діагностичні критерії ІГЕС, до яких відносяться:
- персистуюча еозинофілія крові при кількості еозинофілів ≥1500 кл/мкл впродовж більш ніж шести місяців;
- поліорганність із циркуляцією у крові або проліферацією у тканинах еозинофілів із проявами еозинофільного фіброзуючого ендокардиту з прогресуючою серцевою недостатністю (СН) та тромбоемболічними ускладненнями;
- відсутність доказів алергічних, паразитарних та інших причин еозинофілії.
Проте наявні труднощі діагностики і лікувальної тактики спонукали до розробки рекомендацій HES 2008, 2014 рр. [1].
Етіологічні чинники ГЕС до кінця не вивчені, а патогенез синдрому – багатогранний. Вплив еозинофілів на тканини і органи зумовлений здатністю підвищеної кількості еозинофілів внаслідок їхньої активації з гранул продукувати токсичні медіатори еозинофільного запалення. Все це призводить до пошкодження органів-мішеней (серця, легень, шкіри, нервової системи, суглобів, травного тракту), епітелію судин, мієлінових нервових волокон. Через внутрішньосудинну дегрануляцію таке персистування еозинофілів у периферичній крові неминуче веде до ендотеліального та ендокардіального пошкодження з формуванням ендокардіального фіброзу і тромбозів [2].
Тобто процеси еозинофільного запалення тісно переплітаються із такими тромбозу і фіброзу, що й зумовлює складність перебігу та невтішність прогнозу захворювання, а сама дегрануляція еозинофілів відіграє неабияку роль у процесах тромбоутворення. Слід зауважити, що період напівжиття еозинофілів у крові складає 28 годин, тоді як у тканині – тижні.
При цьому виділяють три типи ГЕС [3]:
- із безсимптомним перебігом, протікає субклінічно з повільним розвитком симптомів і позитивною відповіддю на терапію глюкокортикоїдами (ГК);
- супроводжується утворенням еозинофільних інфільтратів у різних органах і системах;
- мієлопроліферативний варіант, характеризується клональною еозинофілією, спленомегалією, гіперклітинним кістковим мозком, анемією, тромбоцитопенією, підвищеним вмістом ціанокобаламіну, плазмовою триптазою.
Пошкодження серця при ГЕС (ендокардичний фіброеластоз, рестриктивна кардіоміопатія) зустрічається у 55‑75% випадків. Типовими є поява задишки, кашлю, набряків на ногах, виникнення аритмій. Розвиток аритмії є свідченням залучення у запальний процес серцево-судинної системи з морфологічно виявленими у біоптатах вогнищ некрозу і збільшеної кількості еозинофілів у ендокарді. Пристінкові тромби можуть бути загрозливим джерелом тромбоемболії [8]. Приблизно впродовж двох років від виникнення гіпереозинофілії формується ендоміокардіальний фіброз із мітральною та трикуспідальною недостатністю. У клінічній картині розрізняють стадійність, етапність, що розтягнуто в часі: некротичну змінює фібротична та тромботична стадії [7]. Перша може перебігати безсимптомно або дебютувати ознаками прогресувальної гострої СН, і це триває тижнями. Приблизно з 10-го місяця захворювання вступає у тромботичну стадію з утворенням тромбів на пошкодженому ендокарді з наступною емболізацією. Фібротична стадія – кінцевий етап розвитку на другому році захворювання – призводить до формування фібротичної тканини як прояву рестриктивної кардіоміопатії в умовах пошкодженого ендо- та міокарда.
Неврологічні прояви ГЕС торкаються ушкоджень як центральної, так і периферичної нервових систем у вигляді дифузної енцефало- й поліневропатії. Дифузна енцефалопатія проявляється здебільшого когнітивними порушеннями, зниженням пам’яті, сплутаністю свідомості з можливою атаксією і судомами. Периферичні поліневропатії супроводжуються симетричними чи асиметричними сенсорними порушеннями, розладами моторики або змішаними сенсорно-моторними проявами. Найбільш прогностично несприятливими є кардіоемболічні ускладнення із розвитком інсульту, транзиторної ішемічної атаки, які часто рецидивують та є резистентними до антикоагулянтної терапії.
Залучення легень у 40‑50% зумовлене еозинофільною інфільтрацією легень і СН. Клінічна картина варіює від ознак підвищеної реактивності бронхів і відсутності змін із боку паренхіми до формування легеневих інфільтратів, що рентгенологічно підтверджено. У 20% відмічається інтерстиціальне пошкодження. За відсутності проявів СН та тромбоемболії легеневої артерії функціональні проби незмінні. На мультиспіральній комп’ютерній томографії (КТ) виявляються вузлові утворення з дифузними ділянками феномену «матового скла». Плевральний випіт діагностується у половині випадків, а бронхоальвеолярний лаваж із еозинофілією – у 70%. Гістологічне дослідження біопсійних матеріалів демонструє деструкцію архітектоніки з ділянками некрозів органів-мішеней. Рідко виникає гострий дистрес-синдром. Тривалий перебіг захворювання формує легеневий фіброз, інфаркт-пневмонію як результат тромбоемболічних ускладнень.
Серед гематологічних змін превалює анемія, рідше – тромбоцитопенія, лейкоцитоз із виразною еозинофілією, гепатоспленомегалія. У деяких пацієнтів може розвиватись еозинофільний лейкоз. Хронічна гіпереозинофілія пошкоджує ендоваскулярну поверхню і призводить до васкулопатії, може ініціювати процеси коагуляції крові з розвитком тромботичних ускладнень.
Серед симптомів пошкодження травного тракту абдомінальний біль, відчуття насиченості, нудота, блювання, діарея. Еозинофільний езофагіт, гастрит, ентероколіт і коліт є частими у клініці ГЕС. Еозинофільні інфільтати, які проникають глибоко у стінку, можуть бути причиною асциту. Еозинофільний езофагіт супроводжують симптоми рефлюксу й дисфагії. Еозинофільне пошкодження шлунково-кишкового тракту потребує біопсійного підтвердження його еозинофільної природи. Нерідкими є еозинофільні гепатити. Серед загальних симптомів на першому плані слабкість, втомлюваність, лихоманка, нічне потовиділення, втрата ваги, біль у суглобах, нижніх кінцівках і м’язах.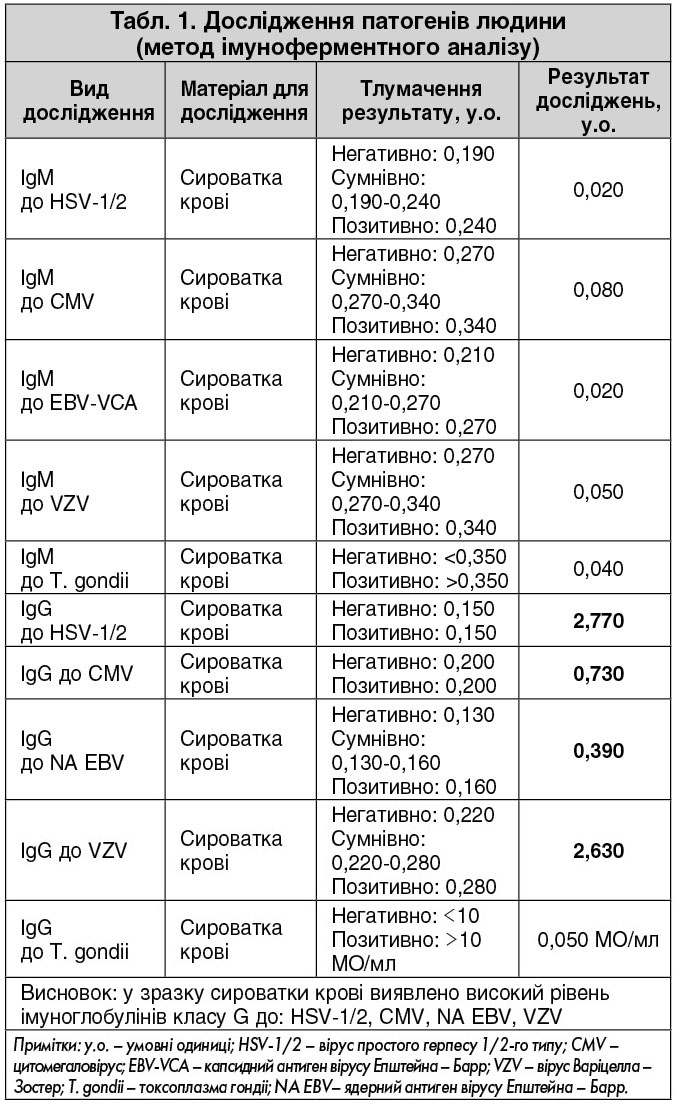
З огляду на вищевикладене, наводимо клінічний випадок ГЕС. У встановленні діагнозу брала участь велика команда фахівців: сімейні лікарі, неврологи, кардіологи, кардіохірурги, радіологи, гематологи.
Клінічний випадок
Пацієнт, 34 роки, поступив у неврологічне відділення клініки «МедБуд» м. Києва 15.11.2017 із попереднім діагнозом: розсіяний склероз, ремітуючо-рецидивуючий перебіг, стадія нестійкої ремісії, EDSS 1.5. Скарги на порушення ходи, головокружіння, зниження пам’яті, концентрації, уваги.
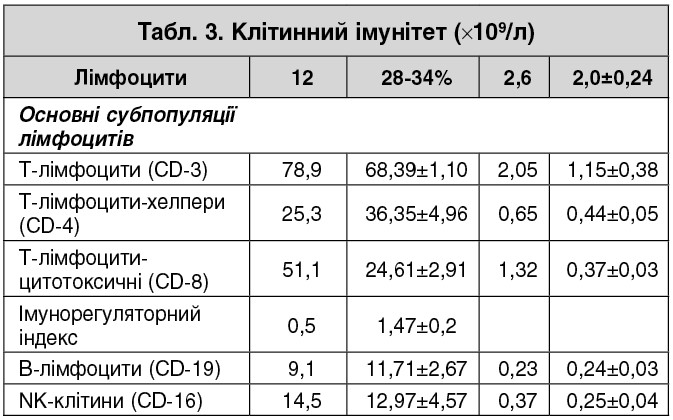
Із анамнезу захворювання. Зі слів пацієнта через два тижні після перебування у Єгипті з’явилися головокружіння, порушення ходи. Проходив амбулаторне і стаціонарне лікування у клініках м. Кременчук, Київському міському центрі лікування розсіяного склерозу, обстежувався в Інституті нейрохірургії імені академіка А.П. Ромоданова НАМН України (м. Київ). Проведено дослідження панелі нейровірусів, динамічна комп’ютерна томографія (КТ), магнітно-резонансна томографія (МРТ) головного мозку (ГМ), імунограма – результат імунологічного обстеження № 2315 від 10.11.2017. Заключення: Звертає на себе увагу лімфоцитоз, лейкоцитоз; гальмування CD‑19-ланки (В-клітинної), велика кількість CD‑8; великий рівень нейроавтоантитіл (табл. 1-3).
Показники функціональної активності імунних клітин:
 проліферативна активність лімфоцитів із різними мітогенами: спонтанна проліферація – 4 (0‑2%); проліферація, викликана Т-клітинним мітогеном ФГА – 36 (55‑65%); простагландин-залежна проліферація (ФГА + індометацин) – 35 (65‑70%); проліферація, викликана В-клітинним мітогеном (декстран-сульфат) – 61 (30‑45%);
проліферативна активність лімфоцитів із різними мітогенами: спонтанна проліферація – 4 (0‑2%); проліферація, викликана Т-клітинним мітогеном ФГА – 36 (55‑65%); простагландин-залежна проліферація (ФГА + індометацин) – 35 (65‑70%); проліферація, викликана В-клітинним мітогеном (декстран-сульфат) – 61 (30‑45%);- фагоцитарна активність нейтрофілів: НСТ-тест: спонтанна – 298,5 (255,5±8,2 у.о.), індукуюча (зимозан) – 31,2 (60‑70%); активність мієлопероксидази нейтрофілів (спонтанна) – 16,4 (18‑23 у.о.);
- адгезивна активність нейтрофілів – 43 (35‑55%).
Гуморальний імунітет: циркулюючі імунні комплекси – 85 (70‑80 у.о.).
Автоімунні реакції (клітинні): індукована нейроавтоантигеном проліферація – 4 (0‑3%); сенсибілізація нейтрофілів до альбуміну – 5 (5‑10%), нейроспецифічних білків: ОБМ – 33 (5‑7%), NSE – 31 (3‑6%).
Автоантитіла до антигенів ГМ: основного білку мієліну – 35,9 (26,05±1,50); білку S‑100‑14,8 (12,60±0,25); нейроспецифічної енолази – 29,8 (23,10±0,35); загального антигена ГМ – 35,1 (29,00±1,50).
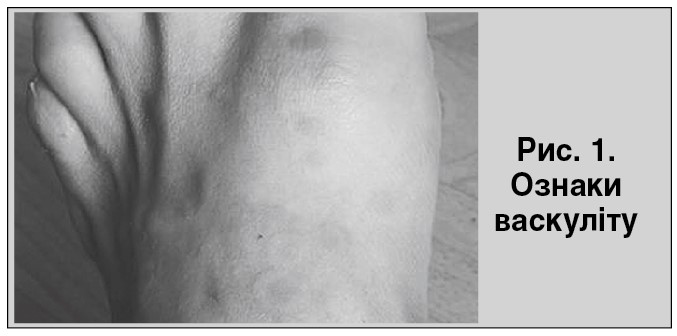 Із анамнезу життя. Пацієнт пригадав, що 2014 р. з’явився висип на шкірі нижніх кінцівок (рис. 1), по медичну допомогу не звертався, висип зник самостійно впродовж певного часу. Отримував терапію згідно зі стандартами лікування розсіяного склерозу в умовах неврологічного стаціонара лікарні «МіськБуд». Пульс-терапія: солу-медрол по 1000 мг, цитостатики в/в, IgG в/в. Після проведеного лікування через три дні з’явилися набряки на ногах, задишка, важкість у правому підребер’ї, збільшився в об’ємі живіт.
Із анамнезу життя. Пацієнт пригадав, що 2014 р. з’явився висип на шкірі нижніх кінцівок (рис. 1), по медичну допомогу не звертався, висип зник самостійно впродовж певного часу. Отримував терапію згідно зі стандартами лікування розсіяного склерозу в умовах неврологічного стаціонара лікарні «МіськБуд». Пульс-терапія: солу-медрол по 1000 мг, цитостатики в/в, IgG в/в. Після проведеного лікування через три дні з’явилися набряки на ногах, задишка, важкість у правому підребер’ї, збільшився в об’ємі живіт.
Об’єктивно. Загальний стан хворого середньої тяжкості. Шкіра бліда, акроціаноз губ. Периферичні лімфатичні вузли не пальпуються. Верхівковий поштовх візуалізується, пальпується у V міжребер’ї по lin. medioclavicularis sinistra – розлитий, резистентний, помірно високий; пальпується серцевий поштовх, гепатоюгулярний рефлекс – позитивний, венний пульс – позитивний. Зміщення меж серця вправо, ліва межа по lin. medioclavicularis cor, діяльність ритмічна, тони звучні, тахікардія, систолічний шум на верхівці, пульс – 105 уд./хв, ритмічний, артеріальний тиск (АТ) 135/80 мм рт. ст. Над легенями вкорочення перкуторного тону нижче кута лопаток. Аускультативно: дихання везикулярне, послаблене у нижніх відділах з обох боків. Живіт збільшений в об’ємі, позитивний симптом флуктуації, наявна асцитична рідина. Печінка збільшена (+4 см), помірно чутлива, заокруглена; при перкусії селезінка збільшена, не пальпується.
Лабораторно-інструментальні методи обстеження. Загальний аналіз крові від 28.11.2017: лейкоцити – 20,2×109/л; лейкоцитарна формула: еозинофіли – 26%, паличкоядерні – 8%, сегментоядерні – 39%, лімфоцити – 20%, моноцити – 7%, еритроцити (RBC) – 4,77×109/л, гемоглобін – 147 г/л, тромбоцити – 196×109/л, швидкість осідання еритроцитів (ШОЕ) – 3 мм/год. Із наведеного аналізу крові увагу привертає еозинофілія – 26%. Із даних амбулаторної картки пацієнта при обстеженні в м. Кременчук у загальному аналізі крові за жовтень 2017 р. також була наявна еозинофілія – 20%.
Загальний аналіз сечі від 01.12.2017: питома вага – 1018 г/л, лейкоцити – 4 у п/з, білок, глюкоза, жовчні пігменти – відсутні.
Біохімічний аналіз крові від 28.11.2017: білірубін загальний – 20,2 мкмоль/л, білірубін прямий – 4,3 мкмоль/л, білірубін непрямий – 15,9 мкмоль/л; аланінамінотрасфераза (АлАТ) – 60 Од/л; аспартатамінотрасфераза (АсАТ) – 20 Од/л; тимолова проба – 1,1 опт.од., гама-глутаматтрансфераза (ГГТ) – 56,8 Од/л, фосфатаза лужна – 63,3 Од/л, лактатдегідрогеназа (ЛДГ) – 548 Од/л, сечовина – 11,6 ммоль/л, креатинін – 98,1 мкмоль/л, загальний білок – 56,2 г/л, альбумін – 39,5 г/л; Д-димер – 600 нг/мл, прокальцитонін – 0,06 (N≤0,1нг/мл), с-реактивний білок (СРБ) – 41,7 мг/л, pANCA, cANCA ≤20 (N≤20).
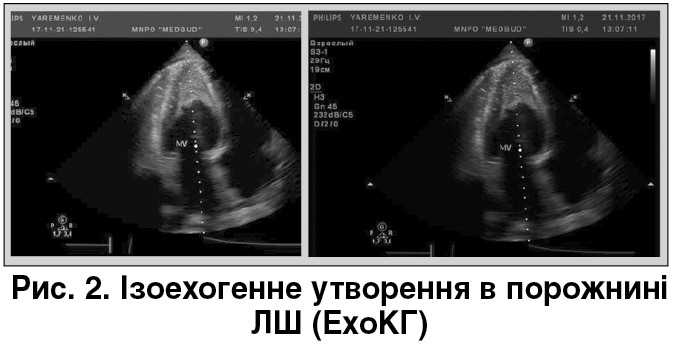 ЕхоКГ від 21.11.2017 показала клапанні структури без змін. Дилатація лівого передсердя (ЛП) – 4,8 см (систола) і незначна лівого шлуночка (ЛШ) – кінцевий діастолічний розмір (КДР) – 6,2 см, кінцевий систолічний розмір (КСР) – 4,7 см, кінцевий діастолічний об’єм (КДО) – 194 мл, кінцевий систолічний об’єм (КСО) – 72,9 мл. Фракція викиду (ФВ) – 62% (скоротлива здатність міокарда не знижена). Легенева гіпертензія – 52 мм рт. ст. (помірна). Діастолічна дисфункція ЛШ за рестриктивним типом, гіпертрофія ЛШ за ексцентричним типом. У порожнині ЛШ, займаючи третину, візуалізується ізоехогенне утворення, що тісно прилягає до стінки міокарда (міксома? рабдоміома?) (рис. 2).
ЕхоКГ від 21.11.2017 показала клапанні структури без змін. Дилатація лівого передсердя (ЛП) – 4,8 см (систола) і незначна лівого шлуночка (ЛШ) – кінцевий діастолічний розмір (КДР) – 6,2 см, кінцевий систолічний розмір (КСР) – 4,7 см, кінцевий діастолічний об’єм (КДО) – 194 мл, кінцевий систолічний об’єм (КСО) – 72,9 мл. Фракція викиду (ФВ) – 62% (скоротлива здатність міокарда не знижена). Легенева гіпертензія – 52 мм рт. ст. (помірна). Діастолічна дисфункція ЛШ за рестриктивним типом, гіпертрофія ЛШ за ексцентричним типом. У порожнині ЛШ, займаючи третину, візуалізується ізоехогенне утворення, що тісно прилягає до стінки міокарда (міксома? рабдоміома?) (рис. 2).
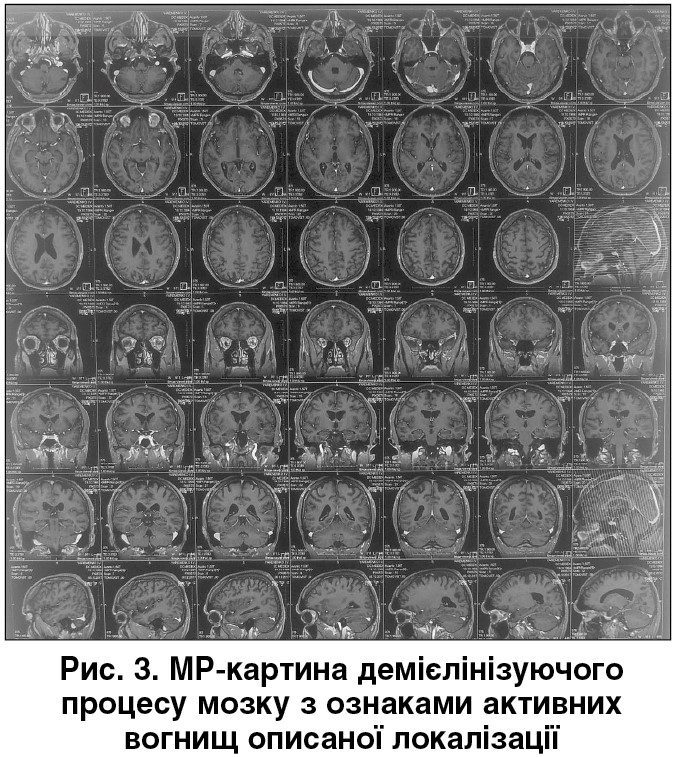 МРТ мозку від 05.12.2017: у проекції білої речовини півкуль великого мозку, юкстакортикально перивентрикулярної області бічних шлуночків мозку визначаються перивентрикулярні та субкортикальні вогнища без чітких контурів, округлої та веретеноподібної форми, умовним діаметром до 0,3‑1,3 см. Висновок: МР-картина демієлінізуючого процесу головного мозку (MS) з ознаками активних вогнищ описаної локалізації (рис. 3).
МРТ мозку від 05.12.2017: у проекції білої речовини півкуль великого мозку, юкстакортикально перивентрикулярної області бічних шлуночків мозку визначаються перивентрикулярні та субкортикальні вогнища без чітких контурів, округлої та веретеноподібної форми, умовним діаметром до 0,3‑1,3 см. Висновок: МР-картина демієлінізуючого процесу головного мозку (MS) з ознаками активних вогнищ описаної локалізації (рис. 3).
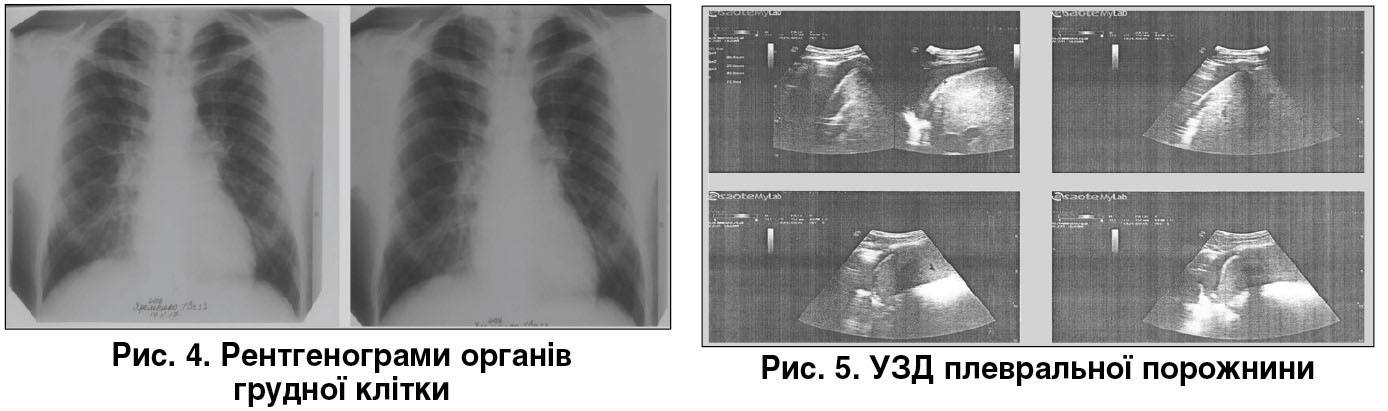
Динаміка серії рентгенограм органів грудної клітки від 17.11.2017 (рис. 4): рівень рідини не візуалізується через незначну кількість. Інформативнішим є ультразвукове дослідження (УЗД) плевральних порожнин.
УЗД плевральної порожнини від 17.11.2017: визначається вільна рідина сумарним об’ємом: справа – 100‑200 мл, зліва – 50‑100 мл, рідина однорідна (рис. 5).
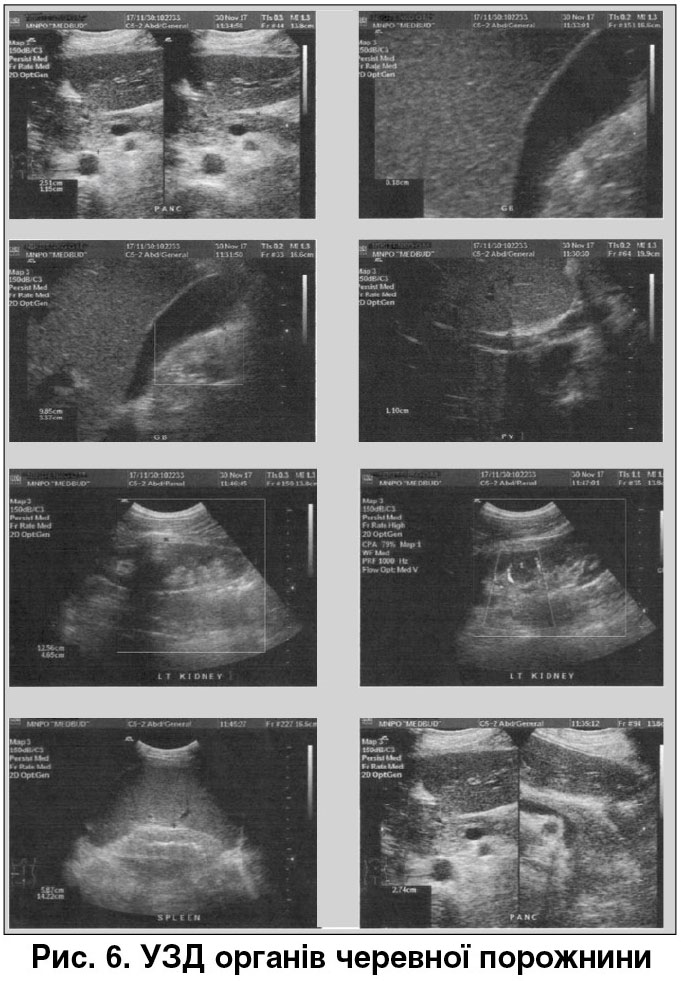
УЗД органів черевної порожнини від 17.11.2017: при УЗД органів черевної порожнини виявлені ознаки гепатолієнального синдрому (рис. 6).
ЕКГ від 30.11.2017: інфарктоподібна крива, неспецифічні зміни інтервалу ST на тлі синусового, правильного ритму із частотою серцевих скорочень (ЧСС) 64 уд./хв (хворий отримував дигоксин) (рис. 7).
 МРТ серця від 27.11.2017 (рис. 8): МР-дані на користь парієтального фібропластичного еозинофільного ендокардиту Лефлера; гідроперикард малого об’єму; правобічний гідроторакс.
МРТ серця від 27.11.2017 (рис. 8): МР-дані на користь парієтального фібропластичного еозинофільного ендокардиту Лефлера; гідроперикард малого об’єму; правобічний гідроторакс.
Встановлений діагноз: рестриктивна кардіоміопатія (хвороба Лефлера), ендоміокардіальний фіброеластоз, тромбо-фібротична стадія, тромб верхівки серця. Мітральна регургітація, часта політопна ектрасистолія, СН ІІБ (двобічний гідроторакс, гідроперикард, асцит). Кардіоемболічний підтип ішемічного інсульту?
Суперечки щодо неврологічного діагнозу тривають. Із погляду кардіолога існує джерело емболізації – тромб ЛШ. Для кардіоемболічних інсультів притаманні часті рецидиви із новою локалізацією вогнищ порівняно з атеротромботичним підтипом ішемічного інсульту. На нашу думку, такі множинні структури ГМ зумовлені процесами емболізації.
Призначене лікування: ГКС (60 мг преднізолону), цитостатики (200 мг ендоксану), низькомолекулярний гепарин (0,8 мг еноксапарину двічі на день п/ш), інгібітори ангіотензинперетворювального ферменту (іАПФ), діуретики, дигоксин. На тлі терапії відмічалася позитивна динаміка. Зменшилися клінічні прояви СН, набрякового синдрому. За наполяганням пацієнта проведено консультації з кардіохірургами із приводу оперативного втручання. Зважаючи на високий ризик несприятливого прогнозу щодо оперативного втручання, питання хірургічного лікування було зняте.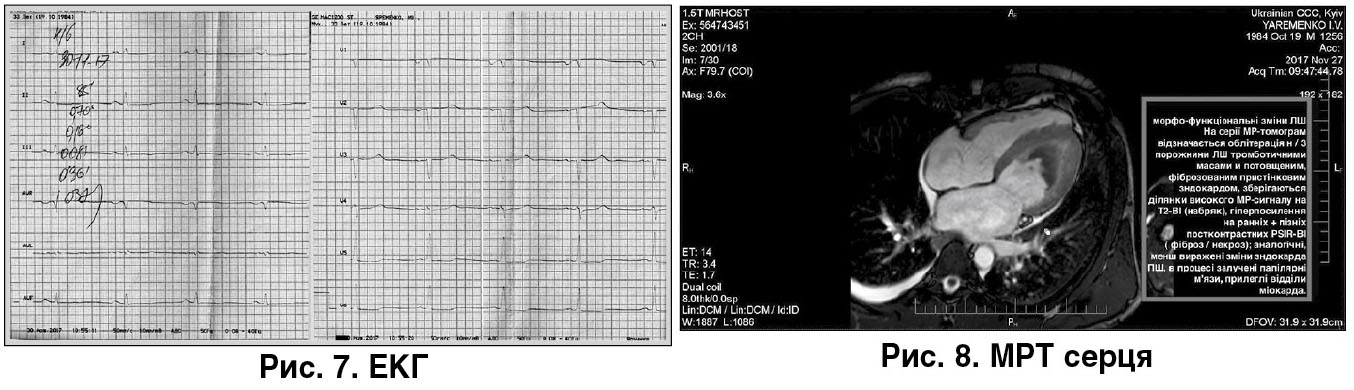
 Рекомендовано продовжити лікування в амбулаторних умовах: фізичні кардіонавантаження під контролем пульсу (≤90 уд./хв), метилпреднізолон за схемою із поступовим зниженням дози, 25 мг/добу метотрексату один раз на тиждень, 0,4 мг клексану 2 р/добу з переходом на 0,4 мг/добу впродовж 12 місяців. З урахуванням результатів коагулограми, 75 мг курантилу 3 р/добу тривало, 200 мг/добу кордарону з наступною відміною після результатів холтеру ЕКГ, 20 мг нольпази на ніч, 5 мг фолієвої кислоти один раз на тиждень не раніше ніж через 48 годин після прийому метотрексату, контроль загального аналізу крові з формулою та біохімічного аналізу крові раз на місяць.
Рекомендовано продовжити лікування в амбулаторних умовах: фізичні кардіонавантаження під контролем пульсу (≤90 уд./хв), метилпреднізолон за схемою із поступовим зниженням дози, 25 мг/добу метотрексату один раз на тиждень, 0,4 мг клексану 2 р/добу з переходом на 0,4 мг/добу впродовж 12 місяців. З урахуванням результатів коагулограми, 75 мг курантилу 3 р/добу тривало, 200 мг/добу кордарону з наступною відміною після результатів холтеру ЕКГ, 20 мг нольпази на ніч, 5 мг фолієвої кислоти один раз на тиждень не раніше ніж через 48 годин після прийому метотрексату, контроль загального аналізу крові з формулою та біохімічного аналізу крові раз на місяць.
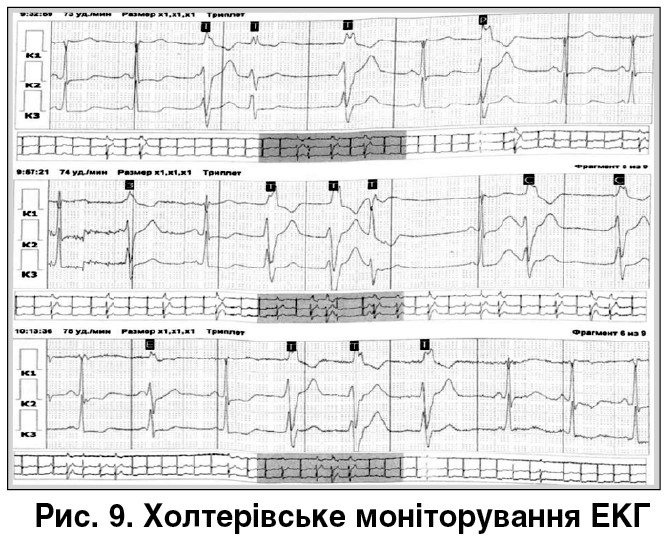
За динамічного спостереження при проведенні холтерівського моніторування ЕКГ від 09.02.2018: на тлі прийому кордарону по 800 мг/добу виявлено нерегулярний синусовий ритм, ЧСС 44‑126 уд./хв. Поодинока передсердна екстрасистолія, атріовентрикулярна блокада I ст., подовження PQ 417‑760 мс. Часті політопні шлуночкові екстрасистоли: куплети, триплети, тригіменія, постійна горизонтальна і косонизхідна депресія інтервалу ST, P pulmonale (рис. 9).
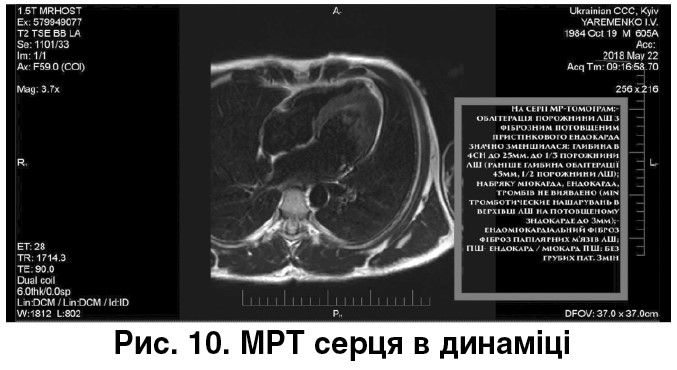 Динаміка МРТ через шість місяців від 22.05.2018 (рис. 10). Висновок: виразна позитивна динаміка, даних щодо «активного» ендоміокардіального запального процесу не отримано; відсутні внутрішньошлуночкові тромби; розміри порожнини ЛШ, ударний об’єм ЛШ збільшилися; загальну скоротливість ЛШ не порушено; нормалізація систолічної функції ПШ, розмірів передсердь.
Динаміка МРТ через шість місяців від 22.05.2018 (рис. 10). Висновок: виразна позитивна динаміка, даних щодо «активного» ендоміокардіального запального процесу не отримано; відсутні внутрішньошлуночкові тромби; розміри порожнини ЛШ, ударний об’єм ЛШ збільшилися; загальну скоротливість ЛШ не порушено; нормалізація систолічної функції ПШ, розмірів передсердь.
Лікування на сьогодні: еноксапарин у дозі 0,4 мг/добу, надалі 0,2 мг/добу підшкірно тривало, з наступним переходом на варфарин; метилпреднізолон із поступовим зниженням дози за схемою: до 12 мг/добу – три тижні; потім 10 мг/добу – чотири тижні; 8 мг/добу – шість тижнів із подальшим зниженням до відміни; метотрексат у дозі 25 мг на тиждень.
Підсумки
Як відомо, прогноз у пацієнтів із синдромом Лефлера є невтішним. Загальний прогноз в осіб із ендокардитом Лефлера є поганим і залежить від ураженої ділянки серця. Для захворювання хоча і притаманний повільний розвиток із залученням різних органів і систем, прогресування правошлуночкової та лівошлуночкової СН, тромбоемболізація в різні судинні басейни визначає фінал хвороби. Раптова смерть і синкопе не настільки поширені, як за інших причин рестриктивної кардіоміопатії.
Насамкінець хотілося б зауважити, що ГЕС може дебютувати різноманітними клінічними масками залежно від превалювання пошкодження органів-мішеней (серце, легені, мозок, травний тракт, шкіра). Хоча маніфестація захворювання у нашому клінічному випадку почалась із неврологічної симптоматики, причиною цього було еозинофільне запалення з наступним тромбоутворенням. Знання особливостей клінічної симптоматики можуть стати важливим знаряддям при завчасному встановленні діагнозу лікарями різного фаху, надавши шанс пацієнту на його порятунок і виживання.
Література
- Bjerrum O.W., Pelliniemi T.-T., Wadenvik H. Guidelines for the diagnosis and treatment of eosinophilia. Nordic MPD Study Group 2-d version, 2012.
- Rothenberg M.E., Hogan S.P. The eosinophil // Annu Rev immunol, 2006. – 24. – Р. 147-174.
- Blanchard C., Rothenberg M.E. Biology of the eosinophil // Adv Immunology. – 2009. – 101. – Р. 81-121.
- Lykkegaard Andersen C., Vestergaard H., Nongaard P. et al. Eosinophilia – pathogenesis, classification and treatment // Ugeskrift for Laeger (J Dan Med Ass). – 2009. – 171. – Р. 3256-3262.
- Gotlieb J. World Health Organization-defined eosinophilic disorders: 2011 update on diagnosis, risk stratification, and management // Am J Hematol. – 2011. – 86. – Р. 678-688.
- Bochner B.S., Gleich G.J. What targeting eosinophils has taught us about their role in disease // J Allergy Clin Immunol. – 2010. – 126. – Р. 16-25.
- Ommen S.R., Seward J.B., Tajik A.J. Clinical and echocardiographic features of hypereosinophilic syndromes // Am J Cardiol. – 2000. – 86. – Р. 110-113.
- Jin X., Ma C., Liu S. et al. Cardiac involvements in hypereosinophilia-associated syndrome: Case reports and a little review of the literature // Echocardiography. – 2017. – 34 (8). – Р. 1242-1246.
- Fletcher S., Bain B. Diagnosis and treatment of hypereosinophilic syndromes // Curr Opinion Hematology. – 2007. – 14. – Р. 37-42.
- Рудіченко В.М., Любченко А.С., Дронюк Л.Р. Рестриктивна кардіоміопатія: літературні дані та власні клінічні спостереження термінального стану // Кардиология от науки к практике. – 2018. – № 5-6. – С. 124-139.
- Alam A., Thampi ., Saba S.G., Jermyn R. Loeffler Endocarditis: A Unique Presentation of Right-Sided Heart Failure Due to Eosinophil-Induced Endomyocardial Fibrosis // Clin Med Insights Case Rep. – 2017. – 10. – 1179547617723643.
- Hernandez C.., Arisha M.J., Ahmad A. et al. Usefulness of three-dimensional echocardiography in the assessment of valvular involvement in Loeffler endocarditis // Echocardiography. – 2017. – 34 (7). – Р. 1050-1056.
- Ogbogu P.U., Rosing D.R., Horne M.K. Cardiovascular manifestations of hypereosinophilic syndromes // Immunol Allergy Clin North Am. – 2007. – 27 (3). – 457-475.
- Gao M., Zhang W., Zhao W. et al. Loeffler endocarditis as a rare cause of heart failure with preserved ejection fraction: A case report and review of literature // Medicine (Baltimore). – 2018. – 97 (11): e0079.
- Dregoesc M.I., Iancu A.C., Lazar A.A. et al. Hypereosinophilic syndrome with cardiac involvement in a patient with multiple malignancies // Med Ultrason. – 2018. – 20 (3). – Р. 399-400.
- Allderdice C., Marcu C., Kabirdas D. Intracardiac Thrombus in Leukemia: Role of Cardiac Magnetic Resonance Imaging in Eosinophilic Myocarditis // CASE (Phila). – 2018. – 2 (3). – Р. 114-117.
- Doyen D., Buscot M., Eker A., Dellamonica J. Endomyocardial fibrosis complicating primary hypereosinophilic syndrome // Intensive Care Med. – 2018. – 44 (12). – Р. 2294-2295.
- Chen Y.W., Chang Y.C., Su C.S. et al. Dramatic and early response to low-dose steroid in the treatment of acute eosinophilic myocarditis: a case report // BMC Cardiovasc Disord. – 2017. – 17 (1). – Р. 115.
- Hayashi S., Isobe M., Okubo I. et al. Improvement of eosinophilic heart disease after steroid therapy: successful demonstration by endomyocardial biopsied specimens. Heart Vessels. – 1999. – 14 (2). – Р. 104-108.
- Gottdiener J.S., Maron B.J., Schooley R.T. et al. Two-dimensional echocardiographic assessment of the idiopathic hypereosinophilic syndrome. Anatomic basis of mitral regurgitation and peripheral embolization // Circulation. – 1983. – 67 (3). – 572-578.
- Valent P., Klion A.D., Horny H.P. et al. Contemporary consensus proposal on criteria and classification of eosinophilic disorders and related syndromes // J Aller Clin Immunol. – 2012. –130. – Р. 607-612 e9.
- Mankad R., Bonnichsen C., Mankad S. Hypereosinophilic syndrome: cardiac diagnosis and management // Heart (British Cardiac Society). – 2016. – 102. – Р. 100-106.
- Ogbogu P.U., Rosing D.R., Horne M.K. 3rd. Cardiovascular manifestations of hypereosinophilic syndromes // Immunol Aller Clin North Am. – 2007. – 27. – Р. 457-475.
- Cogan E, Roufosse F. Clinical management of the hypereosinophilic syndromes // Expert Rev Hematol. – 2012. – 5. – Р. 275-289.
Спецвипуск «Клінічні випадки та сценарії у невідкладній кардіології», вересень 2019 р