10 вересня, 2019
Гипертензивный криз, сопровождающийся острой сердечной недостаточностью
Острая сердечная недостаточность (ОСН) – одно из наиболее частых осложнений при сердечно-сосудистой патологии, которое характеризуется высоким уровнем смертности. По данным литературы, внутригоспитальная летальность у пациентов с ОСН на протяжении девяти суток после выписки из стационара составляет 9-15%, уровень 30-дневной смертности – 6,5%, а смертность в течение года – 30%.
Пациент, 63 года, с повышением уровня артериального давления (АД) до 165/105 мм рт. ст., жалобы (в настоящий момент) на нехватку воздуха в покое, сухой надсадный кашель. Положение вынужденное, полусидя, не спит в горизонтальном положении две ночи. Пульс напряженный, ритмичный с частотой 112 уд./мин, тоны сердца глухие с наличием систолического шума в пятой точке и на верхушке с проведением в подмышечную область. Влажные хрипы над обоими легкими выше угла лопатки, частота дыхательных движений (ЧДД) – 28-30/мин, SpO2 – 85%.
Анамнез: перенесенный два года назад инфаркт миокарда (ИМ) с проведением фибринолитической терапии, артериальная гипертензия (АГ) и сахарный диабет (СД) 2-го типа в течение 10 лет.
Лечение: ацетилсалициловая кислота (АСК) – 100 мг, аторвастатин – 20 мг, рамиприл – 5 мг, метопролола сукцинат – 50 мг, метформин (пролонгированная форма) – 1000 мг.
Был исключен диагноз кардиогенного шока и дыхательной недостаточности, требующей поддержки, и перед нами встал вопрос о том, что являлось ведущим фактором, вызвавшим обострение СН.
Факторы, обусловливающие возникновение ОСН, многочисленны:
- острый коронарный синдром (ОКС);
- тахиаритмии (например, фибрилляция предсердий [ФП] и желудочковая тахикардия);
- высокий уровень АД;
- инфекция (например, пневмония, инфекционный эндокардит, сепсис);
- несоблюдения режима приема жидкости, препаратов, потребления соли;
- брадиаритмия;
- токсические вещества (алкоголь, наркотики);
- лекарственные средства (например, нестероидные противовоспалительные препараты, кортикостероиды, вещества с негативным инотропным эффектом, кардиотоксическая химиотерапия);
- обострение хронического обструктивного заболевания легких;
- легочной эмболизм;
- хирургические вмешательства и периоперативные осложнения;
- усиленное симпатическое влияние, стресс-индуцированная кардиомиопатия;
- метаболические/гормональные расстройства (например, тиреоидная дисфункция, диабетический кетоз, дисфункция надпочечников, беременность и послеродовые осложнения);
- цереброваскулярные осложнения (инсульт);
- острые механические причины: разрыв миокарда как осложнение ОКС; травма грудной клетки или вмешательства на сердце; острая клапанная недостаточность, вторичная по отношению к эндокардиту; аортальная диссекция или тромбоз.
При первичном осмотре необходимо проведение комплексного обследования – как инструментального, так и лабораторного. Методы необходимых при ОСН обследований перечислены в рекомендациях Европейского общества кардиологов (ESC, 2016). Они включают обязательное определение уровня натрийуретического пептида в плазме (BNP, NT-proBNP или MR-proANP) у всех пациентов с острой одышкой и ожидаемой ОСН, для того чтобы помочь дифференцировать ОСН с некардиальными случаями острой одышки (класс рекомендации I, уровень доказательности А). При поступлении в стационар всем больным с подозрением на ОСН также рекомендуется проведение 12-канальной электрокардиографии (ЭКГ), рентген грудной клетки для оценки признаков застоя в легких и определения других кардиальных и некардиальных заболеваний, которые могут вызывать или способствовать развитию симптомов (І, С).
Среди лабораторных исследований – определение уровней сердечных тропонинов, азота мочевины, креатинина крови, электролитов (натрия, калия), глюкозы; а также развернутый анализ крови, биохимический анализ (печеночные ферменты) и определение уровня тиреотропного гормона. Проведение эхокардиографии (ЭхоКГ) рекомендовано немедленно у гемодинамически нестабильных пациентов с ОСН и в течение 48 ч, если сердечные структуры и функции не изучались или могли измениться со времени предыдущего исследования (І, С).
Результаты лабораторных исследований. Креатинин –125 мкмоль/л, скорость клубочковой фильтрации – 52 мл/мин/1,73 м2 (снижение функции почек). Тесты на кардиоспецифические ферменты: креатинфосфокиназа-MB – 15 Ед/л; тропонин Т – 0,02 нг/л. Общий анализ крови: Hb – 121 г/л, лейкоциты – 10,5×109 Ед/л, тромбоциты – 385 тыс. Ед/мкл. Глюкоза крови – 13,5 ммоль/л.
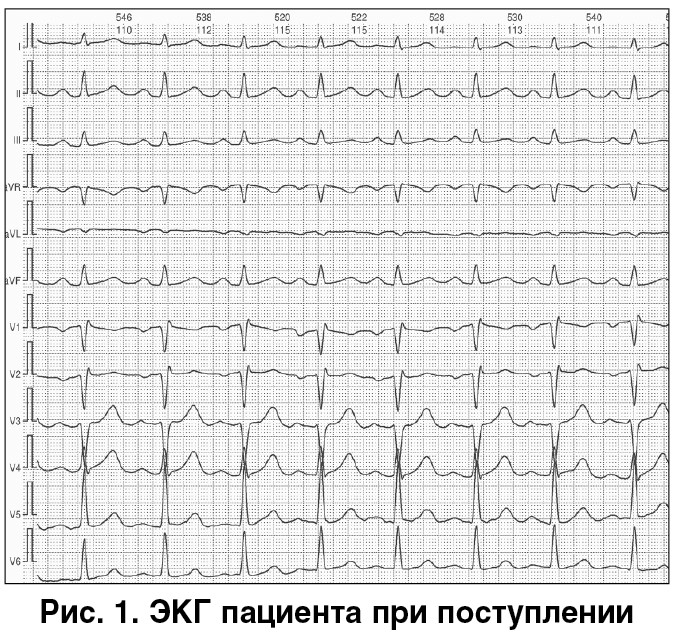 ЭКГ (рис. 1). Не выявлены данные, свидетельствующие о наличии ОКС.
ЭКГ (рис. 1). Не выявлены данные, свидетельствующие о наличии ОКС.
ЭхоКГ (рис. 2). Выявлена дилатация полости левого желудочка (ЛЖ) (конечно-диастолический объем – 192 мл) с систолической дисфункцией (фракция выброса [ФВ] – 32%). Выраженная митральная регургитация с дилатацией левого предсердия (4,6 см). Гипертрофия миокарда ЛЖ (толщина межпредсердной перегородки – 1,35 см, задней стенки ЛЖ – 1,41 см) и нарушение сегментарной сократимости в виде акинеза передней, перегородочной и верхушечной областей. Диастолическая функция нарушена до рестриктивного типа. Е/А – 3,7. Е/е’ – 15,8.
УЗИ легких (рис. 3; выбор в пользу УЗИ связан с возможностью более быстрого проведения по сравнению с рентгенографией при сопоставимой информативности обоих методов при ОСН): выявлены линии В+, что является прямым признаком отека легких. Дополнительно УЗИ легких позволяет исключить гидроторакс и пневмоторакс.
Таким образом, мы располагали достаточно убедительными данными в пользу диагноза ОСН, связанной с повышением АД.
Комментарий
Целями лечения ОСН являются: улучшение гемодинамики и перфузии органов, восстановление оксигенации, уменьшение выраженности симптомов, ограничение повреждения сердца и почек, профилактика тромбоэмболизма, минимализация продолжительности пребывания в ОРИТ.
Все поставленные вопросы решаются с помощью:
- кислородотерапии, неинвазивной вентиляции легких (табл. 1);
- снятия симптомов одышки и возбуждения (морфин, диазепам) (табл. 2);
- диуретической терапии (табл. 3);
- вазодилататоров (табл. 4);
- антикоагулянтов (табл. 5).
Вся вышеуказанная терапия четко прописана в рекомендациях и имеет свои классы и уровни доказательств.
Стандартные подходы, описанные в рекомендациях, включают гемодинамические влияния, контроль коагуляции, объема циркулирующей крови, улучшающие поступление кислорода (вентиляционную функцию) и контролирующие психоэмоциональное состояние пациента.
Тем не менее существует еще одна возможность влияния на процессы, происходящие в миокарде при ОСН, – это воздействие на метаболизм миокарда, головного мозга, скелетной мускулатуры. Наиболее точное определение цитопротекции (кардиопротекции) дал Р. Феррари в 1998 г., отметив, что возможности цитопротекции определяются способностью агента или метода вмешательства прямо воздействовать на ишемизированный или реперфузированный миокард и улучшать выживаемость кардиомиоцитов независимо от гемодинамических сдвигов или регуляции коронарного кровообращения.
В последних европейских рекомендациях по ведению пациентов с СН (2016) определенное место отведено лекарственным средствам, напрямую влияющим на метаболические процессы в миокарде, – триметазидину и ранолазину. Однако при использовании препаратов в таблетированной форме невозможно рассчитывать на быстрый эффект при ОСН. Быстрое прямое влияние на метаболизм жизненно важных органов возможно только при применении лекарств немедленного действия. Препаратом, не внесенным в рекомендации, но обладающим свойствами и механизмом действия, которые помогают восстановить метаболические процессы при ОСН, является фосфокреатин.
Основной механизм действия эндогенного фосфокреатина заключается в реакции Ломана – это перенос энергии от места производства (митохондрии) к месту потребления (мышцам, нервной ткани, множеству энергозависимых клеточных каналов, а также для реакций клеточного синтеза).
Эффекты экзогенного фосфокреатина включают:
- Основной физиологический механизм переноса энергии в жизненно важных органах.
- Антитромбоцитарный эффект, связанный с прямым переводом циркулирующего аденозиндифосфата (АДФ) в аденозинтрифосфат (АТФ) посредством передачи фосфатной группы и с предотвращением АДФ-зависимой агрегации тромбоцитов.
- Улучшение пластичности мембраны эритроцитов, а также эффект донатора фосфата для создания АТФ.
- Улучшение структуры и функции мембран клеток за счет ингибирования образования лизофосфоглицеридов и стабилизации клеточной мембраны путем взаимодействия молекулярных зарядов фосфокреатина и полярных головок фосфолипидов на поверхности мембраны.
- Предотвращение выхода аденина из клетки, так как только аденин проникает через клеточную мембрану, а потеря его клеткой ведет к ее гибели при отсутствии возможности получения энергии.
Учитывая механизм действия фосфокреатина и фармакокинетику препарата, можно предполагать быстрый эффект у пациентов с ОСН при в/в введении. После однократной в/в инфузии фосфокреатина происходит быстрое дозозависимое увеличение его содержания в крови до максимального уровня в течение 1-3 мин. Процесс выведения фосфокреатина из организма делится на две фазы. Первая – быстрая – фаза характеризуется временем полувыведения фосфокреатина, составляющим 30-35 мин. Продолжительность второй – медленной – фазы выведения фосфокреатина составляет несколько часов. Содержание фосфокреатина в моче начинает увеличиваться через 30 мин и достигает максимума через 60 мин после введения.
В описываемой клинической ситуации у нас была возможность оценить эффективность применения фосфокреатина при ОСН. Способом оценки влияния болюсного введения фосфокреатина у пациентов с ОСН является проведение динамической ЭхоКГ с последующим анализом методом спекл-трекинга. Острый тест фосфокреатина состоит во в/в введении 2 г фосфокреатина капельно на 50 мл физиологического раствора в течение 30 мин.
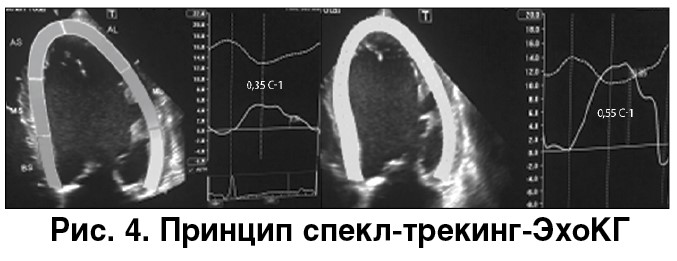 В нашем случае мы проводили ЭхоКГ-контроль исходно до введения фосфокреатина и непосредственно после окончания введения в течение 30 мин. Данные ЭхоКГ оценивали сразу, в процессе проведения исследования: конечно-диастолический объем полости ЛЖ не изменился, несколько улучшились диастолическая функция Е/еI (c 14,2 снизился до 10,3) и ФВ ЛЖ (увеличилась с 18,8 до 25,2%). Более точные данные были получены с помощью метода оценки механизма сокращения ЛЖ в каждом слое миокардиальных волокон – спекл-трекинг-ЭхоКГ. Оценивались продольный, радиальный и циркулярный стрейны, а также их скоростные характеристики. На рисунке 4 показано, какие направления деформации ЛЖ отображают данные виды стрейна. По направлению деформации ЛЖ можно говорить о слоях миокарда, ответственных
В нашем случае мы проводили ЭхоКГ-контроль исходно до введения фосфокреатина и непосредственно после окончания введения в течение 30 мин. Данные ЭхоКГ оценивали сразу, в процессе проведения исследования: конечно-диастолический объем полости ЛЖ не изменился, несколько улучшились диастолическая функция Е/еI (c 14,2 снизился до 10,3) и ФВ ЛЖ (увеличилась с 18,8 до 25,2%). Более точные данные были получены с помощью метода оценки механизма сокращения ЛЖ в каждом слое миокардиальных волокон – спекл-трекинг-ЭхоКГ. Оценивались продольный, радиальный и циркулярный стрейны, а также их скоростные характеристики. На рисунке 4 показано, какие направления деформации ЛЖ отображают данные виды стрейна. По направлению деформации ЛЖ можно говорить о слоях миокарда, ответственных 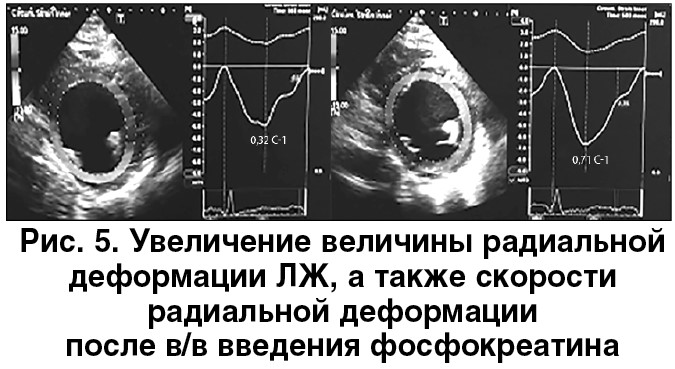 за сокращение. Именно спекл-трекинг-ЭхоКГ может показать наиболее быстрые изменения сократительной функции миокарда. Примером изменения деформации миокарда ЛЖ у пациентов с ОСН при тесте фосфокреатина является увеличение скорости продольного стрейна.
за сокращение. Именно спекл-трекинг-ЭхоКГ может показать наиболее быстрые изменения сократительной функции миокарда. Примером изменения деформации миокарда ЛЖ у пациентов с ОСН при тесте фосфокреатина является увеличение скорости продольного стрейна.
На рисунке 5 показано увеличение величины радиальной деформации ЛЖ, а также скорости радиальной деформации.
В таблице 6 отражены изменения показателей деформации ЛЖ и ее скорости во время проведения в/в теста с фосфокреатином.
Таким образом, данные, полученные при проведении острого в/в теста фосфокреатина при ОСН, демонстрируют потенциальную возможность применения фосфокреатина в комплексном лечении ОСН в сочетании с рекомендованной терапией.
Заключение
Правильная диагностика с ранним выявлением ОСН и причин ее развития являются важными условиями проведения своевременной симптоматической и патогенетической терапии. Комплексная терапия с коррекцией психоэмоционального состояния пациента, гемодинамических параметров, объема циркулирующей крови, вентиляционной функции, а также профилактическая антикоагуляция, в соответствии с рекомендациями, показаны всем больным ОСН. В/в форма фосфокреатина потенциально может быть полезна в комплексной терапии ОСН.
Спецвипуск «Клінічні випадки та сценарії у невідкладній кардіології», вересень 2019 р