25 вересня, 2019
Застосування пантопразолу при серцево-судинних захворюваннях
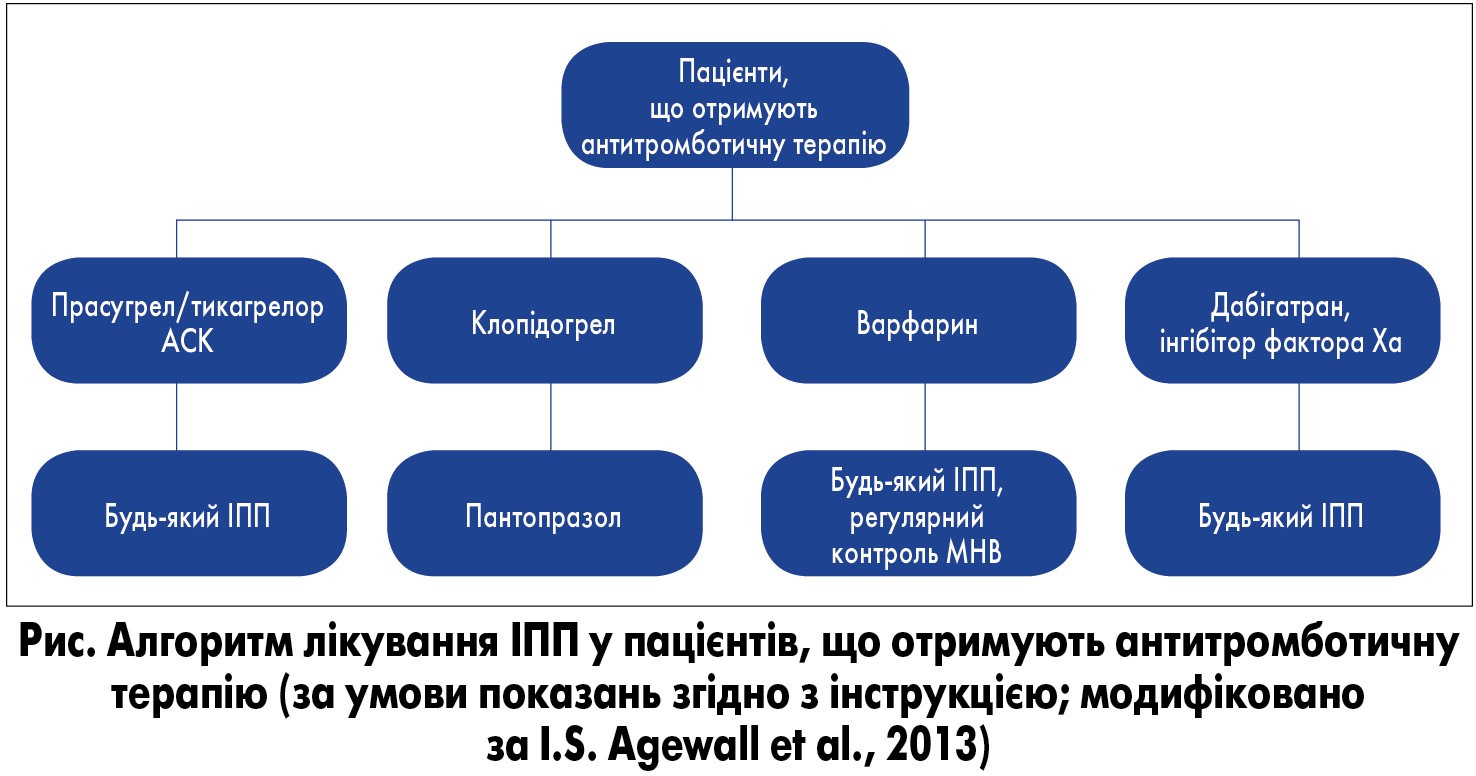
Інгібітори протонної помпи (ІПП) часто призначають пацієнтам із серцево-судинними захворюваннями (ССЗ), що отримують антиагрегантну/антикоагулянтну терапію, одним із найчастіших побічних ефектів якої є розвиток шлунково-кишкових кровотеч (ШКК) [1, 2]. Розуміння показань до призначення ІПП та принципів підбору антисекреторного препарату у пацієнтів з високим кардіоваскулярним ризиком є вкрай важливими для оптимізації терапії з метою зниження ризику розвитку небажаних ефектів від прийому антитромботичних засобів при збереженні їх ефективності.
Механізм дії ІПП ґрунтується на селективному гальмуванні протонної помпи (K+/H+-АТФ-ази), що зумовлює тривале зниження секреції кислоти парієтальними клітинами слизової оболонки шлунка. Варто пам’ятати, що за рахунок зниження кислотності шлунка спостерігається посилення секреції гастрину [3, 4]. Найбільш поширені показання до призначення ІПП включають: лікування виразки шлунка та дванадцятипалої кишки (особливо пов’язаних з інфекцією Helicobacter pylori), гастроезофагеальна рефлюксна хвороба (ГЕРХ) та профілактика її рецидивів, лікування синдрому Золлінгера – Еллісона. ІПП також використовують для профілактики виразкової хвороби при тривалому застосуванні нестероїдних протизапальних препаратів [1-3]. Крім того, ІПП дають змогу ефективно знижувати ризик розвитку ускладнень з боку шлунково-кишкового тракту (ШКТ) у пацієнтів, що отримують антитромботичні препарати та схильні до виникнення таких ускладнень [1, 2].
Одним із найбільш поширених у клінічній практиці ІПП є пантопразол, який характеризується дуже високою ефективністю та забезпечує загоєння виразки шлунка та дванадцятипалої кишки протягом 2-8 тижнів, а усунення симптомів ГЕРХ – через 7 днів [2-4]. Слід також підкреслити, що пантопразол є одним з найбезпечніших ІПП для комбінованого призначення з антиагрегантами, особливо у випадку одночасного застосування з клопідогрелом [1, 2].
Порівняння пантопразолу з іншими ІПП
Після перорального прийому пантопразол повністю всмоктується в травному тракті, а його біодоступність становить 77%. Їжа не впливає на біодоступність препарату, але може вплинути на максимальну затримку його дії. Близько 98% діючої речовини зв’язується з білками плазми крові. Tmax становить приблизно 2-3 год, а T1/2 – всього 1,5 год, однак ці показники не корелюють з реальною тривалістю гальмівного впливу на секрецію соляної кислоти. Метаболізм пантопразолу відбувається тільки у печінці за участю цитохрому P450, метаболіти виводяться головним чином нирками [3, 4]. Істотних взаємодій з іншими препаратами, що метаболізуються системою цитохрому P450, переважно не спостерігається. Проте, як і всі ІПП, пантопразол може впливати на біодоступність інших лікарських засобів, особливо тих, що потребують кислотного середовища для ефективної дії [3, 4]. У клінічній практиці також спостерігався значний вплив пантопразолу та інших ІПП на міжнародне нормалізоване відношення (МНВ), яке значно підвищувалося під час супутньої терапії варфарином. Тому на початку застосування ІПП, особливо у разі призначення цих препаратів у високій дозі, слід контролювати антикоагулянтну терапію для профілактики небезпечних коливань МНВ [1-4].
! Для пантопразолу характерна дуже висока ефективність, що забезпечується його прийомом у дозі 40-80 мг при лікуванні виразкової хвороби, та 40 мг при лікуванні ГЕРХ та ерадикації H. pylory. Доза пантопразолу для підтримувальної терапії та профілактики рецидивів зазвичай не перевищує 20 мг на добу [3, 4].
Лікування усіма ІПП може зумовлювати виникнення таких побічних явищ, як головний біль, запаморочення, біль у животі, діарея, нудота, метеоризм, запори, шкірні висипання. Рідше з’являються слабкість, втома або підвищується рівень печінкових ферментів. Дискомфорт у шлунку найчастіше є наслідком росту кишкової бактеріальної флори на тлі зниження кислотності. Крім того, було продемонстровано достовірну залежність між тривалою терапією ІПП та дефіцитом мікроелементів, особливо магнію. У пацієнтів із цирозом печінки застосування ІПП також може збільшити ризик виникнення спонтанного бактеріального перитоніту [3-4].
Деякі автори припускають несприятливий вплив ІПП на частоту серцево-судинних подій. C.J. Shih та співавт. показали, що застосування ІПП може підвищувати частоту інфаркту міокарда. Подібні спостереження були зроблені також N.H. Shah та співавт. [5-6]. Через відсутність великих рандомізованих досліджень, присвячених цій проблемі, результати зазначених наукових робіт все ще залишаються суперечливими. Крім того, за висновками більшості дослідників, переваги лікування ІПП перевищують потенційний ризик серцево-судинних ускладнень [1, 2, 5].
Показання до застосування ІПП у пацієнтів з ССЗ
В останні роки неухильно зростає кількість пацієнтів, що отримують антитромботичні препарати [7]. У зв’язку з інтенсивним розвитком інвазивної кардіології популяція пацієнтів, що перенесли черезшкірне коронарне втручання (ЧКВ), значно збільшилась. Особливо слід відзначити зростання кількості імплантацій стентів з покриттям, що супроводжуються подвійною антиагрегантною терапією (ПАТ) протягом кількох місяців. До найпоширеніших показань до призначення антитромботичної терапії належать: тромбоемболічна профілактика при фібриляції/тріпотінні передсердь, профілактика та лікування венозної тромбоемболічної хвороби та запобігання її рецидиву, а також профілактика тромбоемболічних подій у пацієнтів зі штучними клапанами серця [7].
Зростає також кількість пацієнтів, що отримують потрійне лікування, тобто окрім двох антиагрегантів додатково приймають антикоагулянт. Переважна кількість таких осіб мають фібриляцію передсердь після проведення планового ЧКВ або після гострого коронарного синдрому. Тривала антитромбоцитарна та/або антикоагулянтна терапія значно підвищує ризик розвитку геморагічних ускладнень [1, 2, 7]. Слід підкреслити, що виникнення геморагічних ускладнень значно погіршує прогноз, збільшує частоту кардіоваскулярних подій та істотно знижує комплаєнс пацієнтів, які отримують антитромботичну терапію.
! За наявності факторів ризику шлунково-кишкових ускладнень пацієнти потребують профілактичних заходів, включаючи фармакологічну профілактику за допомогою ІПП [1, 2, 7]. Таким чином, у всіх пацієнтів, що надалі будуть отримувати антиагрегантну та/або антикоагулянтну терапію, слід оцінювати потенційний ризик виникнення шлунково-кишкових ускладнень.
У 2009 р. національні консультанти у галузі внутрішньої медицини, гастроентерології та кардіології на підставі рекомендацій ACCF/AHA/ACG сформулювали Консенсус з принципів профілактики ускладнень з боку ШКТ під час антитромботичного лікування, в якому особливу увагу приділено наявності факторів ризику й алгоритму прийняття рішень [1]. В останніх рекомендаціях щодо лікування гострого інфаркту міокарда з елевацією сегмента ST було оновлено й уточнено показання до застосування ІПП у пацієнтів, що отримують ПАТ [8]. Терапія ІПП рекомендована пацієнтам з високим ризиком розвитку ШКК, що отримують два антиагрегантних препарати.
Хворі, які приймають три антитромботичні препарати, належать до групи особливо високого ризику розвитку ускладнень з боку ШКТ [1, 2, 7]. Таким пацієнтам рекомендована не тільки рутинна терапія ІПП, а й точна оцінка ішемічного та геморагічного ризику перед призначенням потрійної терапії та визначенням її тривалості, якомога швидший початок потрійної терапії, надання переваги клопідогрелу при виборі антиагрегантного препарату, застосування ацетилсаліцилової кислоти (АСК) у низькій дозі, надання переваги новим пероральним антикоагулянтам (НПАК) перед антагоністами вітаміну К з метою досягнення низького терапевтичного діапазону МНВ (2,0-2,5) [7].
Який ІПП призначити пацієнту, що отримує антитромботичну терапію?
ІПП та антиагреганти
Вибір ІПП у пацієнтів, що отримують антиагрегантну терапію, не повинен бути випадковим. Особливої уваги при цьому потребують пацієнти, які застосовують подвійну антиагрегантну та потрійну антитромботичну терапію, що включає клопідогрел. Клопідогрел є проліками, які проходять двоступеневу конверсію в печінці до активного інгібітора P2Y12. Спочатку за участю ізоферментів CYP1A2, CYP2B6 та CYP2C19 утворюється 2-оксо-клопідогрел, який згодом за участю CYP2B6, CYP2C19 та CYP3A4 окислюється до активного метаболіту, що і зв’язується з рецептором P2Y12 [2-4]. Варто зазначити, що в 1/3 пацієнтів, які отримують клопідогрел, спостерігається поліморфізм CYP2C19, що може бути причиною зниження конверсії проліків до активного метаболіту [7]. На основі результатів багатьох досліджень було показано, що деякі ІПП можуть негативно взаємодіяти з клопідогрелом, і це призводить до зниження його ефективності. Більшість повідомлень стосуються омепразолу, який через пригнічення активності CYP2C19 перешкоджає конверсії проліків до активного метаболіту [9-14]. Насправді всі ІПП, хоча і різною мірою, негативно впливають на антитромбоцитарну активність клопідогрелу.
! Слід підкреслити, що питання несприятливого впливу ІПП на частоту кардіоваскулярних подій у пацієнтів, які отримували клопідогрел, остаточно не вирішене [2].
На думку деяких авторів, тип призначеного ІПП не має істотного впливу на прогноз у таких пацієнтів [2, 15-17]. Так, у дослідженні PRODIGY після проведення ЧКВ у пацієнтів, які отримували ПАТ (АСК + клопідогрел), не спостерігалося вищої частоти виникнення серцево-судинних подій [18]. На думку інших дослідників, додавання ІПП пацієнтам, які отримували ПАТ (АСК + клопідогрел), значно підвищує ризик настання серцево-судинних подій [19-21]. Результати одного дослідження свідчать про вищий ризик розвитку інфаркту міокарда у пацієнтів, що перенесли гострий коронарний синдром та отримували ІПП, за винятком пантопразолу [13]. Варто, однак, зазначити, що до групи пацієнтів, які лікувалися ІПП, найчастіше входили особи з численними супутніми захворюваннями [2]. Однак через відсутність великих рандомізованих досліджень, що враховували б можливості несприятливих фармакологічних взаємодій у пацієнтів, які отримували клопідогрел, при виборі ІПП слід віддавати перевагу саме пантопразолу [1-2].
ІПП та антикоагулянти
Слід окремо розглянути пацієнтів, які отримують потрійну антитромботичну терапію, тобто два антиагреганти та один антикоагулянт (переважно варфарин або НПАК). Ризик розвитку геморагічних ускладнень у цій групі хворих значно підвищується, тому профілактику з використанням ІПП слід починати негайно [1, 2, 7]. В одному з останніх досліджень, проведених у пацієнтів, що отримували АСК, АСК + ривароксабан або тільки ривароксабан, призначення пантопразолу значно знижувало ризик виникнення кровотечі з наявних у пацієнта уражень слизової оболонки ШКТ [25]. Більшість ІПП значно прискорюють абсорбцію варфарину, а також можуть спричиняти коливання рівнів МНВ, яке слід регулярно контролювати під час супутньої терапії АСК. На сьогодні не продемонстровано клінічно значущого впливу ІПП на ефективність антикоагулянтної терапії (як інгібіторами фактора IIa, так і Xa) [2].
Висновки
Профілактика тромбоемболічних подій є важливим напрямом фармакотерапії пацієнтів із різними ССЗ. Проте тривала антитромботична терапія пов’язана зі значним підвищенням ризику виникнення такого ускладнення, як кровотеча. Пацієнти з додатковими факторами ризику становлять групу особливо схильних до геморагічних ускладнень. При необхідності використання у таких хворих ІПП, слід пам’ятати про важливість правильного підбору ІПП для підтримки необхідного балансу між безпекою та ефективністю антитромботичної терапії.
Kowalczys A., Gruchala M. Zastosowanie pantoprazolu w chorobach ukladu sercowo-naczyniowego. Swiat medycyny i farmacji, 8 (219), 2019.
Стаття друкується в скороченні.
Список літератури знаходиться в редакції.
Переклав з польськ. Ігор Кравченко
UA/ (PPIF)/0919/0040
Коментарі експертів
 С.М. Ткач, д. мед. н., профессор, Украинский научно-практический центр эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины, г. Киев
С.М. Ткач, д. мед. н., профессор, Украинский научно-практический центр эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины, г. Киев
Ингибиторы протонной помпы (ИПП) на сегодняшний день являются одними из наиболее применяемых медикаментов в клинике внутренней медицины. В настоящее время ИПП стоят на одном из первых мест среди 5 наиболее распространенных препаратов по количеству потребителей. В настоящее время их применяют приблизительно 5% населения развитых стран, а годовой объем продаж превышает 10 млрд долларов США. Ввиду своей высокой доказанной эффективности и безопасности некоторые ИПП уже перешли в разряд безрецептурных препаратов.
ИПП являются основными препаратами для лечения кислотозависимых заболеваний (ГЭРБ и пищевод Барретта, пептическая язвенная болезнь, синдром Золлингера – Эллисона), НПВП-гастропатий, для эрадикационной терапии Helicobacter рylori, функциональной диспепсии. Кроме того, в последние годы ИПП широко применяются для профилактики желудочно-кишечных кровотечений (ЖКК) у кардиологических больных, получающих антиагрегантную/антикоагулянтную терапию.
Так, в руководстве Европейского общества кардиологов (European Society of Cardiology, ESC) по лечению острого коронарного синдрома у пациентов без персистирующего повышения сегмента ST (2016) ИПП рекомендуются больным, получающим двойную антитромбоцитарную терапию (ДАТТ) и имеющим высокий риск развития ЖКК (отягощенный анамнез по язвенной болезни и желудочно-кишечному кровотечению, прием антикоагулянтов, длительное применение НПВП/кортикостероидов при наличии ≥2 из нижеперечисленных факторов: возраст ≥65 лет, диспепсия, ГЭРБ, инфицирование Helicobacter pylori, хроническое злоупотребление алкоголем). Больные, которые принимают три препарата (2 антиагреганта и один антикоагулянт), относятся к группе особо высокого риска развития осложнений со стороны ЖКТ. Им следует проводить не только рутинную профилактику ИПП, но и точно оценивать риск ишемического и геморрагического инсульта перед назначением тройной терапии и определения ее продолжительности, применять аспирин в низкой дозе, при выборе антиагрегантного препарата отдавать предпочтение клопидогрелу и новым пероральным антикоагулянтам (ривороксабан) перед антагонистами витамина К (варфарин).
Условно классические ИПП делятся на препараты I поколения (омепразол и ланзопразол) и II (пантопразол и рабепразол). Хотя по конечному кислотоснижающему эффекту все ИПП примерно одинаковы, недостатком препаратов I поколения является зависимость их эффективности от генетического полиморфизма печеночного изофермента CYP2C19, ответственного за их метаболизм, а также определенный риск нежелательных межлекарственных взаимодействий при одновременном приеме с некоторыми другими препаратами, также метаболизирующимися изоферментами печеночной системы цитохрома Р450, такими как антиконвульсанты, седативные препараты и миорелаксанты (фенитоин, мефенитоин, диазепам, флунитразепам, фенобарбитал, гексобарбитал, мефобарбитал и карисопродол). К еще более важным субстратам CYP2C19 относятся также антидепрессанты (циталопрам, эсциталопрам, флуоксетин, сертралин, венлафаксин, имипрамин, кломипрамин, тримипрамин, амитриптилин, нортриптилин) и некоторые другие часто применяющиеся лекарства (пропранолол, варфарин и клопидогрел).
При необходимости длительного сочетанного применения ИПП и этих медикаментов в качестве препарата выбора рассматривается ИПП II поколения пантопразол (Контролок), в отношении которого отмечены только единичные случаи лекарственного взаимодействия. Пантопразол также не дает клинически значимых перекрестных реакций с НПВП, в первую очередь с диклофенаком, который является одним из наиболее часто применяющихся препаратов этой группы. Поэтому при высоком риске возникновения НПВП-гастропатий, когда требуется дополнительное превентивное назначение ИПП, препаратом выбора также является пантопразол (Контролок).
 Г.Д. Радченко, д. мед. н., провідний науковий співробітник відділення симптоматичних гіпертензій ДУ ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України, м. Київ
Г.Д. Радченко, д. мед. н., провідний науковий співробітник відділення симптоматичних гіпертензій ДУ ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України, м. Київ
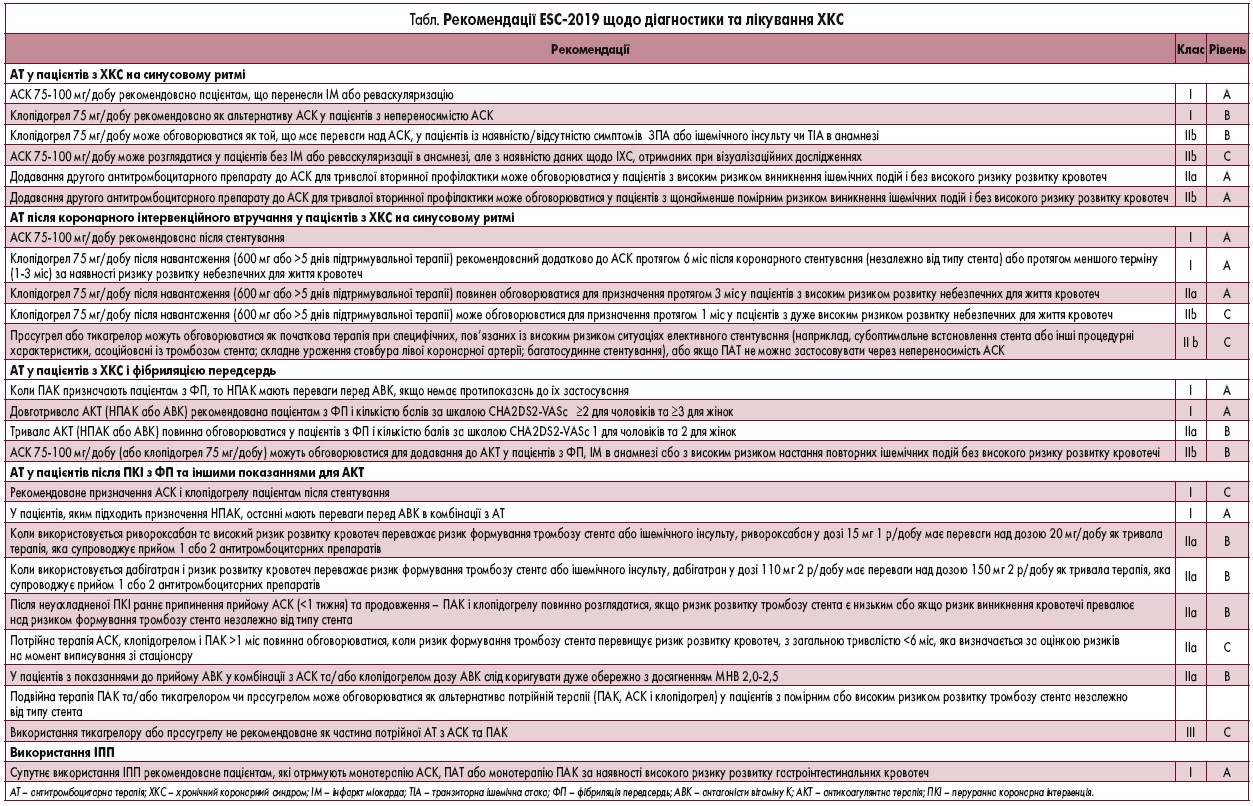
Активація тромбоцитів та їх агрегація є провідним механізмом виникнення коронарного тромбозу, а антитромбоцитарна терапія стала обов’язковою складовою лікування пацієнтів з ішемічною хворобою серця (ІХС). Окрім того, пацієнти з ІХС можуть мати додаткові показання до супутнього застосування пероральних антикоагулянтів (ПАК): фібриляція передсердь (ФП), захворювання периферичних артерій (ЗПА), протезування клапанів серця, профілактика венозних тромбоемболій тощо. При цьому дуже важливо зберегти баланс між запобіганням ішемічним подіям і підвищенням ризику розвитку кровотеч, частота яких значно збільшується при використанні подвійної та потрійної антитромбоцитарної терапії, показання до якої значно розширилися в останні роки (табл.).
Згідно з рекомендаціями Європейського товариства кардіологів (ESC) з діагностики та лікування хронічного коронарного синдрому (ХКС) 2019 р., супутнє використання ІПП показане пацієнтам, які отримують монотерапію АСК, ПАТ або монотерапію ПАК за наявності високого ризику розвитку гастроінтестинальних кровотеч (клас І, рівень А). Ці рекомендації ґрунтуються на результатах досліджень, які продемонстрували, що ІПП значно зменшують вірогідність шлунково-кишкових геморагій. Проте також отримано дані, що свідчать про зменшення ефективності антитромбоцитарної терапії, а особливо клопідогрелу, на фоні використання ІПП. Вважається, що ІПП можуть пригнічувати активність CYP2C19 і таким чином перешкоджати конверсії клопідогрелу до його активного метаболіту інгібітора P2Y12. Це частково поясненює те, що в деяких дослідженнях спостерігалося підвищення ризику виникнення серцево-судинних подій на фоні застосування ІПП порівняно з групою пацієнтів, які не приймали ІПП. Але більшість цих повідомлень стосувалася омепразолу та езомепразолу. Щодо пантопразолу таких даних не отримано, навіть навпаки – в одному досліджені продемонстровано, що ризик виникнення інфаркту міокарда у пацієнтів, які перенесли гострий коронарний синдром, підвищувався на фоні застосування ІПП за винятком пантопразолу. У рекомендаціях з діагностики та лікування ХКС (ESC‑2019) чітко прописано: поєднане призначення омепразолу або езомепразолу з клопідогрелом в цілому не рекомендоване. Сьогодні в Україні найбільш поширеною ПАТ є комбінація АСК саме з клопідогрелом. Останній входить у національний перелік «Доступні ліки» та підлягає державній реімбурсації.
Венозні тромбоемболії є третьою за частотою причиною смерті в США (2015). Їх лікування та профілактика включають застосування ПАК. Всі ПАК поділяють на антагоністи вітаміну К (АВК) та так звані НПАК (інгібітори фактора Х, тромбіну). Але, незважаючи на існування значної кількості препаратів і постійне розроблення нових, частота повторних тромбоемболічних ускладнень залишається відносно високою при тому, що частота кровотеч на тлі прийому ПАК також збільшується. Однією з причин недостатньої ефективності ПАК, а саме АВК, може бути зміна їх всмоктування на фоні застосування ІПП. Необхідно ретельніше контролювати МНВ на фоні супутнього прийому АВК та ІПП. Водночас негативна взаємодія НПАК та ІПП не описана, а в дослідженні COMPASS спостерігалося достовірне зниження ризику шлунково-кишкових кровотеч на фоні застосування пантопразолу.
Таким чином, в еру профілактики тромбоемболічних ускладнень, коли антитромбоцитарна терапія стає більш агресивною, значно зростає ризик виникнення кровотеч, у тому числі шлунково-кишкових. ІПП можуть знижувати ризик останніх, проте прийом деяких ІПП асоціюється із збільшенням ризику розвитку ішемічних ускладнень. Тому важливим є правильний вибір ІПП, який дозволить зберегти оптимальний баланс користь/безпечність.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 3 (53), 2019 р.