2 жовтня, 2019
Современные возможности профилактики бактериальных осложнений ОРЗ у детей
Наиболее раннюю фазу защиты от респираторных инфекций осуществляют механизмы врожденного иммунитета – фагоцитоз, натуральные киллеры, лизоцим и другие компоненты неспецифической резистентности. Они являются важными составляющими элиминации патогенной микрофлоры – вирусов, бактерий, грибов. Поэтому на каждом этапе инфекционного процесса активность компонентов врожденного иммунитета будет обеспечивать быстрое противомикробное действие, не требующее предварительного ознакомления с антигеном. Это особенно актуально для детей, у которых количество контактов с инфекционными агентами еще не достаточно для полноценной работы инструментов приобретенного иммунитета.
Так как функционирование верхнего отдела респираторного тракта предусматривает накопление большого количества антигенного материала для формирования адекватного иммунного ответа, то нередко эти участки слизистых оболочек становятся резервуаром патогенных вирусов и бактерий [1]. При повторных воспалительных процессах инфекционная нагрузка истощает механизмы врожденной защиты, формируя рекуррентный характер инфицирования органов дыхания [2]. Частые острые респираторные заболевания (ОРЗ) у детей являются социальной проблемой – они существенно влияют на качество жизни пациентов.
Спектр бактерий, колонизирующих верхние дыхательные пути, чрезвычайно широк и включает в себя микроорганизмы, которые принято считать обычными возбудителями воспалительного процесса в респираторном тракте (S. pneumoniae, H. influenzae, золотистый стафилококк) [3]. Наиболее активными антигенами на слизистых оболочках дыхательного тракта являются так называемые респираторные патогены [4], к которым, кроме бактерий, относятся также грибы, простейшие и вирусы [5], что нередко приводит к снижению эффективности антибактериальных мероприятий и, в первую очередь, потому требует усиления активности механизмов именно иммунного очищения и исключения – фагоцитоза. При этом показатель незавершенного фагоцитоза <50% может свидетельствовать об удовлетворительном уровне иммунного ответа и благоприятном клиническом прогнозе, а показатель незавершенного фагоцитоза >50% указывает на недостаточность иммунной реакции и является прогностическим признаком развития бактериальных осложнений и хронизации воспалительного процесса [6].
Кроме клеточных элементов, в крови содержатся многочисленные белки, участвующие во врожденной защите. Их эффекты обусловлены обеспечением адекватных воспалительных и иммунных реакций. Некоторые из них, такие как миелопероксидаза, принципиально важны для реализации неспецифического иммунитета. Этот фермент нейтрофилов образует достаточно сильный окислитель гипохлорит-анион, который обладает универсальным бактерицидным действием. При дегрануляции активированных нейтрофилов происходит высвобождение из клетки различных бактерицидных агентов, в том числе миелопероксидазы, которая катализирует окисление галогенидов до соответствующих гипогалоидных кислот, главным образом HOCl и HOBr. Последние являются сильными окислителями, способными модифицировать структуру и изменять функцию многих биологически важных молекул, включая тканевые белки [7].
В условиях частой заболеваемости и, следовательно, воспалительного процесса, будучи катионным белком, миелопероксидаза способна связываться с отрицательно заряженной клеточной мембраной и может вызывать окислительные повреждения тканей организма в очагах воспаления [8]. Это требует соблюдения четких регуляторных параметров ее активации при острых инфекционных процессах, так как снижение ее активности и синтеза приведет к повышенной заболеваемости и развитию бактериальных осложнений, а гиперпродукция-гиперактивация – к воспалительному повреждению тканей с формированием патологических форм воспаления.
Таким образом, защита органов дыхания от инфекционных патогенов происходит за счет сложной системы мукозальных иммунных реакций, включающих факторы как врожденного, так и адаптивного иммунитета. При любой трансформации данных участков иммунной системы слизистых оболочек возникает риск нарушения механизмов противоинфекционной защиты дыхательных путей.
Успех лечения заболеваний респираторного тракта воспалительного генеза зависит от сложных взаимодействий врожденных и приобретенных инструментов локального и системного иммунитета – контроллеров реализации иммунной и воспалительной реактивности организма [9]. Существенной проблемой является то, что активная медикаментозная терапия в детском возрасте может быть губительнее для организма, чем само заболевание. В связи с этим очень важным является использование максимально безопасных лекарственных средств, изготовленных из высококачественного натурального сырья в стандартизированных условиях и обладающих не активирующим или ингибирующим, а регуляторным иммунотропным потенциалом. Этим характеристикам отвечает препарат Имупрет®, профилактическая эффективность которого в отношении снижения количества бактериальных осложнений ОРЗ у детей в осенне-зимний период исследовалась путем анализа показателей врожденного иммунитета.
В связи с этим нами было проведено открытое сравнительное рандомизированное клиническое исследование эффективности и безопасности препарата Имупрет® для профилактики бактериальных осложнений ОРЗ у детей в осенне-зимний период.
Цель работы. Повышение эффективности профилактики бактериальных осложнений ОРЗ у детей в осенне-зимний период путем повышения эффективности врожденного иммунитета при использовании препарата Имупрет®.
Материалы и методы. Под наблюдением находились 60 детей в возрасте от 2 до 6 лет с ОРЗ (острый ринит, фарингит, ларингит, тонзиллит, трахеит), заболевание которых на тот момент длилось уже 1-2 дня. После прохождения скрининга пациенты были разделены на 2 равные группы – основную и группу сравнения (по 30 детей в каждой). В основной группе были дети с ОРЗ, принимавшие препарат Имупрет® в течение 14 дней для профилактики бактериальных осложнений в осенне-зимний период. В группе сравнения состояли дети с ОРЗ, не принимавшие препарат Имупрет®.
Критерии включения. Установленный диагноз ОРЗ, информирование и подписанное родителями согласие; дети обоих полов в возрасте от 2 до 6 лет; пациенты, находящиеся на стационарном и амбулаторном лечении; отсутствие необходимости назначения антибиотикотерапии, а также отсутствие приема антибиотиков в течение 14 предыдущих дней; отсутствие терапии иммуномодулирующими препаратами (такими как интерферон и его индукторы, внутривенные иммуноглобулины, свежезамороженная плазма) в течение 14 предыдущих дней; отсутствие терапии противовирусными препаратами (например, синтетическими аналогами пуриновых нуклеозидов и т.п.) в течение 14 предыдущих дней; отсутствие необходимости приема кортикостероидов; отсутствие терапии кортикостероидами и цитостатиками в течение 14 предыдущих дней; отсутствие показаний к назначению других лекарственных средств с иммуномодулирующим и/или противовирусным действием (помимо разрешенной сопутствующей терапии и исследуемых препаратов) для лечения гриппа или другого ОРЗ.
Критерии исключения. Возраст менее 2 и более 6 лет; несогласие родителей; гиперчувствительность к компонентам исследуемого препарата, которая устанавливается по данным анамнеза; установленный или подозреваемый диагноз первичного иммунодефицита; тяжелое органическое заболевание центральной или периферической нервной системы; соматическое заболевание в стадии декомпенсации; выраженный стеноз гортани (синдром крупа III-IV степени); выраженный бронхообструктивный синдром (III-IV степени); проведение вакцинации менее чем за 21 день до скрининг-визита; любые аутоиммунные заболевания; злокачественные новообразования; туберкулез; наличие любых сопутствующих заболеваний, которые могут влиять на оценку результатов; участие пациента в другом клиническом исследовании в данный момент или менее чем за 30 дней до начала настоящего.
Показание для применения препарата Имупрет®. Предупреждение развития бактериальных осложнений ОРЗ у детей 2-6 лет в осенне-зимний период.
Препарат Имупрет® (Bionorica SE) использовался для перорального применения в форме капель, в 100 мл которых содержится 29 г водно-спиртового экстракта (экстрагент этанол 59%) лекарственных растений: корня алтея (Radix Althaeae) 0,4 г; цветков ромашки (Flores Chamomillae) 0,3 г; травы хвоща (Herba Equiseti) 0,5 г; листьев грецкого ореха (Folia Juglandis) 0,4 г; травы тысячелистника (Herba Millefolii) 0,4 г; коры дуба (Cortex Quercus) 0,2 г; травы одуванчика (Herba Taraxaci) 0,4 г.
Режим дозирования: по 10 капель 5 раз в сутки первые 14 дней, затем следующие 14 дней по 10 капель 3 раза в сутки с небольшим количеством воды после приема пищи.
Группы наблюдения были сопоставимы по возрасту, полу, длительности и тяжести болезни, сопутствующей патологии. Клинический метод включал оценку анамнеза, фенотипическую характеристику ребенка, общеклинические и иммунологические методы обследования.
Кровь для исследования показателей врожденного иммунитета брали из кубитальной вены утром натощак. Определение поглотительной и метаболической функции фагоцитоза производилось путем спонтанного и стимулированного (антигеном Staphylococcus) восстановления нитросинего тетразолия (НСТ-тест), определения индекса завершенности фагоцитоза, фагоцитарного числа, фагоцитарного индекса, индекса НСТ-теста (спонтанного и стимулированного антигеном Staphylococcus), количества натуральных киллеров CD3-, CD16+, CD56+. Активность миелопероксидазы в лизате нейтрофилов оценивали по окислению о-дианизидина при добавлении Н2О2 (перекиси водорода). Нейтрофилы лизировали с помощью 0,1% тритона Х‑100; концентрацию белка в лизате определяли по методу Лоури. Результаты выражали в единицах (ед.): 1 ед. = 1 мкмоль / 5 мин. Удельную активность МПО пересчитывали на 1 г белка клеточного лизата (ед./г).
Для статистической обработки полученных результатов применялся угловой критерий Фишера (для сопоставления двух выборок по частоте встречаемости эффекта). Для анализа состояния ребенка использовалась оценка относительного риска (ОР) формирования исследуемых нарушений. Расчет ОР показывал связь между наличием заболеваний и нарушениями в работе органов и систем. Если ОР=1 – разницы в риске между двумя группами не существует; если ОР<1, значит, в экспериментальной группе событие развивается реже, чем в группе сравнения; если ОР>1, значит, в экспериментальной группе событие развивается чаще, чем в группе сравнения.
Исследование было проведено в соответствии с этическими принципами медицинского исследования, проводимого на людях, которые были приняты Хельсинской декларацией, и Надлежащей клинической практики (GCP).
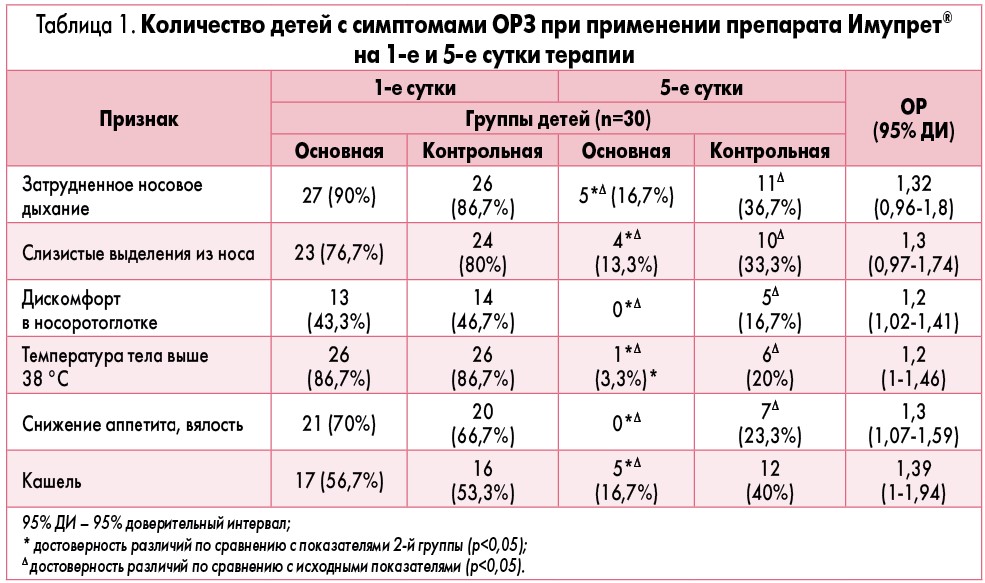
Результаты исследования. Количество детей с динамикой симптомов ОРЗ при применении препарата Имупрет® на 1-е и 5-е сутки терапии представлено в таблице 1.
При сравнении полученных данных детей из основной группы с результатами детей контрольной группы на 5-е сутки терапии было установлено, что при применении капель Имупрет® у статистически значимого количества пациентов с ОРЗ эффективнее купируются затруднение носового дыхания (на 20%; р<0,05), слизистые выделения из носовых ходов (на 20%; р<0,05), дискомфорт в носоротоглотке (на 16,7%; р<0,05), температура тела выше 38 °С (на 16,7%; р<0,05), снижение аппетита и вялость (на 23,3%; р<0,05), кашель (на 23,3%; р<0,05).
Свидетельством эффективности препарата Имупрет® в динамике терапии ОРЗ на 5-е сутки его применения было уменьшение количества пациентов с затрудненным носовым дыханием (на 73,3%; р<0,05), слизистыми выделениями из носовых ходов (на 63,4%; р<0,05), дискомфортом в носоротоглотке (на 43,3%; р<0,05), температурой тела выше 38,0 °С (на 83,4%; р<0,05), снижением аппетита, вялостью (на 70%; р<0,05), кашлем (на 40%; р<0,05).
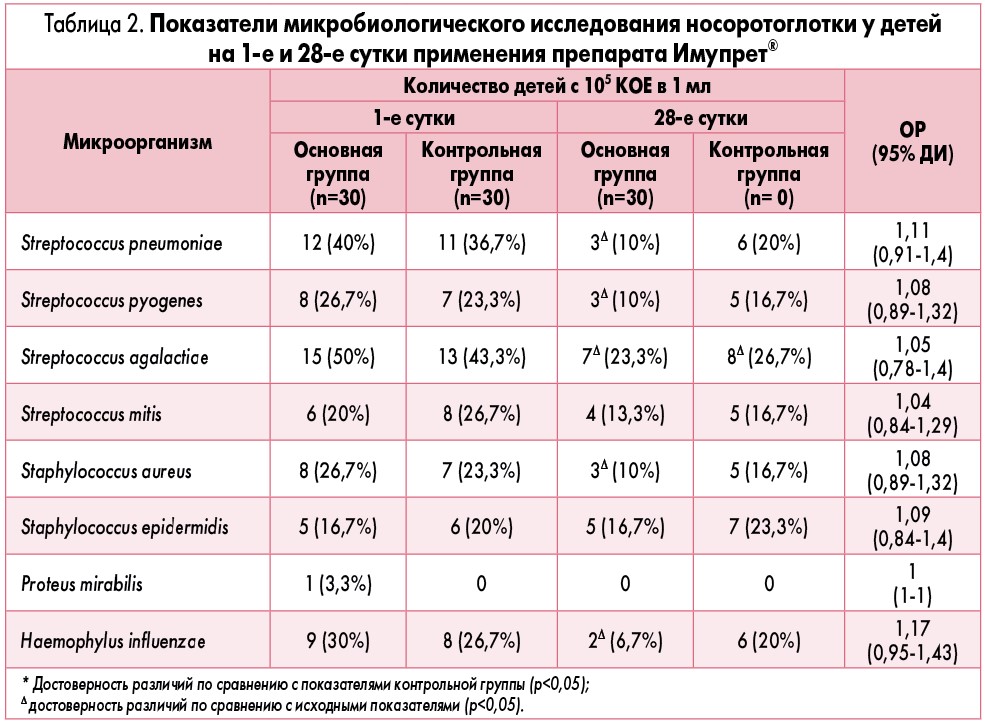
Сравнительная динамика показателей микробиологического исследования носоротоглотки у детей обеих групп наблюдения на 1-е и 28-е сутки применения капель Имупрет® представлена в таблице 2.
По данным микробиологического исследования носоротоглотки, при применении препарата Имупрет® статистически значимо уменьшается количество детей, у которых слизистая оболочка носоротоглотки колонизирована 5 видами патогенных и условно-патогенных микроорганизмов – Streptococcus pneumoniae (на 30%; р<0,05), Streptococcus pyogenes (на 16,7%; р<0,05), Streptococcus agalactiae (на 26,7%; р<0,05), Staphylococcus aureus (на 16,7%; р<0,05) и Haemоphylus influenzae (на 23,3%; р<0,05). Терапия пациентов 2-й группы без применения капель Имупрет® такого эффекта не имела, высокий уровень патологической колонизации сохранялся (кроме Streptococcus agalactiae).
Согласно анализу ОР включение препарата Имупрет® в программу профилактики бактериальных осложнений ОРЗ позволило статистически значимо увеличить вероятность эрадикации патогенных и условно-патогенных микроорганизмов.
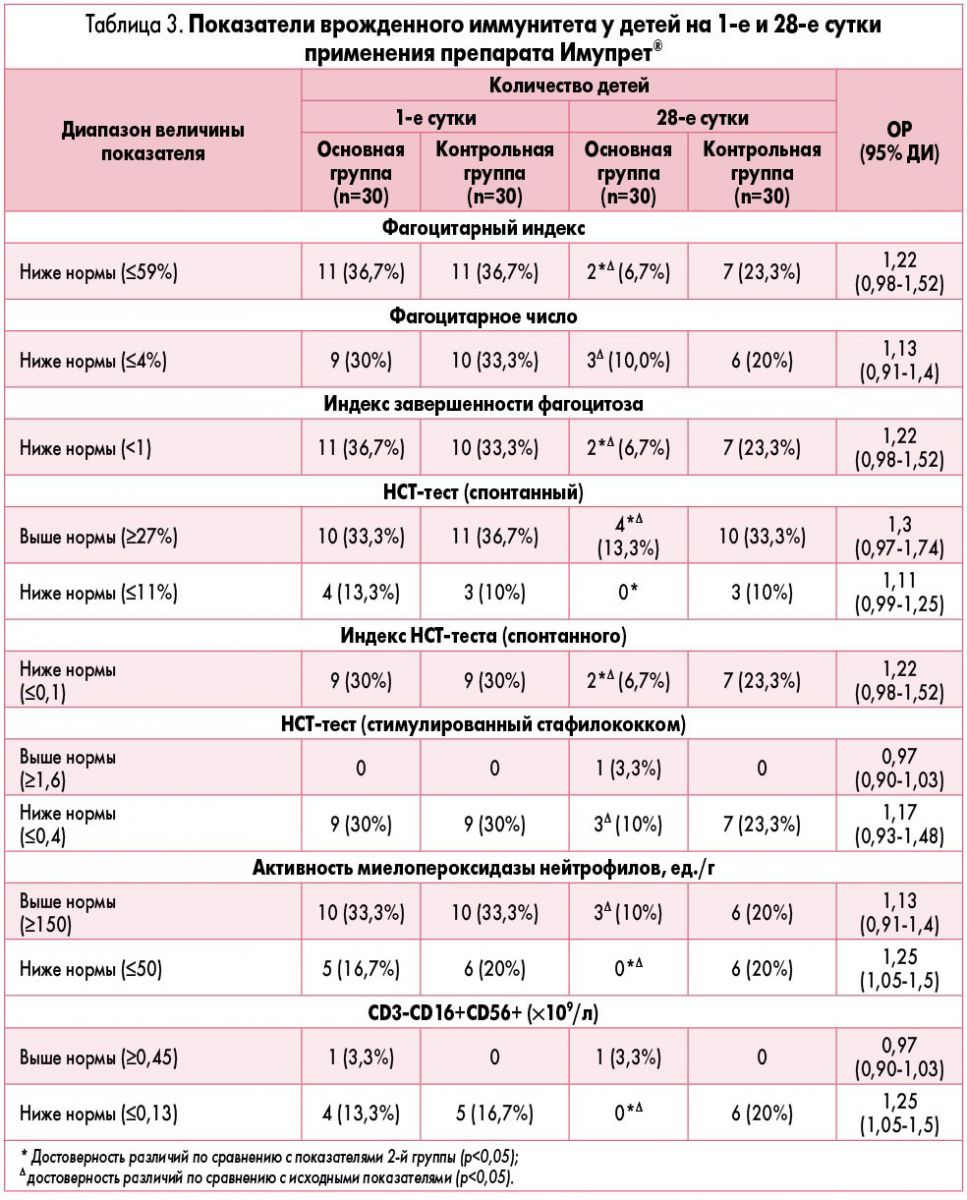
Динамика результатов исследования врожденного иммунитета у детей обеих групп на 1-е и 28-е сутки применения капель Имупрет® представлена в таблице 3.
Анализ динамики показателей врожденного иммунитета продемонстрировал, что после 28 дней применения препарата Имупрет® значительно уменьшилось количество детей с низкими показателями фагоцитарного индекса (на 30%; р<0,05), фагоцитарного числа (на 20%; р<0,05), индекса завершенности фагоцитоза (на 30%; р<0,05), индекса спонтанного НСТ-теста (на 23,3%; р<0,05), стимулированного стафилококком НСТ-теста (на 20%, р<0,05) и его индекса (на 20%; р<0,05), натуральных киллеров CD3-, CD16+, CD56+ (на 13,3%; р<0,05) и повышенной активностью миелопероксидазы нейтрофилов (на 16,7%; р<0,05). Также установлено уменьшение количества детей с высокими показателями спонтанного НСТ-теста (на 16,7%; р<0,05) и повышенной активностью миелопероксидазы нейтрофилов (на 23,3%; р<0,05).
Согласно анализу ОР использование препарата Имупрет® в программе профилактики бактериальных осложнений ОРЗ увеличивает вероятность нормального функционирования врожденного иммунитета – поглотительной и метаболической активности фагоцитоза, неспецифической антителонезависимой киллерной активности, а также нормализации миелопероксидазной активности.
Объективным показателем позитивного эффекта 28-дневного применения капель Имупрет® у детей основной группы является снижение количества бактериальных осложнений ОРЗ (на 16,7%; р<0,05), требующих назначения антибиотиков (табл. 4).
Таким образом, использование капель Имупрет® в программе 28-дневной профилактики бактериальных осложнений ОРЗ позволило добиться не только их уменьшения, но и снижения необходимости назначения системных антибактериальных средств за счет модуляции механизмов врожденного иммунитета и последующей эрадикации патогенной и условно-патогенной микрофлоры из носоротоглотки.
На протяжении 28-дневного приема препарата Имупрет® и последующего наблюдения побочных явлений и аллергических реакций не зарегистрировано.
Обсуждение результатов исследования. Как показали результаты исследования клинической эффективности применения капель Имупрет® с первого дня проявлений ОРЗ, на 5-е сутки использования препарата у детей основной группы отмечалось более быстрое и эффективное купирование эпизодов затрудненного носового дыхания и слизистых выделений из носовых ходов, дискомфорта в носоротоглотке, снижения количества эпизодов фебрильной лихорадки и кашля, уменьшения астенических проявлений. Это свидетельствует о том, что использование препарата Имупрет® как средства патогенетической и симптоматической терапии 5 раз в сутки в острый период респираторной патологии позволяет активировать раннюю неспецифическую противомикробную защиту и добиться положительных результатов.
Применение капель Имупрет® с 15-го дня от начала приема трижды в сутки позволило закрепить полученный защитный потенциал, что проявилось на 28-й день применения. Статистически значимо снизилась колонизация слизистой оболочки носоротоглотки 5 видами патогенных и условно-патогенных микроорганизмов – Streptococcus pneumoniae, Streptococcus pyogenes, Streptococcus agalactiae, Staphylococcus aureus и Haemоphylus influenzae, а также уменьшилось количество бактериальных осложнений, благодаря чему снизилась необходимость назначения антибиотиков.
Иммунотропное действие препарата Имупрет® проявилось в виде нормализации функционирования компонентов врожденного иммунитета – поглотительной и метаболической активности фагоцитоза, неспецифической антителонезависимой киллерной активности. Особое внимание обращает динамика активности миелопероксидазы – фермента нейтрофильных гранулоцитарных фагоцитов.
В физиологических условиях нейтрофильные гранулоциты под влиянием миелопероксидазы используют Н2О2 для синтеза гипохлорита, который уничтожает бактерии [10].
В процессе воспаления во время кислородного взрыва активированные нейтрофилы продуцируют Н2О2 в каскаде активных форм кислорода, в числе которых супероксидный и гидроксильный радикалы, а также синглетный кислород, который нарушает проницаемость клеточных мембран, инициирует перекисное окисление липидов. Н2О2 диффундирует в клетки, но там разрушается в результате активности ферментов каталазы и глутатионпероксидазы, осуществляя процессы антиоксидантной защиты окружающих тканей от чрезмерного повреждения химическими факторами активного воспаления, так как нейтрофилы в присутствии миелопероксидазы способны продуцировать гипохлорную кислоту, которая вместе с Н2О2 выполняет антимикробную функцию, а также играет роль медиатора воспаления и увеличивает проницаемость сосудистого эндотелия [11].
Таким образом, установленное нами снижение уровня осложнений ОРЗ при 28-дневном применении препарата Имупрет® связано как с вышеописанными свойствами миелопероксидазы нейтрофилов, так и с тем, что она обладает дополнительным механизмом микробицидного действия, который заключается в декарбоксилировании и дезаминировании аминокислот бактерий, а также быстрым и обширным подавлением синтеза бактериальной ДНК [11].
Необходимо отметить, что биологическое действие миелопероксидазы в значительной мере определяется балансом между эффективностью секреции этого фермента во внеклеточное пространство на стадии дегрануляции нейтрофилов, его инактивацией и утилизацией в тканях, деградацией окислителей, образующихся в реакциях с участием миелопероксидазы [12].
При секреторной дегрануляции или гибели нейтрофилов может проявляться патологическое действие фермента, при котором образующиеся в результате функционирования миелопероксидазы сильные окислители инициируют пероксидацию липидов, модификацию белков и нуклеиновых кислот (включая галогенирование, нитрование, окисление и образование сшивок), вызывая тем самым повреждение собственных тканей в очагах воспаления [13, 14]. Поэтому важной является установленная способность препарата Имупрет® при 28-дневном применении снижать его чрезмерную активность, что было зафиксировано у некоторых детей из 1-й группы.
Таким образом, исследование показало, что динамика врожденного иммунитета после 28-дневного применения капель Имупрет® проявилась уменьшением частоты низких показателей фагоцитарного индекса, фагоцитарного числа, индекса завершенности фагоцитоза, индекса спонтанного НСТ-теста, стимулированного стафилококком НСТ-теста и его индекса, натуральных киллеров CD3-, CD16+, CD56+, повышенной активности миелопероксидазы нейтрофилов (что повышало противомикробный эффект и снижало количество бактериальных осложнений ОРЗ).
Одновременно с этим зафиксировано уменьшение количества детей с высокими показателями спонтанного НСТ-теста и повышенной активностью миелопероксидазы нейтрофилов, что оказывало защитное действие на ткани шокового органа от повреждающего действия чрезмерного воспалительного процесса.
Такое избирательное действие в отношении активности миелопероксидазы – снижение при исходно высоких уровнях и повышение при исходно низких – свидетельствует о регуляторном характере действия препарата Имупрет® на метаболические параметры фагоцитоза. Это дает возможность усиливать его противомикробные характеристики без риска чрезмерной активации и последующего повреждения пораженных тканей.
Выводы
- Клиническая эффективность применения препарата Имупрет® с 1-го дня проявлений ОРЗ проявилась на 5-е сутки в виде более эффективного купирования эпизодов затрудненного носового дыхания и слизистых выделений из носовых ходов, дискомфорта в носоротоглотке, снижения количества эпизодов фебрильной лихорадки и кашля, уменьшения астенических проявлений.
- Применение капель Имупрет® с 1-го дня клинических проявлений ОРЗ на протяжении 28 дней способствовало уменьшению колонизации слизистой оболочки носоротоглотки 5 видами патогенных и условно-патогенных микроорганизмов – Streptococcus pneumoniae, Streptococcus pyogenes, Streptococcus agalactiae, Staphylococcus aureus и Haemоphylus influenzae.
- Препарат Имупрет® при условии применения с 1-го дня клинических проявлений ОРЗ на протяжении 28 дней является эффективным средством профилактики бактериальных осложнений, одновременно снижая необходимость приема антибиотиков.
- Иммунотропное действие препарата Имупрет® при применении для профилактики бактериальных осложнений ОРЗ способствует нормализации функционирования компонентов врожденного иммунитета – поглотительной и метаболической активности фагоцитоза, неспецифической антителонезависимой киллерной активности.
- Хорошая переносимость и безопасность капель Имупрет® на протяжении 28-дневного применения у пациентов в возрасте от 2 до 6 лет позволяет рекомендовать данный препарат в качестве высокоэффективного средства профилактики бактериальных осложнений ОРЗ в педиатрической практике.
Список литературы находится в редакции.
Тематичний номер «Педіатрія» №3 (50), 2019 р.