7 жовтня, 2019
Лечение ненейрогенных симптомов нарушенного мочеиспускания у мужчин, включая доброкачественную простатическую обструкцию
Клинические рекомендации Европейской ассоциации урологии*
Симптомы нарушенного мочеиспускания (СНМ) являются частой жалобой у взрослых мужчин. Они оказывают серьезное влияние на качество жизни и приводят к значительным экономическим затратам. Настоящие рекомендации представляют собой руководство, основанное на доказательствах, по обследованию и лечению мужчин в возрасте 40 лет и старше с различными ненейрогенными формами СНМ. Представляем вашему вниманию основные фрагменты рекомендаций по консервативной (медикаментозной) терапии СНМ, разработанные специалистами Европейской асоциации урологии. Перевод К.А. Ширанова.
Цели и задачи
Понимание нижних мочевыводящих путей как единого функционального отдела и многофакторная этиология связанных с ними симптомов подразумевают, что в настоящее время основной акцент сделан скорее на СНМ, чем на доброкачественной гиперплазии предстательной железы (ДГПЖ).
Необходимо подчеркнуть, что клинические рекомендации представляют собой наилучшие данные, доступные экспертам на момент публикации. Тем не менее настоящие рекомендации не всегда позволят получить наилучший результат. Они никогда не смогут заменить клинический опыт при определении тактики лечения для отдельного пациента, а, скорее, помогут сделать выбор подходов с учетом индивидуальных особенностей и предпочтений пациента. Рекомендации не являются обязательными для соблюдения и не рассматриваются как юридический стандарт оказания помощи.
Консервативное лечение
Динамическое наблюдение (ДН)
Многие мужчины с СНМ не настолько обеспокоены своими симптомами, чтобы им требовалось медикаментозное или хирургическое лечение. Всех пациентов с СНМ необходимо обследовать до назначения любого вида лечения для оценки тяжести СНМ и разделения между подавляющим большинством больных с так называемыми неосложненными СНМ, которые не несут угрозы жизни, и более редкими пациентами с осложненными СНМ. ДН считается приемлемым вариантом для многих мужчин с невыраженными симптомами, поскольку только у части из них на фоне отсутствия лечения могут развиться острая задержка мочи (ОЗМ) и такие осложнения, как почечная недостаточность или камни [117, 118], а у других мужчин симптоматика остается стабильной при наблюдении в течение года [120].
В исследовании, в котором сравнивали ДН и трансуретральную резекцию предстательной железы (ТУР ПЖ) у мужчин с СНМ умеренной степени, показано, что в группе хирургического лечения лучше сохранялась функция мочевого пузыря (скорость мочеиспускания и объем остаточной мочи), особенно у больных с высокой обеспокоенностью симптомами. При этом 36% пациентов за пять лет перешли в группу ТУР ПЖ, а 64% больных были удовлетворены ДН [121, 122]. Самыми сильными прогностическими факторами неэффективности ДН являются увеличение беспокойства симптомами и объемом остаточной мочи (ООМ). Поэтому для ДН подходят мужчины с неосложненными СНМ легкой/умеренной степени, которые не обеспокоены своими симптомами.
Поведенческая терапия и рекомендации по диете
Динамическое наблюдение обычно включает следующие компоненты:
- обучение (по заболеванию);
- заверение больного в том, что расстройство мочеиспускания не связано с раком;
- периодический мониторинг;
- рекомендации по образу жизни [119, 120, 123, 124];
- уменьшение потребления жидкости в определенные периоды для снижения частоты мочеиспускания в наименее приемлемое время (на ночь или перед походом в общественные места);
- избегание или коррекция потребления кофеина и алкоголя, которые могут оказывать диуретический и ирритативный эффект, тем самым увеличивая диурез и частоту мочеиспускания и усиливая ургентность и ноктурию;
- использование техники расслабленного и двойного мочеиспускания;
- массаж бульбозного отдела уретры для профилактики постмиктурического подкапывания;
- техники прерывания, например сжатие головки полового члена, дыхательные упражнения, сдавление промежности и психологические приемы, чтобы не думать о мочевом пузыре и туалете, чтобы лучше контролировать накопительные симптомы;
- тренировка мочевого пузыря, которая помогает сдерживать позыв, когда появляется сенсорная ургентность, для увеличения вместимости мочевого пузыря и времени между мочеиспусканиями;
- пересмотр препаратов и оптимизация времени приема или замена препаратов на другие с меньшим числом побочных эффектов со стороны мочевыводящих путей; эти рекомендации особенно применимы к диуретикам;
- предоставление необходимой помощи при наличии нарушений движений кисти, подвижности или ментального статуса;
- лечение запоров.
В настоящее время получены данные с уровнем доказательности 1b о том, что самостоятельное ведение как часть ДН уменьшает выраженность симптомов и прогрессирование заболевания [123, 124]. У мужчин, рандомизированных в группу трех сеансов самостоятельного ведения наряду с ДН, отмечалось более выраженное улучшение симптомов и качества жизни через 3 и 6 мес, чем у пациентов в группе только ДН. Через 12 мес эти различия сохранялись [123].
Практические вопросы
Компоненты самостоятельного ведения отдельно не изучались. Вышеперечисленные компоненты рекомендаций по образу жизни получены из официальной методологии консенсуса [125]. Требуются дальнейшие исследования в этой области.
 Лекарственная терапия
Лекарственная терапия
Антагонисты a‑1-адренорецепторов (a‑1-блокаторы)
Механизм действия. Альфа‑1-блокаторы подавляют действие эндогенно выделяемого норадреналина на гладкомышечные клетки ПЖ и тем самым снижают ее тонус и интравезикальную обструкцию (ИВО) [126]. Тем не менее показано, что α‑1-блокаторы оказывают слабое влияние на сопротивление инфравезикального отдела, определяемое уродинамически [127], а улучшение СНМ на фоне лечения слабо коррелирует с обструкцией [128]. В связи с этим могут играть роль другие механизмы.
Доступные препараты включают: альфузозина гидрохлорид (алфузозин); доксазозина мезилат (доксазозин); силодозин; тамсулозина гидрохлорид (тамсулозин); теразозина гидрохлорид (теразозин). Альфа-блокаторы имеют различные формы дозирования. Хотя разные формы обладают разной фармакокинетикой и профилем переносимости, они обеспечивают умеренный общий клинический эффект.
Эффективность. Косвенные и ограниченные прямые сравнения показали, что все α‑1-блокаторы имеют сопоставимую эффективность при применении в соответствующих дозах [129]. Хотя для достижения максимального улучшения симптоматики требуется несколько недель, статистически значимое преимущество перед плацебо наблюдается уже в первые часы или дни приема [130].
Переносимость и безопасность. Распределение рецепторов в нижних мочевыводящих путях, избирательность по подтипам рецепторов и особенности фармакокинетики обусловливают профиль переносимости каждого из препаратов. К наиболее частым побочным эффектам при приеме α‑1-блокаторов относят астению, головокружение и (ортостатическую) гипотензию. Вазодилатирующее влияние наиболее выражено при применении доксазозина и теразозина, но встречается гораздо реже при приеме алфузозина и тамсулозина [135]. Пациенты с сопутствующими сердечно-сосудистыми заболеваниями и/или сопутствующей терапией вазоактивными препаратами могут быть восприимчивы к вазодилатации, индуцированной α-блокаторами [136]. Напротив, частота гипотензии на фоне селективного α‑1-блокатора силодозина сравнима с плацебо [137]. В крупном ретроспективном когортном анализе среди мужчин в возрасте >66 лет установлено, что прием α-блокаторов повышает риск падений (отношение риска (ОР) 1,14) или переломов (ОР 1,16), вероятнее всего, вследствие артериальной гипотензии [138].
В 2005 году в рамках хирургического лечения катаракты было обнаружено их неблагоприятное воздействие на глаза в виде так называемого синдрома интраоперационной вялости радужной оболочки (intra-operative floppy iris syndrome – IFIS) [139].
Практические вопросы. Альфа-блокаторы, как правило, являются первой линией лекарственной терапии СНМ у мужчин из-за быстрого начала действия, хорошей эффективности и низкой частоты и тяжести нежелательных явлений. При этом α-блокаторы не предотвращают риск развития ОЗМ или необходимости хирургического лечения. Офтальмологи должны знать о применении α‑1-блокаторов перед операцией по поводу катаракты. Также необходимо информировать пациентов о риске ортостатической гипотензии при приеме неселективных α‑1-блокаторов. Пациентов следует информировать о риске эякуляторной дисфункции на фоне приема α-блокаторов.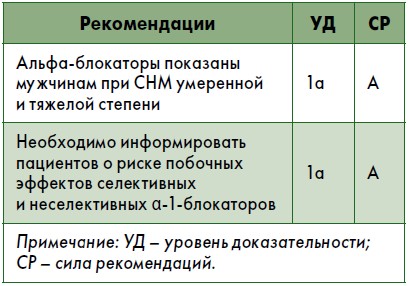
Ингибиторы 5-альфа-редуктазы (5-АР)
Механизм действия. Влияние андрогенов на ПЖ опосредовано дигидротестостероном (ДГТ), который образуется из тестостерона под действием 5-АР, стероидного фермента, связанного с ядром [143]. Этот фермент существует в виде двух изоформ:
- 5-АР 1-го типа, экспрессируемая в небольших количествах и малоактивная в ПЖ, но обеспечивающая основную часть активности фермента в других тканях, например в коже и печени;
- 5-АР 2-го типа, экспрессируемая и действующая главным образом в ПЖ.
Для клинического применения доступны два ингибитора 5-АР: дутастерид и финастерид. Финастерид подавляет только 5-АР 2-го типа, тогда как дутастерид одинаково эффективно подавляет 5-АР 1-го и 2-го типов (двойной ингибитор 5-АР). Ингибиторы 5-АР, действующие путем индуцирования апоптоза эпителиальных клеток ПЖ [144], способствуют уменьшению размера ПЖ на 18‑28% и уровня простатспецифического антигена (ПСА) до 50% после 6‑12 мес лечения [145]. Средний объем уменьшения ПЖ и снижение уровня ПСА могут быть более выражены после длительного лечения. При длительном приеме финастерида уровень ДГТ снижается примерно на 70%, а при приеме дутастерида – на 95%. При этом концентрация ДГТ в ПЖ на фоне приема обоих ингибиторов 5-АР уменьшается примерно одинаково (на 85‑90%).
Эффективность. Клиническая эффективность по сравнению с плацебо наблюдается при длительности лечения минимум 6‑12 мес. После 2‑4 лет терапии ингибиторами 5-АР у пациентов с СНМ, вызванными увеличением ПЖ, выраженность СНМ (по Международному индексу простатических симптомов – IPSS) уменьшается примерно на 15‑30%, объем ПЖ – примерно на 18‑28%, а Qмакс повышается примерно на 1,5‑2,0 мл/с [56, 133, 134, 146‑152]. Непрямое сравнение результатов и данные одного сравнительного исследования свидетельствуют о том, что дутастерид и финастерид в одинаковой степени эффективны при лечении СНМ [145, 153]. Уменьшение выраженности симптомов зависит от исходного размера ПЖ.
Переносимость и безопасность. Наиболее выраженные нежелательные явления ингибиторов 5-АР связаны с сексуальной функцией и включают в себя снижение либидо, эректильную дисфункцию и, реже, нарушение эякуляции, например ретроградную эякуляцию, отсутствие эякуляции или уменьшение объема эякулята [56, 134, 145]. Частота развития сексуальной дисфункции и других неблагоприятных явлений остается низкой и даже уменьшается по мере продолжения приема. Примерно у 1‑2% пациентов развивается гинекомастия (увеличение грудных желез у мужчин с чувствительностью груди и сосков).
Практические вопросы. Ингибиторы 5-АР следует назначать мужчинам с СНМ умеренной/тяжелой степени и увеличенной ПЖ (>40 см3) и/или повышенным уровнем ПСА (>1,4‑1,6 нг/мл). Из-за медленного начала действия они подходят только для длительного лечения (в течение многих лет). Их влияние на уровень ПСА необходимо учесть при скрининге рака ПЖ.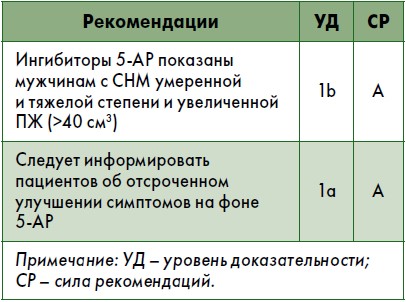
Антагонисты мускариновых рецепторов
Механизм действия. Детрузор иннервируется парасимпатическими нервами, основным нейротрансмиттером которых является ацетилхолин, обладающий способностью стимулировать мускариновые рецепторы (М-холинорецепторы) на поверхности гладкомышечных клеток. Однако мускариновые рецепторы плотно экспрессируются не только на гладкомышечных клетках, но и на клетках других типов, например на переходно-клеточном эпителии мочевого пузыря, эпителиальных клетках слюнных желез, нервных клетках периферической и центральной нервной системы. У человека описано пять подтипов мускариновых рецепторов (М1-М5), из которых подтипы М2 и М3 представлены в основном в детрузоре. Хотя большую часть рецепторов относят к подтипу М2, функционально более важную роль в сокращении детрузора у здоровых лиц играет подтип M3 [166, 167]. Антимускариновые эффекты может индуцировать или регулировать переходно-клеточный эпителий мочевого пузыря и/или центральная нервная система [168, 169].
Для лечения гиперактивного мочевого пузыря (ГАМП)/накопительных симптомов зарегистрированы следующие антагонисты мускариновых рецепторов: дарифенацина гидробромид (дарифенацин); фезотеродина фумарат (фезотеродин); оксибутинина хлорид (оксибутинин); пропиверина хлорид (пропиверин); солифенацина сукцинат (солифенацин); толтеродина тартрат (толтеродин) и троспия хлорид. Кроме того, опубликованы данные по трансдермальной форме дозирования оксибутинина [170, 171].
Эффективность. Применение антагонистов мускариновых рецепторов ранее в основном изучали у женщин, поскольку считалось, что СНМ у мужчин вызваны заболеваниями ПЖ, поэтому лечить их предлагалось простатспецифичными препаратами. Однако научных данных в пользу такого предположения нет [172]. При дополнительном анализе исследований с открытым приемом, в которые входили пациенты с симптомами ГАМП, показано, что влияние на ургентность, частоту мочеиспускания или императивное недержание мочи оказывает возраст, а не пол пациента [173].
Эффективность антимускариновых препаратов в качестве монотерапии оценивали у взрослых мужчин с симптомами ГАМП при отсутствии ИВО [175‑180]. Длительность большинства исследований составила всего 12 недель. Проведено четыре дополнительных анализа результатов крупных РКИ по лечению ГАМП у женщин и мужчин без ИВО с акцентом только на мужчинах [176, 178, 181]. Толтеродин позволяет уменьшить выраженность императивного недержания мочи, учащенного мочеиспускания за сутки или в дневное время, мочеиспускания, связанного с ургентностью, а также улучшить восприятие пациентом эффективности лечения. Солифенацин статистически значимо улучшает средние показатели восприятия состояния мочевого пузыря, средние показатели опросников по ГАМП и общее восприятие проблем с мочевым пузырем, а фезотеродин позволяет уменьшить частоту мочеиспускания, число эпизодов ургентности и императивного недержания мочи. В исследованиях с открытым приемом толдеродина показано уменьшение частоты мочеиспускания за сутки, выраженности ноктурии, императивного недержания и показателя шкалы IPSS через 12‑25 недель терапии [177, 180].
Переносимость и безопасность. Около 3‑10% пациентов отказываются от участия в исследованиях по мускариновым препаратам, что сопоставимо с показателями в группах плацебо. Нежелательные явления, связанные с лечением, включают сухость во рту (до 16% случаев), запоры (до 4%), проблемы при мочеиспускании (до 2%), назофарингит (до 3%), головокружение (до 5%).
Практические вопросы. Не все холиноблокаторы оценивали в исследованиях, и к настоящему времени не проводилось длительных исследований эффективности антагонистов мускариновых рецепторов у мужчин, страдающих СНМ. Кроме того, в опубликованные исследования входили только пациенты с низким исходным ООМ. По этой причине антагонисты мускариновых рецепторов следует назначать с осторожностью, и при этом рекомендуется регулярно оценивать показатель шкалы IPSS и ООМ. В случае ухудшения СНМ или струи мочи на фоне антимускариновых препаратов рекомендуется отменить их прием.
Ингибиторы фосфодиэстеразы 5-го типа (ФДЭ‑5)
Механизм действия. Ингибиторы ФДЭ повышают концентрацию и пролонгируют активность внутриклеточного циклического гуанозинмонофосфата (цГМФ), снижая таким образом тонус гладкой мускулатуры детрузора, ПЖ и уретры. Оксид азота NО и ингибиторы ФДЭ‑5 также могут вносить вклад в мочеиспускание, подавляя рефлекторные проводящие пути спинного мозга и нейротрансмиссию в уретре, ПЖ, мочевом пузыре [185]. Кроме того, при длительном применении ингибиторы ФДЭ‑5 увеличивают кровоснабжение и оксигенацию нижних мочевыводящих путей [186]. Наконец, они уменьшают выраженность воспаления в ПЖ и мочевом пузыре [187]. Точный механизм действия ингибиторов ФДЭ‑5 остается неизученным.
Доступные препараты. Хотя в клинических исследованиях изучали применение нескольких селективных ингибиторов ФДЭ‑5, только тадалафил (в дозе 5 мг 1 р/сут) зарегистрирован для лечения СНМ у мужчин.
Эффективность. В ряде РКИ показано, что ингибиторы ФДЭ‑5 снижают показатель шкалы IPSS, выраженность накопительных и миктурических СНМ и повышают качество жизни. При этом в большинстве исследований Qмакс не отличалась от показателей в группе плацебо. В метаанализе показано, что ингибиторы улучшают показатели шкалы IPSS и МИЭФ (Международный индекс эректильной функции), но не оказывают влияния на Qмакс [188].
Переносимость и безопасность. Описанные в РКИ нежелательные явления всех ингибиторов ФДЭ‑5 включают приливы, гастроэзофагеальный рефлюкс, головную боль, диспепсию, боль в спине и заложенность носа [188]. Частота отказа от лечения из-за нежелательных явлений для тадалафила составляет 2,0% [198] и, по данным объединенного анализа, не зависит от возраста, выраженности СНМ, уровня тестостерона или объема ПЖ [192].
Ингибиторы ФДЭ‑5 противопоказаны пациентам, получающим нитраты, активатор калиевых каналов никорандил или α‑1-блокаторы доксазозин или теразозин. Кроме того, они противопоказаны больным с нестабильной стенокардией, недавно перенесенным инфарктом миокарда (в течение последних 3 мес) или инсультом (за последние 6 мес), миокардиальной недостаточностью (по классификации Нью-Йоркской ассоциации сердца >2 баллов), артериальной гипотензией, плохо контролируемым артериальным давлением, серьезным нарушением функции печени или почек и уже имеющейся либо возникшей после предыдущего приема ингибиторов ФДЭ‑5 передней ишемической оптической нейропатией с внезапной потерей зрения.
Практические вопросы. В настоящее время только тадалафил в дозе 5 мг зарегистрирован для лечения СНМ у мужчин с эректильной дисфункцией или без нее. Результаты регрессионного метаанализа свидетельствуют о более высокой эффективности препаратов у мужчин молодого возраста с низким индексом массы тела и более выраженными СНМ [188]. Длительный прием у мужчин с СНМ оценивали только в одном исследовании с длительностью наблюдения более года [191], поэтому нельзя сделать выводы о его эффективности или переносимости при более длительном применении. Также получены ограниченные данные об уменьшении объема ПЖ и отсутствует информация о замедлении прогрессирования заболевания.
Растительные препараты – фитотерапия
Механизм действия. Лекарственные препараты на основе растений изготавливаются из корней, семян, цветочной пыльцы, коры и могут быть из экстрактов одного растения (монопрепараты) или двух и более (комбинированные препараты). Наиболее часто применяют такие растения, как Cucurbita pepo (семена тыквы); Hypoxis rooperi (южноафриканское растение); Pygeum africanum (кора африканского сливового дерева); Secale cereale (ржаная пыльца); Serenoa repens (синоним Sabal serrulata; плоды американской карликовой пальмы, пальмы сереноа) и Urtica dioica (корень крапивы двудомной).
Самыми важными составляющими фитотерапии служат фитостеролы, β-ситостерол, жирные кислоты и лектины [199]. В исследованиях in vitro показано, что экстракты растений обладают противовоспалительным, антиандрогенным или эстрогенным свойствами; уменьшают уровень глобулина, связывающего половые гормоны (ГСПГ); подавляют ароматазу, липооксигеназу, фактор роста, стимулирующий пролиферацию клеток ПЖ, α-адренорецепторы, 5-α-редуктазу, мускариновые холинорецепторы, рецепторы дигидропиридина или ванилоидные рецепторы и нейтрализуют свободные радикалы [199‑201]. Эти свойства не подтверждены в условиях in vivo, и точный механизм действия растительных экстрактов остается неясным.
Эффективность. Экстракты одного и того же растения, произведенные разными компаниями, не всегда имеют одинаковую биологическую или клиническую эффективность, поэтому эффективность одного и того же препарата, изготовленного разными производителями, может быть различной [202]. Кроме того, даже две разные партии препарата, изготовленные одним производителем, могут содержать различные концентрации активных ингредиентов [203]. При анализе современных техник выделения веществ и их влияния на состав/биологическую активность препаратов на основе Serenoa repens показано, что результаты различных исследований можно сравнивать только при соответствии валидированных техник выделения и/или содержания активного вещества [204]. Таким образом, фармакокинетические свойства у растительных экстрактов могут значительно отличаться.
Переносимость и безопасность. Побочные эффекты фитотерапии обычно слабо выражены и сопоставимы с плацебо. Серьезные нежелательные явления не были связаны с препаратами, применяемыми во время исследования. К наиболее частым побочным эффектам относились жалобы со стороны желудочно-кишечного тракта. При использовании препаратов с растением Hypoxis rooperi у 0,5% пациентов развивается эректильная дисфункция.
Практические вопросы. Фитотерапевтические препараты – гетерогенная группа растительных экстрактов, которая содержит различные концентрации активных ингредиентов. По этой причине метаанализы экстрактов одного и того же растения не являются достоверными, и их результаты следует интерпретировать с осторожностью.
Интерпретация рабочей группы. Группа экспертов по клиническим рекомендациям не дает специфичных рекомендаций в отношении фитотерапии при СНМ у мужчин из-за неоднородности продукта, отсутствия регулирующего контроля и значительных методологических недостатков в опубликованных исследованиях и метаанализах.
Агонисты β‑3-адренорецепторов
Механизм действия. Бета‑3-адренорецепторы являются преобладающим типом β-рецепторов, экспрессируемых в гладких мышечных клетках детрузора, и их стимуляция, как считается, вызывает расслабление детрузора.
Эффективность. Мирабегрон в дозе 50 мг стал первым агонистом β‑3-адренорецепторов, доступным для клинической практики, который одобрен для лечения ГАМП у взрослых. Мирабегрон интенсивно изучали в трех 12-недельных РКИ, проведенных в Европе, Австралии и Северной Америке [210‑214]. Результаты показали эффективность мирабегрона в отношении симптомов ГАМП, включая учащенное мочеиспускание, ургентное недержание мочи, ургентность и восприятие пациентом эффективности лечения. Эти исследования включали преимущественно женщин.
Переносимость и безопасность. Наиболее частые нежелательные явления, связанные с лечением, в группе мирабегрона включают артериальную гипертензию, ИМВП, головную боль и назофарингит [210‑213]. Мирабегрон противопоказан пациентам с тяжелой неконтролируемой артериальной гипертензией (систолическое артериальное давление >180 мм рт. ст., или диастолическое >110 мм рт. ст., или их сочетание). Перед началом терапии необходимо измерять артериальное давление и контролировать его с регулярными интервалами.
Практические вопросы. К настоящему времени не доступны отдаленные результаты исследований по эффективности и безопасности мирабегрона у мужчин любого возраста с СНМ. Кроме того, отсутствуют исследования по комбинации мирабегрона с другими препаратами при СНМ у мужчин. Однако фармакокинетические взаимодействия при дополнительном приеме мирабегрона или тамсулозина к монотерапии этими препаратами не должны вызывать клинически значимых изменений в профиле безопасности [218]. В небольшом исследовании изучали изменение показателя шкалы симптомов у мужчин, которые получали мирабегрон в комбинации с тамсулозином (0,2 мг в сутки) [219]. В японском исследовании IV фазы в небольшой группе мужчин показана эффективность добавления мирабегрона к солифенацину в случае сохранения ургентности [220].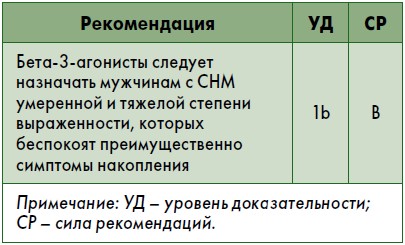
Комбинированная терапия
Альфа-блокаторы + ингибиторы 5-АР
Механизм действия. При комбинированной терапии применяют α-блокатор в сочетании с ингибитором 5-АР. Альфа-блокаторы начинают оказывать клиническое действие в течение нескольких часов или дней, а ингибиторам 5-АР для наступления клинической эффективности требуется несколько месяцев. В клинических исследованиях оценивали финастерид в сочетании с алфузозином, доксазозином или теразозином и дутастерид в комбинации с тамсулозином.
Эффективность. В ряде исследований оценивали эффективность комбинированной терапии по сравнению с монотерапией α-блокаторами, ингибиторами 5-АР или плацебо. В первых исследованиях с наблюдением от 6 до 12 мес показана более высокая эффективность α‑1-блокаторов по сравнению с финастеридом в отношении симптомов, в то время как комбинированная терапия не превосходила по эффективности монотерапию α-блокаторами [147, 148, 221]. В исследованиях с группой плацебо α‑1-блокаторы всегда превосходили по эффективности плацебо в отличие от финастерида. Аналогичные результаты получены в исследовании MTOPS (1 год наблюдения) [56].
Согласно отдаленным результатам исследования MTOPS (длительность наблюдения 4 года) и исследования комбинированной терапии аводартом и тамсулозином CombAT (Combination of Avodart and Tamsulosin), комбинированная терапия эффективнее любого из вариантов монотерапии в уменьшении выраженности симптомов и улучшении Qмакс и превосходит монотерапию α-блокаторами по снижению риска развития ОЗМ и необходимости хирургического лечения [56, 133, 134].
Переносимость и безопасность. При комбинированной терапии встречаются нежелательные явления, характерные для обоих классов препаратов [56, 133, 134]. Нежелательные явления, развивающиеся на фоне комбинированной терапии, типичны для α-блокаторов и ингибиторов 5-АР. При комбинированной терапии статистически значимо выше частота развития нежелательных явлений.
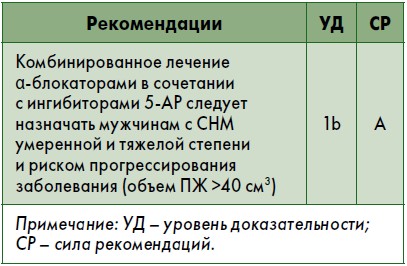 Практические вопросы. По сравнению с монотерапией α-блокаторами или ингибиторами 5-АР комбинированная терапия более эффективно улучшает СНМ, повышает показатель Qмакс и предупреждает прогрессирование заболевания. Однако комбинированная терапия сопровождается и большим числом побочных эффектов. Поэтому ее следует назначать прежде всего мужчинам с СНМ умеренной или тяжелой степени и риском прогрессирования заболевания (более высокий объем ПЖ, повышенный уровень ПСА, пожилой возраст, высокий ООМ, низкая Qмакс и др.). Комбинированную терапию следует применять только при длительном лечении (>12 мес). Данный факт необходимо обсудить с пациентом до начала лечения. Мужчинам с СНМ умеренной степени можно предложить отменить прием α-блокаторов спустя 6 месяцев.
Практические вопросы. По сравнению с монотерапией α-блокаторами или ингибиторами 5-АР комбинированная терапия более эффективно улучшает СНМ, повышает показатель Qмакс и предупреждает прогрессирование заболевания. Однако комбинированная терапия сопровождается и большим числом побочных эффектов. Поэтому ее следует назначать прежде всего мужчинам с СНМ умеренной или тяжелой степени и риском прогрессирования заболевания (более высокий объем ПЖ, повышенный уровень ПСА, пожилой возраст, высокий ООМ, низкая Qмакс и др.). Комбинированную терапию следует применять только при длительном лечении (>12 мес). Данный факт необходимо обсудить с пациентом до начала лечения. Мужчинам с СНМ умеренной степени можно предложить отменить прием α-блокаторов спустя 6 месяцев.
Альфа-блокаторы + антагонисты мускариновых рецепторов
Механизм действия. Комбинированная терапия α-блокатором в сочетании с антагонистом мускариновых рецепторов направлена на блокирование α-адренорецепторов и мускариновых холинорецепторов. К настоящему времени в клинических исследованиях не изучались возможные комбинации препаратов.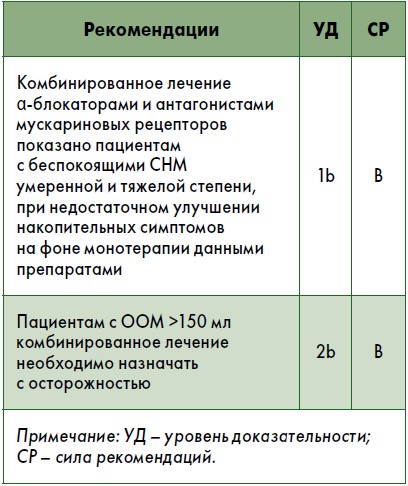
Практические вопросы. Сочетание препаратов, по-видимому, обусловливает увеличенную эффективность и качество жизни пациентов, получающих α-блокаторы и антагонисты мускариновых рецепторов. В исследованиях с короткой длительностью наблюдения оценивали преимущественно изменение накопительных симптомов и включали только мужчин с низким исходным ООМ. По этой причине на фоне комбинированного лечения рекомендуется измерять ООМ.
Отбор пациентов
Выбор лечения зависит от результатов обследования, способности данного метода лечения изменить оцененные результаты, предпочтений пациента по поводу метода лечения и предполагаемых ожиданий с точки зрения скорости начала действия препарата, эффективности, побочных эффектов, качества жизни и прогрессирования заболевания.
Методом первой линии обычно является поведенческая терапия с или без медикаментозного лечения. На рис. 1 представлена диаграмма выбора лечения на основании принципов доказательной медицины и характеристик пациентов.
Хирургическое лечение обычно показано пациентам с повторной или рефрактерной задержкой мочи, парадоксальной ишурией, рецидивными ИМВП, камнями мочевого пузыря или дивертикулами, консервативно не купируемой макрогематурией, вызванной ДГПЖ/ДПО или гидронефрозом, вызванным ДПО, с почечной недостаточностью или без таковой (абсолютные показания к операции, необходимо хирургическое лечение).
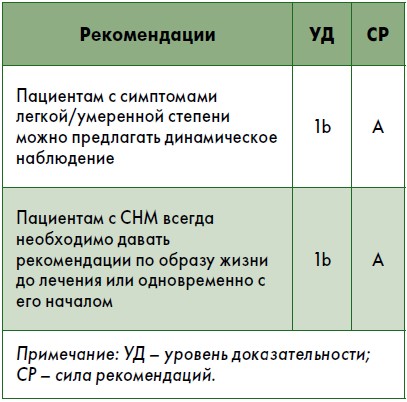
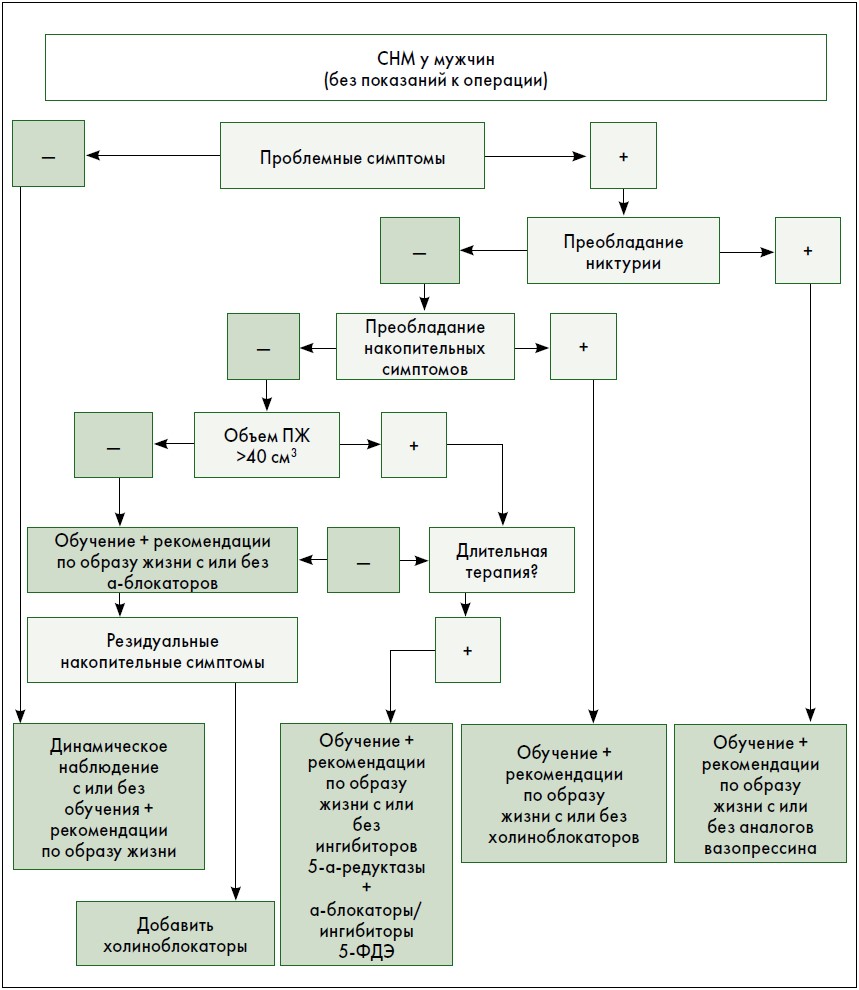 Рис. 1. Алгоритм медикаментозного и/или консервативного лечения СНМ у мужчин
Рис. 1. Алгоритм медикаментозного и/или консервативного лечения СНМ у мужчин
Кроме того, хирургическое лечение обычно необходимо при отсутствии адекватного улучшения СНМ или ООМ на фоне консервативной или медикаментозной терапии (относительные показания к операции). Выбор метода хирургического лечения зависит от объема ПЖ, сопутствующих заболеваний, возможности проведения анестезии, предпочтений пациента, приемлемости возможных осложнений, связанных с лечением, доступности хирургических методов и опыта хирурга в проведении определенных операций. Алгоритм выбора хирургического лечения на основании принципов доказательной медицины и характеристик пациента представлен на рис. 2.
Следует отметить, что тактика лечения зависит от результатов первичного обследования. Кроме того, предпочтения пациента также могут повлиять на тактику лечения.
Рис. 2. Алгоритм лечения проблемных СНМ, устойчивых к консервативному/ медикаментозному лечению, или при абсолютных показаниях к операции (диаграмма стратифицирована по возможности проведения анестезии, сердечно-сосудистому риску и объему ПЖ)
Полная версия документа (2017) представлена на сайте www.uroweb.org.
Тематичний номер «Урологія. Нефрологія. Андрологія» № 1 (16), березень 2019 р.