8 жовтня, 2019
Особенности лечения кандидозного кольпита*
Кандидозный кольпит (КК) рассматривается в группе инфекций, характеризующихся патологическими вагинальными выделениями. Особенностями данной патологии являются высокая частота, длительное течение, частое рецидивирование процесса, возможность распространения на другие органы и системы с развитием генерализованных форм кандидоза, высокая резистентность возбудителей к антимикотическим препаратам, трудности в применении терапии у беременных женщин и новорожденных. КК занимает одно из ведущих мест в структуре акушерско-гинекологической заболеваемости и является одной из наиболее частых причин обращения женщин за медицинской помощью.
Частота КК составляет 30-45% в структуре инфекционных поражений влагалища и вульвы. При беременности заболеваемость возрастает примерно на 10-20% и является одной из причин развития осложнений. Кандидозный кольпит обнаруживают у 30% онкологических больных и у 64% больных с различными эндокринными нарушениями.
Значительное учащение случаев КК обусловлено действием ряда предрасполагающих факторов, таких как длительный (а иногда и бесконтрольный) прием антибиотиков, цитостатиков, оральных контрацептивов, лучевая терапия; нарушение обмена веществ и функции эндокринной системы (гипо- и диспротеинемия, гипергликемия, грубые длительные погрешности в питании, хронические заболевания желудочно-кишечного тракта, дисфункция щитовидной и половых желез, надпочечников и т.д.); гипо- и авитаминозы: дисбактериоз на фоне хронических заболеваний желудочно-кишечного тракта; иммунодефициты, развившиеся на фоне инфекционного или гематологического заболевания, онкологического процесса, интоксикации и т.д.
Патогенез кандидозного кольпита
Учитывая тот факт, что штаммы C. albicans, выделенные у больных КК и у носителей, существенно не различаются по ряду биохимических характеристик, можно сделать заключение о ведущей роли состояния макроорганизма в развитии кандидозного вульвовагинита, а не свойств возбудителя. Триггером развития заболевания является не изменение свойств гриба, а снижение резистентности организма хозяина.
Грибы рода Candida могут быть выделены из влагалища практически здоровых женщин при отсутствии клинических признаков КК (носительство). При определенных условиях под действием экзогенных и/или эндогенных факторов эти грибы становятся патогенными, вызывая заболевание. Однако четкие критерии разграничения носительства и стертых форм патологии отсутствуют. По мнению некоторых авторов, при наличии существенных факторов риска, например при беременности, всякое обнаружение во влагалище грибов рода Candida свидетельствует о наличии КК, а не о носительстве. Это подтверждается результатами исследования, в котором только у 2% беременных с наличием C. albicans во влагалище было установлено отсутствие каких-либо патологических изменений [1].
В развитии кандидозной инфекции различают следующие этапы: адгезия грибов к поверхности слизистой оболочки → колонизация грибами слизистой оболочки → инвазия в эпителий, преодоление эпителиального барьера слизистой оболочки, попадание в соединительную ткань собственной пластинки, преодоление тканевых и клеточных защитных механизмов → проникновение в сосуды и гематогенная диссеминация с поражением различных органов и систем (однако при КК инфекционный процесс чаще затрагивает поверхностные слои эпителия влагалища).
В силу существующего на этом уровне динамического равновесия между микроорганизмами (грибами), которые стремятся, но не могут проникнуть в более глубоко расположенные слои слизистой оболочки, и макроорганизмом, который пытается, но не способен полностью элиминировать возбудитель, инфекция может персистировать годами. А сдвиги этого равновесия могут привести либо к обострению заболевания, либо к ремиссии или выздоровлению.
Вульвовагинальный кандидоз
- инфекционное поражение кожи и слизистых оболочек органов мочеполовой системы, вызванное грибами рода Сandida
Факторы риска
- дисметаболические расстройства
- дисфункция иммунной системы
- снижение резистентности организма
Клиническая картина кандидозного кольпита
В настоящее время различают три основные клинические формы КК:
- кандидоносительство;
- острая форма КК;
- хронический (рецидивирующий) КК.
Кандидоносительство характеризуется отсутствием симптомов заболевания. Однако при микробиологическом исследовании в отделяемом влагалища в небольшом количестве (<104 КОЕ/мл) обнаруживаются почкующиеся формы дрожжеподобных грибов рода Сandida при отсутствии псевдомицелия. Бессимптомное носительство Сandida отмечается у 15-20% небеременных женщин репродуктивного возраста. При бессимптомном носительстве большинство из дрожжеподобных грибов находятся в фазе бластоспоры. Клинические проявления заболевания связаны с переходом в гифальную фазу.
Острая форма КК характеризуется ярко выраженной клинической картиной: гиперемия, отек, обильные или умеренные творожистые выделения из половых путей, высыпания в виде везикул на коже и слизистых оболочках вульвы и влагалища. При микробиологическом исследовании в отделяемом влагалища дрожжеподобные грибы рода Сandida присутствуют в высоком титре (>104 КОЕ/ мл). Длительность заболевания острой формой кандидоза не превышает 2 мес.
Хронический КК характеризуется длительностью заболевания более 2 мес. На коже и слизистых оболочках вульвы и влагалища преобладают вторичные элементы в виде инфильтрации, лихенизации и атрофичности тканей.
После завершения курса лечения, несмотря на отрицательные результаты культурального исследования, эрадикация микроорганизма может быть неполной. Это может привести к возникновению рецидивов, при этом этиологическую роль в их развитии обычно играет тот же штамм.
Рецидивирующий КК определяется как четыре или более обострения заболевания, доказанных микологически, в течение 12 мес. Развивается примерно у 5% пациенток с КК. При этом у 50% женщин с рецидивирующим КК симптомы заболевания появляются в интервале от нескольких дней до 3 мес после успешного излечения острой формы.
Хроническое и рецидивирующее течение объясняется некоторыми авторами глубоким проникновением гриба в клетки многослойного эпителия и образованием фагосом, в которых морфологически не измененные кандиды могут длительное время существовать и даже размножаться, будучи защищенными от действия лекарственных препаратов.
По мнению ряда авторов, причиной рецидива КК может быть снижение чувствительности грибов Сandida к противогрибковым препаратам. По мнению других авторов, причинами рецидивирующего КК являются изменения в локальном и клеточном иммунитете на уровне слизистой оболочки влагалища. Меньшее значение имеют гуморальный и врожденный иммунитет. Т-хелпер(Т)1- и Т2-опосредованные клеточные реакции коррелируют с резистентностью и предрасположенностью к кандидозу слизистых оболочек.
Реактивность Т1-типа с продукцией стимулирующих макрофагов и полиморфноядерных лимфоцитов, а также IgА слизистой оболочки являются доминирующими реакциями во влагалище. Они поддерживают бессимптомную колонизацию кандид. Реактивность Т2-типа с образованием интерлейкина(ИЛ)-4-6, ИЛ‑10, IgG, гистамина и простагландина Е2 преобладает в тех случаях, когда эндогенные и экзогенные факторы приводят к увеличению числа микроорганизмов C. albicans. Этот ответ «выключает» защитные реакции Т1-типа и запускает реакции гиперчувствительности немедленного типа [2]. Candida из фазы бластоспоры переходит в фазу гифы, и возникает инвазия эпителия. Определенное значение в развитии рецидивирующего КК имеют факторы вирулентности Candida, среди которых выделяют чувствительность к антимикотикам, трансформацию бластоспор C. albicans в гифы.
Распространение КК, вызванного дрожжевыми грибами, отличными от C. albicans, привело к появлению термина «non-albicans кандидоз» (НАК). Некоторые исследователи склонны относить НАК к осложненному КК, мотивируя это частой ассоциацией НАК с хроническим рецидивирующим течением заболевания, трудно излечиваемого традиционными антимикотическими препаратами. Отличная от C. albicans этиология отмечается чаще у женщин старше 35 лет. Имеется ряд клинико-эпидемиологических и лабораторных характеристик, позволяющих клиницисту диагностировать НАК. Подобный диагноз можно предположить у больных с рецидивами КК после неоднократного применения антимикотиков, у пациенток, предъявляющих жалобы на зуд при незначительных выделениях из половых путей, у пациенток с проявлениями бактериального вагиноза или при обнаружении сопутствующей инфекции, передающейся половым путем, а также в случае отсутствия псевдомицелия грибов при микроскопии вагинального мазка.
Лечение кандидозного кольпита
Проблема резистентности к терапии
Одним из вопросов, важных для гинекологов, которые сталкиваются с проблемой КК, является причина резистентности к терапии. Среди известных видов Candida 20 патогенны для человека, из которых 8 чаще выделяются от больных кандидозом, а 4 признаны главными возбудителями: Candida albicans, Candida tropicalis, Candida рarapsilosis, Candida glabrata.
Основная причина, которая заставляет обращать внимание на этиологическую неоднородность кандидоза, – это устойчивость части видов к антимикотическим препаратам. Для понимания причин устойчивости к антимикотикам необходимо вспомнить о механизмах их действия. В большинстве случаев это фунгистатический эффект, благодаря которому антимикотики не убивают, а лишь останавливают размножение грибов, за счет чего колонии возбудителя со временем погибают. Данный фунгистатический, а не фунгицидный, механизм и предопределяет возможность развития устойчивости.
Несмотря на бурное развитие фармакологической индустрии и огромный выбор антимикотических препаратов, проблема лечения КК не утрачивает своей актуальности.
Выбор антимикотика для лечения кандидозного кольпита
Необходимость использования наиболее эффективных антимикотиков адекватного спектра действия для исключения возможных рецидивов после лечения острого КК является важной задачей.
Залаин – антимикотик сертаконазол, производное бензотиофена и имидазола в виде вагинального суппозитория.
По механизму действия Залаин оказывает не только фунгистатическое, но и фунгицидное воздействие на возбудителя. Дополнительный фунгицидный механизм действия обусловлен наличием в структуре препарата, помимо азолового кольца, бензотиофена. Азоловая структура препятствует синтезу эргостерина (эргостерол), одного из основных компонентов мембраны грибковой клетки, обусловливая тем самым фунгистатический эффект. Непосредственной мишенью для действия азолов является фермент ланостирол-С-14-деметилаза, участвующий в синтезе эргостерола.
В развитии устойчивости могут быть задействованы механизмы снижения концентрации препарата в клетке за счет сокращения его поступления или, наоборот, усиленного выведения из клетки, разрушение или химическая модификация препарата на его пути к мишени, нарушенное взаимодействие с мишенью за счет ее видоизменения или исчезновения.
Кроме того, существуют адаптационные механизмы, при которых количество ферментов-мишеней возрастает до такой степени, что препарата для связи с ними не хватает, а также запасные пути метаболизма [3]. Бензотиофен в составе сертаконазола вызывает разрыв плазматической мембраны грибковой клетки, что и приводит к ее гибели, т. е. оказывает фунгицидное действие. Бензотиофен обладает высокой липофильностью, чем усиливает проникновение сертаконазола в ткани. Благодаря такому механизму действия риск развития рецидивов при лечении КК становится минимальным. Механизм действия препарата Залаин представлен на рис. 1.
Помимо высокоэффективного антимикотического действия (грибы рода Candida и другие дрожжевые грибы, дерматофиты: Trichophyton, Microsporum, Epidermophiton) Залаин обладает действием на неспецифическую флору: Streptococcus spp., Staphillococcus spp. Сертаконазол при местном применении обладает практически нулевой биодоступностью, не обнаруживается в плазме и моче, в связи с чем возможно его применение во время беременности, если врач считает необходиым.
Назначение Залаина при КК характеризуется быстрым исчезновением симптомов и клинических проявлений заболевания и отрицательным результатом микроскопического исследования влагалищных мазков и культурального анализа [4]. По данным В.Н. Серова (2014) [5], эффективность терапии Залаином составила 100% у 84 пациенток с КК, ранее использовавших терапию как местными, так и системными антимикотиками (клотримазол, флуконазол, натамицин, кетоконазол, эконазол, миконазол).
Возможна также комбинированная терапия Залаина с системными антимикотиками при рецидивах. Также отмечена эффективность использования крема Залаин при признаках распространения КК на кожу вульвы и при баланопостите у полового партнера [6].
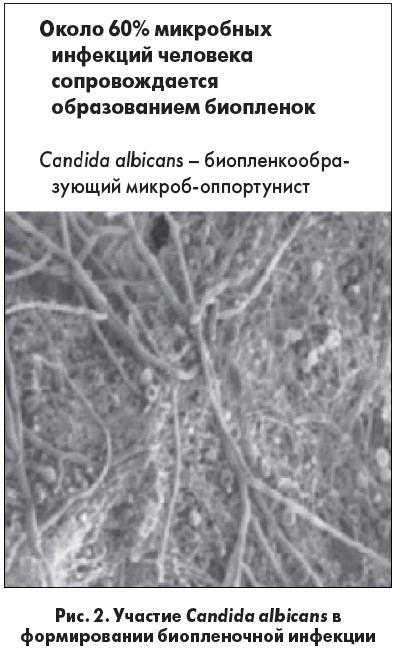
КК – распространенный пример биопленочной инфекции, в которой грибы рода Candida выступают в роли оппортунистов, участвуя в формировании биопленок другими микроорганизмами – инициаторами построения биопленок [8] (рис. 2). В этом отношении доказанная антимикробная активность Залаина (грибы, стрептококки, стафилококки) повышает результативность лечения КК.
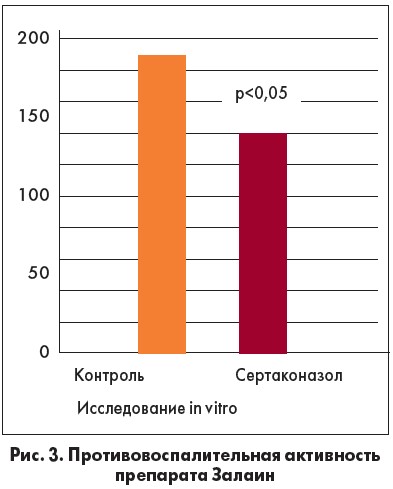
Кроме этого установлено, что препарат уменьшает клинические проявления воспаления на 40% по сравнению с контролем за счет продукции оксида азота, который ингибирует активность 5-циклооксигеназы, липооксигеназы, т.е. ингибирует метаболизм арахидоновой кислоты в очаге воспаления, что было доказано в экспериментах на лабораторных животных (рис. 3).
При этом у препарата Залаин отсутствует системная абсорбция – препарат можно применять без негативных последствий для организма. Использование Залаина не нарушает защитный механизм вагинального биотопа – препарат не ингибирует рост Lactobacillus, а значит, нет «эффекта пинг-понга»: был кандидоз – стал вагиноз [9].
Высокий уровень клинической эффективности сертаконазола (более 95%), короткий курс лечения и удобство применения (однократно 1 свеча на ночь), широкий спектр активности, отсутствие побочных эффектов и системного воздействия, возможность использования по назначению врача при беременности и лактации подтверждают эффективность назначения Залаина при лечении острого вульвовагинального кандидоза.
Список литературы находится в редакции.