19 грудня, 2019
Коррекция нарушений адаптации как неотъемлемый компонент лечения ОРВИ у детей
 Несколько лет назад Всемирная организация здравоохранения (ВОЗ) определила основные задачи устойчивого развития здравоохранения, которые необходимо выполнить до 2030 года. В контексте этой стратегии одно из главных заданий педиатров – положить конец предотвратимой смертности новорожденных и детей в возрасте до 5 лет. В процессе достижения этой цели детские врачи столкнулись с двумя проблемами: интенсивным ростом инфекционных заболеваний (по мнению международных сообществ, эта тенденция влияет на темп прогресса человечества) и критическим дефицитом детских лекарственных препаратов во всем мире из-за ограниченных возможностей проведения клинических исследований с участием детей. Поэтому реализация определенных ВОЗ задач невозможна без внедрения современных препаратов с максимальным уровнем эффективности и безопасности.
Несколько лет назад Всемирная организация здравоохранения (ВОЗ) определила основные задачи устойчивого развития здравоохранения, которые необходимо выполнить до 2030 года. В контексте этой стратегии одно из главных заданий педиатров – положить конец предотвратимой смертности новорожденных и детей в возрасте до 5 лет. В процессе достижения этой цели детские врачи столкнулись с двумя проблемами: интенсивным ростом инфекционных заболеваний (по мнению международных сообществ, эта тенденция влияет на темп прогресса человечества) и критическим дефицитом детских лекарственных препаратов во всем мире из-за ограниченных возможностей проведения клинических исследований с участием детей. Поэтому реализация определенных ВОЗ задач невозможна без внедрения современных препаратов с максимальным уровнем эффективности и безопасности.
По последним данным Центра медицинской статистики Министерства здравоохранения Украины, в структуре детской заболеваемости доминируют болезни органов дыхания – их доля составляет 67%. Около 85% детей с поражением дыхательной системы – часто болеющие дети (ЧБД). ЧБД – это проблема, для решения которой необходимо расширить границы знаний об острых респираторных вирусных инфекциях (ОРВИ) и рассматривать патологию не только в аспекте купирования проявлений острой фазы, но и возможного воздействия на нарушения процессов адаптации детского организма.
Этиология ОРВИ
На сегодня насчитывается более 200 вирусных возбудителей ОРВИ. Их классифицируют на типичные возбудители (вирус гриппа А, В и С), респираторно-синцитиальный вирус (РСВ А и В), вирус парагриппа (типа 1, 2, 3, 4А, 4В), аденовирусы (>51 серотипа), риновирусы (>100 типов), коронавирус (229Е, ОС43), вирус Коксаки, ЕСНО, герпес-вирусы (HSV 1, 2, 4, 5 и 6 типа A, B), новые и активируемые типичные возбудители (коронавирус ТОРС, NL63, HKU1, MERS-CoV), риновирус (тип С), аденовирус (тип 14), а также новые возбудители (метапневмовирус, бокавирус, мимивирус, полиомавирусы KI, WU и Merkel Cell, вирусы Мелака, гриппа A (H1N1)pdm09, Эбола – 2014 г., Зика – 2015 г. (Е.И. Бурцева, 2015).
В большинстве случаев при ОРВИ у пациента врач сталкивается с микст-инфекцией, справиться с которой гораздо сложнее, и в результате из-за неадекватной терапии таких пациентов пополняется категория ЧБД.
Часто болеющие дети: междисциплинарная проблема адаптации
Проблема ЧБД – это «черный ящик» для педиатров, так как в ходе их ведения сложно спрогнозировать отдаленные последствия. Изначально такие пациенты имеют повышенную восприимчивость иммунной системы, хронические очаги инфекции, аллергические, аутоиммунные, обменные расстройства. Обычно ЧБД поздно назначается противовирусная терапия, либо арсенал применяемых препаратов очень ограничен. При оптимистическом сценарии все-таки удается достичь выздоровления ребенка, но через некоторое время заболевание рецидивирует. Это связано с отсутствием адекватного восстановления иммунной системы, формированием хронического нейровегетативного стресса, астенизацией, развитием дисбактериоза, ферментативной недостаточности, и это далеко не весь перечень возможных нарушений.
Таким образом, ЧБД – это междисциплинарная проблема адаптации, и лечение таких пациентов должно быть направлено не только на устранение возбудителя ОРВИ, иммунного дисбаланса, но и на коррекцию дисфункции нервной системы.
В основе патогенеза ОРВИ лежат две составляющие – цитопатическое влияние вируса и реакция внутритканевых и органных систем защиты. Известно, что репродукция вирусов происходит в митохондриях. Это провоцирует уменьшение синтеза АТФ и возникновение «энергетического голода», что приводит к снижению функциональной активности иммунокомпетентных клеток у ЧБД и обострению хронических воспалительных заболеваний и хронизации вирусной инфекции, развитию частых инфекционных процессов, синдрома поствирусной астении (Т.П. Маркова и соавт., 2010). Кроме того, в состоянии энергетического дефицита иммунокомпетентные клетки создают условия астенизации с развитием дисфункций нервной системы.
 Результаты современных исследований объясняют общие принципы функционирования нервной и иммунной систем и механизмы двустороннего нейроиммунологического взаимодействия. «Прямой диалог» нервной и иммунной систем осуществляется через лимфоциты, которые имеют рецепторы к нейромедиаторам и нейропептидам, Т-клетки, которые способны преодолевать гематоэнцефалический барьер, и цитокины, влияющие на выделение и обмен норадреналина и серотонина в головном мозге, в особенности в гипоталамусе – ключевом звене центрального аппарата нервной регуляции и функций иммунной системы (J.L. Paradise et al., 2014). Установлено, что тучные клетки, кроме цитокинов, интерлейкинов и гистаминов, вырабатывают фактор роста нервных клеток, который определяет выживаемость нейронов, защищает их от апоптоза, регулирует метаболизм в центральной нервной системе. В свою очередь, нейроны продуцируют нейротинин, субстанцию Р, влияние которых приводит к увеличению числа тучных клеток и их гиперплазии (А.П. Парахонский, 2007). Эти открытия объясняют наличие у ЧБД функциональных расстройств нервной системы (астеновегетативного синдрома), которые клинически проявляются соматическими нарушениями (учащенное сердцебиение, затрудненное дыхание, дискомфорт в эпигастральной области, учащенное мочеиспускание, боль в мышцах), эмоциональными (лабильность, повышенная утомляемость, сонливость, беспричинный плач, капризность) и поведенческими (потеря интереса и мотивации к учебе, снижение концентрации, памяти, нарушения речи, почерка) расстройствами (Е.В. Михайлова, 2009).
Результаты современных исследований объясняют общие принципы функционирования нервной и иммунной систем и механизмы двустороннего нейроиммунологического взаимодействия. «Прямой диалог» нервной и иммунной систем осуществляется через лимфоциты, которые имеют рецепторы к нейромедиаторам и нейропептидам, Т-клетки, которые способны преодолевать гематоэнцефалический барьер, и цитокины, влияющие на выделение и обмен норадреналина и серотонина в головном мозге, в особенности в гипоталамусе – ключевом звене центрального аппарата нервной регуляции и функций иммунной системы (J.L. Paradise et al., 2014). Установлено, что тучные клетки, кроме цитокинов, интерлейкинов и гистаминов, вырабатывают фактор роста нервных клеток, который определяет выживаемость нейронов, защищает их от апоптоза, регулирует метаболизм в центральной нервной системе. В свою очередь, нейроны продуцируют нейротинин, субстанцию Р, влияние которых приводит к увеличению числа тучных клеток и их гиперплазии (А.П. Парахонский, 2007). Эти открытия объясняют наличие у ЧБД функциональных расстройств нервной системы (астеновегетативного синдрома), которые клинически проявляются соматическими нарушениями (учащенное сердцебиение, затрудненное дыхание, дискомфорт в эпигастральной области, учащенное мочеиспускание, боль в мышцах), эмоциональными (лабильность, повышенная утомляемость, сонливость, беспричинный плач, капризность) и поведенческими (потеря интереса и мотивации к учебе, снижение концентрации, памяти, нарушения речи, почерка) расстройствами (Е.В. Михайлова, 2009).
Доказанная взаимосвязь функционирования нервной и иммунной систем, их влияние друг на друга в патологических условиях (в данном случае при ОРВИ) обосновывают включение в комплексную схему терапии мероприятий по улучшению функций нервной системы ребенка. Лечение астеновегетативного синдрома у детей включает немедикаментозные методы (правильный распорядок дня и питание, адекватную физическую нагрузку) и медикаментозную коррекцию с помощью вегетотропных, ноотропных препаратов, успокоительных средств, витаминно-минеральных комплексов. Но могут применяться средства комплексного действия, позволяющие избежать полипрагмазии. Таким препаратом является Тенотен Детский, который оказывает одновременно и ноотропное, и успокаивающее, и вегетотропное, и нейропротекторное действие. При изучении динамики клинических проявлений в период напряжения адаптационно-компенсаторных реакций у пациентов с ОРВИ после 3 месяцев терапии препаратом Тенотен Детский выявлено, что данное лекарственное средство ускоряет процесс восстановления после перенесенного заболевания (Ю.Н. Хлыповка и соавт., 2017). В ходе клинического исследования установлено, что применение препарата Тенотен Детский в составе комплексного лечения детей с астеновегетативным синдромом после перенесенной ОРВИ позволяет устранить более чем у 70% пациентов вегетативные и психоэмоциональные нарушения (рис. 1). Таким образом Тенотен Детский способствует более быстрому завершению реабилитационного периода после ОРВИ.
Этиотропное лечение ОРВИ: проблемы и решения
 Современная теория «идеального лекарства» заключается в создании препаратов, комплементарных биологической мишени, что лежит в основе таргетной терапии. Единственными таргетными препаратами являются средства, содержащие антитела. Но широкое применение этих препаратов ограничено из-за видовых различий фрагментов антител человека и животных (на основе которых синтезируется большинство медикаментов) и риска аллергизации организма из-за чужеродности антител. Решением этих проблем является использование высоких разведений антител. Это позволяет модификатору действующего вещества легко проникать через мембраны пораженных клеток, регулировать некоторые биохимические процессы и восстанавливать функции клеток изнутри.
Современная теория «идеального лекарства» заключается в создании препаратов, комплементарных биологической мишени, что лежит в основе таргетной терапии. Единственными таргетными препаратами являются средства, содержащие антитела. Но широкое применение этих препаратов ограничено из-за видовых различий фрагментов антител человека и животных (на основе которых синтезируется большинство медикаментов) и риска аллергизации организма из-за чужеродности антител. Решением этих проблем является использование высоких разведений антител. Это позволяет модификатору действующего вещества легко проникать через мембраны пораженных клеток, регулировать некоторые биохимические процессы и восстанавливать функции клеток изнутри.
В 2017 г. украинские врачи получили право руководствоваться в своей работе международными клиническими протоколами. Это расширило возможности специалистов в лечении многих заболеваний, кроме ОРВИ, так как в современных европейских и американских рекомендациях в терапевтические схемы лечения пациентов с ОРВИ не входят противовирусные препараты (кроме ингибиторов нейраминидазы, которые используют только для лечения гриппа у ограниченной категории пациентов) из-за их возможного непредсказуемого иммуностимулирующего воздействия. Возникает вопрос: неужели мировое медицинское сообщество отказывается от этиотропного лечения ОРВИ? Напротив, согласно официальной инициативе ВОЗ 2013 г., «в борьбе с респираторными вирусами остро стоит вопрос о необходимости разработки и внедрения новых безопасных и эффективных противовирусных средств с широким спектром активности».
Современное противовирусное средство: критерии, механизм действия, эффективность
Учитывая все преимущества препаратов таргетной терапии с одновременным устранением возможных ограничений их применения и с целью максимально безопасного восстановления иммунной системы во многих странах с 2010 г. успешно применяется препарат иммуномодулирующего действия – Эргоферон. Он отвечает основным требованиям к противовирусным средствам: имеет широкий спектр противовирусной активности и низкую токсичность (возможность использования с 6 мес), оказывает саморегулирующее иммуномодулирующее действие, подавляет сенсибилизацию слизистых оболочек вирусом, снижает риск развития осложнений ОРВИ и обострения хронической патологии, не провоцирует развитие резистентности, поэтому его можно применять многократно.
 В состав комплексного препарата Эргоферон входят сотенные разведения антител к интерферону (ИФН) гамма, CD4 и гистамину. Антитела к ИФН-γ и CD4 обеспечивают распознавание вирусов, останавливают их размножение, обезвреживают возбудителей (противовирусное и иммуномодулирующее действие), антитела к гистамину уменьшают отек слизистой оболочки дыхательных путей, выраженность аллергических реакций, снижают тонус гладких мышц бронхов (противовоспалительное и антигистаминное действие). Таким образом, препарат реализует одновременно этиотропную и патогенетическую терапию ОРВИ с широким спектром активности, включая грипп.
В состав комплексного препарата Эргоферон входят сотенные разведения антител к интерферону (ИФН) гамма, CD4 и гистамину. Антитела к ИФН-γ и CD4 обеспечивают распознавание вирусов, останавливают их размножение, обезвреживают возбудителей (противовирусное и иммуномодулирующее действие), антитела к гистамину уменьшают отек слизистой оболочки дыхательных путей, выраженность аллергических реакций, снижают тонус гладких мышц бронхов (противовоспалительное и антигистаминное действие). Таким образом, препарат реализует одновременно этиотропную и патогенетическую терапию ОРВИ с широким спектром активности, включая грипп.
Эргоферон обладает комплексным действием за счет усиленного противовирусного, противовоспалительного, антигистаминного эффектов. Спектр действия препарата Эргоферон распространяется на основные респираторные вирусные возбудители, в том числе и на микст-инфекции. Эргоферон воздействует на адаптивный отдел врожденного иммунитета, запуская продукцию Т-клеток памяти, стимулирует образование сигнальных путей толерантности, угнетает аллергическую готовность организма.
Важное условие достижения эффекта терапии – соблюдение схемы лечения. В первый день противовирусной терапии необходимо принять 8 таблеток (независимо от возраста и массы тела пациента): по 1 таблетке каждые 30 мин (5 таблеток), затем по 1 таблетке через равные промежутки времени (3 таблетки). Со второго дня лечения Эргоферон следует принимать по 1 таблетке 3 раза в сутки.
Эргоферон одинаково эффективен при гриппе и других ОРВИ вне зависимости от сроков начала заболевания, он действует через систему собственных ИНФ (продукцию и рецепцию ИФН) и CD4-клеток.
Эргоферон и доказательная база
 Эффективность и безопасность препарата Эргоферон подтверждается результатами двойных слепых плацебо-контролируемых исследований, которые имеют высокий уровень доказательности А.
Эффективность и безопасность препарата Эргоферон подтверждается результатами двойных слепых плацебо-контролируемых исследований, которые имеют высокий уровень доказательности А.
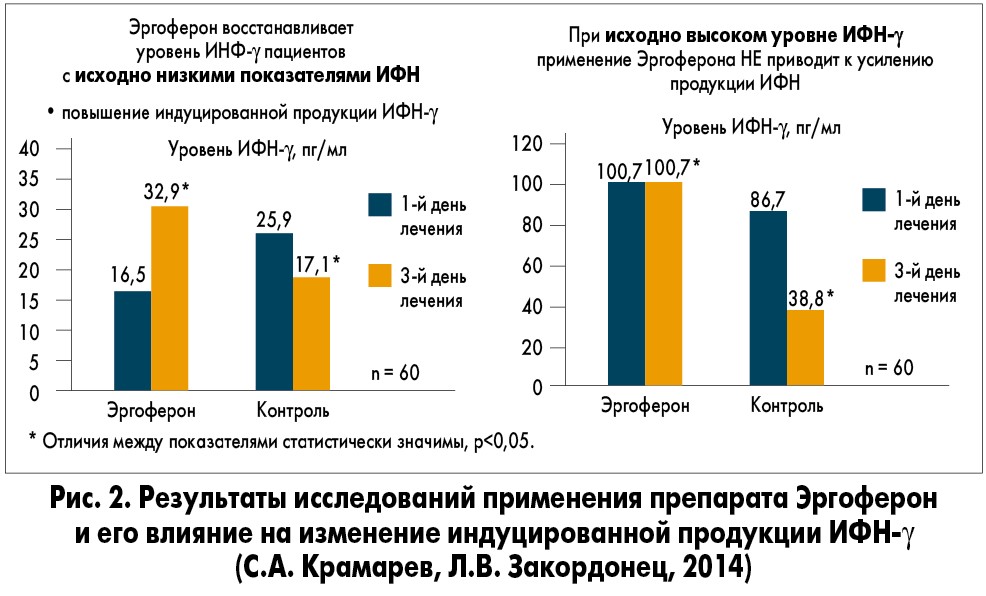
В исследовании украинских ученых С.А. Крамарева и Л.В. Закордонец (2014) было доказано саморегулирующее воздействие на иммунитет за счет восстановления уровня ИФН-γ на фоне лечения препаратом Эргоферон детей со среднетяжелым течением ОРВИ при исходно низком показателе. Прием препарата не приводит к усилению продукции ИФН при его исходно высоком уровне (рис. 2).
Основная угроза здоровью пациента, которую представляют респираторные вирусы, состоит в том, что они подавляют функциональную активность различных звеньев иммунной системы и приводят к обострению хронических заболеваний, развитию вторичных бактериальных осложнений, а также способны индуцировать аллергические реакции (Л.А. Степанищева, 2012; И.В. Николаева, 2014). В ряде исследований было показано, что Эргоферон помогает предотвратить развитие бактериальных осложнений (С.А. Крамарев и соавт., 2014; В.К. Веревщиков, 2011).
В масштабном наблюдательном исследовании ЭРМИТАЖ (8 стран, 8411 пациентов*) было доказано, что препарат Эргоферон – эффективное и безопасное средство для лечения гриппа и ОРВИ (Н.А. Геппе и соавт., 2017).
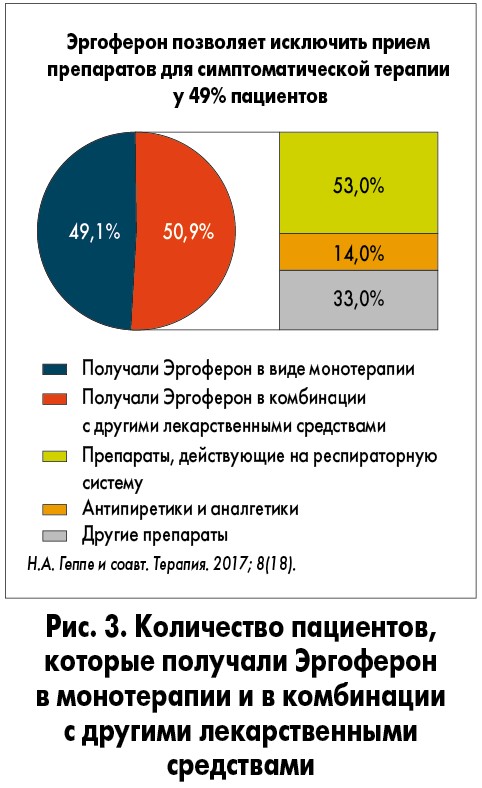
- Эргоферон позволяет исключить прием средств для симптоматической терапии ОРВИ и гриппа у каждого 2-го (49%) пациента (рис. 3).
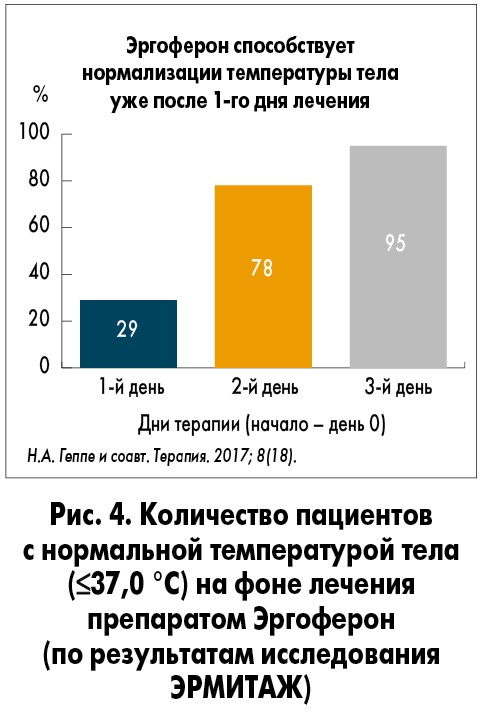
- Эргоферон нормализует температуру тела уже после 1-го дня лечения у 29% пациентов, после 2-го – у 78% (рис. 4).
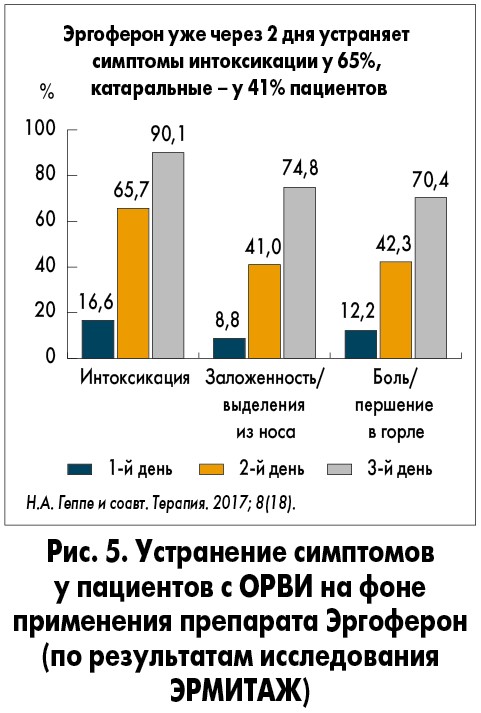
- Эргоферон уже через 2 дня устраняет симптомы интоксикации у 65%, катаральные – у 41% пациентов (рис. 5).
* Из 8411 пациентов участников исследования ЭРМИТАЖ 71,4% составили дети (n=6005; 49,2% – мальчики, 48,1% – девочки, 1,5% – без уточнения пола) и 24,6% (n=2069) – взрослые (42,8% – мужчины, 55,5% – женщины, 1,8% – без уточнения пола по данным ИРК). В 337 ИРК (4,0%) отсутствовало указание возраста пациента. Средний возраст детей составил 6,8±4,6 года (от 6 мес до 18 лет), взрослых – 36,8±14,1 года (от 18 до 90 лет).
Тематичний номер «Педіатрія» №4 (51), 2019 р.