23 грудня, 2019
Дискуссионные вопросы диагностики, применения антибиотиков и лекарственных средств растительного происхождения при острых риносинуситах у взрослых
.jpg) Риносинусит – это воспаление околоносовых пазух и полости носа, сопровождающееся симптомами [1]. Данный термин предпочтительнее, нежели «синусит», поскольку последний почти всегда сопровождается воспалением прилегающей слизистой оболочки носа [2-4].
Риносинусит – это воспаление околоносовых пазух и полости носа, сопровождающееся симптомами [1]. Данный термин предпочтительнее, нежели «синусит», поскольку последний почти всегда сопровождается воспалением прилегающей слизистой оболочки носа [2-4].
При неосложненном риносинусите отсутствует клинически явное распространение воспаления за пределы околоносовых пазух и полости носа (например, неврологические, офтальмологические симптомы или признаки вовлечения мягких тканей). Если больной в течение года переносит ≥4 задокументированных эпизодов риносинусита длительностью не менее 7 дней каждый, а в промежутках между ними симптомы заболевания отсутствуют, имеет место рецидивирующий острый риносинусит (ОРС) [8].
Этиология
Подавляющее большинство случаев ОРС – вирусной этиологии. Только 0,5-2,0% эпизодов вирусного ОРС у взрослых осложняются присоединением бактериальной инфекции [9]. Среди бактериальных возбудителей чаще всего встречаются S. pneumoniae (20-43% случаев), H. influenzae (22-35%) и M. catarrhalis (2-10%, чаще у детей) [1, 5, 10]. Примерно у 10% пациентов удается выделить S. aureus, однако его роль в возникновении острого бактериального риносинусита (ОБРС) убедительно не доказана. Выделение стафилококков или других бактерий при посеве мазков из полости носа или носоглотки не позволяет ни судить об этиологии ОРС, ни отличить вирусный синусит от бактериального, поскольку плохо коррелирует с результатами культурального исследования аспирата из околоносовых пазух [11]. В свою очередь, пункция верхнечелюстных (гайморовых) пазух в амбулаторной практике используется крайне редко из-за трудоемкости, болезненности для пациентов, да и отсутствия, как правило, клинической необходимости. Поэтому антибиотики – при наличии показаний – назначаются в подавляющем большинстве случаев эмпирически.
Диагностика ОРС
В Европе и Украине принято следующее клиническое определение ОРС:
- воспаление носа и околоносовых пазух, характеризующееся ≥2 симптомами, одним из которых должна быть заложенность/закупорка/отек носа или выделения из носа (переднее или заднее назальное стекание):
- ± боль или давление в области лица;
- ± ослабление или утрата обоняния
и/или
- эндоскопические признаки:
- назальных полипов и/или
- слизисто-гнойного отделяемого, главным образом из среднего носового хода, и/или
- отека/закупорки слизью, главным образом из среднего носового хода
и/или
- изменения на КТ:
- изменения слизистой оболочки в остиомеатальном комплексе и/или синусах [3, 4].
Такое определение уравнивает значимость клинических признаков (жалоб и симптомов заболевания) и результатов инструментальных исследований (эндоскопии и КТ). Далеко не все профессиональные сообщества врачей придерживаются подобного подхода.
Американские академия и колледж аллергии, астмы и иммунологии опираются прежде всего на клинические признаки. Согласно их рекомендациям, ОРС диагностируется при наличии некоторых или всех из нижеперечисленных признаков, если они сохраняются менее 12 нед:
- персистирующая инфекция верхних дыхательных путей;
- гнойная ринорея;
- постназальный дренаж;
- аносмия (утрата обоняния);
- отек носа;
- боль в области лица;
- головная боль;
- лихорадка;
- кашель [12].
В свою очередь, эксперты Американской академии отоларингологии / Фонда хирургии головы и шеи (AAO/HNS) предлагают диагностировать ОРС при наличии гнойного отделяемого из носа (переднее/заднее стекание либо и то и другое) в сочетании с заложенностью носа или болью / давлением / ощущением тяжести в области лица либо обоими этими симптомами [1].
Среди отдельных жалоб и объективных признаков в наибольшей степени в пользу ОРС свидетельствуют обнаружение врачом гнойного секрета в среднем носовом ходе пациента, гнусавый голос, жалобы больного на зубную боль и выявление гнойного секрета на задней стенке глотки или заднего стекания. Напротив, отсутствие предшествующей инфекции дыхательных путей и отсутствие любых выделений из носа в наибольшей мере способствуют исключению диагноза ОРС. Клиническое суждение врача о наличии или отсутствии у больного ОРС обладает наибольшей диагностической разграничительной точностью [13].
Бактериальные риносинуситы
ОБРС следует клинически различать с вирусным ОРС. Согласно действующим европейским рекомендациям, диагноз ОБРС устанавливают при наличии не менее 3 из 5 нижеследующих признаков:
- бесцветные выделения из носа (с преобладанием с одной стороны) и гнойное содержимое в полости носа;
- выраженная локальная боль (с преобладанием с одной стороны);
- лихорадка (температура тела >38 °C);
- повышение скорости оседания эритроцитов / концентрации С-реактивного белка;
- «вторая волна» заболевания (то есть ухудшение после начальной нетяжелой фазы болезни) [4].
Эти критерии перечислены и в действующем в Украине протоколе по оказанию помощи больным ОРС [3], причем первый из них сформулирован несколько иначе: «выделения из носа (с преобладанием с одной стороны) [опущено слово «бесцветные»] и одновременное наличие слизистого или гнойного содержимого в полости носа (при риноскопии) [подчеркивается значимость инструментального исследования и обнаружения неважно какого содержимого]».
Согласно рекомендациям AAO/HNS, ОБРС диагностируется, когда жалобы или симптомы ОРС (гнойное отделяемое из носа, сопровождающееся заложенностью носа, лицевой болью / ощущением тяжести либо обоими признаками) не улучшаются на протяжении не менее 10 дней после появления признаков поражения верхних дыхательных путей или вновь ухудшаются в течение 10 дней после первоначального улучшения («вторая волна заболевания»). В отличие от прежней версии этих рекомендаций, для лучшего разграничения бактериального и вирусного ОРС подчеркивается не столько персистирование симптомов заболевания на протяжении 10 дней, сколько отсутствие улучшения [1]. Предложения экспертов AAO/HNS не нашли отражения в отечественном протоколе по оказанию помощи больным синуситом, однако упомянуты, наряду с европейскими, в документе, на основании которого готовился протокол [8].
В соответствии с действующим в Украине протоколом оказания помощи больным ОРС, степень тяжести заболевания определяется врачом. Критерии тяжелого течения риносинусита четко не прописаны, хотя отмечается, что лихорадка >38 °C и гнойные выделения из носа более 3 дней подряд относятся к тяжелым симптомам. Если пациент не соглашается с оценкой степени тяжести какого-либо симптома или общего состояния, сделанной врачом, то она проводится самим пациентом – с использованием визуальной аналоговой шкалы либо произвольно [3]. Использование визуальной аналоговой шкалы или субъективная оценка пациентом как отдельных симптомов («отсутствует», «легкий», «умеренный», «тяжелый»), так и всей их совокупности рекомендуются и в Европе [4].
Синуситы и антибиотики
Учитывая невысокую пользу от лечения антибиотиками, повышенный риск возникновения нежелательных явлений и антибиотикорезистентности, крайнюю редкость осложнений ОРС, авторы Кокрановского обзора не нашли места для использования антибиотиков при лечении взрослых больных с неосложненным ОРС. Не говоря о детях, данный вывод не распространяется на потенциально более уязвимые категории больных, такие как взрослые с иммунодефицитами или тяжелым синуситом (например, с очень высокой температурой тела, длительно сохраняющимися симптомами, признаками сепсиса) и пациенты, направленные к оториноларингологам из-за возникновения (или опасений возникновения) осложнений.
Выводы авторов Кокрановского обзора не совпадают с результатами других метаанализов [15, 16]. Иначе в рутинной клинической практике поступают и врачи. Так, синусит является пятой по значимости причиной назначения антибиотиков врачами первичного звена [17]. Хотя в подавляющем большинстве случаев риносинусит – заболевание вирусной этиологии, вполне вероятно, что в определенных клинических ситуациях антибактериальная терапия оправдана. В каких же именно?
Когда и кому назначать антибиотики?
Несмотря на определенные разногласия в оценках специалистов, антибиотики назначают больным с клиническим диагнозом неосложненного ОБРС при:
- исходно тяжелом течении заболевания (клиническое суждение лечащего врача);
- «второй волне» болезни (ухудшении состояния после первоначального улучшения);
- отсутствии улучшения спустя 7-10 дней симптоматического лечения без антибиотиков.
По-видимому, нет необходимости выжидать 10 дней, прежде чем назначать антибиотики. Авторы Кокрановского обзора не нашли доказательств того, что у больных с симптомами синусита длительностью ≥7 дней до обращения за медицинской помощью вероятность бактериальной этиологии заболевания выше [14]. В согласованном европейском документе рекомендуется назначать антибиотики пациентам с ОРС в случаях, когда длительность симптоматики превышает 10 дней [4]. Авторы недавнего метаанализа планировали оценить эффективность антибактериальной терапии как раз у данной категории пациентов, но не нашли ни одного оригинального исследования, в котором критерием включения была бы длительность симптоматики ≥10 дней. В результате они использовали иной критерий – длительность симптоматики ≥7 дней [16]. Поэтому представляется разумным ограничить период «отсутствия улучшения во время симптоматического лечения без антибиотиков» 7 днями.
Какие антибиотики назначать и как долго?
Антибиотики должны быть активными в отношении вероятных возбудителей ОБРС, а уровень резистентности к ним – невысоким. Для лечения инфекций, вызванных преимущественно пневмококками и гемофильными палочками, обычно используются препараты 4 классов: β-лактамы (пенициллины и цефалоспорины), макролиды, респираторные фторхинолоны и тетрациклины, из которых последние (почти исключительно доксициклин) применяются в последние десятилетия редко, а данные о чувствительности к ним указанных возбудителей в Украине скудные (94% у пневмококков 10 лет назад [18]).
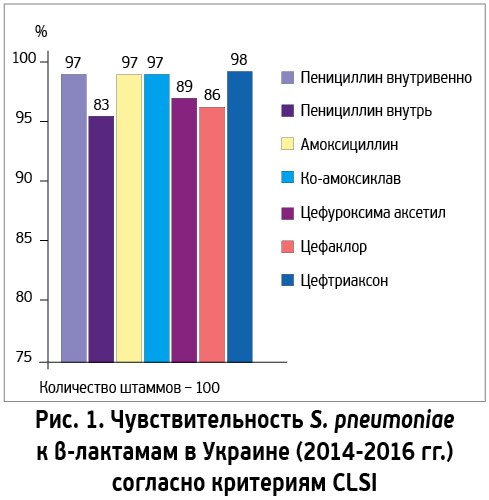 Надежные данные об антибиотикочувствительности пневмококков в Украине доступны за последние 10 лет, гемофильных палочек – за 3 года. В 2010 г. зарегистрирована 100% чувствительность S. pneumoniae к амоксициллину и левофлоксацину, чувствительность к макролидам (кларитромицину и азитромицину) составляла 94-96% [18]. В настоящее время сохраняется очень высокая чувствительность пневмококков к респираторным фторхинолонам (левофлоксацину и моксифлоксацину – 100%), цефтриаксону (98% согласно критериям Института клинических и лабораторных стандартов США (CLSI) и 90% согласно критериям тестирования антибиотикочувствительности Европейского Союза – EUCAST), амоксициллину и амоксициллину/клавуланату (97% по критериям CLSI; рис. 1, 2) [19].
Надежные данные об антибиотикочувствительности пневмококков в Украине доступны за последние 10 лет, гемофильных палочек – за 3 года. В 2010 г. зарегистрирована 100% чувствительность S. pneumoniae к амоксициллину и левофлоксацину, чувствительность к макролидам (кларитромицину и азитромицину) составляла 94-96% [18]. В настоящее время сохраняется очень высокая чувствительность пневмококков к респираторным фторхинолонам (левофлоксацину и моксифлоксацину – 100%), цефтриаксону (98% согласно критериям Института клинических и лабораторных стандартов США (CLSI) и 90% согласно критериям тестирования антибиотикочувствительности Европейского Союза – EUCAST), амоксициллину и амоксициллину/клавуланату (97% по критериям CLSI; рис. 1, 2) [19].
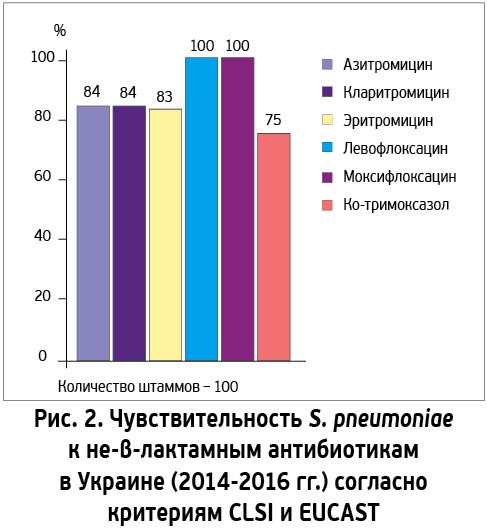
А вот ситуация с макролидами последовательно ухудшалась. Чувствительность к ним S. pneumoniae снизилась до 88% в 2016 г. [20] и 84% – в 2018 г. [19]. Если такая тенденция сохранится и в будущем, эмпирическое использование макролидов для лечения пневмококковых инфекций станет невозможным из-за существенного риска клинических неудач (замедленного выздоровления, осложненного течения болезней, даже гибели пациентов).
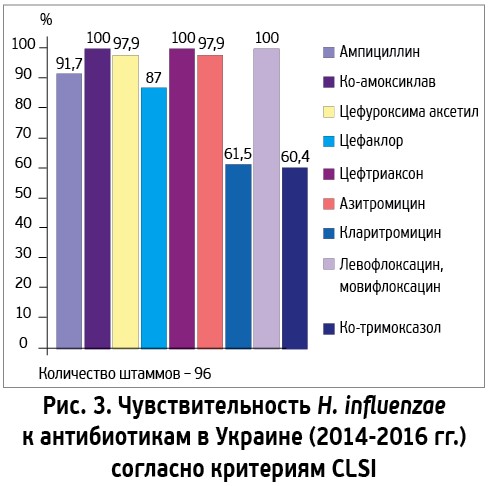
 Что касается гемофильных палочек, то сохраняется 100% чувствительность к цефтриаксону и респираторным фторхинолонам (по критериям CLSI и EUCAST), очень высокая – к амоксициллину/клавуланату (100% – по критериям CLSI; 95,8% – по критериям EUCAST) (рис. 3). Чувствительность H. influenzae к ампициллину снизилась незначительно – с 94 до 91,7% (по критериям CLSI), причем 7,3% резистентности обусловлены выработкой бактериями β-лактамаз, еще 1% – другими механизмами резистентности [19, 20]. Наиболее противоречивы данные о чувствительности гемофильных палочек к макролидам. Согласно американским критериям, чувствительность к азитромицину остается очень высокой (97,9%), хотя и не 100%, как было 2 года назад [19, 20]. Однако в соответствии с европейскими критериями она составляет ничтожные 2,1% [19]. Дело в том, что европейские микробиологи рассматривают H. influenzae как бактерии, обладающие природной резистентностью к макролидам. Нет оснований упрекать американских или европейских микробиологов в непрофессионализме, но все же хотелось бы, чтобы они пришли к единому мнению, поскольку их данные непосредственно влияют на принятие клинических решений об использовании тех или иных антибиотиков для лечения больных.
Что касается гемофильных палочек, то сохраняется 100% чувствительность к цефтриаксону и респираторным фторхинолонам (по критериям CLSI и EUCAST), очень высокая – к амоксициллину/клавуланату (100% – по критериям CLSI; 95,8% – по критериям EUCAST) (рис. 3). Чувствительность H. influenzae к ампициллину снизилась незначительно – с 94 до 91,7% (по критериям CLSI), причем 7,3% резистентности обусловлены выработкой бактериями β-лактамаз, еще 1% – другими механизмами резистентности [19, 20]. Наиболее противоречивы данные о чувствительности гемофильных палочек к макролидам. Согласно американским критериям, чувствительность к азитромицину остается очень высокой (97,9%), хотя и не 100%, как было 2 года назад [19, 20]. Однако в соответствии с европейскими критериями она составляет ничтожные 2,1% [19]. Дело в том, что европейские микробиологи рассматривают H. influenzae как бактерии, обладающие природной резистентностью к макролидам. Нет оснований упрекать американских или европейских микробиологов в непрофессионализме, но все же хотелось бы, чтобы они пришли к единому мнению, поскольку их данные непосредственно влияют на принятие клинических решений об использовании тех или иных антибиотиков для лечения больных.
 Итак, самая высокая чувствительность у S. pneumoniae и H. influenzae зарегистрирована по отношению к респираторным фторхинолонам и цефтриаксону. Однако по ряду причин фторхинолоны не рекомендуется использовать в качестве препаратов выбора для лечения нетяжелых, склонных к самостоятельному излечению инфекций – в силу их широкого спектра действия, из-за опасений возникновения к ним резистентности, из-за риска промедления с диагностикой туберкулеза и др. Цефтриаксон, который существует только в лекарственной форме для парентерального введения, также мало пригоден для широкого использования в амбулаторной практике. Поэтому препаратом выбора при лечении больных ОБРС является амоксициллин – с клавулановой кислотой или без нее [1]. Продолжительность антибактериальной терапии у взрослых составляет 5-7-10 дней, у детей – 10-14 дней [1, 5].
Итак, самая высокая чувствительность у S. pneumoniae и H. influenzae зарегистрирована по отношению к респираторным фторхинолонам и цефтриаксону. Однако по ряду причин фторхинолоны не рекомендуется использовать в качестве препаратов выбора для лечения нетяжелых, склонных к самостоятельному излечению инфекций – в силу их широкого спектра действия, из-за опасений возникновения к ним резистентности, из-за риска промедления с диагностикой туберкулеза и др. Цефтриаксон, который существует только в лекарственной форме для парентерального введения, также мало пригоден для широкого использования в амбулаторной практике. Поэтому препаратом выбора при лечении больных ОБРС является амоксициллин – с клавулановой кислотой или без нее [1]. Продолжительность антибактериальной терапии у взрослых составляет 5-7-10 дней, у детей – 10-14 дней [1, 5].
Почему амоксициллин? Прежде всего потому, что он:
- активен в отношении ключевых возбудителей ОБРС;
- эффективен (доказано в многочисленных рандомизированных клинических исследованиях (РКИ) в разных странах мира);
- безопасен;
- недорогой;
- обладает сравнительно узким спектром микробиологической активности.
Эксперты Американского общества инфекционных заболеваний (IDSA) высказались за то, чтобы лечение ОБРС у детей и взрослых начинать сразу с амоксициллина/клавуланата [5]. Основными аргументами в пользу такой рекомендации были следующие:
- в США доля H. influenzae в этиологии риносинуситов существенно возросла со времени внедрения в клиническую практику конъюгированных противопневмококковых вакцин [21];
- резистентность H. influenzae к ампициллину вследствие выработки β-лактамаз в 2005-2007 гг. составляла 27-43% [22].
Однако в Украине 7- и 13-валентые конъюгированные противопневмококковые вакцины не используются (по крайней мере, широко). Поэтому можно полагать – хотя бы до тех пор, пока не будет доказано обратное, – что этиологическая значимость пневмококков в нашей стране остается высокой, а гемофильных палочек – существенно ниже. Распространенность же штаммов H. influenzae, продуцирующих β-лактамазы, в Украине невысокая (7,3%) [19]. Поэтому в настоящее время нет оснований отказываться от приоритетного выбора амоксициллина. В его поддержку высказались и американские эксперты AAO/HNS в последних рекомендациях (2015 г.) [1]. В действующем в Украине протоколе по оказанию помощи больным ОРС препаратом выбора указан амоксициллин/клавуланат [3]. И во многих случаях он действительно таковым и является. Для характеристики соблюдения больным рекомендаций врача специалисты Международного общества по фармакоэкономике и изучению исходов (ISPOR) используют два понятия: приверженность к лечению (синоним – комплаентность) и постоянство. Проблема постоянства, то есть приема антибиотиков на протяжении всего предписанного курса лечения, на самом деле далеко не праздная. Досрочное прекращение лечения (потому что больной ощущает себя выздоровевшим, возникли побочные эффекты или по любой другой причине) сопряжено с риском рецидивов, возникновения осложнений, повторного инфицирования и т. д. В этой связи обнадеживают недавние данные о сопоставимой эффективности менее продолжительных (5-7 дней) и традиционных (10-14 дней) курсов антибактериальной терапии риносинуситов. Поэтому рекомендуемая длительность курса лечения взрослых больных составляет 5-7 (до 10) дней [1, 5]. В то же время доступные данные не позволяют обосновать эффективность и безопасность менее продолжительных курсов антибактериальной терапии риносинуситов у детей. Поэтому ее длительность пока остается неизменной – 10-14 дней [5].
Эффективность антибактериальной терапии при многих инфекциях, в частности при пневмониях, принято оценивать спустя 48-72 ч после начала лечения. Эксперты AAO/HNS предлагают расширить сроки оценки клинической неудачи у больных ОБРС до 7 суток [1]. Саму клиническую неудачу они определяют как ухудшение или отсутствие улучшения в указанный временной промежуток. Ухудшение трактуется ими как прогрессирование имеющихся или появление новых жалоб и симптомов ОБРС. Отсутствие улучшения они понимают буквально и не распространяют этот термин на больных с персистирующими, но постепенно улучшающимися симптомами.
 Свое предложение использовать 7-дневный срок для оценки эффективности терапии эксперты AAO/HNS обосновывают так. Согласно данным РКИ, частота улучшения в группе пациентов, получавших антибиотики, на 3-5-й день от начала вмешательства составляет 41% (рис. 4) [26]. То есть у 6 из 10 больных ОБРС спустя 3-5 дней от начала антибактериальной терапии не то что не наступит выздоровление, но не будет даже улучшения. Следовательно, оценка эффективности антибактериальной терапии на 5-й, а тем более на 3-й день лечения приведет к завышению числа пациентов, не ответивших на лечение. Эксперты обращают внимание на то, что и врачи, и больные должны понимать: промежуток времени до наступления улучшения при ОБРС может быть значительным, до 7 дней, а сохранение симптомов или даже незначительное ухудшение в эти сроки вовсе не обязательно означают клиническую неудачу. При этом для полного выздоровления (отсутствия всех жалоб и симптомов) может понадобиться 14 дней, а то и больше [1].
Свое предложение использовать 7-дневный срок для оценки эффективности терапии эксперты AAO/HNS обосновывают так. Согласно данным РКИ, частота улучшения в группе пациентов, получавших антибиотики, на 3-5-й день от начала вмешательства составляет 41% (рис. 4) [26]. То есть у 6 из 10 больных ОБРС спустя 3-5 дней от начала антибактериальной терапии не то что не наступит выздоровление, но не будет даже улучшения. Следовательно, оценка эффективности антибактериальной терапии на 5-й, а тем более на 3-й день лечения приведет к завышению числа пациентов, не ответивших на лечение. Эксперты обращают внимание на то, что и врачи, и больные должны понимать: промежуток времени до наступления улучшения при ОБРС может быть значительным, до 7 дней, а сохранение симптомов или даже незначительное ухудшение в эти сроки вовсе не обязательно означают клиническую неудачу. При этом для полного выздоровления (отсутствия всех жалоб и симптомов) может понадобиться 14 дней, а то и больше [1].
В то же время эксперты AAO/HNS специально оговаривают, что 7-дневный срок для оценки успеха или неуспеха терапии не распространяется на больных с тяжелым или осложненным ОБРС, лиц с иммунодефицитами, пациентов, перенесших ранее хирургические вмешательства на околоносовых пазухах, или с сопутствующими бактериальными инфекциями. В таких случаях врачам предлагается судить о сроках наступления клинической неудачи индивидуально. Для верной оценки таких сроков клиницистам следует обращать внимание также на возраст больного, общее состояние его здоровья, состояние сердечно-сосудистой и дыхательной систем, наличие сопутствующих заболеваний [1].
При подтверждении клинической неудачи при ОБРС (после исключения альтернативных диагнозов и/или осложнений) стартовую антибактериальную терапию изменяют. Если больной начинал лечение с амоксициллина, можно использовать высокие дозы амоксициллина/клавуланата (вплоть до 4,0 г/сут по амоксициллину). Другими альтернативами могут быть респираторные фторхинолоны (особенно при подозрении на инфицирование пенициллинорезистентными возбудителями), доксициклин или комбинация клиндамицина с пероральным цефалоспорином III поколения (цефиксим или цефподоксима проксетил). Длительность терапии в подобных случаях определяется индивидуально.
Применение лекарственных средств растительного происхождения
Хотя лекарственные средства растительного происхождения (ЛСРП) широко используются для лечения ОРС во многих странах мира, доказательная база относительно подавляющего большинства из них оставляет желать лучшего. Доступных клинических исследований, нередко с существенными методологическими погрешностями, немного, да и те не отражают весь спектр ЛСРП, которые применяются в терапии ОРС. Во многих случаях активные компоненты ЛСРП не выделены, не очищены и не стандартизованы. Мало известно и о фармакокинетических и фармакодинамических свойствах активных компонентов. Поэтому европейские эксперты не смогли сформулировать свое отношение к использованию ЛСРП [4].
В действующем в Украине протоколе по оказанию помощи больным ОРС рекомендуются 3 препарата из числа ЛСРП: миртол стандартизованный, экстракт из корня южноафриканской герани (Pelargonium sidoides) и комбинированный препарат – сухой экстракт фиксированной комбинации 5 растительных препаратов: корня горечавки (Gentianae radix), цветков первоцвета (Primula flos), травы щавеля (Rumicis herba), цветков бузины черной (Sambuci flos) и травы вербены (Verbenae herba) [3]. Хотя первый из них рекомендован для использования и в Германии [27], доказательная база ограничивается одним успешным РКИ более чем 20-летней давности [28].
Экстракт из корня южноафриканской герани (Pelargonium sidoides) выпускается многими производителями, но РКИ у больных ОРС проводились только с экстрактом EPs 7640. В метаанализе двух РКИ продемонстрировано его превосходство над плацебо: статистически значимое снижение индекса тяжести синусита, начиная с 7-го дня вмешательства, и более раннее наступление лечебного эффекта (почти на полтора дня; разница в средних величинах времени наступления лечебного эффекта -1,44; 95% ДИ от -2,42 до -0,47). Однако следует отметить, что в обоих исследованиях EPs 7640 назначался в высоких дозах. Это в 2 раза превосходит рекомендованную дозировку в готовой лекарственной, что не позволяет автоматически экстраполировать данные этих исследований на готовые лекарственные формы (60 капель 3 р/день; стандартная доза для взрослых – 30 капель 3 р/день) и на продолжительное время – 3 нед [29].
Фиксированная комбинация стандартизованных компонентов 5 лекарственных растений (корня генцианы, цветов первоцвета с чашечкой, цветов бузины черной, травы щавеля и травы вербены), в зависимости от дозировок компонентов, известна под международными индексами BNO 1010 и 1016. Она представляет собой новый технологический продукт, созданный по принципам фитоинженерии (англ. phytoneering). Сначала с помощью масс-спектрометрии в дикой природе отбирается «идеальное растение», отличающееся рекордным содержанием ключевых биологически активных веществ (БАВ), обусловливающих лекарственные свойства, далее путем вегетативного размножения формируется и культивируется пул растений для получения биохимически гомогенного сырья с высоким содержанием ключевых БАВ и затем с использованием высоких технологий по разделению ингредиентов создаются специальные стандартизованные экстракты, содержащие БАВ в концентрациях выше, чем в экстракте из дикорастущих лекарственных растений [30].
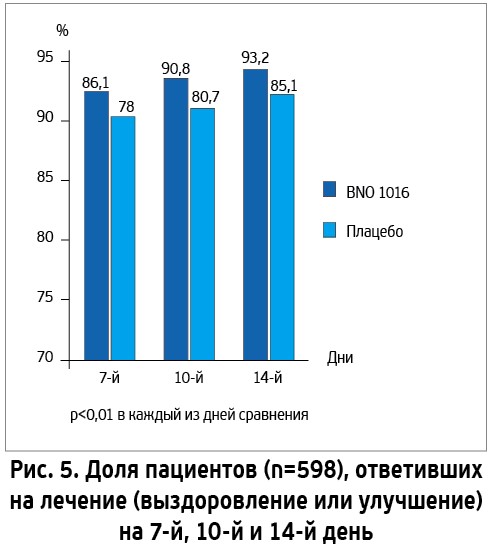 В объединенном анализе 2 рандомизированных двойных слепых плацебо-контролированных исследований, проведенных по одинаковому дизайну (всего 589 человек в возрасте 18-75 лет), убедительно продемонстрировано превосходство BNO 1016 (активная субстанция препарата Синупрет® экстракт) над плацебо (рис. 5) [31].
В объединенном анализе 2 рандомизированных двойных слепых плацебо-контролированных исследований, проведенных по одинаковому дизайну (всего 589 человек в возрасте 18-75 лет), убедительно продемонстрировано превосходство BNO 1016 (активная субстанция препарата Синупрет® экстракт) над плацебо (рис. 5) [31].
BNO 1016 внутрь по 160 мг 3 р/сут (терапевтические дозировки, совпадающие с рекомендованными в готовой лекарственной форме) vs плацебо у больных ОРС: доли пациентов с положительным результатом вмешательства: выздоровление + улучшение (уменьшение симптоматики на 75% от исходного уровня).
Помимо заметного увеличения количества выздоровевших или ответивших на лечение пациентов, применение экстракта из 5 лекарственных растений приводило к терапевтическому выигрышу в отношении скорости регрессии симптомов риносинусита на 3,8 дня по сравнению с плацебо.
Целесообразность использования BNO 1016 подтверждена и в других исследованиях [32]. Согласно информации в листке-вкладыше к препарату, принимать его следует после еды, не разжевывать, запивать достаточным количеством воды. Комбинация с антибиотиками возможна и целесообразна, а продолжительность лечения составляет 7-14 дней.
Выводы
В подавляющем большинстве случаев (98-99,5%) этиология риносинуситов у взрослых – вирусная. Антибиотики назначают больным с клиническим диагнозом неосложненного ОБРС при:
- исходно тяжелом течении заболевания;
- «второй волне» болезни (ухудшении состояния после первоначального улучшения);
- отсутствии улучшения спустя 7 (до 10) дней симптоматического лечения без антибиотиков.
Препаратами выбора для лечения ОБРС являются амоксициллин или амоксициллин/клавуланат. Продолжительность антибактериальной терапии у взрослых составляет 5-7 (до 10) дней. Из ЛСРП наиболее изучены экстракт из корня Pelargonium sidoides (препарат EPs 7640) и сухой экстракт фиксированной комбинации 5 растительных средств (BNO 1016 – активная субстанция препарата Синупрет® экстракт), созданный по принципам фитоинженерии (англ. phytoneering).
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 22 (467), листопад 2019 р.


