25 грудня, 2019
Целіакія сьогодні
Від рекомендацій 2019 року до практичних дій лікарів
 У 2019 р. відбулися дуже важливі події, пов’язані з розвитком наукових та удосконаленням практичних знань з проблеми діагностики та лікування захворювань, зумовлених підвищеною чутливістю до глютену. Саме цього року побачило світ оновлене керівництво Європейського товариства з вивчення целіакії (ESsCD) та відбувся 18-й міжнародний симпозіум. Основним положенням цього документа і проблемам, які порушувалися на симпозіумі, насамперед гострим питанням діагностики та лікування целіакії, й присвячена ця публікація.
У 2019 р. відбулися дуже важливі події, пов’язані з розвитком наукових та удосконаленням практичних знань з проблеми діагностики та лікування захворювань, зумовлених підвищеною чутливістю до глютену. Саме цього року побачило світ оновлене керівництво Європейського товариства з вивчення целіакії (ESsCD) та відбувся 18-й міжнародний симпозіум. Основним положенням цього документа і проблемам, які порушувалися на симпозіумі, насамперед гострим питанням діагностики та лікування целіакії, й присвячена ця публікація.
Загальні поняття
Несприйняття їжі, яка містить глютен (основний білок злакових), пов’язане з формуванням цілої низки клінічних розладів, об’єднаних назвою «глютенозалежні захворювання». Ця група мультифакторних розладів поступово набула епідеміологічно важливого значення та стала відображенням складних епідеміологічних процесів, спільних для різних країн та регіонів світу.
Основними захворюваннями, пов’язаними з порушеннями нормальної біотрансформації та взаємодії глютену з органами та системами людини, є целіакія (аутоімунне захворювання), несприйняття глютену без целіакії (НГБЦ) та алергія на злакові, зокрема пшеницю. З огляду на аутоімунну складову формування патологічної відповіді, окрім целіакії, ця група захворювань включає також герпетиформний дерматит (дерматит Дюрінга) та глютенову атаксію.
! Головним чинником розвитку целіакії та пов’язаних з нею захворювань є глютен. Це збірна назва водонерозчиної білкової складової злакових культур (пшеничного борошна), яка залишається в борошні після виділення водою крохмалю, альбумінів та інших водорозчинних білків. Глютеноподібні білки містяться у пшениці, житі та ячмені, які широко використовуються у харчовій промисловості з метою поліпшення властивостей випічки, а саме отримання бажаної еластичності, пухкості та структурності.
Целіакія – це хронічне поліорганне аутоімунне захворювання, яке уражає генетично скомпрометованих осіб (носіїв генів HLA-DQ2 та/або -DQ8) лише на тлі споживання глютеновмісних продуктів і характеризується ушкодженням слизової оболонки тонкої кишки. Відповідно до певних клінічних, імунологічних і гістопатологічних характеристик целіакію сьогодні запропоновано класифікувати на серонегативну, рефрактерну та сповільненої відповіді.
Герпетиформний дерматит є нашкірною маніфестацією целіакії та одним з її позакишкових проявів. Патологія характеризується герпетиформними скупченнями уртикарних папул і везикул на поверхні шкіри та відкладенням імуноглобуліну (Ig) A у сосочковому шарі шкіри.
Глютенова атаксія – це патологічний стан, який пов’язаний з целіакією та проявляється ідіопатичною спорадичною атаксією в поєднанні з позитивними результатами серологічних тестів на целіакію, з наявністю сформованої глютенової ентеропатії або без неї.
! Несприйняття глютену без целіакії – це стан, який характеризується подібною до синдрому подразненого кишечнику симптоматикою та поліморфними позакишковими клінічними проявами. Він характеризується появою за декілька годин або днів після споживання глютеновмісних страв несприятливої симптоматики та її швидким зникненням після припинення споживання останніх, а також появою знову після подальших спроб використання таких продуктів.
Головною тактикою ведення хворих із припущенням наявності НГБЦ є виключення целіакії та алергії на пшеницю на тлі споживання глютеновмісних продуктів.
Окрім глютену, в патогенезі НГБЦ задіяні інгібітори амілази і трипсину та фруктани (ферментовані оліго-, ди-, моносахариди та поліоли, або FODMAPS), які також є складовими пшениці та інших глютеновмісних та безглютенових продуктів харчування.
Генетика
Специфічне значення генів системи HLA (DQ2 та DQ8) полягає у презентації глютенових білків як антигенів. Це пояснює винятково важливу роль локусів головного комплексу гістосумісності як найважливішого генетичного фактора розвитку целіакії. Проте наявність алелів відповідних генів сама по собі є важливим, але не визначальним фактором у розвитку целіакії.
Фактори навколишнього середовища
Для того щоб у генетично скомпрометованої особи розвинулася целіакія, необхідне споживання продуктів, що містять глютен. Раніше вивчали різні стратегії відтермінованого введення глютеновмісних продуктів і вплив тривалості грудного вигодовування немовлят на виникнення целіакії. У численних дослідженнях не підтверджено доцільність уникнення раннього (у віці 4 місяці) або пізнього (від 6 до 12 місяців) введення страв, що містять глютен, у раціон для зниження ризику розвитку целіакії. Втрата толерантності до глютену може виникати у будь-якому віці як наслідок дії інших, окрім глютену, факторів. Шлунково-кишкові інфекції, деякі лікарські препарати та хірургічні втручання можуть ставати тригерами розвитку целіакії.
! Тривалість грудного вигодовування та час введення глютеновмісних продуктів у раціон не пов’язані зі зниженням ризику розвитку целіакії.
Кого слід обстежувати на целіакію?
Нижче подано перелік груп ризику, в яких відповідно до рекомендації ESsCD необхідно проводити скринінг на целіакію.
Групи ризику, в яких проведення скринінгу на целіакію обґрунтоване високим рівнем доказовості
- Дорослі пацієнти зі скаргами, клінічними проявами, що можуть бути зумовлені характерними для целіакії ураженнями тонкої кишки, або лабораторними показниками, які свідчать про наявність мальабсорбції (високий рівень доказовості, рекомендація високої сили).
- Родичі першої лінії спорідненості хворих на целіакію потребують обстеження навіть за відсутності симптомів целіакії. За можливості необхідне визначення носійства генів HLA-DQ2/DQ8. У разі негативних результатів генетичного тестування подальше обстеження не рекомендоване (високий рівень доказовості, умовна рекомендація).
- Пацієнти з нез’ясованим підвищенням активності трансаміназ у сироватці крові (високий рівень доказовості, умовна рекомендація).
- Хворі на цукровий діабет 1 типу (високий рівень доказовості, рекомендація високої сили).
Як обстежувати пацієнтів?
Роль серологічних методів дослідження у діагностиці целіакії
На сьогодні розроблені різноманітні тести для діагностики целіакії.
Тканинна трансглутаміназа та ендомізіальні антитіла. Виявлення тканинної трансглутамінази (ТТГ2) як антигену-мішені для ендомізіальних антитіл (EMA) IgA сьогодні є значним проривом у діагностиці целіакії. При нелікованому захворюванні чутливість та специфічність зазначеного маркера досягає 95%. При цьому визначення ТТГ2 є найчутливішим тестом, тоді як антиендомізіальних антитіл – найбільш специфічним. Саме тому серологічним маркером першого порядку експертами встановлено виявлення ТТГ2. IgA-EMA можна використовувати як метод підтвердження, особливо коли титр TТГ2 є низьким (меншим за 2 норми).
Дезаміновані пептиди гліадину (IgA та IgG) – білки, які володіють потужною здатністю до утворення афінних зв’язків з HLA-DQ2 або DQ8 на антигенпрезентуючих клітинах і стимулюють запальну Т-опосередковану відповідь на слизовій оболонці тонкої кишки у хворих на целіакію. Виявлення антитіл до дезамінованих пептидів гліадину (ДПГ) є значно більш специфічним маркером, ніж антитіл до нативного глютену.
Дефіцит IgA встановлюють у 2-3% хворих на целіакію. Тому необхідно визначати загальний вміст IgA одночасно з рекомендованими серологічними дослідженнями.
! У Медичній лабораторії «ДІЛА» розроблений алгоритм серологічних методів діагностики глютенозалежних захворювань із тестами другого покоління (Elia), що відповідає світовим та європейським тенденціям діагностики.
Ендоскопія та морфологічне дослідження біоптатів слизової оболонки дванадцятипалої кишки
Ендоскопія з біопсією слизової оболонки (СО) тонкої кишки (ТК) є окремим діагностичним етапом. Саме виявлення патологічних структурних змін СО, які зазвичай є нерівномірними, різного ступеня тяжкості та локалізуються у різних ділянках дванадцятипалої кишки, дає змогу зробити висновок щодо наявності специфічного для целіакії ураження. Отже, для підтвердження діагнозу целіакії необхідно проводити множинні (принаймні чотири) біопсії дванадцятипалої кишки.
Гістологічне дослідження. На підставі динаміки розвитку уражень та частоти відповідних морфологічних знахідок М. Marsh запропонував чинну й на сьогодні гістологічну класифікацію стадій целіакії. Початкові стадії ураження СО ТК не виключають, але самі собою й не підтверджують діагнозу.
! Діагноз целіакії встановлюють на підставі комплексу клінічних, серологічних і гістологічних даних.
Нижче представлені основні вимоги до проведення біопсії СО дванадцятипалої кишки в різних клінічних ситуаціях.
Вимоги до проведення біопсії за наявності серологічної відповіді:
- синдром подразненого кишечнику;
- підвищення рівня печінкових трансаміназ невідомого генезу;
- гастроентерологічні скарги у хворих, що не мають сімейного анамнезу за целіакією або інших аутоімунних захворювань;
- мікроскопічний коліт;
- зоб Хашімото та дифузний токсичний зоб;
- остеопенія/остеопороз;
- нез’ясована атаксія або периферична нейропатія;
- рецидивуючі афтозні виразки;
- безпліддя, пізнє менархе, рання менопауза;
- синдром хронічної втоми;
- гострий або хронічний панкреатит після виключення усіх інших можливих причин;
- епілепсія; головний біль, у тому числі мігрень; перепади настрою та розлади уваги;
- гіпоспленізм або функціональна аспленія;
- псоріаз або інші ураження шкіри (не герпетиформний дерматит);
- синдром Тернера або Дауна;
- легеневий гемосидероз;
- IgA-асоційована нефропатія.
Ендоскопію та біопсію дванадцятипалої кишки при негативних результатах серологічних тестів слід проводити за наявності:
- хронічної діареї без домішок крові;
- діареї з ознаками мальабсорбції, втрати маси тіла;
- залізодефіцитної анемії нез’ясованої етіології;
- гастроентерологічних скарг та обтяженого за целіакією сімейного анамнезу;
- гастроентерологічних скарг у пацієнтів з аутоімунними захворюваннями або дефіцитом ІgА;
- відставання дітей у розвитку;
- підтвердженого біопсією шкіри герпетиформного дерматиту;
- атрофії СО ТК, підтвердженої шляхом відеокапсульної ентероскопії.
Інші методи дослідження, що використовуються в діагностиці целіакії
За результатами метааналізу відеокапсульна ентероскопія (ВКЕ) має високу чутливість (89%) та специфічність (95%) у діагностиці целіакії. Порівняно з традиційною ендоскопією верхніх відділів шлунково-кишкового тракту ВКЕ має вищу загальну чутливість щодо виявлення макроскопічних ознак атрофії (92 проти 55%). Проте чутливість ВКЕ є нижчою при частковій атрофії ворсин, а також при неатрофічних, субмікроскопічних стадіях ураження СО (Марш I-II), які, таким чином, можуть залишитися не виявлені без біопсії та морфологічного аналізу. Перевагою ВКЕ є можливість ідентифікації ускладнень целіакії за рахунок повноцінного огляду СО ТК на всій її довжині.
Встановлення діагнозу целіакії
Симптоми, що виникають при глютенозумовлених та/або інших захворюваннях шлунково-кишкового тракту, а також при ураженнях інших органів і систем часто подібні та неспецифічні. Усе це ускладнює діагностику кожного з них.
! Погіршення симптоматики та збільшення кількості скарг після повторного (тобто після попереднього виключення) введення до раціону глютеновмісних продуктів не є підтвердженням наявності целіакії або НГБЦ за відсутності інших доказів.
Діагноз целіакії зазвичай підтверджується наявністю позитивних результатів серологічних досліджень (ТТГ2, ДПГ та EMA) та верифікованою атрофією ворсин СО ТК.
Саме тому в рекомендаціях ESsCD представлені окремі сценарії дій лікарів, які дозволяють ухвалювати рішення в різних клінічних ситуаціях. Розглянемо окремі діагностичні сценарії, наведені у цьому документі.
1. Титр IgA-ТТГ2 може бути від’ємним у 5-15% хворих на целіакію, що діагностується на підставі результатів гістологічних досліджень, у пацієнтів, які споживають глютеновмісні продукти.
У цьому разі «гістологічна відповідь» на агліадинову дієту у хворих, що спочатку мали атрофію ворсин ТК, дозволяє підтвердити наявність целіакії та, зрозуміло, потребує обов’язкового повторного проведення біопсії в динаміці. Визначення генів дозволяє заперечити або схилитися до діагнозу в пацієнтів із серонегативними станами.
2. У разі наявності підвищених титрів ТТГ2 та відсутності типових для целіакії гістологічних змін рекомендується висновок другого морфолога, який має достатній досвід у діагностиці целіакії. Також рекомендується повторне виконання біопсії після глютенової провокації (тобто після відновлення споживання глютеновмісних продуктів) особам, які не споживали їх на момент первинної діагностики. Генотипування (HLA-DQ2/8) в таких випадках є обов’язковим. Використання додаткових біомаркерів може дозволити приймати додаткові клінічні рішення.
3. Для пацієнтів, які на момент звернення до лікаря вже дотримувалися агліадинової дієти, необхідне проведення серологічного та генетичного досліджень. Якщо результати серологічних тестів позитивні, наступним кроком в обстеженні є проведення біопсії. У таких випадках слід також розглядати проведення глютенової провокації хворим, які є носіями генів HLA-DQ2/DQ8.
Таким чином, при діагностиці целіакії лікарі можуть зіткнутися з різними комбінаціями клінічних, лабораторних і гістологічних ознак, взаємозв’язок між якими буде підтверджувати або виключати наявність цієї патології.
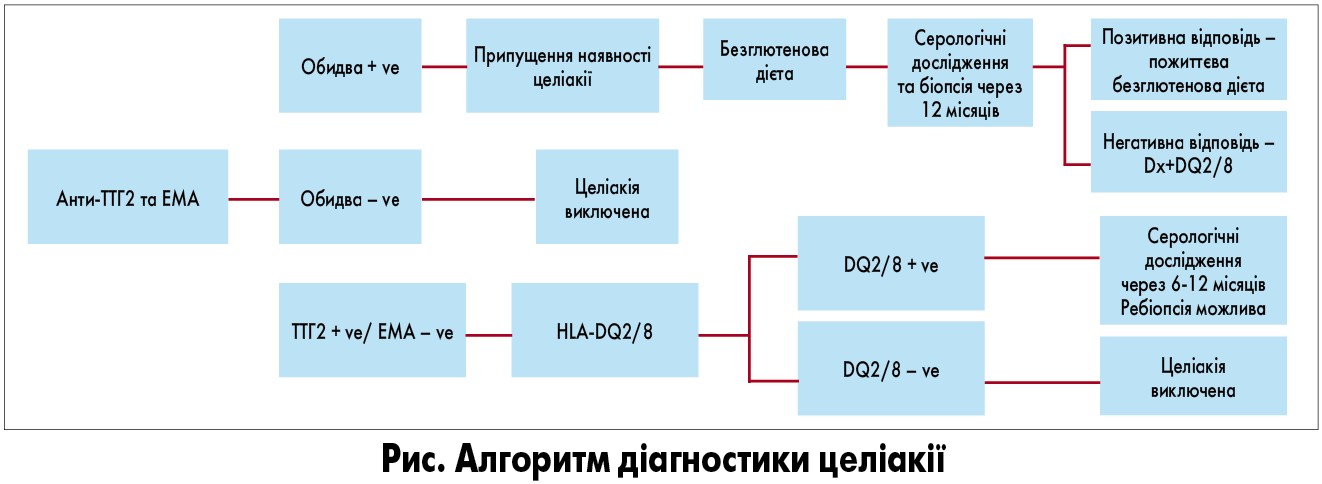
Новий алгоритм діагностики целіакії з урахуванням результатів клініко-лабораторних досліджень у пацієнтів з мінімальними морфологічними змінами СО ТК поданий на рисунку.
Лікування
У лікуванні целіакії єдиним методом з доведеною ефективністю залишається сувора пожиттєва агліадинова дієта. Пацієнтам, що проходять первинну діагностику целіакії, необхідно проводити додаткові обстеження для виключення дефіцитних станів, зумовлених мальабсорбцією мікронутрієнтів (заліза, фолієвої кислоти, вітамінів D, В12). Під час дотримання агліадинової дієти хворим необхідно рекомендувати продукти з підвищеним умістом харчових волокон.
Таким чином, діагностика целіакії залишається складним і трудомістким завданням. Актуальною залишається необхідність підвищення обізнаності медичної спільноти та населення щодо існування захворювань, пов’язаних із несприйняттям злакових, і ситуацій, які потребують виконання специфічного обстеження.
Список літератури знаходиться в редакції.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 4 (54), 2019 р.