1 травня, 2020
Клінічні рекомендації Української гастроентерологічної асоціації із ведення пацієнтів з диспепсією
 Диспепсія – це один з найбільш поширених симптомокомплексів, що зустрічаються у практиці внутрішньої медицини. Диспепсія є глобальною проблемою, проте її розповсюдженість суттєво відрізняється у різних регіонах. Систематичні огляди свідчать, що симптоми диспепсії в усьому світі мають близько 20% населення, у різних країнах вони є причиною 4-10% усіх звернень за медичною допомогою. Загалом захворюваність на диспепсію є вищою у західних популяціях порівняно зі східними.
Диспепсія – це один з найбільш поширених симптомокомплексів, що зустрічаються у практиці внутрішньої медицини. Диспепсія є глобальною проблемою, проте її розповсюдженість суттєво відрізняється у різних регіонах. Систематичні огляди свідчать, що симптоми диспепсії в усьому світі мають близько 20% населення, у різних країнах вони є причиною 4-10% усіх звернень за медичною допомогою. Загалом захворюваність на диспепсію є вищою у західних популяціях порівняно зі східними.
Диспепсія частіше зустрічається у жінок, курців, у осіб з H. рylori (Hp) та пацієнтів, що приймають нестероїдні протизапальні препарати (НПЗП). Люди з диспепсією мають нормальну тривалість життя, проте симптоми цього захворювання негативно впливають на якість життя, що пов’язано з емоційним пригніченням, необхідністю придбання ліків та зниженням працездатності. Хоча більша частина пацієнтів з диспепсією за медичною допомогою не звертаються, їх ведення пов’язане з істотними економічними витратами, оскільки пацієнти з диспепсією використовують значно більше різних медичних ресурсів, ніж люди з іншою гастроентерологічною патологією. Таким чином, діагностика, лікування і тривале ведення пацієнтів з диспепсією є актуальною медичною проблемою в усьому світі, включаючи Україну.
Диспепсія не є специфічним синдромом і може зустрічатися при різній патології шлунково-кишкового тракту (ШКТ) – як органічній, так і функціональній. Приблизно у 60-70% пацієнтів з диспепсією будь-яких структурних змін з боку гастродуоденальної ділянки при езофагогастродуоденоскопії (ЕГДС) не виявляється і ці хворі вважаються такими, що страждають на функціональну диспепсію (ФД). ФД зустрічається приблизно у 7-12% усього населення розвинутих країн, причому значно частіше хворіють люди у молодому та середньому віці. Приблизно у 30-40% пацієнтів диспепсичні скарги зумовлені органічною патологією. В таких випадках мова йде про вторинну (органічну) диспепсію (ВД), основні причини якої наведені у таблиці 1.
Ці рекомендації по веденню пацієнтів з диспепсією запропоновані Українською гастроентерологічною асоціацією та засновані на даних, що є в електронних базах PubMed, NCBI, CochraneLibrary, Research-Gate, GoogleScholar, а також на рекомендаціях провідних міжнародних гастроентерологічних та інших асоціацій та товариств – AGA, СAG, ACG, NICE, UEG. При підготовці рекомендацій враховували тільки оригінальні (проспективні, рандомізовані, контрольовані та подвійні сліпі) дослідження, систематичні огляди та метааналізи. Для оцінки якості фактичних даних щодо фармакологічних методів лікування диспепсії застосована система GRADE, у якій виділяють високий, середній, низький та дуже низький рівні доказів. Високий рівень доказів свідчить про те, що подальші дослідження для зміни думки відносно ефективності втручання не потрібні. Середній (помірний) рівень доказів передбачає необхідність додаткових досліджень, а низький означає, що очікуються нові дослідження, які можуть змінити думку відносно ефективності втручання. Дуже низький рівень означає, що докази сумнівні або конфліктні, а співвідношення ризик/користь точно не встановлене. Усі рекомендації представлені з урахуванням їх сили: сильні передбачають суттєву перевагу метода/втручання над ризиком його застосування, у зв’язку з чим суворо рекомендовані; слабкі рекомендації балансують на грані співвідношення ризик/користь.
Визначення та види диспепсії
Твердження 1
Диспепсія – це будь-який серединний епігастральний біль, печіння, дискомфорт, відчуття переповнення після їди або раннього насичення, відрижка, печія, нудота, блювання, здуття в епігастрії, що вказують на залучення верхніх відділів ШКТ та наявні не менше 4 тижнів. Диспепсію слід трактувати подвійно – і як синдром (ВД), і як самостійну нозологічну форму (ФД).
Твердження 2
В якості попереднього діагнозу в необстеженого первинного пацієнта слід використовувати термін «необстежена диспепсія». Після відповідного клініко-анамнестичного, лабораторного та інструментального дообстеження всі пацієнти з симптомами диспепсії можуть бути поділені на дві основні групи – з ВД та ФД.
Твердження 3
ВД діагностується у пацієнтів з органічними, системними або метаболічними причинами диспепсичних симптомів, що можуть бути ідентифіковані при проведенні таких діагностичних процедур, як ЕГДС та ультразвукове дослідження (УЗД) органів черевної порожнини (ОЧП), а також шляхом лабораторної діагностики (таблиця 1). При відповідному лікуванні симптоми диспепсії зазвичай значно зменшуються або повністю зникають.
Твердження 4
Hp-асоційована диспепсія, згідно з Кіотським глобальним консенсусом, розглядається як підгрупа ВД, симптоми якої протягом 6-12 місяців зникають або значно зменшуються після ерадикації.
Твердження 5
ФД, яка є самостійною нозологічною формою, діагностується у пацієнтів з наявністю одного або більше симптомів: почуття переповнення після їди, швидке насичення, епігастральний біль або печіння, які неможливо пояснити стандартними клінічними обстеженнями – ЕГДС, УЗД ОЧП та лабораторними аналізами.
Етіологія та патофізіологія диспепсії
Твердження 6
Етіологія та патофізіологія ВД зумовлена супутнім захворюванням чи станом (таблиця 1).
Етіологія ФД точно не відома. В якості ймовірних факторів ризику розвитку ФД розглядають зв’язок з перенесеними гострими гастроінтестинальними інфекціями (так звана постінфекційна ФД), інфекція Hp, алергія, генетична схильність (поліморфізм гена GNB3). В якості патофізіологічних факторів ФД розглядають дисмоторні розлади (сповільнення спорожнення та порушення акомодації шлунка), вісцеральну гіперчутливість до розтягнення шлунка або дванадцятипалої кишки (ДПК), гіперчутливість ДПК до кислоти та ліпідів, низькоінтенсивне запалення та імунну активацію слизової оболонки, дуоденальну еозинофілію, психосоціальні розлади.
Діагностика
Рекомендація 1
 Пацієнтам старше 50 років з диспепсією або наявністю симптомів тривоги, так званих симптомів червоних прапорців (таблиця 2), для виключення неоплазії верхніх відділів ШКТ та іншої органічної патології рекомендоване обов’язкове проведення ЕГДС (умовна рекомендація, докази помірної якості).
Пацієнтам старше 50 років з диспепсією або наявністю симптомів тривоги, так званих симптомів червоних прапорців (таблиця 2), для виключення неоплазії верхніх відділів ШКТ та іншої органічної патології рекомендоване обов’язкове проведення ЕГДС (умовна рекомендація, докази помірної якості).
Рекомендація 2
Пацієнтам молодше 50 років з диспепсією та відсутністю симптомів тривоги рекомендоване проведення неінвазивного тесту на Hр (13С-сечовинний дихальний тест або визначення фекального антигена Нр) та ерадикаційної терапії Нр-інфекції у разі позитивності, так звана стратегія test-and-treat (сильна рекомендація, докази високої якості).
Рекомендація 3
Діагностика ФД базується на основі Римських критеріїв IV, що рекомендують розглядати ії як широке поняття (таблиця 3), яке описує пацієнтів з постпрандіальним дистрес-синдромом (ПДС), пацієнтів з епігастральним больовим синдромом (ЕБС), а також пацієнтів із перехресними симптомами ПДС та ЕБС – оверлеп-синдромом або поєднанням ЕБС та ПДС (сильна рекомендація, докази високої якості).
Рекомендація 4
Пацієнтам з ФД не рекомендується проводити рутинне дослідження шлункової моторики або шлункової секреції (умовна рекомендація, докази дуже низької якості).
Рекомендація 5
Спеціальне дослідження шлункової моторики рекомендується проводити тільки пацієнтам з ФД з високою підозрою на наявність гастропарезу (умовна рекомендація, докази дуже низької якості).
Ведення пацієнтів з диспепсією
Рекомендація 6
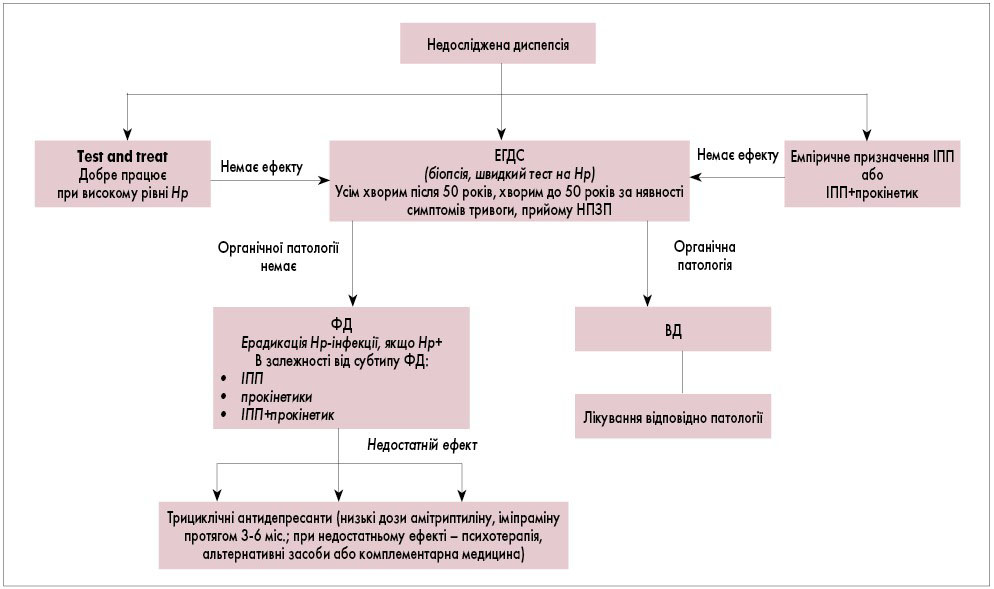
Hp-негативним хворим на диспепсію молодше 50 років за відсутності симптомів тривоги або хворим, у яких залишаються симптоми після ерадикації, рекомендується емпірична терапія (таблиця 4) інгібіторами протонної помпи (ІПП) або призначення (рис. 1) комбінації ІПП+прокінетик (сильна рекомендація, докази високої якості).
В Україні комбінація ІПП+прокінетик (омепразол+домперидон) зареєстрована як препарати Омез Д (звичайна форма) та Омез ДСР (пролонгована форма).
Рис. 1. Алгоритм ведення пацієнта з необстеженою диспепсією
Рекомендація 7
У разі виникнення НПВП-індукованої диспепсії альтернативним препаратом є ребаміпід (умовна рекомендація, докази низької якості).
В Україні препарат ребаміпід зареєстрований під торговою назвою Мукоген.
Рекомендація 8
Пацієнтам з диспепсією молодше 50 років за відсутності симптомів тривоги та відповіді на ерадикацію Hр, прийом ІПП, прокінетиків або їх комбінації рекомендується терапія низькими дозами трициклічних антидепресантів (ТЦА) (умовна рекомендація, докази дуже низької якості).
Рекомендація 9
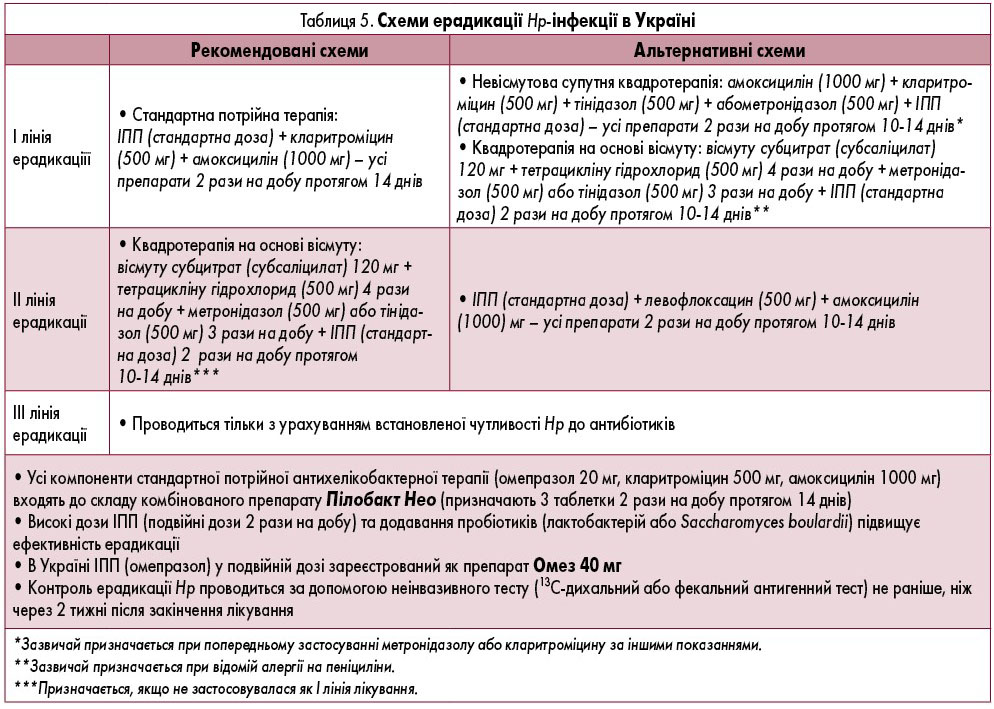
Hp-позитивним пацієнтам з ФД рекомендується ерадикаційна терапія із застосуванням високих доз ІПП (таблиця 5) згідно з рекомендаціями Маастрихтського консенсусу V (cильна рекомендація, докази високої якості).
Рекомендація 10
Hp-негативним хворим на ФД ЕБС або хворим, у яких залишаються симптоми після ерадикаціїї Hр-інфекції, рекомендується терапія ІПП (таблиця 4) у стандартних дозах (сильна рекомендація, докази помірної якості).
Рекомендація 11
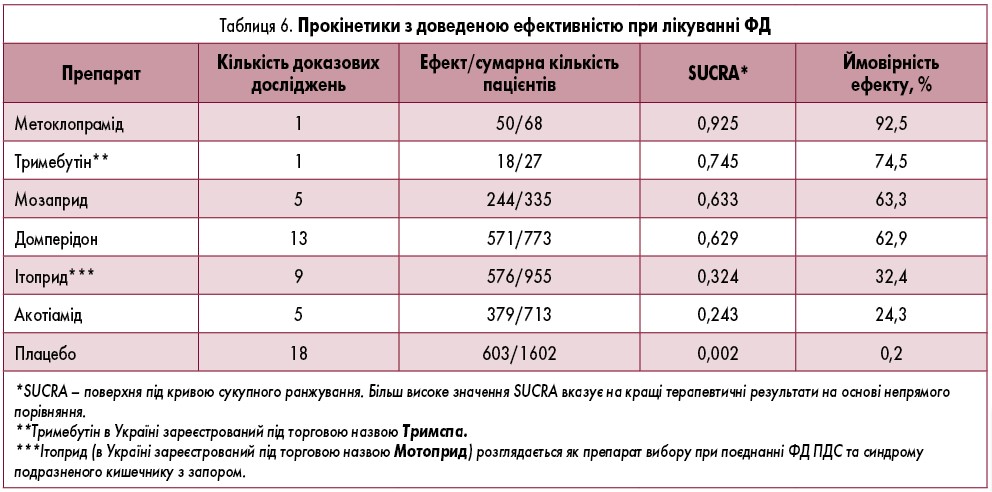
Hp-негативним пацієнтам з ФД ПДС рекомендується терапія прокінетиками (таблиця 6) з доведеною ефективністю (умовна рекомендація, докази низької якості).
Рекомендація 12
Hp-негативним пацієнтам з поєднанням ФД ПДС та ФД ЕБС (оверлеп-синдром) рекомендується комбінований прийом ІПП та прокінетика (умовна рекомендація, докази низької якості).
В Україні комбінація ІПП+прокінетик (омепразол+домперидон) зареєстрована як препарати Омез Д (звичайна форма) та Омез ДСР (пролонгована форма).
Пацієнтам з ФД, що не відповідають на лікування ІПП, прокінетиками, комбінацією ІПП+прокінетик або ерадикацію Hр-інфекції, рекомендується призначати низькі дози ТЦА (амітриптилін, іміпрамін) (умовна рекомендація, докази помірної якості).
Рекомендація 14
Пацієнтам з ФД не рекомендується рутинне застосування альтернативних препаратів або комплементарної медицини (умовна рекомендація, докази низької якості).
Рекомендація 15
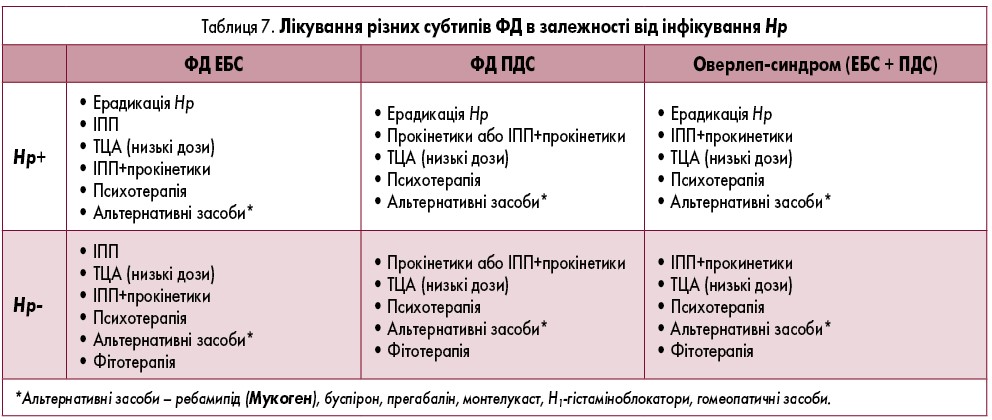
Пацієнтам з ФД, що не відповіли на лікування ІПП, прокінетиками, комбінацією ІПП+прокінетик, ТЦА, ерадикацію Hр-інфекції, можна розглядати терапію (таблиця 7) альтернативними препаратами резерву (слабка рекомендація, докази дуже низької якості).
Рекомендація 16
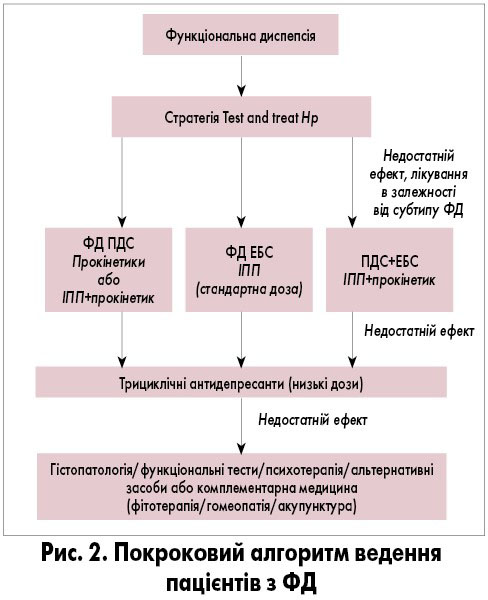
Пацієнтам з ФД, що не відповіли на будь-яке медикаментозне лікування, рекомендована консультація психотерапевта та проведення психотерапевтичного лікування (умовна рекомендація, докази дуже низької якості, рис. 2).
Література
- Camillieru M, Stanghellini V. Current management strategies and emerging treatments for functional dyspepsia. Nat Rev Gastroenterol Hepatol. – 2013; 10: 187-194.
- Drossman D.A. Functional Gastrointestinal Disorders: History, Pathophysiology, Clinical Features and Rome IV. Gastroenterology, 2016. – Vol. 150. – № 6. – P. 1262-1279.
- Ford A.C., Marwaha A., Sood R., Moayyedi P. Global prevalence of and risk factors for uninvestigateddyspepsia: a meta-analysis. Gut 2015; 64: 1049.
- Gisbert J.P., Calvet X. Helicobacter pylori test-and-treat strategy for management of dyspepsia: a comprehensive review. Clin Transl Gastroenterol, 2013; 4: e32.
- Jaafar M., Safi S., Tan Met al. Efficacy of Rebamipide in Organic and Functional Dyspepsia: A Systematic Review and Meta‑Analysis. Digestive Diseases and Sciences. https://doi.org/10.1007/s10620-017-4871-9.
- Koretz R.L., Rotblatt M. Complementary and alternative medicine in gastroenterology: the good, thebad and the ugly. Clin Gastroenterol Hepatol, 2004; 2: 957.
- Lacy B.E., Talley N.J., Locke G.R. 3 rd et al. Review article: current treatment options and management offunctional dyspepsia. AlimentPharmacol Ther, 2012; 36: 3.
- Lan L., Zeng F., Liu G.J. et al. Acupuncture for functional dyspepsia. Cochrane Database Syst Rev, 2014; CD008487.
- Malfertheiner P., Megraud F., O’Morain C.A. et al. Management of Helicobacter pylori infection – the Maastricht V/Florence Consensus Report. European Helicobacter and Microbiota Study Group and Consensus panel. Gut. 2017 Jan; 66(1): 6-30.
- Mazzoleni L.E., Sander G.B., Francesconi C.F. et al. Helicobacter pylori eradication in functionaldyspepsia: HEROES trial. Arch Intern Med 2011; 171: 1929.
- Moayyedi P.M., Lacy B.E., Andrews C.N. et al. ACG and CAG Clinical Guideline: Management of Dyspepsia. Am J Gastroenterol 2017; 112: 988.
- Moayyedi P. Helicobacter pylori eradication for functional dyspepsia: what are we treating? commenton «Helicobacter pylori eradication in functional dyspepsia». Arch Intern Med 2011; 171: 1936.
- Palsson O.S., Van Tiburg M.A., Spiegek B.M. et al. Uninvestigated dyspepsia in the US general population results from the Rome Normative Gsatrointestinal Symptoms Survey. Gastroenterologe 2014; 146: S179.
- Pike B.L., Porter C.K., Sorrell T.J., Riddle M.S. Acute gastroenteritis and the risk of functional dyspepsia: asystematic review and meta-analysis. Am J Gastroenterol, 2013; 108: 1558.
- Quigley E.M., Lacy B.E. Overlap of functional dyspepsia and GERD-diagnostic and treatmentimplications. Nat Rev Gastroenterol Hepatol, 2013; 10: 175.
- Stanghellini V., Chan F.K., Hasler W.L. et al. Gastroduodenal Disorders. Gastroenterology 2016; 150: 1380.
- Sugano K., Tack J., Kuipers E.J. et al. Kyoto global consensus report on management of Helicobacter pylori gastritis. Gut, 2015; 64: 1353-1367.
- Tack J., Janssen P., Masaoka T. et al. Efficacy of buspirone, a fundus-relaxing drug, in patients withfunctional dyspepsia. Clin Gastroenterol Hepatol, 2012; 10: 1239.
- Tack J., Ly H.G., Carbone F. et al. Efficacy of Mirtazapine in Patients With Functional Dyspepsia and Weight Loss. Clin Gastroenterol Hepatol, 2016; 14: 385.
- Talley N.J., Ford A.C. Functional Dyspepsia. N Engl J Med, 2015; 373: 1853.
- Talley N.J. American Gastroenterological Association. American Gastroenterological Associationmedical position statement: evaluation of dyspepsia. Gastroenterology, 2005; 129: 1753.
- Talley N.J., Locke G.R., Saito Y.A. et al. Effect of Amitriptyline and Escitalopram on Functional Dyspepsia: A Multicenter, Randomized Controlled Study. Gastroenterology 2015; 149: 340.
- Vanheel H., Carbone F., Valvekens L. et al. Pathophysiological Abnormalities in Functional Dyspepsia Subgroups According to the Rome III Criteria. Am J Gastroenterol, 2017; 112: 132.
- Wang W.H., Huang J.Q., Zheng G.F. et al. Effects of proton-pump inhibitors on functional dyspepsia: a meta-analysis of randomized placebo-controlled trials. Clin Gastroenterol Hepatol, 2007; 5: 178.
- Wu J.C., Cheong P.K., Chan Y.C. et al. A randomized, double-blind, placebo-controlled trial of low doseimipramine for treatment of refractory functional dyspepsia (FD) (abstract #216). Gastroenterology, 2011; 140: S50.
- Yang J., Chang S., Gwang H. et al. Prokinetics for the treatment of functional dyspepsia: Bayesian network meta-analysis. BMC Gastroenterology, 2017; 17: 83 DOI 10.1186/s12876-017-0639-0.
- Zhao B., Zhao J., Cheng W.F. et al. Efficacy of Helicobacter pylorieradication therapy on functional dyspepsia: a meta-analysis ofrandomized controlled studies with 12-month follow-up. J Clin Gastroenterol, 2014; 48: 241-247.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (55) 2020 р.