8 березня, 2016
Купирование болевого синдрома с помощью мелоксикама в форме ородиспергируемых таблеток
Боль является спутником многих состояний, в том числе неврологических и ревматических заболеваний. С болевым синдромом ассоциируются такие болезни, как васкулит, ревматоидный артрит, бурсит, тендинит, люмбаго, ишиас, а также повреждения и заболевания межпозвоночных дисков.
Постоянная боль при артрите (артралгия) – это показатель непрекращающегося воспалительного процесса в суставе. То же можно сказать и о боли в мышцах (миалгии), которая беспокоит при их воспалении. При ревматической полимиалгии болезненные ощущения затрагивают практически все мышцы, ограничивается их подвижность. Острые, хронические или часто повторяющиеся ревматические боли в суставах, костях и мышцах встречаются более чем у 30% населения земного шара, особенно часто у пожилых людей. В возникновении ревматических болей играют роль механические факторы: перегрузка больного сустава, растяжение сухожильно-связочного аппарата, воспаление синовиальной оболочки; микроциркуляторные расстройства; обменные нарушения в костях; воспалительные и дегенеративные изменения суставов. Вследствие этих процессов в тканях суставов накапливаются алгогенные субстанции – тканевые протеазы, кинины, простагландины, гистамин, серотонин, которые раздражают болевые рецепторы (ноцицепторы), расположенные по всему телу, за исключением головного мозга, и дают начало дуге болевого рефлекса.
Рассматривается возможность ревматического поражения различных внутренних органов. Данные патологоанатомических исследований свидетельствуют о значительной частоте висцеральных ревмоваскулитов. Существенное место также занимают васкулиты головного мозга, способствующие формированию хронических нарушений мозгового кровообращения. Нередкой причиной неврологических синдромов у больных ревматизмом являются эмболические инсульты, которые возникают как осложнение ревмокардита, порока сердца или нарушения сердечного ритма, поражения подкорковых образований, что нередко ведет к развитию бульбарных и псевдобульбарных нарушений. Одним из проявлений этих нарушений является дисфагия – затруднение глотания. Дисфагия чаще всего наблюдается при остро развивающихся неврологических расстройствах, например при инсульте, черепно-мозговой или позвоночно-спинномозговой травме. Нарушение глотания также распространено у больных с дегенеративными заболеваниями нервной системы, такими как болезнь двигательного нейрона (включая амиотрофический боковой склероз), постполиомиелитический синдром, миастения, рассеянный склероз, болезнь Паркинсона. При хронических нарушениях мозгового кровообращения – дисциркуляторных энцефалопатиях (ДЭ) – также имеет место симптом дисфагии в структуре псевдобульбарного синдрома. Необходимо отметить, что затруднение глотания и пережевывания пищи могут объясняться и воспалительными процессами, вызывающими выраженные болевые ощущения в области лицевой и жевательной мускулатуры.
Одной из универсальных групп лекарственных средств, занимающих центральное место среди симптом-модифицирующих медикаментов при лечении алгического синдрома, в том числе ревматических болей, являются нестероидные противовоспалительные препараты (НПВП). Они сочетают в себе противовоспалительное, жаропонижающие, аналгезирующее и антитромботическое свойства, воздействуют практически на все основные симптомы, характерные для ревматических заболеваний. НПВП относятся к числу наиболее часто применяемых в практической медицине лекарственных средств. Препараты этой группы регулярно используют в своей работе более 80% врачей различных специальностей [1]. Одним из НПВП, обладающих высокой противовоспалительной, аналгетической и жаропонижающей активностью, является мелоксикам. Он относится к классу оксикамов, является производным еноловой кислоты. Показано, что по сравнению с другими НПВП (пироксикамом, индометацином, напроксеном и др.) мелоксикам обладает селективностью в отношении изофермента ЦОГ-2, чем объясняется его высокий профиль гастроинтестинальной безопасности по сравнению с таковым других представителей данной группы. Очень важным преимуществом является то, что в сравнении с другими НПВП мелоксикам не повышает риск развития инфаркта миокарда, сердечной недостаточности, отеков и артериальной гипертензии, а вероятность возникновения печеночной недостаточности при применении этого препарата минимальна (Singh G., Triadafilopoulos G., 2001). Клиническая эффективность мелоксикама (7,5 или 15 мг/сут) изучена более чем в 230 исследованиях, в которых принимали участие свыше 30 тыс. пациентов с ревматической патологией. Мелоксикам продемонстрировал высокую эффективность и хорошую переносимость как при внутримышечном введении, так и при пероральном приеме.
На рынке Украины представлены НПВП в форме саше – нимесулид, диклофенак калия. Несмотря на удобство применения, их существенным недостатком является воздействие на показатели свертываемости крови, что ограничивает время применения препарата до 3 дней. Именно поэтому острые и хронические неврологические осложнения, возникающие на фоне ревматической патологии (ревматоидного артрита, анкилозирующего спондилита, остеоартроза и др.), требуют более обдуманного выбора НПВП.
Недавно на украинском фармацевтическом рынке была представлена новая быстрая форма препарата мелоксикам – ородиспергируемые таблетки Мовиксикам® ОДТ (Movi Health, Швейцария). Мовиксикам® ОДТ, единственный в Украине инновационный мелоксикам в диспергированной форме, который одобрен в 36 странах мира, является альтернативой другим таблетированным формам НПВП с быстрым эффектом. В Европе проведены исследования биоэквивалентности новой ородиспергируемой формы мелоксикама, результаты которых демонстрируют ее полное соответствие оригинальному мелоксикаму. Мовиксикам® ОДТ удобно принимать пациентам, которые не могут использовать пероральные формы в связи с нарушением функции глотания или наличием выраженного болевого синдрома при краниальных невралгиях либо лицевых повреждениях. Новая форма также позволяет более гибко дозировать препарат в зависимости от веса и диагноза пациента.
Метаболизм лекарственного вещества до проникновения в системный кровоток при прохождении через желудочно-кишечный тракт и печень называют эффектом первого прохождения. Степень метаболизма лекарственных веществ при этом определяется взаимодействием с ферментами CYP3А4 и CYP2C9, скоростью метаболических реакций и абсорбции. Если лекарственное вещество применяют перорально в небольшой дозе, а содержание ферментов и скорость метаболизма его значительны, то большая часть препарата биотрансформируется, в результате чего снижается его биодоступность. Поскольку всасывание Мовиксикама ОДТ начинается уже в полости рта, влияние на его метаболизм CYP3А4 и CYP2C9, которые в основном находятся в стенке кишечника и печени соответственно, значительно ниже, чем при использовании традиционных таблеток.
Мовиксикам® ОДТ представлен на рынке Украины в виде ородиспергируемых таблеток в дозе 7,5 мг (по 20 таблеток в блистере) либо 15 мг (по 10 или 20 таблеток в блистере). Его применяют 1 р/сут: таблетку кладут под язык, не разжевывая и не глотая, ждут 10-20 с до полного ее растворения; после растворения при необходимости можно запить водой. Рекомендуемая суточная доза – 15 мг/сут. По спектру переносимости (частота побочных эффектов, особенно гастроинтестинальных), вероятности лекарственных взаимодействий мелоксикам обладает рядом преимуществ по сравнению с другими НПВП. Его можно комбинировать с большинством медикаментов, используемых для лечения острой и хронической боли при различных нозологиях.
Следует обратить внимание на еще одно важное достоинство мелоксикама – он не уменьшает антитромбоцитарный потенциал низких доз аспирина. Подтверждением этого факта стало эпидемиологическое исследование G. Singh и соавт., в котором был проведен анализ Калифорнийской базы данных больных, перенесших инфаркт миокарда. Вместе с тем при приеме мелоксикама следует тщательно контролировать состояние пациентов, особенно получающих антикоагулянты, поскольку возможны побочное влияние на функцию тромбоцитов, нарушения свертываемости крови.
Материалы и методы
В нашем исследовании принимали участие 77 пациентов с болевыми синдромами различной этиологии и дисфагией: больные c острым нарушением мозгового кровообращения в вертебробазилярном бассейне (n=12), ДЭ ІІ-ІІІ ст. на фоне ревматоидного артрита, анкилозирующего спондилита или остеоартроза (n=30), герпетическим поражением тройничного нерва (n=7), травматическими повреждениями челюстно-лицевой области различной локализации (n=28).
Кроме тщательного клинического обследования, использовались международные опросники, позволяющие объективизировать состояние больных. Обследование участника осуществляли в день поступления и на фоне проводимой традиционной терапии с применением Мовиксикама ОДТ, используя визуально-аналоговую шкалу боли (ВАШ) и опросник боли McGill (MPQ). Сопоставление результатов исследования до и после лечения позволяло оценить динамику восприятия пациентом своих болевых ощущений.
В качестве задачи-максимум предполагалось фиксировать исчезновение боли или наличие минимального болевого ощущения (<1 балла по ВАШ); как хороший ответ на аналгетическую терапию рассматривали уменьшение боли на 50% в сравнении с исходным уровнем (≥2 балла по ВАШ); клинический эффект оценивали как значимый при снижении интенсивности боли на 20% в сравнению с исходным уровнем (≥1 балл по ВАШ).
Результаты и обсуждение
Под наблюдением находилось 12 пациентов с нейрогенной дисфагией на фоне ишемического инсульта (ИИ), преимущественно (60% случаев) в вертебробазилярном бассейне. Клинико-неврологическое, дополнительные инструментальные и лабораторные обследования выполнялись в соответствии со стандартными протоколами лечения ИИ. Все больные имели в анамнезе ревматическое поражение сердечно-сосудистой системы, средняя продолжительность которого составила 4,8 года.
У обследованных пациентов были выделены такие неврологические синдромы, ассоциирующиеся с нейрогенной дисфагией: бульбарный (n=6); псевдобульбарный (n=3); мозжечковой дисфункции (n=1); полушарные – агностический (при поражении правого полушария; n=1) и апраксический (при локализации инсульта в левом полушарии; n=1). Нарушения функции глотания у этих пациентов возникли на фоне атеротромботического и кардиоэмболического ИИ, лакунарного инфаркта мозга в сочетании с другими неврологическими симптомами. Нарушение глотания было значительно выраженным у 39,3% больных, умеренным и незначительным – у 37,7 и 11,5% пациентов соответственно. При этом у участников с инсультами в вертебробазилярном бассейне неврологический дефицит и нарушения глотания чаще расценивались как тяжелые (у 9 больных), в то время как при полушарных инсультах (бассейн внутренней сонной артерии) неврологический дефицит и дисфагия были выражены в меньшей мере (3 случая). Эти результаты согласуются с данными о локализации центров глотательной функции в ЦНС. Нейрогенная дисфагия чаще всего выступает проявлением бульбарного синдрома при стволовых инсультах (поражается рефлекторная дуга глотательного рефлекса) или псевдобульбарного синдрома при инсультах с билатеральным полушарным поражением (вследствие нарушений корково-ядерного взаимодействия). Двустороннее повреждение корково-ядерных путей, поражение ствола мозга вызывают дисфункцию оральной и глоточной фаз акта глотания, а при патологических изменениях мозжечка нарушается координация работы оральной мускулатуры. У всех больных, помимо описанных неврологических синдромов, возникших на фоне ИИ, наблюдались сопутствующие болевые феномены, типичные для ревматической патологии (миофасциальные боли, мышечно-тонические синдромы и радикулопатии шейно-грудного и пояснично-крестцового отделов) и требующие симптоматической медикаментозной коррекции с помощью НПВП.
Всем больным на фоне базисной сосудистой, метаболической терапии назначали оригинальный препарат Мовиксикам® ОДТ: при выраженном болевом синдроме – по 1 таблетке (7,5 мг) дважды в день курсом 3-10 дней, при умеренном – по 1 таблетке в день 3-10 дней. Диспергируемые таблетки мелоксикама не нужно глотать, они хорошо растворяются в ротовой полости и не требуют запивания водой.
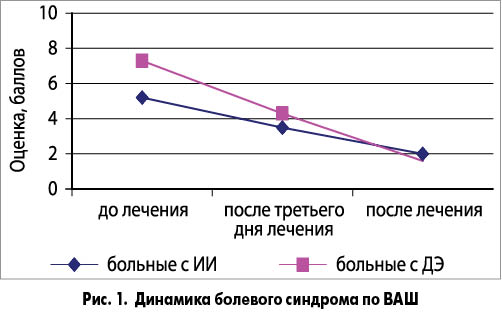
Подтверждением эффективности терапии, помимо исследования неврологического статуса, служили изменения показателей международных шкал. Так, если средняя суммарная оценка по ВАШ до лечения составляла 5,1±0,23 балла, то через 3 дня от начала терапии этот показатель уменьшился до 3,5±0,41 балла, а через 10 дней – до 2,0±0,34 балла (рис. 1). Следовательно, на 3-й день от начала лечения средний показатель суммарной оценки по ВАШ по сравнению с исходным уменьшился на 1,6 балла, через 10 дней – на 3,1 балла, то есть на 39%. Это свидетельствует о клинически значимом ответе на проводимую противоболевую терапию.
Известно, что при резко выраженной ДЭ в связи с усугублением морфологических изменений мозговой ткани клиническая картина становится более тяжелой: прогрессирует снижение памяти и внимания, сужается круг интересов, развивается деменция. Течение заболевания усугубляется повторными сосудистыми церебральными кризами и инсультами. В неврологическом статусе в этот период отмечаются отчетливые органические симптомы: недостаточность черепной иннервации, нистагм, признаки пирамидной недостаточности; иногда – речевые расстройства, парезы конечностей, нарушения чувствительности и тазовые расстройства. Часто наблюдается псевдобульбарный синдром: дисфония, дизартрия и дисфагия, сочетающиеся с симптомами орального автоматизма, повышением глоточного и нижнечелюстного рефлексов, насильственным плачем и смехом. Псевдобульбарный синдром обусловливается множественными мелкоочаговыми изменениями в белом веществе обоих полушарий мозга или мозгового ствола, разрушающими супрануклеарные волокна обеих сторон. При поражении подкорковых узлов возникают различные экстрапирамидные симптомы, которые могут достигать степени паркинсонизма.
Очень часто при ДЭ и после перенесенных ИИ, особенно у пациентов пожилого и старческого возраста, в вертебробазилярном сосудистом бассейне формируется хронический болевой синдром. При этом применение инъекционных препаратов для купирования боли у данной группы больных нежелательно, поскольку они, как правило, получают множество лекарственных средств в рамках лечения основного заболевания; в то же время прием НПВП в таблетированной форме или в саше невозможен из-за нарушений глотания.
Под нашим наблюдением находились 30 больных в возрасте от 60 до 70 лет с ДЭ ІІ-ІІІ ст. с псевдобульбарным синдромом, ведущим к затруднению акта глотания, и хроническим болевым синдромом в виде миофасциальных болей, мышечно-тонического синдрома, радикулопатий шейно-грудной и пояснично-крестцовой локализации. Локальные боли диагностированы у 5 пациентов, проекционные (в сочетании с локальными и миофасциальными) – у 8 участников, радикулярные – у 4, диффузные боли в результате мышечного спазма имели место у 20 больных. Всем пациентам на фоне базисной сосудистой, метаболической терапии рекомендовали Мовиксикам® ОДТ (Movi Health) по описанной выше схеме приема. Учитывалось то, что пациенты, принимающие одновременно диуретики и мелоксикам, должны употреблять достаточное количество жидкости. Терапевтический эффект разной степени выраженности наблюдали у 93% больных. Так, до начала лечения сильную и очень сильную боль испытывали 76% участников. Последняя в процессе терапии сохранилась у 6,7% больных. У 16 пациентов отмечено выраженное снижение алгии, у остальных зарегистрированы слабые ее проявления. Достоверное уменьшение болевого синдрома наступало с 3-го дня лечения (р<0,05). Динамика средней суммарной оценки боли по ВАШ демонстрирует достаточно высокую эффективность исследуемого препарата. Значение среднего показателя по ВАШ до лечения равнялось 7,34±0,23 балла, через 3 дня от начала терапии – 4,3±0,41, а через 10 дней – 1,6±0,34. Следовательно, по сравнению с исходным показателем на 3-й день терапии средняя суммарная оценка по ВАШ уменьшилась на 3,04 балла, а через 10 дней лечения – на 5,74 балла, то есть на 22%. Оценка эффективности лечения с помощью MPQ показала, что сумма рангов составляет 8,6±1,7, число слов (дескрипторов боли) – 5,5±1,0 (р<0,05). Это подтверждает достоверность улучшения состояния больного, снижения интенсивности и характера болевых ощущений. Полученные данные свидетельствуют о клинически значимом ответе на терапию.
Проведенное лечение обеспечило достижение положительного результата у 64% пациентов, незначительное улучшение отмечали у 25% участников, отсутствие динамики – у 10% больных.
В лечении герпетических поражений нервной системы часто используются такие НПВП, как диклофенак натрия, нимесулид и др. Мы отдали предпочтение ородиспергируемой форме мелоксикама в качестве аналгезирующей и противовоспалительной терапии при герпетическом поражении тройничного нерва, отмечавшегося у 7 участников испытания. Заболевание манифестировало болевым синдромом в зоне иннервации ветвей тройничного нерва, где впоследствии появились кожные высыпания (множественные папулы, трансформирующиеся в везикулы). Боль в течение всего периода высыпаний носила интенсивный постоянный или приступообразный характер. Чаще всего ее описывали как жгучую, стреляющую, колющую или пульсирующую. Обычно боль усиливалась ночью и при воздействии различных раздражителей (тактильных, температурных и др.), особенно при активизации жевательной мускулатуры. При объективном осмотре были обнаружены расстройства чувствительности в виде гиперестезии, гипестезии или анестезии, включая anesthesia dolorosa и др. Расстройства чувствительности обычно ограничены областью высыпаний, однако весьма изменчивы по форме и интенсивности. Также больные предъявляли жалобы на болезненный акт глотания и жевания, что заставляло их отказываться от приема оральных препаратов. Любые движения челюстью, неизбежные при запивании традиционных таблетированных форм НПВП, вызывали у пациентов интенсивные болевые ощущения, что препятствовало применению указанных медикаментов. В этот период у пациентов также имели место общие нарушения (лихорадка, цефалгия, миалгия, утомляемость, недомогание).
На фоне проводимой этиотропной противовирусной терапии валацикловиром по традиционной схеме в режим лечения были включены Мовиксикам® ОДТ, противоотечные и десенсибилизирующие препараты. Преимущества Мовиксикама ОДТ в данной клинической ситуации обеспечиваются его оптимальными физико-химическими и структурными характеристиками, уникальной формой выпуска препарата, способностью проникать в очаги воспаления и накапливаться в них, хорошей совместимостью с другими лекарственными средствами, а также удобством применения при болевом синдроме в области головы.
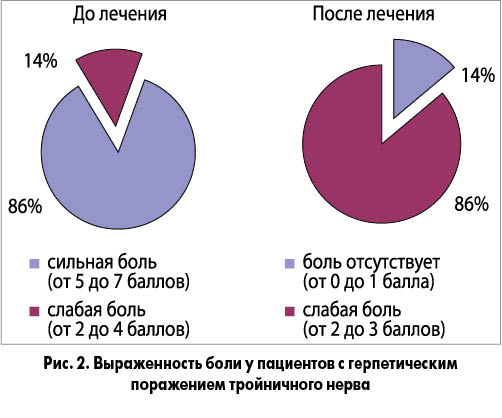
На фоне применения Мовиксикама ОДТ у больных значительно уменьшились болевые ощущения, связанные с работой жевательной мускулатуры и раздражением слизистой оболочки полости рта (рис. 2), что создало условия для последующего приема этиотропных средств.
Выводы
Проведенное исследование показало высокую эффективность препарата Мовиксикам® ОДТ (Movi Health, Швейцария) в лечении пациентов с болевым синдромом различной этиологии на фоне дисфагий. Положительный терапевтический эффект разной степени выраженности наблюдался у 98% больных. Под влиянием терапии НПВП Мовиксикам® ОДТ отмечен значительный регресс интенсивности болевого синдрома, а следовательно, и степени ограничения двигательной функции. Значимых побочных эффектов терапии за время исследования не зарегистрировано. Благодаря удобству применения ородиспергируемой формы (Мовиксикам® ОДТ) область применения мелоксикама значительно расширяется, препарат может использоваться у больных с нарушением глотания.
Важным преимуществом является то, что в сравнении с другими НПВП мелоксикам (Мовиксикам® ОДТ) не повышает риск развития инфаркта миокарда, сердечной недостаточности, отеков и артериальной гипертензии, что делает возможным его использование (после адекватной клинической оценки) у больных с острыми и хроническими нарушениями кровообращения на фоне ревматических заболеваний.
Медична газета «Здоров’я України 21 сторіччя» №3 (376), лютий 2016 р.