27 липня, 2015
Нерешенные проблемы и перспективы исследований в области рассеянного склероза: вирусологические, иммунологические и терапевтические аспекты

Демиелинизирующие заболевания нервной системы являются крайне сложной и до сих пор до конца не решенной проблемой. Одной из самых тяжелых, гетерогенных и непредсказуемых по течению и исходам демиелинизирующих болезней человека является рассеянный склероз (PC). Это распространенное аутоиммунное заболевание, проявляющееся рассеянными в месте и времени очагами демиелинизации в нервной системе, все еще остается важной медико-социальной проблемой современности, несмотря на огромные усилия, приложенные за последние десятилетия для ее разрешения.
Частота рассеянного склероза в мире на сегодняшний день составляет 1:10 000, однако болезнь распространена крайне неоднородно, и существуют зоны, где рассеянный склероз встречается чаще. Несмотря на обилие публикаций и достигнутый прогресс в понимании патогенеза, в современной концепции РС остается очень много принципиальных вопросов, до сих пор не получивших исчерпывающего ответа.
Важными открытиями последних десятилетий стали определение роли микробных факторов в инициации и поддержании аутоиммунного процесса, описание основных механизмов аутоиммунитета, которые могут быть мишенями для терапевтического воздействия, а также углубление понимания ассоциации болезни с иммунодефицитами. Накоплен большой опыт дифференциальной диагностики и описаны новые заболевания, которые могут имитировать РС по клиническим и нейровизуализационным признакам. Произошли революционные изменения в лечебных стратегиях, состоящие во внедрении эффективных иммунотерапевтических подходов как для купирования обострений заболевания, так и для профилактики экзацербаций аутоиммунного процесса в будущем.
Тем не менее, за последнее десятилетие произошло своеобразное разобщение достижений микробиологии и иммунологии в области РС и действующих клинических рекомендаций по ведению пациентов, которые остаются излишне консервативными и во многих аспектах не соответствуют современному пониманию проблемы. В настоящей публикации освещены белые пятна в патогенезе болезни и намечены наиболее перспективные направления исследований, результаты которых могут пролить свет на оптимизацию существующих диагностических и лечебных алгоритмов.
Инфекционные агенты
Хотя существуют единичные сообщения о связи дебюта РС с вакцинацией, инфекционные факторы считаются основными триггерами этой аутоиммунной болезни. Впервые было отмечено, что РС может быть ассоциирован с вирусом кори, поскольку у пациентов зачастую выявляется аномально высокий титр антител к этому вирусу. Сегодня для многих такие взгляды выглядят архаичными, однако недавние работы снова привлекли внимание к указанной ассоциации [8, 19]. Тем не менее, существует мнение, что высокий титр антител к вирусу кори у пациентов с РС может быть следствием поликлональной активации В-лимфоцитов под влиянием Эпштейна–Барр-вируса (EBV) [8]. На данный момент именно EBV рассматривается как основной триггер РС [39]. Однако накопилось много данных о роли других вирусов герпеса – HHV-6 и варицелла зостер-вирус (VZV) [22, 25, 26]. По-видимому, реже провокатором болезни может быть Mycoplasma pneumoniae [109], а еще реже – эндогенные ретровирусы [79]. Напротив, цитомегаловирусная (СMV) инфекция ассоциирована со сниженным риском развития РС и более благоприятным течением уже развившегося аутоиммунного заболевания [112]. Подобное положительное влияние ранее было описано у HHV-7 по отношению к синдрому Уэста у детей [75].
Относительно новыми данными являются доказательства причастности HSV-1 к РС [37]. Описано как непосредственное воздействие вируса [32], так и опосредованное – через активацию других инфекционных агентов, особенно ретровирусов [79]. Таким образом, РС является довольно гетерогенным состоянием по провоцирующим факторам. Возможно, именно это и определяет клиническую неоднородность самого РС.
Действительно, главным механизмом срыва иммунной толерантности рассматривается молекулярная мимикрия между антигенами микробных агентов и мозга, но степень такой мимикрии, равно как и задействованные антигенные детерминанты, существенно отличаются при каждой инфекции [28, 95, 96]. В то же время, показано, что инфекционные факторы не только запускают, но и поддерживают аутоиммунную реакцию при РС. Так, продемонстрировано, что реактивация вируса совпадает с обострениями болезни [48]. Пока еще накоплено мало данных о влиянии микробного агента на клиническую картину и течение РС. Однако есть основания полагать, что вирус кори вызывает преимущественно первично-прогрессирующие формы болезни [19], а EBV и HHV-6 ассоциированы с рецидивирующе-ремиттирующим течением РС [11]. Тем не менее, при HHV-6-инфекции все же больше удельный вес атипичных форм болезни, чем при EBV [81]. VZV, по-видимому, ассоциирован с вторично-прогрессирующим РС [77].
Не ясно, как влияют на течение РС M. pneumoniae и ретровирусы, равно как и комбинации микроорганизмов. Если эти данные будут подтверждены и расширены в последующих исследованиях, возможной станет классификация РС в зависимости от инфекционного фактора. Также описаны случаи обратной связи – реактивации герпесвирусов под влиянием РС, например активации HSV-1 из гассерового ганглия в виде herpes labialis при демиелинизации в области тройничного нерва [94].
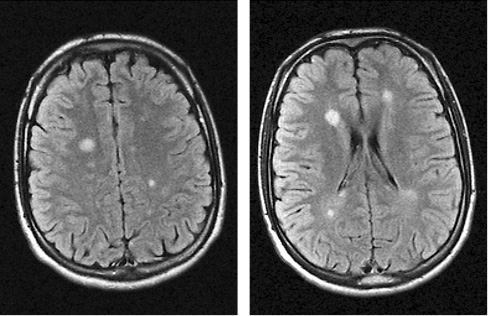
Также забывают, что не только аутоиммунный процесс, но и сами вирусы способны индуцировать демиелинизацию, поражая шванновские клетки и индуцируя воспалительную реакцию. Так, описаны неединичные случаи мультифокального демиелинизирующего лейкоэнцефалита, вызванного HHV-6 и EBV, которые были затруднительными в плане дифференциальной диагностики с РС (рис. 1) [9, 16, 21, 59, 73, 82]. Как стало известно в последнее время, альфа-герпесвирусы (HSV-1, HSV-2, VZV) также могут вызывать различные формы лейкоэнцефалита, хотя такие случаи встречаются реже.
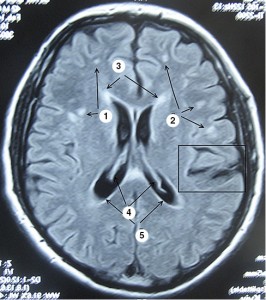 Рис. 2. Васкулопатия мелких церебральных сосудов VZV‑этиологии (наблюдение автора). 1, 2 – очаги лакунарных инфарктов; 3, 5 – лейкоареоз; 4 – дилятация желудочковой системы; фокальная атрофия обозначена квадратом
Рис. 2. Васкулопатия мелких церебральных сосудов VZV‑этиологии (наблюдение автора). 1, 2 – очаги лакунарных инфарктов; 3, 5 – лейкоареоз; 4 – дилятация желудочковой системы; фокальная атрофия обозначена квадратомМы сообщили о 4 случаях HHV-6-энцефалита, при которых требовалась тщательная дифференциальная диагностика с прогрессирующей мультифокальной лейкоэнцефалопатией и РС [4]. VZV-васкулопатия мелких церебральных сосудов также весьма напоминает РС по нейровизуализационным признакам, хотя очаги при этой патологии являются лакунарными инфарктами, а не бляшками демиелинизации (рис. 2). Мы не раз встречались с ошибочной диагностикой РС у этой категории пациентов, что приводило к назначению неадекватного лечения.
Мы описали реактивированную VZV-инфекцию у молодого пациента с последовательным поражением спинного мозга, церебральных сосудов и зрительного нерва, весьма напоминающую РС, однако имеющую обратную динамику патологического процесса [5]. K. Hamano и соавт. сообщили о мультифокальном демиелинизующем энцефалите, вызванном HSV-1, который имитировал РС по клиническим симптомам, МР-признакам и течению [45]. Случаи ретробульбарного неврита описаны при EBV- [12] и HHV-6-инфекции [68]. VZV вызывает оптический неврит который может быть ошибочно расценен как проявление дебюта РС. Мы сообщили о случаях HHV-6-лейкоэнцефалита, напоминающих атипичные формы РС – марбургский вариант болезни с диффузной перивентрикулярной демиелинизацией (рис. 3) и концентрический склероз Балло (рис. 4) [4].
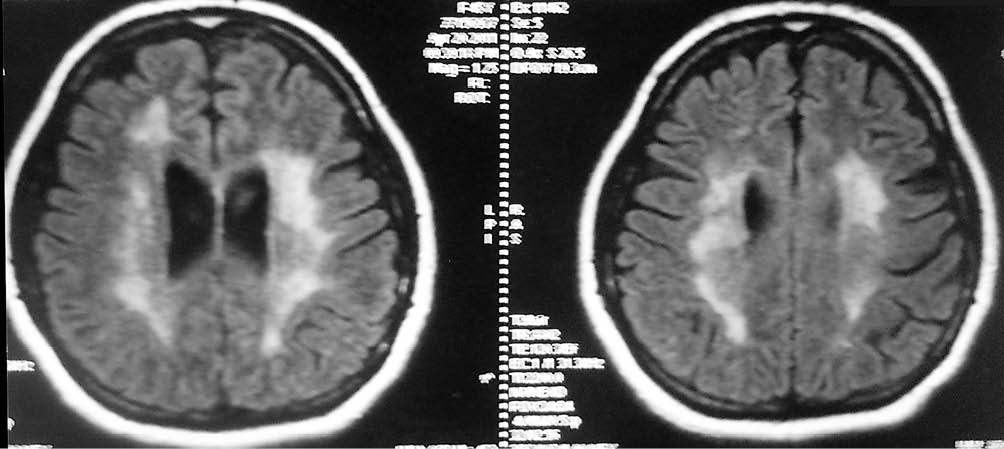 Рис. 3. Диффузный лейкоэнцефалит HHV-6-этиологии у пациентки с дефицитом миелопероксидазы фагоцитов (наблюдение автора)
Рис. 3. Диффузный лейкоэнцефалит HHV-6-этиологии у пациентки с дефицитом миелопероксидазы фагоцитов (наблюдение автора)Таким образом, герпесвирусные нейроинфекции могут имитировать РС по клиническим и нейровизуализационным проявлениям, что требует проведения соответствующей дифференциальной диагностики.
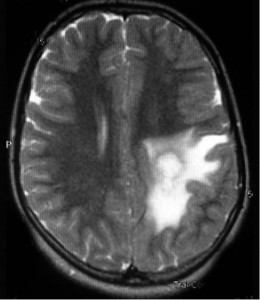 Рис. 4. Монофокальный крупноочаговый HHV-6-лейкоэнцефалит у пациентки с дефицитом миелопероксидазы фагоцитов (наблюдение автора)
Рис. 4. Монофокальный крупноочаговый HHV-6-лейкоэнцефалит у пациентки с дефицитом миелопероксидазы фагоцитов (наблюдение автора)E. Merelli и соавт. рекомендуют разделять вирусные и аутоиммунные обострения при РС, особенно при HHV-6-инфекции, что важно для подбора адекватной терапии. Авторы описали сочетание РС с HHV-6-лейкоэнцефалитом, причем последний имитировал экзацербацию аутоиммунной болезни [69]. R.L. Singhal, L.C. Corman доложили о подостром HSV-1-энцефалите, развившемся на фоне РС, что сопровождалось появлением новых клинических симптомов и очагов на МРТ, которые можно было спутать с обострением аутоиммунной болезни [91]. Совсем недавно C. Juan Pablo и соавт. сообщили о развитии VZV-миелита у больного с РС, который поначалу был ошибочно расценен как обострение аутоиммунной болезни, что привело к назначению неадекватного лечения и продольному распространению воспалительного очага по спинному мозгу с существенным нарастанием неврологического дефицита.
Кроме того, поражения, связанные с VZV-васкулопатией, также могут формироваться уже на фоне существующего РС, что усложняет диагностику. В частности, J.N. Ratchford и соавт. описали диффузную VZV-васкулопатию мелких церебральных артерий у пациента с РС, принимавшего финголимод, которая имитировала обострение аутоиммунного заболевания [85]. Крайне трудно было отличить очаги демиелинизации, обусловленные РС, от фокусов некроза мозга, опосредованных васкулопатией.
Как показывает практика, у пациентов с РС все имеющиеся симптомы обычно автоматически связывают именно с аутоиммунным процессом, игнорируя клинико-инструментальные проявления возможной вирусной нейроинфекции. Необходимо разработать четкие критерии дифференциальной диагностики вирусных и аутоиммунных атак при РС, что невозможно без рационального использования микробиологических и иммунологических тестов.
Иммунологические тесты
Краеугольным камнем диагностики аутоиммунных болезней является проведение иммунологических тестов, выявляющих специфический субстрат аутоиммунной реакции – аутоантитела и аутореактивные клетки. Например, при ревматоидном артрите определяют антитела к циклическому цитруллиновому пептиду, а при системной красной волчанке – к двухспиральной ДНК. Вместе с тем, при РС до сих пор не используются иммунологические тесты, а диагноз устанавливают по клинико-инструментальным данным. Это является существенным недостатком, поскольку связано с многочисленными диагностическими ошибками. На данный момент опубликовано немало работ, в которых анализируются наиболее типичные ошибки в диагностике РС.
V.V. Brinar, M. Habek выделяют основные и второстепенные инфекционные заболевания, которые часто путают с РС. К первым относят болезнь Уиппла, нейроборрелиоз, сифилис, ВИЧ-энцефалопатию, бруцеллез, HHV-6-лейкоэнцефалит, гепатит С, микоплазменный энцефалит и болезнь Крейтцфельдта–Якоба, а ко вторым – болезнь кошачьей царапины, вызванную Bartonella hensellae, среднеземноморскую лихорадку риккетсиозной этиологии и лептоспироз мозга [20]. Не следует забывать о прогрессирующей мультифокальной лейкоэнцефалопатии, вызванной JC-вирусом, как справедливо подчеркивают M. Dupuis и соавт. [36]. L.R. Beeravolu и соавт. описали случай HTLV-1-нейроинфекции, напоминающий РС [15]. J.R. Berger и соавт. сообщили о менингоэнцефалите, вызванном вирусом Коксаки группы В, который был похож на РС [17]. Более того, даже системная HSV-2-инфекция может напоминать РС и быть причиной диагностической ошибки, как это описывают W.B. White и соавт. [108].
К неифекционным болезням, имеющим сходные с РС клинико-инструментальные признаки, следует отнести антифосфолипидный синдром [51], нейроформу синдрома Шегрена [97], оптическую невропатию Лебера (рис. 5) [64, 102], параинфекционные неврологические поражения [103], целиакию [67], полигландулярный аутоиммунный синдром [35], адренолейкодистрофию у женщин-гетерозигот [92], узелковый периартериит [105], синдром Макла–Уэльса [31] и некоторые случаи генетически детерминированного нарушения митохондриальной бета-оксидации [83]. Крайне важен дифференциальный диагноз с оптикомиелитом Девика и мультифазным диссеминированным энцефаломиелитом, поскольку терапия, модифицирующая течение РС, может навредить таким больным [27].
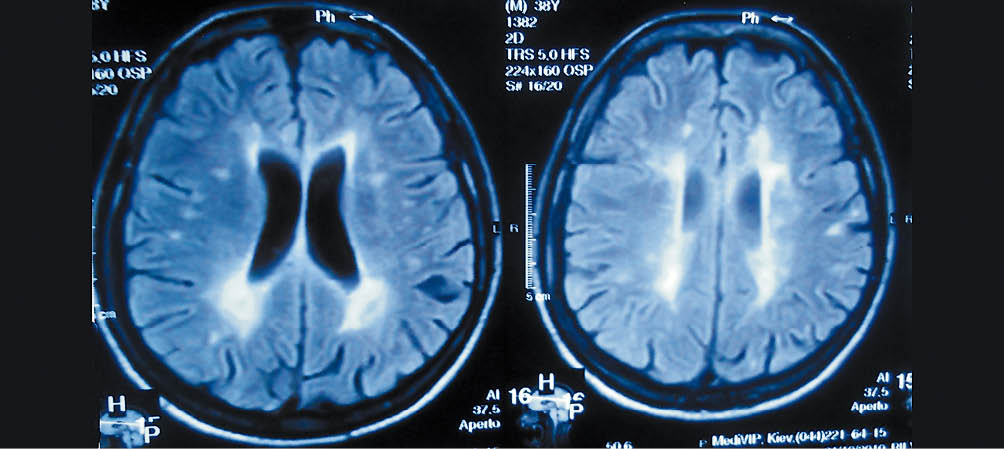 Рис. 5. Оптическая невропатия Лебера «плюс» с МР-картиной болезни, напоминающей РС (multiple sclerosis-like disease; наблюдение автора)
Рис. 5. Оптическая невропатия Лебера «плюс» с МР-картиной болезни, напоминающей РС (multiple sclerosis-like disease; наблюдение автора)Сегодня предложен специальный термин «болезнь, напоминающая РС» (multiple sclerosis-like disease), который охватывает все случаи различных заболеваний, при которых часто ошибочно устанавливается диагноз РС [35]. Только использование иммунологических тестов, объективизирующих специфический субстрат аутоиммунной реакции при РС, позволит избежать многочисленных диагностических ошибок и проволочек с назначением адекватной терапии. Эти тесты доступны в Украине, однако почти не используются на практике.
На сегодняшний день известно, по крайней мере, 3 механизма аутоагрессии при РС, каждый из которых может быть оценен в лабораторных исследованиях:
- Классическим является Th1-опосредованный путь, связанный с аутоантителами к основному белку миелина, заканчивающийся реакцией антитело-зависимой цитотоксичности в ткани ЦНС [28].
- Позже был открыт механизм, опосредованный Th17, в результате которого в мозге накапливаются сенсибилизированные нейтрофилы [101].
- Также в патогенезе РС принимают участие специфические цитотоксические CD8+-Т-лимфоциты, рестриктированные по молекулам HLA I [50, 54].
Есть основания полагать, что каждый механизм накладывает отпечаток как на характер очагов демиелинизации на МР-снимках, так и на течение и прогноз болезни, а также чувствительность к препаратам терапии, модифицирующей течение РС. Однако эти связи еще предстоит изучить, так как имеющихся данных явно недостаточно для дальновидных выводов. Если такие связи будут детально охарактеризованы, мы получим несколько информативных диагностических и прогностических лабораторных тестов при РС. Использование антител к аквапорину-4 для дифференциальной диагностики РС и оптикомиелита Девика является обнадеживающим сигналом для перспективы рационального применения иммунологических тестов при РС [52].
Помимо этого, иммунологические тесты позволяют установить первичный иммунодефицит, осложнением которого может быть РС. В последнее время углубилось понимание ассоциации РС, равно как и других аутоиммунных заболеваний, с первичными иммунодефицитами. Теория иммунодефицита на сегодняшний день является основной в объяснении причины аутоиммунитета в человеческом организме, поскольку имеет наибольшую доказательную базу.
G. Lamoureux и соавт. представляли РС как мультиспецифическую иммунодефицитную болезнь еще в 1977 г., подчеркивая, что это аутоиммунное осложнение может быть ассоциировано с разными иммунными дисфункциями [65]. Теория иммунодефицита может объяснить семейные случаи РС [107], дебют болезни в молодом возрасте, реактивацию оппортунистических микроорганизмов, сочетание с другими аутоиммунными расстройствами, например буллезным пемфигоидом [60], а также чувствительность к иммунотерапии [41]. О причинной роли иммунодефицита свидетельствуют и результаты последних популяционных исследований. Так, Mette Nørgaard и соавт. (2006) на большой выборке показали, что риск развития РС повышен у пациентов, которые часто принимали пенициллин или другие антибиотики для лечения инфекционных эпизодов. По мнению авторов, это указывает на то, что РС формируется преимущественно у часто и длительно болеющих лиц, вынужденных неоднократно использовать антибактериальные препараты.
Согласно нашей практике, изолированный дефицит естественных киллеров и дефицит молекулы CD16 являются наиболее частыми первичными иммунодефицитами, опосредующими развитие этого аутоиммунного осложнения. S. Koch и соавт. в 2005 г. продемонстрировали ассоциацию РС с генетически детерминированным дефицитом ILT6 естественных киллеров (NK) [61]. Позже G. Kabalak и соавт. показали связь этого первичного иммунодефицита с синдромом Шегрена, нейроформы которого весьма напоминают РС [58]. K.P. Wandinger и соавт. выявили функциональный дефицит киллерных клеток у пациентов с РС, состоящий в аномально низкой продукции интерферонов (ИФН) I типа и интерлейкина-2 (ИЛ-2) [106]. Мы описали ассоциацию РС с семейным дефицитом больших гранулярных лимфоцитов, основу которых составляют NK [3], а также с дефицитом IgE [2]. E. Merelli и соавт. показали, что во время обострения РС в ликворе отмечается крайне низкое количество NK, что контрастировало с другими воспалительными заболеваниями ЦНС [70].
Риск развития РС у пациентов с дефицитом NK можно объяснить сниженным надзором за эндогенными вирусами, выступающими в роли провокаторов аутоиммунной реакции.
Действительно, ядром клинической картины изолированного дефицита NK являются рецидивирующие герпесвирусные инфекции [76]. R. Rizzo и соавт. недавно описали неэффективный ответ со стороны NK-клеток по отношению к HSV-1 у пациентов с РС из-за нарушенной экспрессии KIR2DL2 [87]. В то же время, J. Hao и соавт. показали, что резидентные NK в ЦНС в норме угнетают активность Th17, обеспечивая профилактику аутоиммунных осложнений при действии инфекционных триггеров [46]. Поэтому ассоциацию дефицита NK и РС можно объяснить также нарушением иммунорегуляторных механизмов, препятствующих аутоагрессии. Кроме того, показано значение полиморфизма гена IRF5 как фактора высокого риска развития РС [100]. Иногда РС может быть связан с первичной нейтропенией, как сообщают E.J. Münzel и соавт. [71]. В нашей практике также имел место подобный случай (рис. 6).
Такое сочетание может создавать препятствия для назначения средств профилактической терапии РС, угнетающих миелопоэз. Мы разрешили такую проблему за счет базисных препаратов для лечения идиопатической нейтропении. Существует, по крайней мере, 4 сообщения об ассоциации РС с дефицитом IgA [53, 78, 86, 99] и 2 публикации – о связи с первичным дефицитом компонента комплемента С2 [18, 98]. E.S. Resnick и соавт. (2012) сообщили о ряде случаев РС при общем вариабельном иммунодефиците, характеризующемся гипоиммуноглобулинемией. В нашей клинической практике встречался пациент с изолированным дефицитом IgG1, у которого впоследствии развился РС. Эти ассоциации могут объяснить эффективность в/в иммуноглобулинотерапии при РС у некоторых пациентов [62].
R.A. Clarke и соавт. описали РС в семье с синдромом Луи–Барр [29]. Существует несколько сообщений о связи РС с точечными мутациями в гене PTPRC, приводящими к дефициту СD45 [55]. F. Blanco-Kelly с соавт. (2010) показали ассоциацию РС с генетически детерминированной дисфункцией молекулы СD40. В дальнейшем Е.А. Соколова и соавт. (2013) подтвердили такую ассоциацию среди жителей России. R.I. Mazzucchelli и соавт. (2012) сообщили о полиморфизме гена рецептора ИЛ-7 как о факторе риска развития РС.
Более того, иногда сами иммунодефициты имитируют РС, что может стать причиной диагностической ошибки. M.K. Jensen и соавт. описали EBV-положительную первичную лимфому ЦНС у монозиготных близнецов с общим вариабельным иммунодефицитом, которую было трудно отличить от РС по клинико-нейровизуализационным признакам [57]. M.G. Hadfield и соавт. доложили о множественных очаговых поражениях мозга при хронической гранулематозной болезни, весьма сходных с таковыми при РС [44]. Описана также мультифокальная демиелинизация при мутации TNFRSF1A R92Q [47], первичной аутоиммунной полиэндокринопатии [35] и синдроме Макла–Уэльса [31]. Мы показали, что множественные очаги демиелинизации, вызванные HHV-6, могут наблюдаться у пациентов с дефицитом миелопероксидазы фагоцитов [4].
Недавно описано 2 новых иммунодефицита, которые очень похожи на РС по клиническим и нейровизуализационным проявлениям. M. Henneke и соавт. (2009) описали мутацию гена, кодирующего гликопротеин RNASET-2 из рода РНК-аз. Авторы отметили, что утрата функции протеина может нарушать ангиогенез, что приводит к многоочаговому некрозу паренхимы мозга или гидролизу с дальнейшим накоплением одноцепочечной РНК и индукции ответа со стороны системы врожденного иммунитета с развитием демиелинизации. Другая форма иммунодефицита, синдром Айкарди–Гутьере, может имитировать РС у детей. Как сообщили G.L. Rice и соавт. (2009), этот синдром связан с различными мутациями, нарушающими метаболизм РНК или синтез протеинов, предупреждающих самоактивацию клеток врожденного иммунитета мозга внутриклеточными компонентами.
Если говорить о связи вторичных иммунодефицитов и РС, то следует выделить дефицит витамина D, приводящий к дисфункции регуляторных Т-клеток и повышенному риску аутоагрессии [88]. Влияние этого вторичного иммунодефицита объясняет географические отличия в распространенности РС. На сегодняшний день рекомендуют витамин D3 и кальций как вспомогательную терапию при РС [84]. В то же время, ВИЧ может имитировать РС путем индукции мультифокальной энцефалопатии [30].
Таким образом, внедрение иммунологических тестов поможет в диагностике и лечении РС сразу на нескольких уровнях, а именно в дифференциальной диагностике с инфекционными и неинфекционными заболеваниями, которые имеют сходную клинико-нейровизуализационную картину, в понимании механизма аутоиммунитета у конкретного пациента, что может стать отправной точкой для оптимизации проводимой терапии, а также в идентификации причины РС путем диагностики первичного иммунодефицита. Поэтому проведение дальнейших исследований в этом направлении является весьма перспективным и востребованным.
Лечебные стратегии
Внедрение иммунотерапии позволило совершить определенный прорыв в лечении РС, особенно рецидивирующе-ремиттирующей формы болезни, которая встречается чаще всего. Несмотря на успешную апробацию большого количества препаратов, на сегодняшний день именно β-ИФН и глатирамера ацетат составляют основу профилактической терапии РС. Эффективность глатирамера ацетата не превышает 30-40%, и его механизм действия затрагивает лишь один путь патогенеза болезни, опосредованный Th1 [93].
β-ИФН воздействуют сразу на два механизма – Th1-опосредованный, уменьшая проницаемость гематоэнцефалического барьера и изменяя экспрессию ряда провоспалительных субстанций, и Th17-индуцированный, угнетая накопление сенсибилизированных нейтрофилов в ткани ЦНС [101]. По-видимому, эти отличия объясняют более высокую эффективность β-ИФН как средств базисной терапии РС, достигающую 60% по данным некоторых исследований. Совсем новым механизмом иммуномодулирующего воздействия β-ИФН является подавление экспрессии TLR-9, задействованного в патогенезе РС [13]. Однако механизм действия этих препаратов может быть шире, нежели постулируется ныне.
Так, существует ряд серьезных работ, указывающих на прямой противовирусный эффект β-ИФН по отношению к герпетическим агентам у пациентов с РС [10, 34, 40, 42, 49]. Более того, у больных, принимающих эти препараты, снижается частота и тяжесть ОРВИ, что указывает на более обширный противовирусный потенциал терапии [74]. В соответствии с этим, T. Petersen и соавт. продемонстрировали подавление эндогенных ретровирусов HERV-H и HERV-W у пациентов с РС под влиянием препарата β-ИФН [80]. Н.Я. Спивак и соавт. показали, что прямой противовирусный эффект β-ИФН в зависимости от условий эксперимента в 10-100 раз выше, чем у α-ИФН, которые являются признанными противовирусными агентами [7]. Об эффективности β-ИФН при дефиците NK стало известно еще в 80-х годах прошлого столетия [14, 111]. J. Jaworska и соавт. выявили способность HHV-6 подавлять продукцию эндогенных β-ИФН в организме человека [56]. Поэтому такие препараты можно рассматривать и как противомикробные агенты, и как средства базисной терапии иммунодефицита, лежащего в основе многих случаев РС. В то же время, переносимость терапии обычно удовлетворительная. Гриппоподобный синдром и повышение сывороточных концентраций АЛТ и АСТ являются основными побочными эффектами β-ИФН [10]. Необходимо больше препаратов с таким многоуровневым воздействием при РС, как β-ИФН.
Однако следует учитывать, что препараты β-ИФН имеют различную эффективность при РС, что связано с отличиями в действующем веществе, дозах и режимах введения. Следует принимать во внимание результаты исследования EVIDENCE, которые показали преимущества высокодозовой частой терапии β-ИФН (Rebif, 44 мкг, 3 раза в неделю) по сравнению с низкодозовым лечением с редким введением препарата (Avonex, 30 мкг, 1 раз в неделю). Также препараты различных производителей отличаются по количеству и качеству исследований, в которых их апробировали.
6 июня 2013 г. авторитетная организация Кокрановское Сотрудничество опубликовала метаанализ исследований иммуномодуляторов и иммуносупрессантов, используемых для лечения РС. Этот независимый метаанализ включал 44 исследования и более 17 400 пациентов. В анализ вошли 11 лекарственных препаратов: Rebif, Avonex, Betaseron, Copaxone, Tysabri, митоксантрон, метотрексат, циклофосфамид, азатиоприн, в/в иммуноглобулин и кортикостероиды длительного действия. Со всей очевидностью было показано, что именно Tysabri и Rebif превосходят все остальные препараты в отношении предупреждения обострений и замедления инвалидизации в течение более 2 лет у пациентов с рецидивирующе-ремиттирующим РС.
В то же время, не ясна эффективность β-ИФН при РС, индуцированном микоплазменной инфекцией, априори менее чувствительной к подобной терапии, чем герпесвирусы. По-видимому, рациональное использование микробиологических и иммунологических тестов позволит улучшить подбор средств терапии, модифицирующей течение РС, который производится сегодня эмпирически.
В последнее время наметилась тревожная тенденция к возврату к иммуносупрессивным методам профилактического лечения РС, которые потерпели фиаско в недалеком прошлом, уступив место иммунотерапии. Новые иммуносупрессивные препараты зачастую дают более быстрый эффект, чем иммунотерапевтические агенты, подобно глюкокортикоидам во время обострений. Однако безопасность такой терапии остается под вопросом, особенно в долгосрочной перспективе.
Как указывалось выше, натализумаб имеет такую же доказательную базу эффективности, как и β-ИФН, однако переносимость терапии существенно отличается. Об ассоциации приема натализумаба и прогрессирующей мультифокальной лейкоэнцефалопатии стало хорошо известно благодаря наблюдениям при РС и болезни Крона. Недавно A. Kwiatkowski и соавт. описали случай височного долевого некротически-геморрагического энцефалита HSV-1-этиологии после назначения натализумаба у 36-летней женщины с РС [63]. В соответствии с этим, E.S. Shenoy и соавт. сообщили о HSV-2-менингите при приеме натализумаба [90]. Более того, K. Yao и соавт. показали, что натализумаб приводит к усилению репродукции HHV-6 в олигодендроцитах больных РС из-за снижения иммунного надзора, что может привести к развитию мультифокального лейкоэнцефалита HHV-6-этиологии [110]. A. Schweikert и соавт. сообщили о развитии первичной лимфомы ЦНС у пациента с РС, получавшего натализумаб [89]. Совсем недавно A.J. Fine и соавт. (2013) сообщили о 20 пациентах с РС, принимающих натализумаб, у которых развились тяжелые формы HSV-1- и VZV-нейроинфекции, оказавшие выраженное инвалидизирующее влияние или вызвавшие летальный исход.
Как продемонстрировали L. Costelloe и соавт., алемтузумаб оказался несколько эффективнее β-ИФН при ремиттирующем РС в рандомизированном контролируемом исследовании, однако в трети случаев индуцировал другие аутоиммунные осложнения, чаще всего – тиреоидит [33]. G. Buccoliero и соавт. (2010) сообщили о развитии тяжелого энцефалита, вызванного VZV, у пациента, получавшего адалимумаб – еще один препарат моноклональных антител – по поводу псориатического артрита.
H. Nakano и соавт. сообщили о развитии neuromyelitis optica и VZV-менингита под влиянием митоксантрона у пациента с РС. Тяжесть осложнений терапии существенно превышала таковую самого РС [72]. A. Caruso и соавт. описали угрожающий жизни DIHS/DRESS у пациента с РС, принимающего митоксантрон [23]. Как известно, это осложнение сегодня связывают с HHV-6-инфекцией.
Финголимод может не только помогать при РС, но и вызывать драматическое ухудшение клинической и нейровизуализационной картины, как сообщили в нескольких недавних исследованиях [24, 43, 104]. Ухудшение состояния при приеме финголимода возможно также вследствие индукции реактивации герпесвирусов. Так, J.N. Ratchford и соавт. описали развитие VZV-энцефалита и васкулопатии церебральных сосудов у пациента с РС, принимавшего этот селективный цитостатик [85].
Учитывая доказанную роль некоторых инфекционных агентов в патогенезе РС, перспективной представляется профилактическая антимикробная терапия при этой болезни. В таком направлении уже приложены первые усилия, однако об эффективности подобного подхода к лечению известно еще очень мало. J. Lycke и соавт. продемонстрировали пользу от профилактической терапии при помощи ацикловира в дозе 800 мг 3 раза в сутки у пациентов с ремиттирующим РС в двойном слепом плацебо-контролируемом исследовании (n=60) [66]. В то же время, применение валацикловира привело лишь к тенденции к клинико-инструментальному улучшению, однако исследованию не хватило статистической мощности для однозначных выводов об эффективности апробируемого терапевтического подхода [38]. В недавнем исследовании, проведенным под руководством Л.И. Соколовой, показана отчетливая польза от противовирусного лечения при РС [6]. Наши наблюдения также указывают на положительное влияние ациклических аналогов гуанозина.
Напротив, рокситромицин, подавляющий M. pneumoniae, оказался бесполезным в профилактической терапии РС [109]. Тем не менее, С.К. Евтушенко в известной монографии по РС у детей указывает на пользу от применения антибиотиков у некоторых пациентов [1]. L.M. Metz и соавт. (2009) в мультицентровом двойном слепом плацебо-контролируемом исследовании показали дополнительную пользу от применения миноциклина в дозе 100 мг дважды в день per os в сочетании с глатирамера ацетатом при рецидивирующе-ремиттирующем РС. Ранее A. Minagar и соавт. (2008) в небольшом пилотном испытании продемонстрировали клинико-инструментальное улучшение при дополнительном назначении доксициклина в дозе 100 мг в сутки у пациентов с РС, получающих β-ИФН. Эти антибиотики обладают выраженной противовоспалительной активностью, поэтому остается неизвестным – связан ли полученный положительный эффект миноциклина и доксициклина с собственно антибактериальным, противовоспалительным или же сочетанным воздействием препаратов.
К сожалению, во многих из проведенных исследований не осуществлялся надлежащий микробиологический контроль, что могло быть систематической ошибкой, повлиявшей на результаты испытания. Действительно, ациклические аналоги гуанозина не воздействуют на такие инфекционные агенты, как вирус кори, ретровирусы и M. pneumoniae, с которыми мог быть ассоциирован РС у некоторых пациентов, принимавших участие в исследованиях. С другой стороны, рокситромицин потенциально полезен только при РС, индуцированном микоплазменной инфекцией, что требовало специального отбора пациентов, который, тем не менее, не проводился.
Помимо этого, следует проверять – действительно ли достигнуто подавление интересующего микроба под влиянием испытуемого препарата в организме конкретного больного, чтобы избежать случаев резистентности, которые могут повлиять на результат исследования. Нельзя допускать подмену понятий, когда под представлениями о несостоятельности лечебного подхода скрываются данные всего лишь о несовершенстве апробированного медикамента. Необходимы дальнейшие исследования в области профилактической противомикробной терапии при РС с более продуманным дизайном.
Выводы
Новые достижения в области микробиологии и иммунологии подрывают основы устоявшейся концепции о сугубо аутоиммунной природе РС, а также делают сомнительными представления о цельности и самостоятельности болезни. Недаром P.K. Stys задает справедливый вопрос: является ли РС действительно аутоиммунной болезнью или всего лишь реакцией? [93] Слишком велики отличия между концентрическим склерозом Балло, марбургским вариантом и классическим рецидивирующе-ремиттирующим РС. Даже в рамках ремитирующей формы болезни отмечается широкая вариабельность во времени дебюта, частоте и тяжести атак, зонах поражения нервной системы, клинических симптомах, исходах и чувствительности к терапии.
Открытия в области микробиологии и иммунологии объясняют неоднородность РС разнообразием микробных триггеров, иммунопатологических механизмов и иммунодефицитов, лежащих в основе болезни. Есть основания полагать, что тот комплекс проявлений, который мы ныне именуем РС, на самом деле является не одной болезнью, а группой гетерогенных синдромов различных заболеваний со сходной клинико-инструментальной картиной. Это объяснило бы беспрецедентную неоднородность РС и невозможность идентификации одной причины болезни. Подобные мировоззренческие изменения сегодня происходят и в учении о бронхиальной астме. Тем не менее, последние достижения в понимании патогенеза РС открывают новые, многообещающие пути оптимизации диагностики и терапии.
Необходимо шире использовать иммунологические тесты для верификации диагноза РС и идентификации микробных триггеров, а также поиска причинного иммунодефицита. Целесообразно сконцентрировать усилия не только на усовершенствовании иммуносупрессивного лечения, которое никогда не даст большего эффекта, чем временное подавление иммунного воспаления без влияния на глубинные механизмы развития РС, но и на способах иммунотерапии, которые влияли бы на контроль над эндогенными микроорганизмами, выступающими в роли триггеров аутоиммунной атаки, и способствовали компенсации лежащих в основе РС иммунодефицитов. β-ИФН – прекрасный пример успеха в этом направлении, который является хорошим путеводным знаком для будущих исследований. Профилактическая антимикробная терапия как дополнительная лечебная стратегия также выглядит вполне перспективно, однако рациональное воздействие возможно только после точной идентификации микробного триггера в каждом конкретном случае.
В изменении традиционных взглядов нет ничего плохого, если эти трансформации основываются на доказательствах, ведь, в конечном итоге, мы все, пациенты, врачи и функционеры министерства здравоохранения, крайне заинтересованы в достижения прогресса в профилактике и лечении РС, который не возможен без понимания истинной природы болезни. Однако нужно еще много поработать над тем, чтобы проникнуть в неизвестные глубины патогенеза РС.
Литература
1. Евтушенко С.К., Москаленко М.А. Рассеянный склероз у детей. – Киев, 2009. – 250 с.
2. Казмірчук В.Є., Мальцев Д.В., Царик В.В. Клініка, діагностика і лікування ізольованого дефіциту IgE: огляд літератури і описання клінічних випадків // Імунологія та алергологія. – 2012. – №3. – С. 5 –21.
3. Мальцев Д.В. Клинический полиморфизм семейного дефицита больших гранулярных лимфоцитов // Клиническая иммунология, аллергология, инфектология. – 2009. – 3(22). – С. 36-40.
4. Мальцев Д.В. Прогресуюча мультифокальна лейкоенцефалопатія, асоційована з вірусом герпесу людини 6-го типу // Укр. мед. часопис. – 2012. – 1(87). – С. 136–142.
5. Мальцев Д.В., Климчук В.В. Труднощі у діагностиці неврологічних ускладнень VZV-інфекції: випадки з клінічної практики // Укр. мед. часопис. – 2011. – 5(85). – С. 122–127.
6. Соколова Л.И. Герпесвирусная инфекция и прогноз при рассеянном склерозе // Імунологія та алергологія. – 2012. – №3 (додаток). – С. 12.
7. Спивак Н.Я., Лазаренко Л.Н., Михайленко О.Н. Интерферон и система мононуклеарных фагоцитов. – Киев, 2002. — 163 с.
8. Ahlgren C., Odén A., Bergström T., Lycke J. Serum and CSF measles antibody levels increase over time in patients with multiple sclerosis or clinically isolated syndrome // J. Neuroimmunol. 2012.— Vol. 247(1-2).— P.70-74.
9. Akasaka M., Sasaki M., Ehara S., Kamei A., Chida S. Transient decrease in cerebral white matter diffusivity on MR imaging in human herpes virus-6 encephalopathy // Brain Dev.— 2005. — Vol. 27(1).— P.30-33.
10. Alvarez-Lafuente R., De Las Heras V., Bartolomé M., Picazo JJ., Arroyo R. Beta-interferon treatment reduces human herpesvirus-6 viral load in multiple sclerosis relapses but not in remission // Eur. Neurol.— 2004.— Vol. 52(2).— 87-91.
11. Alvarez-Lafuente R., de las Heras V., García-Montojo M., Bartolomé M., Arroyo R. Human herpesvirus-6 and multiple sclerosis: relapsing-remitting versus secondary progressive // Mult. Scler.— 2007.— Vol. 13(5).— P.578-583.
12. Anderson M.D., Kennedy C.A., Lewis A.W., Christensen G.R. Retrobulbar neuritis complicating acute Epstein-Barr virus infection // Clin. Infect. Dis.— 1994.— Vol. 18(5).— P.799-801.
13. Balashov K.E., Aung L.L., Vaknin-Dembinsky A., Dhib-Jalbut S., Weiner H.L. Interferon-β inhibits toll-like receptor 9 processing in multiple sclerosis // Ann Neurol.— 2010.— Vol. 68(6).— P.899-906.
14. Bandyopadhyay S., Miller D.S., Matsumoto-Kobayashi M. et al. Effects of interferons and interleukin 2 on natural killing of cytomegalovirus-infected fibroblasts // Clin. Exp. Immunol. – 1987. – Vol. 67(2). – Р. 372–382.
15. Beeravolu L.R., Frohman E.M., Frohman T.C., Remington G.M., Lee S., Levin M.C. Pearls & Oy-sters: “Not multiple sclerosis” and the changing face of HTLV-1: A case report of downbeat nystagmus // Neurology.— 2009.— Vol. 72(24). — P. e119-120.
16. Beović B., Pecaric-Meglic N., Marin J., Bedernjak J., Muzlovic I., Cizman M. Fatal human herpesvirus 6-associated multifocal meningoencephalitis in an adult female patient // Scand. J. Infect. Dis.— 2001.— Vol. 33(12).— P.942-944.
17. Berger J.R., Fee D.B., Nelson P., Nuovo G. Coxsackie B meningoencephalitis in a patient with acquired immunodeficiency syndrome and a multiple sclerosis-like illness // J Neurovirol.— 2009.— Vol. 15(3).— P. 282-287.
18. Bertrams J., Opferkuch W., Grosse-Wilde H., Luboldt W., Schuppien W., Kuwert E. C2 Hypocomplementaemia in multiple sclerosis // Lancet.— 1976.— Vol. 2(7999).— P.1358-1359.
19. Brettschneider J., Tumani H., Kiechle U., Muche R., Richards G., Lehmensiek V., Ludolph A.C., Otto M. IgG antibodies against measles, rubella, and varicella zoster virus predict conversion to multiple sclerosis in clinically isolated syndrome // PLoS One.— 2009.— Vol. 4(11).— P. e7638.
20. Brinar V.V., Habek M. Rare infections mimicking MS // Clin. Neurol. Neurosurg.— 2010.— Vol. 112(7).— P.625-628.
21. Carrigan D.R., Harrington D., Knox K.K. Subacute leukoencephalitis caused by CNS infection with human herpesvirus-6 manifesting as acute multiple sclerosis // Neurology.— 1996.— Vol. 47(1).— P. 145-148.
22. Carrigan D.R., Knox K.K. Human herpesvirus six and multiple sclerosis // Mult. Scler. – 1997. – Vol. 3(6). – P. 390-394.
23. Caruso A., Vecchio R., Patti F., Neri S. Drug rash with eosinophilia and systemic signs syndrome in a patient with multiple sclerosis // Clin. Ther.— 2009.— Vol. 31(3).— P.580-584.
24. Centonze D., Rossi S., Rinaldi F., Gallo P. Severe relapses under fingolimod treatment prescribed after natalizumab // Neurology.— 2012.— Vol. 79(19).— P.2004-2005.
25. Cermelli C., Berti R., Soldan S.S., Mayne M., D’ambrosia J.M., Ludwin S.K., Jacobson S. High frequency of human herpesvirus 6 DNA in multiple sclerosis plaques isolated by laser microdissection // J. Infect. Dis.— 2003.— Vol. 187(9).— P. 1377-1387.
26. Challoner P.B., Smith K.T., Parker J.D., MacLeod D.L., Coulter S.N., Rose T.M., Schultz E.R., Bennett J.L., Garber R.L., Chang M., et al. Plaque-associated expression of human herpesvirus 6 in multiple sclerosis // Proc. Natl. Acad. Sci. U S A.— 1995.— Vol. 92(16).— P. 7440-7444.
27. Chen S., Wu A., Zhang B., Li J., Zhang L., Lin Y., Hu X., Lu Z. A case of exacerbated multiphasic disseminated encephalomyelitis after interferon beta treatment // J. Neurol. Sci.— 2013.— Vol. 325(1-2).— P.176-179.
28. Cirone M., Cuomo L., Zompetta C., Ruggieri S., Frati L., Faggioni A., Ragona G. Human herpesvirus 6 and multiple sclerosis: a study of T cell cross-reactivity to viral and myelin basic protein antigens // J. Med. Virol.— 2002.— Vol. 68(2).— P.268-272.
29. Clarke R.A., Fang Z.M., Lee C.S., Sarris M., Murrell D., Kearsley J.H. Multiple sclerosis in a radiosensitive family with low levels of the ATM protein // Australas Radiol.— 2002.— Vol. 46(3).— P.267-274.
30. Coban A., Akman-Demir G., Ozsut H., Eraksoy M. Multiple sclerosis-like clinical and magnetic resonance imaging findings in human immunodeficiency virus positive-case // Neurologist.— 2007.— Vol.13(3).— P.154-157.
31. Compeyrot-Lacassagne S., Tran T.A., Guillaume-Czitrom S., Marie I., Koné-Paut I. Brain multiple sclerosis-like lesions in a patient with Muckle-Wells syndrome // Rheumatology (Oxford).— 2009.— Vol. 48(12).— P.1618-1619.
32. Cortese I., Capone S., Luchetti S., Cortese R., Nicosia A. Cross-reactive phage-displayed mimotopes lead to the discovery of mimicry between HSV-1 and a brain-specific protein // J. Neuroimmunol.— 2001.— Vol. 113(1).— P.119-128.
33. Costelloe L., Jones J., Coles A. Secondary autoimmune diseases following alemtuzumab therapy for multiple sclerosis // Expert Rev. Neurother.— 2012.— Vol. 12(3).— P.335-341.
34. Dominguez-Mozo M.I., Garcia-Montojo M., De Las Heras V., Garcia-Martinez A., Arias-Leal A.M., Casanova I., Arroyo R., Alvarez-Lafuente R. MHC2TA mRNA levels and human herpesvirus 6 in multiple sclerosis patients treated with interferon beta along two-year follow-up // BMC Neurol.— 2012.— Vol. 12.— P.107.
35. Donadio V., Cortelli P., Liguori R., Di Stasi V., Montagna P. Multiple sclerosis-like disease in polyglandular autoimmune syndrome // J. Neurol.— 2001.— Vol. 248(1).— P.61-62.
36. Dupuis M., Fernandes Xavier F.G., Gonsette R.E., Brucher J.M. Progressive multifocal leukoencephalopathy mimicking multiple sclerosis as the sole clinical manifestation of acquired immunodeficiency syndrome // Acta Neurol. Belg.— 1986.— Vol. 86(5).— P.285-296.
37. Ferrò M. T., Franciotta D., Prelle A., Bestetti A., Cinque P. Active intrathecal herpes simplex virus type 1 (HSV-1) and human herpesvirus-6 (HHV-6) infection at onset of multiple sclerosis // J. Neurovirol.— 2012.— Vol. 18(5).— P.437-440.
38. Friedman J.E., Zabriskie J.B., Plank C., Ablashi D., Whitman J., Shahan B., Edgell R., Shieh M., Rapalino O., Zimmerman R., Sheng D. A randomized clinical trial of valacyclovir in multiple sclerosis // Mult. Scler. —2005.— Vol. 11(3).— P. 286-295.
39. Gabibov A.G., Belogurov A.A. Jr., Lomakin Y.A., Zakharova M.Y., Avakyan M.E., Dubrovskaya V.V., Smirnov I.V., Ivanov A.S., Molnar A.A., Gurtsevitch V.E., Diduk S.V., Smirnova K.V., Avalle B., Sharanova S.N., Tramontano A., Friboulet A., Boyko A.N., Ponomarenko N.A., Tikunova N.V. Combinatorial antibody library from multiple sclerosis patients reveals antibodies that cross-react with myelin basic protein and EBV antigen // FASEB J.— 2011.— Vol. 25(12).— P.4211-4221.
40. Garcia-Montojo M., De Las Heras V., Bartolome M., Arroyo R., Alvarez-Lafuente R. Interferon beta treatment: bioavailability and antiviral activity in multiple sclerosis patients // J. Neurovirol.— 2007.— Vol. 13(6).— P.504-512.
41. Garcia-Montojo M., Martinez A., De Las Heras V., et al. Herpesvirus active replication in multiple sclerosis: a genetic control? // J. Neurol. Sci. – 2011. – Vol. 311(1-2). – P. 98-102.
42. Garcia-Montojo M., De Las Heras V., Dominguez-Mozo M., Bartolome M., Garcia-Martinez M.A., Arroyo R., Alvarez-Lafuente R.; HHV-6 and Multiple Sclerosis Study Group. Human herpesvirus 6 and effectiveness of interferon β1b in multiple sclerosis patients // Eur. J. Neurol.— 2011.— Vol. 18(8).— P.1027-1035.
43. Gross C.M., Baumgartner A., Rauer S., Stich O. Multiple sclerosis rebound following herpes zoster infection and suspension of fingolimod // Neurology.— 2012.— Vol. 79(19).— P.2006-2007.
44. Hadfield M.G., Ghatak N.R., Laine F.J., Myer E.C., Massie F.S., Kramer W.M. Brain lesions in chronic granulomatous disease // Acta Neuropathol.— 1991.— Vol. 81(4).— P.467-470.
45. Hamano K., Robain O., Gray F., Farkas-Bargeton E. Focal perivascular alterations of white matter in herpes simplex encephalitis — a histological and immunocytochemical study // Jpn. J. Psychiatry Neurol.— 1986.— Vol. 40(2).— P.209-219.
46. Hao J., Liu R., Piao W. et al. Central nervous system (CNS)-resident natural killer cells suppress Th17 responses and CNS autoimmune pathology // J. Exp. Med. – 2010. – Vol. 207(9). – Р. 1907–1921.
47. Hoffmann L.A., Lohse P., König F.B., Feneberg W., Hohlfeld R., Kümpfel T. TNFRSF1A R92Q mutation in association with a multiple sclerosis-like demyelinating syndrome // Neurology.— 2008.— Vol. 70(13 Pt 2).— P.1155-1156.
48. Höllsberg P., Kusk M., Bech E., Hansen H. J., Jakobsen J., Haahr S. Presence of Epstein-Barr virus and human herpesvirus 6B DNA in multiple sclerosis patients: associations with disease activity // Acta Neurol. Scand.— 2005.— Vol. 112(6).— P.395-402.
49. Hong J., Tejada-Simon M.V., Rivera V.M., Zang Y.C., Zhang J.Z. Anti-viral properties of interferon beta treatment in patients with multiple sclerosis // Mult. Scler.— 2002.— Vol. 8(3).— P. 237-242.
50. Hong J., Zang Y.C., Li S., et al. Ex vivo detection of myelin basic protein-reactive T cells in multiple sclerosis and controls using specific TCR oligonucleotide probes // Eur. J. Immunol.– 2004. – Vol. 34(3). – P. 870-881.
51. Hughes G.R. Migraine, memory loss, and «multiple sclerosis». Neurological features of the antiphospholipid (Hughes’) syndrome // Postgrad. Med. J.— 2003.— Vol. 79(928).— P.81-83.
52. Isobe N., Yonekawa T., Matsushita T., Masaki K., Yoshimura S., Fichna J., Chen S., Furmaniak J., Smith B.R., Kira J.I. Clinical Relevance of Serum Aquaporin-4 Antibody Levels in Neuromyelitis Optica. // Neurochem Res.— 2013. Mar 2. [Epub ahead of print].
53. Iwasaki Y., Kinoshita M., Uchida A. A case of multiple sclerosis demonstrating ossification of anterior, posterior longitudinal ligament, thickening of the skull, and selective IgA deficiency // Rinsho Shinkeigaku.— 1987.— Vol. 27(9).— P.1122-1126.
54. Jacobsen M., Cepok S., Quak E., Happel M., Gaber R., Ziegler A., Schock S., Oertel W.H., Sommer N., Hemmer B. Oligoclonal expansion of memory CD8+ T cells in cerebrospinal fluid from multiple sclerosis patients // Brain.— 2002.— Vol. 125(Pt 3).— P.538-550.
55. Jacobsen M., Schweer D., Ziegler A., Gaber R., Schock S., Schwinzer R., Wonigeit K., Lindert R.B., Kantarci O., Schaefer-Klein J., Schipper H.I., Oertel W.H., Heidenreich F., Weinshenker B.G., Sommer N., Hemmer B. A point mutation in PTPRC is associated with the development of multiple sclerosis // Nat. Genet.— 2000.— Vol. 26(4).— P.495-499.
56. Jaworska J., Gravel A., Fink K., Grandvaux N., Flamand L. Inhibition of transcription of the beta interferon gene by the human herpesvirus 6 immediate-early 1 protein // J. Virol.— 2007.— Vol. 81(11).— P.5737-5748.
57. Jensen M.K., Koch-Henriksen N., Johansen P., Varming K., Christiansen C.B., Knudsen F. EBV-positive primary central nervous system lymphomas in monozygote twins with common variable immunodeficiency and suspected multiple sclerosis // Leuk Lymphoma.— 1997.— Vol. 28(1-2).— P.187-193.
58. Kabalak G., Dobberstein S.B., Matthias T. et al. Association of immunoglobulin-like transcript 6 deficiency with Sjögren’s syndrome // Arthritis Rheum. – 2009. – Vol. 60(10). – Р. 2923–2925.
59. Kamei A., Ichinohe S., Onuma R., Hiraga S., Fujiwara T. Acute disseminated demyelination due to primary human herpesvirus-6 infection // Eur. J. Pediatr.— 1997.— Vol. 156(9).— P.709-712.
60. Kirtschig G., Walkden V.M., Venning V.A., Wojnarowska F. Bullous pemphigoid and multiple sclerosis: a report of three cases and review of the literature // Clin. Exp. Dermatol.— 1995.— Vol. 20(6).— P.449-453.
61. Koch S., Goedde R., Nigmatova V. et al. Association of multiple sclerosis with ILT6 deficiency // Genes Immun. – 2005. – Vol. 6(5). – Р. 445–447.
62. Kraus D., Konen O., Straussberg R. Schilder’s disease: non-invasive diagnosis and successful treatment with human immunoglobulins // Eur. J. Paediatr. Neurol.— 2012.— Vol. 16(2).— P.206-208.
63. Kwiatkowski A., Gallois J., Bilbault N., Calais G., Mackowiak A., Hautecoeur P. Herpes encephalitis during natalizumab treatment in multiple sclerosis // Mult. Scler.— 2012.— Vol. 18(6).— P.909-911.
64. La Russa A., Cittadella R., Andreoli V., Valentino P., Trecroci F., Caracciolo M., Gallo O., Gambardella A., Quattrone A. Leber’s hereditary optic neuropathy associated with a multiple-sclerosis-like picture in a man // Mult. Scler.— 2011.— Vol. 17(6).— P.763-766.
65. Lamoureux G., Toupin J., Leyva F. Multiple sclerosis: a multi-specific immune deficiency disease // Ann. Immunol. (Paris).— 1977.— Vol. 128(1-2).— P.531-536.
66. Lycke J., Svennerholm B., Hjelmquist E., Frisén L., Badr G., Andersson M., Vahlne A., Andersen O. Acyclovir treatment of relapsing-remitting multiple sclerosis. A randomized, placebo-controlled, double-blind study // J. Neurol.— 1996.— Vol. 243(3).— P.214-224.
67. Mansueto P., Di Stefano L., D’Alcamo A., Carroccio A. Multiple sclerosis-like neurological manifestations in a coeliac patient: nothing is as it seems // BMJ Case Rep.— 2012.— pii: bcr2012006392.
68. Méchaï F., Boutolleau D., Manceron V., Gasnault J., Quertainmont Y., Brosseau J.P., Delfraissy J.F., Labetoulle M., Goujard C. Human herpesvirus 6-associated retrobulbar optic neuritis in an HIV-infected patient: response to anti-herpesvirus therapy and long-term outcome // J. Med. Virol.— 2007.— Vol. 79(7).— P.931-934.
69. Merelli E., Sola P., Barozzi P., Torelli G. An encephalitic episode in a multiple sclerosis patient with human herpesvirus 6 latent infection // J. Neurol. Sci.— 1996.— Vol. 137(1).— P. 42-46.
70. Merelli E., Sola P., Faglioni P., Giordani S., Mussini D., Montagnani G. Natural killer cells and lymphocyte subsets in active MS and acute inflammation of the CNS // Acta Neurol. Scand.— 1991.— Vol. 84(2).— P.127-131.
71. Münzel E.J., Wimperis J.Z., Williams A. Relapsing-remitting multiple sclerosis and chronic idiopathic neutropenia: a challenging combination // BMJ Case Rep.— 2013.— pii: bcr2012007936.
72. Nakano H., Motoyama R., Tanaka K., Tanaka M. A case of neuromyelitis optica with varicella zoster virus meningitis during mitoxantrone treatment // Rinsho Shinkeigaku.— 2011.— Vol. 51(9).— P. 703-705.
73. Novoa L.J., Nagra R.M., Nakawatase T., Edwards-Lee T., Tourtellotte W.W., Cornford M.E. Fulminant demyelinating encephalomyelitis associated with productive HHV-6 infection in an immunocompetent adult // J. Med. Virol.— 1997.— Vol. 52(3).— P.301-308.
74. Oikonen M.K., Erälinna J.P. Beta-interferon protects multiple sclerosis patients against enhanced susceptibility to infections caused by poor air quality // Neuroepidemiology.— 2008.— Vol. 30(1).— P.13-19.
75. Ono J., Imai K., Tanaka-Taya K., Kurahashi H., Okada S. Decreased frequency of seizures in infantile spasms associated with lissencephaly by human herpes virus 7 infection // Pediatr. Int.— 2002.— Vol. 44(2).— P.168-170.
76. Orange J.S.Human natural killer cell deficiencies // Curr. Opin.Allergy Clin.Immunol.– 2006.– Vol.6(6).– P.399–409.
77. Ordoñez G., Martinez-Palomo A., Corona T., Pineda B., Flores-Rivera J., Gonzalez A., Chavez-Munguia B., Sotelo J. Varicella zoster virus in progressive forms of multiple sclerosis // Clin. Neurol. Neurosurg.— 2010.— Vol. 112(8).— P.653-657.
78. Pereira L.F., Gómez M., García Trujillo J.A., Romero Chala S., Cámara Hijón C. Selective immunoglobulin A deficiency is exceptionally associated with multiple sclerosis // Neurologia.— 2012.— Vol. 27(5).— P.316.
79. Perron H., Suh M., Lalande B., Gratacap B., Laurent A., Stoebner P., Seigneurin J.M. Herpes simplex virus ICP0 and ICP4 immediate early proteins strongly enhance expression of a retrovirus harboured by a leptomeningeal cell line from a patient with multiple sclerosis // J. Gen. Virol.— 1993.— Vol. 74 (Pt1).— P.65-72.
80. Petersen T., Møller-Larsen A., Ellermann-Eriksen S., Thiel S., Christensen T. Effects of interferon-beta therapy on elements in the antiviral immune response towards the human herpesviruses EBV, HSV, and VZV, and to the human endogenous retroviruses HERV-H and HERV-W in multiple sclerosis // J. Neuroimmunol.— 2012.— Vol. 249(1-2).— P.105-108.
81. Pohl D., Rostasy K., Krone B., Hanefeld F. Baló’s concentric sclerosis associated with primary human herpesvirus 6 infection // J. Neurol. Neurosurg. Psychiatry.— 2005.— Vol. 76(12).— P.1723-1725.
82. Poppe M., Brück W., Hahn G., Weissbrich B., Heubner G., Goebel H.H., Todt H. Fulminant course in a case of diffuse myelinoclastic encephalitis — a case report // Neuropediatrics.— 2001.— Vol.32(1) — P. 41-44.
83. Powell B.R., Kennaway N.G., Rhead W.J., Reece C.J., Burlingame T.G., Buist N.R. Juvenile multiple sclerosis-like episodes associated with a defect of mitochondrial beta oxidation // Neurology.— 1990.— Vol. 40 (3 Pt 1).— P.487-491.
84. Pozuelo-Moyano B., Benito-León J., Mitchell A.J., Hernández-Gallego J. A Systematic Review of Randomized, Double-Blind, Placebo-Controlled Trials Examining the Clinical Efficacy of Vitamin D in Multiple Sclerosis // Neuroepidemiology.— 2012.— Vol. 40(3).— P.147-153.
85. Ratchford J.N., Costello K., Reich D.S., Calabresi P.A. Varicella-zoster virus encephalitis and vasculopathy in a patient treated with fingolimod // Neurology.— 2012.— Vol. 79(19).— P.2002-2004.
86. Remolina López A.J., Uribe Rueda C., Patrucco L., Rojas J.I., Cristiano E. Selective IgA deficiency and multiple sclerosis // Neurologia.— 2011.— Vol. 26(6).— P.375-377.
87. Rizzo R., Gentili V., Casetta I., Caselli E., De Gennaro R., Granieri E., Cassai E., Di Luca D., Rotola A. Altered natural killer cells’ response to herpes virus infection in multiple sclerosis involves KIR2DL2 expression // J Neuroimmunol.— 2012.— Vol. 251(1-2).— P.55-64.
88. Royal W. 3rd, Mia Y., Li H., Naunton K. Peripheral blood regulatory T cell measurements correlate with serum vitamin D levels in patients with multiple sclerosis // J. Neuroimmunol.— 2009.— Vol. 13(1-2).— P.135-141.
89. Schweikert A., Kremer M., Ringel F., Liebig T., Duyster J., Stüve O., Hemmer B., Berthele A. Primary central nervous system lymphoma in a patient treated with natalizumab // Ann. Neurol.— 2009.— Vol. 66(3).— P.403-406.
90. Shenoy E.S., Mylonakis E., Hurtado R.M., Venna N. Natalizumab and HSV meningitis // J. Neurovirol.— 2011.— Vol. 17(3).— P.288-290.
91. Singhal R.L., Corman L.C. Subacute herpes simplex virus type 1 encephalitis as an initial presentation of chronic lymphocytic leukemia and multiple sclerosis: a case report // J. Med. Case Rep.— 2011.— Vol. 5.— P.59.
92. Stöckler S., Millner M., Molzer B., Ebner F., Körner E., Moser H.W. Multiple sclerosis-like syndrome in a woman heterozygous for adrenoleukodystrophy // Eur. Neurol.— 1993.— Vol. 33(5).— P.390-392.
93. Stys P.K. Multiple sclerosis: autoimmune disease or autoimmune reaction? // Can. J. Neurol. Sci.— 2010.— Vol. 37 (2).— S16-23.
94. Suzuki N., Mizuno H., Nakashima I., Itoyama Y. Herpes labialis in multiple sclerosis with a trigeminal lesion // Intern. Med.— 2011.— Vol. 50(3).— P.259.
95. Tait A.R., Straus S.K. Phosphorylation of U24 from Human Herpes Virus type 6 (HHV-6) and its potential role in mimicking myelin basic protein (MBP) in multiple sclerosis // FEBS Lett.— 2008.— Vol. 582(18).— P.2685-2688.
96. Tejada-Simon M.V., Zang Y.C., Hong J., Rivera V.M., Zhang J.Z. Cross-reactivity with myelin basic protein and human herpesvirus-6 in multiple sclerosis // Ann. Neurol.— 2003.— Vol. 53(2).— P. 189-197.
97. Thong B.Y., Venketasubramanian N. A case of Sjögren’s syndrome or multiple sclerosis? A diagnostic and therapeutic dilemma // Rheumatol. Int.— 2002.— Vol. 22(6).— P.256-258.
98. Trouillas P., Berthoux F., Betuel H., Boisson D., Aimard G., Devic M. Hypocomplementaemic multiple sclerosis: heterozygous C2 deficiency linked to HLA A10, B18 // Lancet.— 1976.— Vol. 2(7993).— P.1023.
99. Van Thiel D.H., Smith W.I. Jr., Rabin B.S., Fisher S.E., Lester R. A syndrome of immunoglobulin A deficiency, diabetes mellitus, malabsorption, a common HLA haplotype.Immunologic and genetic studies of forty-three family members // Ann. Intern. Med.— 1977.— Vol. 86(1).— P.10-19.
100. Vandenbroeck K., Alloza I., Swaminathan B., Antigüedad A., Otaegui D., Olascoaga J., Barcina M.G., de las Heras V., Bartolomé M., Fernández-Arquero M., Arroyo R., Alvarez-Lafuente R., Cénit M.C., Urcelay E. Validation of IRF5 as multiple sclerosis risk gene: putative role in interferon beta therapy and human herpes virus-6 infection // Genes Immun.— 2011.— Vol. 12(1).— P.40-45.
101. Veldhuis W.B., Floris S., van der Meide P.H., Vos I.M., de Vries H.E., Dijkstra C.D., Bär P.R., Nicolay K. Interferon-beta prevents cytokine-induced neutrophil infiltration and attenuates blood-brain barrier disruption // J. Cereb. Blood Flow Metab.— 2003.— Vol. 23(9).— P.1060-1069.
102. Verny C., Loiseau D., Scherer C., Lejeune P., Chevrollier A., Gueguen N., Guillet V., Dubas F., Reynier P., Amati-Bonneau P., Bonneau D. Multiple sclerosis-like disorder in OPA1-related autosomal dominant optic atrophy // Neurology. — 2008. — Vol. 70(13 Pt 2).— P.1152-1153.
103. Vidal R., Uriz S., Ledesma L., Quintana M., Martínez A., López R., Sáenz A., Curià X. Parainfectious transverse myelitis in an adolescent. Difficulties in the etiological diagnosis // Rev Neurol.— 1996. — Vol. 24(127).— P.296-299.
104. Visser F., Wattjes M.P., Pouwels P.J., Linssen W.H., van Oosten B.W. Tumefactive multiple sclerosis lesions under fingolimod treatment // Neurology.— 2012.— Vol. 79(19).— P.2000-2003.
105. Waisburg H., Meloff K.L., Buncic R. Polyarteritis nodosa complicated by a multiple sclerosis like syndrome // Can. J. Neurol. Sci.— 1974.— Vol. 1(4).— P.250-252.
106. Wandinger K.P., Wessel K., Neustock P., Siekhaus A., Kirchner H. Diminished production of type-I interferons and interleukin-2 in patients with multiple sclerosis // J. Neurol. Sci.— 1997.— Vol. 149(1).— P.87-93.
107. Wellek A., Korsukewitz C., Bach J.P., Schock S., Eienbröker C., Seitz F., Spengler A., Hemmer B., Schlegel K., Oertel W.H., Sommer N., Tackenberg B. Sibling distability risk at onset and during disease progression in familial multiple sclerosis // Mult. Scler.— 2011.— Vol. 17(9).— P.1060-1066.
108. White W.B., Hanna M., Stewart J.A. Systemic herpes simplex virus type 2 infection. Proctitis, urinary retention, arthralgias, and meningitis in the absence of primary mucocutaneous lesions // Arch. Intern. Med.— 1984.— Vol. 144(4).— P.826-827.
109. Woessner R., Grauer M.T., Frese A., Bethke F., Ginger T., Hans A., Treib J. Long-term antibiotic treatment with roxithromycin in patients with multiple sclerosis // Infection.— 2006.— Vol. 34(6).— P.342-344.
110. Yao K., Gagnon S., Akhyani N., Williams E., Fotheringham J., Frohman E., Stuve O., Monson N., Racke M.K., Jacobson S. Reactivation of human herpesvirus-6 in natalizumab treated multiple sclerosis patients // PLoS One.— 2008.— Vol. 3(4).— P.e2028.
111. Ziegler H.W., Kay N.E., Zarling J.M. Deficiency of natural killer cell ativity in patients with chronic lymphocytic leukemia // Int. J. Cancer. – 1981. – Vol. 27(3). – Р. 321–327.
112. Zivadinov R., Nasuelli D., Tommasi M.A., Serafin M., Bratina A., Ukmar M., Pirko I., Johnson A.J., Furlan C., Pozzi-Mucelli R.S., Monti-Bragadin L., Grop A., Zambon M., Antonello R.M., Cazzato G., Zorzon M. Positivity of cytomegalovirus antibodies predicts a better clinical and radiological outcome in multiple sclerosis patients // Neurol. Res.— 2006.— Vol. 28(3).— P.262-269.
Впервые опубликовано в журнале «Лікарська справа» № 5–6, 2014.
Повторная публикация согласована с редакцией журнала