17 липня, 2015
Применение антипсихотических препаратов у детей: принципы выбора и клинические рекомендации

В последнее время отмечается значительное увеличение количества применяемых психотропных лекарственных средств во всех возрастных группах, в том числе в детской и подростковой популяции. По данным реестра Национальной амбулаторной медицинской помощи США, в период с 1993 по 2009 г. количество применяемых антипсихотиков на 100 человек увеличилось с 0,24 до 1,83 у детей, с 0,78 до 3,76 у подростков и с 3,25 до 6,18 у взрослых. Из приведенных данных следует, что частота назначения психотропных препаратов детям выросла более чем в 7 раз, тогда как у подростков – в 4 раза, а у взрослых – всего в 2 раза.
С изменением понимания природы ряда расстройств меняются и подходы к их медикаментозному лечению. В период с 2005 по 2009 г. поведенческие расстройства стали наиболее распространенными диагнозами у детей и подростков, при которых назначались антипсихотические средства: 63,0 и 33,7% соответственно, в то время как у взрослых препараты данной группы чаще всего применялись при депрессиях (21,2%) и биполярных расстройствах (20,2%). Антипсихотические препараты в психиатрической практике чаще назначаются детям (67,7%) и подросткам (71,6%), чем взрослым (50,3%) [1].
Данные исследований свидетельствуют, что подобная тенденция отмечается и в большинстве европейских стран. Так, рост количества назначений антипсихотических препаратов лицам моложе 19 лет в Нидерландах составил 0,3% в 1997 г. и 0,7% в 2005 г. [2]. В Великобритании частота назначений увеличилась в 2 раза (0,04% в 1992 г. и 0,08% в 2005 г.) [3].
Чаще всего в детской психиатрической практике используются атипичные нейролептики. Перечень зарегистрированных показаний для назначения антипсихотиков ограничен шизофренией, бредовыми и биполярными расстройствами у подростков, агрессивными, в том числе аутоагрессивными, импульсивными поведенческими реакциями в контексте психического расстройства и/или расстройства спектра аутизма у детей [4].
В результате проведенных статистических исследований в Германии было установлено, что наиболее часто назначаемым антипсихотическим препаратом является рисперидон. В таблице 1 представлено соотношение частоты назначения рисперидона детям и подросткам с разными психиатрическими диагнозами за 2011 г. Диагнозы, приведенные в таблице 1, могут являться как основными, так и сопутствующими заболеваниями. У одного пациента может отмечаться наличие более одного диагноза, поэтому представленные данные не отображают реальную структуру показаний для применения рисперидона в детской психиатрической практике [5].
Данные метааналитических исследований не свидетельствуют об увеличении количества психических расстройств за последнее десятилетие. Также не было внесено существенных изменений в рекомендации по применению нейролептиков у детей и подростков.
Полученные в ходе исследований данные можно объяснить рядом причин. Увеличение количества назначений может быть обусловлено недостаточной информированностью врачей о клиническом течении психических расстройств. Усиление интенсивности маркетинговой деятельности фармацевтических компаний может влиять на то, что лечащий врач сделает выбор в пользу атипичных антипсихотических препаратов ввиду их более благоприятного профиля «риск-польза». Часто решение о назначении антипсихотиков обусловлено тем, что медикаментозное лечение может быть начато быстрее, чем психотерапия, и требует меньше затрат времени и средств, что, возможно, связано с отсутствием должной мотивации у пациента и его семьи [6].
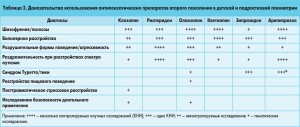
В таблице 2 представлены доказательства эффективности антипсихотических препаратов при раздражительности и агрессивности у больных с аутизмом, поведенческих расстройствах или для лечения тиков и синдрома Туретта. Но при сравнении показателя NNT (number needed to treat – количество больных, которым необходимо назначить препарат, чтобы получить один положительный результат терапии) наблюдается более высокая эффективность лекарственных средств данной группы в лечении агрессии при аутизме, чем при состояниях мании или шизофрении. Это позволяет говорить о более широком назначении атипичных нейролептиков именно пациентам с расстройствами спектра аутизма в качестве средств медикаментозной коррекции нежелательного поведения [7].
Часто в погоне за достижением положительного клинического эффекта специалисты забывают сообщать родственникам пациентов о возможных побочных эффектах или делают это осознанно, во избежание постановки под сомнение эффективности назначаемых препаратов или с целью экономии времени для разъяснения всех «за» и «против» медикаментозной терапии.
Эффективность антипсихотических препаратов несколько ниже при лечении негативных и когнитивных симптомов, чем при терапии позитивных симптомов. Следует отметить, что блокада D2-рецепторов может сопровождаться ухудшением негативных симптомов. Применение чрезмерных доз атипичных нейролептиков может приводить к возникновению вторичной дефицитарной симптоматики. При наличии негативных симптомов важно установить, не являются ли они следствием медикаментозного лечения, для принятия решения о продолжении терапии.
Пока не ясно, можно ли с помощью атипичных нейролептиков уменьшить дефицит познавательных функций у пациентов с шизофренией. Известно, что блокада D2-рецепторов ослабляет познавательные функции, поэтому ряд дефицитов, обнаруженных у некоторых больных, могут быть связаны с чрезмерно высокой дозой применяемых антипсихотических препаратов. Ввиду того, что как негативные, так и когнитивные симптомы являются одними из основных предикторов функционального исхода при шизофрении, для осуществления оценки значимым является влияние препарата на выраженность клинических проявлений этих симптомов или, наоборот, способность препарата приводить к их частичной редукции.
Учитывая данные о влиянии лекарственных средств на головной мозг, можно выделить основные шаги при назначении антипсихотических препаратов детям и подросткам.
Ниже приведены рекомендации Международной ассоциации детской и подростковой психиатрии и смежных специальностей (IACAPAP) по назначению терапии в детском или подростковом возрасте. Большинство руководящих принципов опираются на здравый смысл и отражают основные этапы правильного выбора антипсихотиков. Основные шаги включают: точный диагностический процесс, получение информированного согласия ребенка и родителей, определение критериев для оценки позитивной терапевтической динамики, мониторинг состояния пациентов по мере необходимости, использование минимально эффективной дозы лекарственного средства, регулярность переоценки необходимости продолжения приема препарата и, наконец, рассмотрение вопроса о необходимости использования другого подхода к терапии [8].
Ключевые шаги при применении психофармакотерапии у детей и подростков
Проведите комплексную диагностическую оценку, документально подтверждающую наличие симптомов, при которых назначается указанный препарат.
Проинформируйте родителей и ребенка (в пределах, доступных по уровню развития и когнитивных функций) о потенциальных выгодах и рисках, связанных с лечением, по сравнению с альтернативными вариантами.
Если лекарственные средства не имеют нормативно утвержденных показаний к применению у детей, проинформируйте родителей и ребенка о том, что препарат используется не по прямому назначению.
Определяйте и отслеживайте изменения базовых симптомов и функций, на которые ожидается воздействие препарата.
Учитывая назначение препарата, получите исходный клинический уровень или уровень лабораторных параметров (например, вес, рост, уровень артериального давления, частота пульса, уровень холестерина, функция почек).
Начинайте медикаментозную терапию в дозах нижней границы эффективного диапазона доз с целью определения минимальной возможной дозы, на фоне применения которой достигается желаемый результат.
Осуществляйте мониторинг эффективности, побочных реакций и, при необходимости, уровня препарата в плазме крови (например, при терапии литием) в течение первых нескольких недель лечения, выполняйте коррекцию дозы в зависимости от обстоятельств.
Если наблюдается улучшение, оптимизируйте дозу для достижения максимального воздействия на симптомы и улучшения функционирования.
Установите поддерживающую дозу и, в зависимости от состояния и лекарства, спрогнозируйте предварительную продолжительность лечения.
Периодически рассматривайте вопрос о необходимости непрерывного лечения или прекращения терапии.
В случае прекращения лечения изучите необходимость постепенного уменьшения дозы, что рекомендуется для большинства лекарственных средств после длительного приема (например, антидепрессантов, лития, антипсихотических препаратов), хотя возможно и резкое прекращение, что может быть целесообразно для некоторых препаратов (например, метилфенидат).
В большинстве случаев до момента начала терапии перед врачом стоит задача постановки соответствующего диагноза. Ряд заболеваний характеризуются появлением психотических симптомов, что имеет большое значение для точности диагноза. Не все дети и подростки, демонстрирующие психотические симптомы, имеют психическую патологию. Например, при анти-NMDA-рецепторном энцефалите возможно течение, схожее по клинической картине с шизофренией, но подходы к лечению должны быть абсолютно разными.
Какие же требования предъявляются к «идеальному» антипсихотику? Он должен хорошо переноситься пациентами, легко поддаваться титрованию доз, быть удобным для применения, положительно влиять на когнитивное функционирование, улучшать ежедневное функционирование, не иметь побочных эффектов, в том числе не вызывать развития экстрапирамидной симптоматики.
Базовым критерием выбора антипсихотического препарата является спектр побочных эффектов с учетом общего медицинского состояния пациента. На основании этого в качестве первой группы выбора рекомендованы арипипразол, рисперидон или зипразидон [9].
Наиболее распространенными побочными эффектами при использовании антипсихотиков являются экстрапирамидные симптомы (паркинсонизм, острая дистония и акатизия, поздняя дискинезия), нейроэндокринные нарушения (гиперпролактинемия, увеличение массы тела), седация, ортостатическая гипотония, изменения частоты сердечных сокращений и сердечного ритма, антихолинергические эффекты (например, запоры, нечеткость зрения, сухость во рту, задержка мочи). Антипсихотические лекарственные средства могут вызвать снижение когнитивных функций.
Экстрапирамидные побочные эффекты чаще возникают у детей и подростков, чем у взрослых. В ряде исследований было доказано, что режим медленного титрования и использование более низких доз антипсихотических препаратов в детской и подростковой психиатрической практике значительно снижают риск развития экстрапирамидных побочных эффектов.
Из-за высокого риска возникновения метаболических побочных эффектов оланзапин не рекомендован в качестве препарата первого выбора. Результаты, полученные в ряде исследований, свидетельствуют о том, что кветиапин имеет схожий с оланзапином профиль метаболических побочных эффектов.
Рисперидон вызывает повышение уровня пролактина, но при длительном приеме препарата наблюдается постепенное снижение и выравнивание уровня указанного гормона. На основании полученных данных рисперидон нельзя оценить как менее эффективный препарат в сравнении с арипипразолом или зипразидоном в отношении переносимости и безопасности.
Отсутствие удовлетворительного результата лечения при назначении полной терапевтической дозы препарата курсом 4-6 недель свидетельствует о необходимости смены лекарственного средства. В случае хорошей переносимости пациентом арипипразола, рисперидона или зипразидона во время лечения с учетом адекватной терапевтической дозы препарата, но без достижения желаемого положительного результата следует рассмотреть вопрос о возможности дальнейшей терапии оланзапином, ввиду того что остальные препараты группы первичного выбора имеют сравнительно одинаковый профиль эффективности. В сравнительных исследованиях оланзапин демонстрирует более выраженный терапевтический эффект. Для достижения максимальной клинической эффективности терапевтическая доза оланзапина должна составлять >30 мг/сут. При недостаточном терапевтическом результате применения оланзапина в адекватных терапевтических дозах в качестве альтернативы можно рассмотреть клозапин. В пользу данной стратегии свидетельствует ряд клинических исследований [11].
С другой стороны, если арипипразол, рисперидон или зипразидон не могут быть назначены в адекватных дозах из-за плохой переносимости, следует подобрать другой препарат. В случае плохой переносимости атипичных нейролептиков допускается назначение галоперидола или перфеназина, или кветиапина, которые могут приводить к развитию более значимых побочных эффектов (нарушения движений, ухудшение познавательной деятельности, прирост массы тела), ввиду того что эти проблемы вызывают меньше опасений, чем возникновение метаболических нарушений на фоне применения оланзапина. При непереносимости последних следует назначить оланзапин.
У больных шизофренией при резистентности положительных симптомов после двух адекватных попыток монотерапии препаратом выбора является клозапин.
Однако прежде чем рассматривать вопрос об эффективности и безопасности применения антипсихотических препаратов у лиц молодого возраста, необходимо обратить внимание на один факт. В ходе сравнительных исследований эффективности между антипсихотиками главным предиктором, определяющим результат, чаще всего является спонсор исследований. Во многих странах именно спонсор исследований определяет более эффективный препарат при лечении ряда патологий [8]. По этой причине следует критично относиться к оценкам результатов опубликованных исследований и здраво оценивать приведенные доказательства.
Типичные нейролептики являются эффективными для управления симптомами психотических расстройств, тем не менее их применение ассоциируется с высоким риском развития побочных эффектов, таких как экстрапирамидная симптоматика и седация. Единственным антипсихотическим препаратом, который оказался эффективнее, чем оланзапин и галоперидол, для управления позитивными и негативными симптомами в клинических исследованиях, является клозапин, в связи с чем он рассматривается в качестве препарата выбора для медикаментозной терапии у детей и подростков с резистентными формами шизофрении [9].
В случае развития такого побочного эффекта, как повышение уровня пролактина при долгосрочной терапии, отмечается значительное увеличение уровня последнего на фоне приема рисперидона, палиперидона или галоперидола. Арипипразол является частичным антагонистом D2-рецепторов, вследствие чего уровень пролактина во время терапии не повышается, а у некоторых пациентов – снижается в сравнении с исходным показателем при длительной терапии.
Стратегии управления неблагоприятными метаболическими эффектами у пациентов, принимающих антипсихотические препараты, могут быть разделены на группы в соответствии с направлениями профилактических мероприятий.
Первичные профилактические меры целесообразны перед началом лечения. Они могут включать консультацию относительно преимуществ здорового образа жизни, выбор нейролептика с низким уровнем риска развития побочных метаболических эффектов в качестве начальной терапии.
Вторичные профилактические меры необходимы в случае возникновения негативных метаболических эффектов. Они могут состоять из консультирования и вмешательств, направленных на мотивирование пациента к ведению здорового образа жизни, перехода к применению антипсихотических препаратов, имеющих низкий риск развития метаболических нарушений, и назначения терапии лекарственными средствами, способствующими снижению массы тела.
Третичные профилактические меры представлены консультациями и вмешательствами, направленными на мотивирование пациента к ведению здорового образа жизни, переходом на нейролептик с низким риском возникновения побочных эффектов, усилением терапии препаратами, влияющими на массу тела. Кроме того, при достижении любых аномальных значений во время лечения пациента следует направить к соответствующему специалисту (кардиологу, эндокринологу) [10].
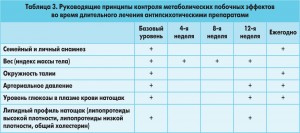
В таблице 3 приведен основной перечень клинических и лабораторных исследований, периодичность консультаций с целью контроля над метаболическими побочными эффектами при длительной терапии антипсихотическими препаратами [7].
В ряде случаев врачи забывают уделять достаточное внимание контролю и профилактике побочных эффектов, связанных с применением антипсихотических препаратов. Очень часто специалисты в Украине назначают антипсихотические препараты в необоснованно высоких дозах или в дозах, которые значительно меньше минимальной терапевтической дозы, не проводя титрования на начальных этапах и не предусматривая кратность приема медикаментов. Подобные действия влекут за собой снижение эффективности терапии, увеличение риска проявлений негативных побочных эффектов, снижение комплайенса среди пациентов и их родственников. В отдельных случаях при развитии минимальных побочных эффектов специалисты прекращают терапию и вместо подбора другого препарата отказываются от лечения, а часто – и от пациента. Многие врачи слепо следуют рекомендациям клинических руководств и не осмеливаются использовать свой клинический опыт применения препаратов. Также часто назначаются препараты, не одобренные для применения у детей, и препараты, эффективность которых не соответствует критериям доказательной медицины. Подобные действия могут навредить или усугубить течение заболевания.
Решение о приеме антипсихотических препаратов должны принимать совместно врач и пациент/его опекуны. Врач обязан предоставлять максимум информации об эффективности препаратов, о возможных побочных реакциях и приводить примеры из своего клинического опыта. И ни в коем случае специалист не должен принимать решение вместо пациента или навязывать ему свое мнение.
Существующие руководства и протоколы по лечению ряда заболеваний созданы с целью помочь врачу в выборе правильных тактик и стратегий терапии, а не для ограничения его действий или запрета других терапевтических подходов, основанных на собственном клиническом опыте специалиста.
Нет плохих или хороших лекарств. Важно помнить и понимать, что в первую очередь применение лекарственных препаратов необходимо для улучшения качества жизни пациентов, а не для лечения симптомов болезни.
Литература
1. Olfson M., Blanco C., Liu S.M. et al. National trends in the office-based treatment of children, adolescents, and adults with antipsychotics // Arch Gen Psychiatry. – 2012 (Dec). – Vol. 69 (12). – P. 1247-56.
2. Kalverdijk L.J., Tobi H., van den Berg P.B. et al. Use of antipsychotic drugs among Dutch youths between 1997 and 2005 // Psychiatr Serv. – 2008 (May). – Vol. 59 (5). – P. 554-60.
3. Rani F., Murray M.L., Byrne P.J. et al. Epidemiologic features of antipsychotic prescribing to children and adolescents in primary care in the United Kingdom // Pediatrics. – 2008 (May). – Vol. 121 (5). – P. 1002-9.
4. Gerd Lehmkuhl, Ingrid Schubert. Psychotropic Medication in Children and Adolescents // Dtsch Arztebl Int. – 2014 (Jan) – Vol. 111 (3). – P. 23-24.
5. Bachmann C.J., Lempp T., Glaeske G. et al. Antipsychotic Prescription in Children and Adolescents (An Analysis of Data From a German Statutory Health Insurance Company From 2005 to 2012) // Dtsch Arztebl Int. 2014 (Jan). – Vol. 111(3). – P. 25-34.
6. Olfson M., Marcus S.C., Weissman M.M., Jensen P.S. National trends in the use of psychotropic medications by children // J Am Acad Child Adolesc Psychiatry. – 2002. – Vol. 41. – P. 514-521.
7. American Academy of Child and Adolescent Psychiatry. Practice parameter on the use of psychotropic medications in children and adolescents // J Am Acad Child Adolesc Psychiatry. – 2009. – Vol. 48. – P. 961-973.
8. http://iacapap.org/iacapap-textbook-of-child-and-adolescent-mental-health
9. Lieberman J. et al. Effectiveness of antipsychotic drugs in patients with chronic schizophrenia. NEJM. – 2005. – Vol. 353 (12). – P. 1209-1223.
10. McEvoy J.P., Meyer J.M., Goff D.C. et al. Prevalence of the metabolic syndrome in patients with schizophrenia: baseline results from the Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE) schizophrenia trial and comparison with national estimates from NHANES III. Schizophr Res. – 2005 .– Vol. 80. – P. 19-32.
11. Potkin S.G. et al. Aripiprazole, an antipsychotic with a novel mechanism of action, and risperidone vs. placebo in patients with schizophrenia and schizoaffective disorder // Archives of General Psychiatry. – 2003. – Vol. 60. – P. 681-690.