10 липня, 2020
Неврологічні ускладнення коронавірусної інфекції
У людства є лише три великі вороги: лихоманка, голод і війна; з них на сьогодні найбільша і, безумовно, найстрашніша – це лихоманка.
Вільям Ослер
 Поширення небезпечних вірусів – чи не найпопулярніший сюжет апокаліптичних фільмів. Та всі ці сюжети людство пережило і в реальності – пошесті, що навіть крізь століття змушують людину завмирати й замислюватись. Історія пам’ятає багато страшних та спустошувальних епідемій.
Поширення небезпечних вірусів – чи не найпопулярніший сюжет апокаліптичних фільмів. Та всі ці сюжети людство пережило і в реальності – пошесті, що навіть крізь століття змушують людину завмирати й замислюватись. Історія пам’ятає багато страшних та спустошувальних епідемій.
У 1976 р. вперше зафіксували спалах геморагічної лихоманки Ебола. Відтоді небезпечною хворобою заразилися понад 30 тис. осіб, більш ніж 11 тис. – померли. У 2014‑2016 рр. зафіксовано найтяжчу за весь період спостережень за цим захворюванням епідемію у Західній Африці, яка поширилася за межі цього регіону до США, Іспанії, Великої Британії. Спалахи недуги продовжуються й дотепер. Так, лише минулого літа від Еболи у Демократичній Республіці Конго загинуло понад 2 тис. осіб [20].
У 1947 р. вперше зафіксували спалах лихоманки Зіка в Африці. У 2015 р. її експлозивне поширення відбулося на частину Америки. Хвороба привернула до себе пильну увагу через імовірність уражень нервової системи у вигляді синдрому Гійєна – Барре, високої тератогенної дії вірусу, яку підозрюють у зв’язку зі збільшенням кількості новонароджених із вродженою вадою – мікроцефалією [20].
Лихоманку Денге було вперше розпізнано у 1950-х рр. під час епідемій у Філіппінах і Таїланді. На даний час тяжка Денге вражає більшість азіатських і латиноамериканських країн та є однією із провідних причин госпіталізації та смертності серед дітей у цих регіонах. Кількість зареєстрованих випадків захворювання зросла з 2,2 млн 2010 р. до 3,34 млн 2016 р. [20].
Лихоманка Чікунгунья у ХХ ст. була відома переважно як ендемічне для Африки захворювання. Однак на початку 2000-х рр. відбулося істотне розширення ареалу розповсюдження хвороби. З 2001 по 2007 рр. було зареєстровано понад 30 епідемічних спалахів із загальною кількістю до 7 млн хворих з охопленням понад 15 держав регіону, а в окремих населених пунктах вона досягала 63% [4].
Пандемія свинячого грипу, викликаного вірусом штаму H1N1, спалахнула 2009 р. На відміну від інших пандемій до того, свинячий грип протистояв усій могутній сучасній системі охорони здоров’я, проте зміг відзначитися високою смертоносністю. За офіційною інформацією, представленою ВООЗ, загальна частка лабораторно підтверджених летальних випадків пандемічного грипу по всьому світу становила понад 17,4 тис. [20].
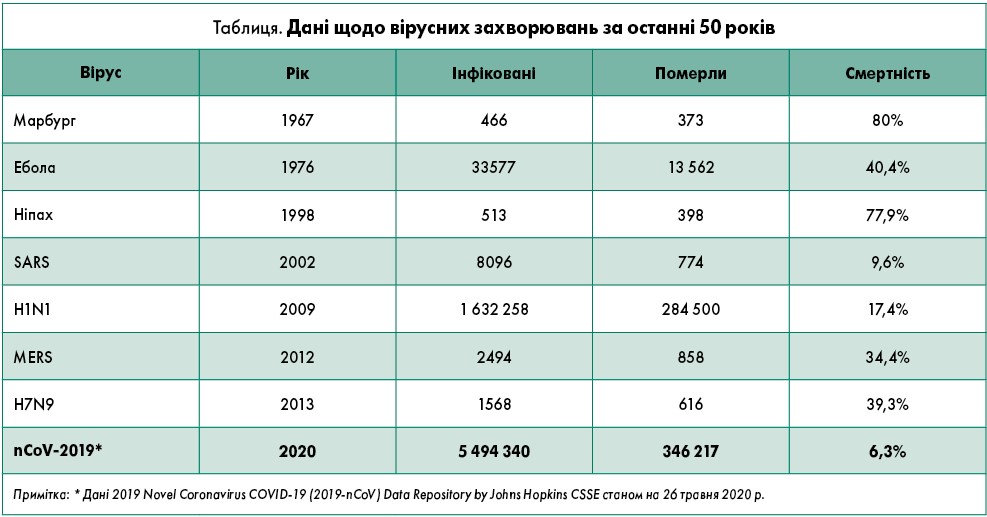
Найбільші за останні 50 років епідемії захворювань – це ті, якими людина заразилася від тварин (таблиця), із виключенням вірусів, що переносяться комарами (лихоманка Зіка, малярія, лихоманка Денге).
 Експерти вважають, що людство живе в епоху епідемій, і нові хвороби з’являтимуться у міру зростання населення планети. Весь початок 2020 р. світ намагається впоратись із новим випробуванням – коронавірусною інфекцією, розповсюдження якої почалося з китайського міста Ухань наприкінці 2019 р. Немає сумнівів, що вірус SARS-CoV2 викликає страх і паніку серед людства – працівників охорони здоров’я, пацієнтів, політиків, на фінансових ринках тощо. При цьому страх вражає розум непідготовлених [17].
Експерти вважають, що людство живе в епоху епідемій, і нові хвороби з’являтимуться у міру зростання населення планети. Весь початок 2020 р. світ намагається впоратись із новим випробуванням – коронавірусною інфекцією, розповсюдження якої почалося з китайського міста Ухань наприкінці 2019 р. Немає сумнівів, що вірус SARS-CoV2 викликає страх і паніку серед людства – працівників охорони здоров’я, пацієнтів, політиків, на фінансових ринках тощо. При цьому страх вражає розум непідготовлених [17].
SARS-CoV2 поширюється дуже стрімко. До березня 2020 р. понад сто країн світу повідомили про випадки інфікування та смерті у всіх вікових категоріях. Наступні прогнози невтішні. Всю систему охорони здоров’я може бути перевантажено і зруйновано [16, 17].
Основні клінічні прояви інфекції SARS-CoV2 пов’язані з легеневими ускладненнями. У більшості пацієнтів наявні легкі симптоми – лихоманка, головний біль, кашель, задишка, біль у м’язах і аносмія, проте у деяких розвивається гострий респіраторний дистрес-синдром приблизно через тиждень після початку захворювання, який може спричинити смерть [28]. Рабдоміоліз буває пізнім ускладненням інфекції [11]. Рівень летальності становить близько 3‑4%. У підсумку пацієнти впадають в кому, що, як вважають, асоційована з гіпоксією та поліорганною недостатністю. Однак лишається багато запитань без відповідей.
Чи може головний біль бути ознакою вірусного менінгіту? З’являються повідомлення про можливий зв’язок між COVID‑19 і пошкодженням центральної нервової системи (ЦНС). Зокрема відомо, що в Китаї у 56-річного чоловіка, в якого виявили COVID‑19, згодом був встановлений вірус у спинномозковій рідині. Пацієнт одужав та був виписаний із лікарні. Існує невелика кількість повідомлень про залучення ЦНС при коронавірусній інфекції. Можливо, ураження ЦНС – рідкісне ускладнення інфекції. Невідомо про наступний розвиток інфекції, але ймовірність захворіти на енцефаліт від COVID‑19 незначна.
Одним із характерних симптомів захворювання є аносмія, яка, очевидно, пов’язана із залученням у патологічний процес нюхових цибулин. При вивченні коронавірусного енцефаліту на моделях мишей встановлено, що вірус може проникати у мозок транснейронально через нюхові шляхи [5]. Відповідно, аносмія як відносно нешкідливий симптом, імовірно, вказує на потенційно серйозніше ускладнення. Візуалізація мозку необхідна, щоб зрозуміти повноцінну дію вірусу.
Артеріальна гіпертензія і цукровий діабет визначають як найпоширеніші супутні захворювання в осіб із тяжкими проявами інфекції. Цікавою є гіпотеза, що виникла навколо використання інгібіторів ангіотензинперетворювального ферменту (іАПФ) у лікуванні артеріальної гіпертензії і цукрового діабету для пояснення вищої схильності пацієнтів до інфікування і тяжчого перебігу захворювання. ACE2 є рецептором SARS-CoV2 [25]. Застосування інгібіторів ACE призводить до підвищення експресії ACE2, що робить клітини уразливішими для вірусу. Ведуться клінічні дослідження для перевірки цієї гіпотези. Є вірогідність виявлення ACE2 в ендотеліальних клітинах головного мозку та його індукування у нейронах. Це підвищує імовірність того, що інсульти, пов’язані з SARS-CoV2, безпосередньо пов’язані з інфекцією, а енцефаліт є потенційним ускладненням [17].
Відомі кілька штамів коронавірусу людини. Більшість викликають легкі респіраторні симптоми. Проте за останні роки виявлено, що нові штами спричиняють захворювання з руйнівними наслідками для організму. Зокрема, кілька гострих неврологічних синдромів пов’язані з коронавірусом.
Гострі неврологічні ускладнення коронавірусної інфекції
- Вірусний менінгіт
- Аносмія
- Енцефаліт
- Постінфекційний гострий дисемінований енцефаломієліт
- Постінфекційний енцефаліт стовбура мозку
- Синдром Гійєна – Барре
- Міозит
SARS-CoV1 був виявлений у спинномозковій рідині пацієнта з енцефалітом і гострим респіраторним дистрес-синдромом [10]. MERS-CoV може викликати тяжкий гострий дисемінований енцефаломієліт і васкулопатії [1]. Також описані випадки постінфекційного енцефаліту стовбура мозку і синдрому Гійєна – Барре [12]. HCoV-OC43 зумовлює розвиток гострого енцефаломієліту з дисемінованими вогнищами по всьому мозку, мозочку і спинному мозку [23].
Особливо уразливими є люди з ослабленим імунітетом. Фатальний енцефаліт може виникати у пацієнтів з ослабленим імунітетом та спричинятися HCoV-OV43. У цих хворих на секції виявляли інфекційне нейрональне ураження [15]. Подібну проблему було встановлено для SARS-CoV2.
Більшість осіб з автоімунними синдромами (розсіяний склероз, міастенія, зоровий нейромієліт чи саркоїдоз) отримують широкий спектр імуносупресивних засобів. Таким пацієнтам доцільно вживати додаткові запобіжні заходи, щоб запобігти впливу вірусу, і переглянути дозування ліків. Проте відміна призначеного лікування може бути недоцільною, оскільки основне захворювання, без сумніву, викличе загострення [17].
Особи похилого віку і пацієнти з ослабленим імунітетом особливо уразливі. Більшість із них мають основні неврологічні супутні захворювання. Про серопозитивність щодо коронавірусів повідомлялося при різних неврологічних розладах, таких як енцефаліт, неврит зорового нерва, розсіяний склероз і хвороба Паркінсона [3, 6, 14, 18]. Вірус також був виділений зі спинномозкової рідини та головного мозку пацієнтів із розсіяним склерозом [1]. Це стосується HCoV‑229E, HCoV‑293 і HCoV-OC43. Проте важливість цих результатів незрозуміла, адже віруси дуже поширені, а їхнє причинне значення при даних захворюваннях не встановлене.
Нещодавно були опубліковані дані двох пацієнтів, інфікованих SARS-CoV2, із розвитком незвичайних неврологічних проявів у вигляді синдрому Міллера – Фішера та краніального поліневриту. Дані отримані з університетських лікарень Мадриду (Іспанія).
Перший хворий – 50-річний чоловік, мав аносмію, агевзію, правий між’ядерний офтальмопарез, правий фасцикулярний і окоруховий параліч, атаксію, арефлексію, альбуміно-цитологічну дисоціацію та позитивне тестування на антитіла до GD1b-IgG. За п’ять днів до того у пацієнта з’явилися кашель, головний біль, нездужання, біль у попереку та лихоманка.
Другий пацієнт – 39-річний чоловік, мав агевзію, двобічний окоруховий параліч, арефлексію та альбуміно-цитологічну дисоціацію. За три дні до того у нього розвинулася діарея, з’явилася субфебрильна температура та погіршився загальний стан. Аналіз полімеразно-ланцюгової реакції був позитивним в обох випадках. Першого пацієнта лікували внутрішньовенним введенням імуноглобуліну, другого – ацетамінофеном. Через два тижні в обох хворих спостерігали повне неврологічне одужання, за винятком залишкової аносмії та агевзії у першому випадку [8].
Потенційні нервово-м’язові ускладнення при COVID‑19
1. Ризик зараження інфекцією, що може спричинити нові нервово-м’язові захворювання, як-то:
- синдром Гійєна – Барре
- міозит
- міопатія та/або поліневропатія
2. Ризик загострення відомої інфекції або маскування раніше нерозпізнаного нервово-м’язового захворювання, як-то:
- автоімунні порушення (хронічна запальна демієлінізувальна поліневропатія, мультифокальна набута демієлінізувальна сенсорно-моторна невропатія, багатовогнищева моторна невропатія, міастенія, міастенічний синдром Ламберта – Ітона, міозит)
- дегенеративні розлади (боковий аміотрофічний склероз, спінальна м’язова атрофія, спадкові невропатії, м’язові дистрофії, вроджені, мітохондріальні, метаболічні міопатії тощо)
3. Ризики імунодепресантів / імуномодулювальних методів лікування у пацієнтів з автоімунними нервово-м’язовими захворюваннями:
- підвищений ризик зараження COVID‑19 та тяжчими патологіями
- підвищені ризики й тяжкість інших інфекцій в осіб із COVID‑19 та нервово-м’язовими захворюваннями, які отримували імунотерапію
- імунотерапія може зробити вакцини менш ефективними
4. Ризики лікування COVID‑19:
- гідроксихлорохін та хлорохін можуть викликати токсичну невропатію та міопатію
- противірусні методи лікування: лопінавір/ритонавір, ремдезивір тощо
5. Ризики щеплень: можлива запальна невропатія (синдром Гійєна – Барре, плексит, мононеврит)
Синдром Міллера – Фішера характеризується гострим розвитком зовнішньої офтальмоплегії, атаксії та втрати сухожилкових рефлексів. Йому передують інфекції, подібні до тих, які призводять до виникнення синдрому Гійєна – Барре, що свідчить про пара- або поствірусний процес. Haemophilus influenzae, Campylobacter jejuni та цитомегаловіруси є найпоширенішими збудниками хвороби [13]. Поява синдрому Міллера – Фішера та краніального поліневриту в зазначених пацієнтів із SARS-CoV2 може бути випадковою. Проте не можна виключати, що COVID‑19 відповідає за розвиток цих двох неврологічних станів. Дана гіпотеза підтримується нещодавньою публікацією про випадки можливого зв’язку між синдромом Гійєна – Барре та інфекцією SARS-CoV2 [27].
У другого пацієнта не було класичного синдрому Міллера – Фішера. Однак є неповні форми даного стану, зокрема гостра атаксична невропатія, яку можна діагностувати за відсутності офтальмоплегії, та гострий офтальмопарез, що інколи виникає за відсутності атаксії, як у зазначеному другому випадку [21]. Проте краніальний поліневрит взагалі буває окремим підтипом захворювання – проміжним станом між синдромами Міллера –Фішера та Гійєна – Барре [22].
Патогенез синдрому Міллера – Фішера та краніального поліневриту при COVID19 може включати імунні механізми або пряму вірусну нейропатогенну дію. Головним механізмом є аберантна імунна відповідь.
Під час теперішньої пандемії слід бути пильними щодо нервово-м’язових ускладнень, які можуть прямо або опосередковано бути пов’язані з коронавірусною інфекцією.
Першочергово у свідомості більшості неврологів постає синдром Гійєна – Барре. Відомі ризики розвитку даного стану внаслідок вірусних інфекцій, зокрема грипу, H1N1, Зіка, Еболи. Доведено, що молекулярна мімікрія існує між специфічними вірусними білками та білками периферичних нервів (наприклад, гангліозидами), що спричиняє ушкодження мієліну або аксону периферичних нервів. На даний час зареєстрований один випадок синдрому Гійєна – Барре через COVID‑19, проте прямий причинно-наслідковий зв’язок невідомий [24]. Також немає доказів прямої вірусної інвазії із запаленням та дегенерацією мотонейронів і периферичних нервів, як це спостерігається при деяких вірусних інфекціях, як-то поліовірус, ентеровірус D68, Herpes zoster, цитомегаловірус тощо. У літературі описаний лише один випадок, при якому трирічна дитина з гострим млявим паралічем була інфікована двома коронавірусами (HCoV 229E та OC43) [19].Однак діагноз виявився сумнівним, оскільки дослідження електроміограми, нервової провідності, склад ліквору та дані магнітно-резонансної томографії головного і спинного мозку не відхилялися від норми. Хоча й не слід виключати, що вірус може бути нейтротропним, безпосередньо інфікувати та пошкоджувати мотонейрони й периферичні нерви [7].
Коронавірусні інфекції можуть бути асоційовані з міопатіями. В опублікованих дослідженнях із COVID‑19 у Китаї міалгії та м’язова слабість встановлені у 44‑70% госпіталізованих пацієнтів, при цьому збільшення креатинкінази спостерігали у 33% випадків [9, 23]. На жаль, не повідомляється про результати додаткових досліджень, таких як електроміографія, візуалізація м’язів або гістопатологія.
Особи з ураженням рухових нейронів, як-то боковий аміотрофічний склероз, спінальна м’язова атрофія, спадковими невропатіями, метаболічними міопатіями (хвороби накопичення ліпідів), мітохондріальними розладами при підвищеному рабдоміолізі, різними м’язовими дистрофіями (міотонічна дистрофія) і метаболічними захворюваннями (хвороба Помпе) можуть бути особливо схильними до тяжкого перебігу інфекції [7].
Висновки
За минуле століття досягнуто значних успіхів у профілактиці, діагностиці та лікуванні багатьох захворювань. Практична медицина здатна розчинити тромби у сонних артеріях, виправити мутовані гени, перш ніж вони зможуть завдати шкоди, та відобразити мозок і його мережі з вишуканою точністю, проте наразі ми поставлені на коліна найменшим з організмів, розмір якого сягає близько 60 нм. Слід переосмислити те, як проводиться підготовка лікарів-неврологів і вчених-медиків у галузі академічної неврології, як розставляються пріоритети у розробці ліків для неврологічних захворювань. Потрібно дозволити академічним і фармацевтичним закладам створювати методи лікування, що мають ґрунтуватися не на прибутку, а, скоріше, витратах для людства. Наука визнає сотні вірусів, які здатні спричинити розвиток енцефаліту і призвести до спустошення великих груп населення, проте ми не можемо вплинути на жодний із цих організмів (окрім герпетичного енцефаліту). Настав час визнати, що в неврології настала криза. Потрібно діяти вже сьогодні.
Література
- Arabi Y.M. Severe neurologic syndrome associated with Middle East respiratory syndrome corona virus (MERS-CoV) / Y.M. Arabi, A. Harthi, J. Hussein // Infection. – 2015. – Vol. 43. – Р. 495‑501.
- Burks J.S. Two coronaviruesisolated from central nervous system tissue of two multiple sclerosis patients / J.S. Burks, B.L. Devald, L.D. Janovsky, J.C. Gerdes // Science. – 1980. – Vol. 209. – Р. 933‑934.
- Dessau R.B. Coronaviruses in spinal fluid of patients with acute monosymptomatic optic neuritis / R.B. Dessau, G. Lisby, J.L. Frederiksen // Acta Neurol Scand. – 1999. – Vol. 100. – Р. 88‑91.
- Devaux C.A. Emerging end re-emerging viruses: a global challenge illustrated by Chikungunya virus outbreaks / C.A. Devaux // World J Virol. – 2012. – Vol. 1 (1). – Р. 11‑22.
- Dubé M. Axonal transport enables neuron-to-neuron propagation of human coronavirus OC43 / M. Dubé, А. Le Coupanec, А.Н.М. Wong, J.M. Rini // J Virol. – 2018. – Vol. 92. – Р. 404‑418.
- Fazzini E. Cerebrospinal fluid antibodies to coronavirus in patients with Parkinson’s disease / E. Fazzini, J. Fleming, S. Fahn // Mov Disord. – 1992. – Vol. 7. – Р. 153‑158.
- Guidon A.C. COVID‑19 and neuromuscular disorders / A.C. Guidon, A.A. Amato // Neurology. – April 13, 2020; https://n.neurology.org/content/early/2020/04/13/WNL.0000000000009566.
- Gutiérrez-Ortiz C. Miller Fisher Syndrome and polyneuritis cranialis in COVID‑19 / C. Gutiérrez-Ortiz, А. Méndez, S. Rodrigo-Rey, E. San Pedro-Murillo, L. Bermejo-Guerrero, R. Gordo-Mañas, F. de Aragón-Gómez, J. Benito-León // Neurology. – April 17, 2020; https://n.neurology.org/content/early/2020/04/17/WNL.0000000000009619.
- Huang C. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China / С. Huang, Y. Wang, Х. Li, L. Ren, J. Zhao, Y. Hu, L. Zhang, G. Fan et al. // Lancet. – 2020. – Vol. 395 (10223). – Р. 497‑506.
- Hung E.C. Detection of SARS coronavirus RNA in the cerebrospinal fluid of a patient with severe acute respiratory syndrome / E.C. Hung, S.S. Chim, P.K. Chan // Clin Chem. – 2003. – Vol. 49. – Р. 2108‑2109.
- Jin M. Rhabdomyolysis as potential late complication associated with 2019 novel coronavirus disease / M. Jin, Q. Tong // Emerg Infect Dis. – 2020; https://doi.org/10.3201/eid2607.200445.
- Kim J.E. Neurological Complications during Treatment of Middle East Respiratory Syndrome / J.E. Kim, J.H. Heo, H.O. Kim // J Clin Neurol. – 2017. – Vol. 13. – Р. 227‑233.
- Koga M. Antecedent infections in Fisher syndrome: sources of variation in clinical characteristics / М. Koga, М. Kishi, Т. Fukusako, N. Ikuta, М. Kato, Т. Kanda // J Neurol. – 2019. – Vol. 266. – Р. 1655‑1662.
- Li Y. Coronavirus Infections in the central nervous system and respiratory tract show distinct features in hospitalized children / Y. Li, H. Li, R. Fan, B. Wen // Intervirology. – 2016. – Vol. 59. – Р. 163‑169.
- Morfopoulou S. Human Coronavirus OC43 Associated with Fatal Encephalitis / S. Morfopoulou, J.R. Brown, E.G. Davies // N Engl J Med. – 2016. – Vol. 375 – Р. 497‑498.
- Nath A. Neuroinfectious diseases: A crisis in neurology and a call for action / A. Nath // JAMA Neurol. – 2015. – Vol. 72. – Р. 143‑144.
- Nath A. Neurologic complications of coronavirus infections / А. Nath // Neurology. – March 30, 2020; https://n.neurology.org/content/early/2020/03/27/WNL.0000000000009455.
- Salmi A. Antibodies to coronaviruses OC43 and 229E in multiple sclerosis patients / A. Salmi, B. Ziola, T. Hovi, M. Reunanen // Neurology. – 1982. – Vol. 32. – Р. 292‑295.
- Turgay C. A rare cause of acute flaccid paralysis: Human coronaviruses / С. Turgay, Т. Emine, K. Ozlem, S.P. Muhammet, A.T. Haydar // J Pediatr Neurosci. – 2015. – Vol. 10. – Р. 280‑281.
- Waggoner J.J. Viremia and Clinical Presentation in Nicaraguan Patients Infected With Zika Virus, Chikungunya Virus, and Dengue Virus / J.J. Waggoner // Clinical Infectious Diseases. – 2016. – Vol. 63 (12). – Р. 1584‑1590.
- Wakerley B.R. Guillain-Barre and Miller Fisher syndromes – new diagnostic classification / B.R. Wakerley, A. Uncini, N. Yuki // Nature reviews Neurology. – 2014. – Vol. 10. – Р. 537‑544.
- Wakerley B.R. Polyneuritis cranialis – subtype of Guillain–Barré syndrome? / B.R. Wakerley, N. Yuki // Nature Reviews Neurology. – 2015. – Vol. 11. – Р. 664‑664.
- Wang D. Clinical Characteristics of 138 Hospitalized Patients With 2019 Novel CoronavirusInfected Pneumonia in Wuhan, China / D. Wang, B. Hu, C. Hu, F. Zhu, Х. Liu, J. Zhang, B. Wang, Н. Xiang et all // JAMA. – Feb 7, 2020; doi: 10.1001/jama.2020.1585.
- World Health Organization. Clinical management of severe acute respiratory infection (SARI) when COVID‑19 disease is suspected. – 2020; 1‑21.
- Yan R. Structural basis for the recognition of the SARS-CoV‑2 by full-length human ACE2 / R. Yan, Y. Zhang, Y. Li, L. Xia, Y. Guo, Q. Zhou // Science. – 2020 – Vol. 10. – Р. 27‑62.
- Yeh E.A. Detection of coronavirus in the central nervous system of a child with acute disseminated encephalomyelitis / Е.А. Yeh, А. Collins, М.Е. Cohen, P.K. Duffner, Н. Faden // Pediatrics. – 2004. – Vol. 113. – Р. 73‑76.
- Zhao H. Guillain-Barre syndrome associated with SARS-CoV‑2 infection: causality or coincidence? / Н. Zhao, D. Shen, H. Zhou, J. Liu, S. Chen // The Lancet Neurology. – April 1, 2020; https://doi.org/10.1016/S1474‑4422(20)30109‑5.
- Zhou F. Clinical course and risk factors for mortality of adult inpatients with COVID‑19 in Wuhan, China: a retrospective cohort study / F. Zhou, T. Yu, R. Du // Lancet. – 2020. – Vol. 36. – Р. 140‑143.
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 2 (53) 2020 р.


