5 вересня, 2015
Порушення статевого розвитку у дівчаток

Содержание статьи:
>>__У статті висвітлено сучасні аспекти проблеми порушення статевого дозрівання у дівчаток. Представлено клінічні прояви основних форм патології, можливості діагностики та лікування.
Ключові слова: статевий розвиток дівчаток, передчасне дозрівання, затримка статевого розвитку.
Статевий розвиток – це генетично запрограмований процес, який починається у дівчаток віком 7-8 років і закінчується до 17-18 років. Поява вторинних статевих ознак і менструальноподібних виділень до 7 років слід розцінювати як передчасне статеве дозрівання (ПСД). Недорозвинення або відсутність вторинних статевих ознак до 15-16 років відноситься до затримки статевого розвитку. Якщо показники статевого дозрівання не з’являються у дівчини старше 16 років, то йдеться про відсутність статевого розвитку.
Найбільш прийнятною у повсякденній практиці є класифікація порушень статевого розвитку Г. М. Савельєвої. У ній враховуються локалізація та характер процесу, що призводить до патології, а також основні клінічні прояви (табл. 1).
Таблиця 1. Класифікація порушень статевого розвитку (за Савельєвою Г. М., 2000)
|
Характер порушення статевого дозрівання |
Локалізація патологічного процесу |
Характер патологічного процесу |
Основні клінічні прояви |
|
ПСД |
ЦНС |
Органічні та функціональні порушення |
Ізосексуальне ПСД |
|
Яєчники |
Гормонально активна пухлина |
ПСД з порушенням послідовності появи вторинних статевих ознак |
|
|
Фолікулярна кіста |
Транзиторна форма ПСД |
||
|
Кірковий шар наднирників |
Вроджена дисфункція (вроджений адреногенітальний синдром [АГС]) |
Гетеросексуальне ПСД(за чоловічим типом) |
|
|
Затримка статевого дозрівання |
ЦНС |
Функціональні порушення |
Недорозвиненість вторинних статевих ознак і статевих органів, аменорея або гіпоменструальний синдром |
|
Яєчники |
Функціональна недостатність |
Виражена недорозвиненість вторинних статевих ознак і статевих органів, первинна аменорея |
|
|
Відсутність статевого розвитку |
Дисгенезія гонад (аномалії статевих хромосом) |
Анатомічна недостатність яєчників |
Відсутність вторинних статевих ознак, різка недорозвиненість зовнішніх та внутрішніх статевих органів, первинна аменорея |
|
Порушення статевого розвитку в пубертатному віці |
ЦНС |
Функціональні діенцефальні порушення |
Обмінно-вегетативні порушення, ожиріння, гіпертрихоз, олігоменорея |
|
Яєчники |
Дисфункція яєчників (гіперандрогенія яєчникова) |
Гіпертрихоз, олігоменорея, збільшення маси тіла |
|
|
Наднирники |
Дисфункція наднирників (пубертатний АГС), гіперандрогенія наднирникова |
Гіпертрихоз, олігоменорея, вірильні ознаки будови тіла |
Передчасне статеве дозрівання
ПСД (pubertas praecox) – це група захворювань, об’єднаних однією чи кількома ознаками, що зумовлені передчасним впливом статевих гормонів на організм дівчинки.
Появу вторинних статевих ознак у дівчаток віком до 8 років називають ПСД, а після 8 і до 10 років – раннім статевим розвитком. За даними різних авторів, частота ПСД серед гінекологічної патології у дівчаток становить 2,5-5 %.
Виділяють такі форми ПСД: істинне (справжнє) та несправжнє (хибне). Справжня форма зумовлена надмірною секрецією гонадотропінів і гонадоліберину, а несправжня – автономною продукцією статевих гормонів внаслідок патології яєчників або надниркових залоз.
Незалежно від генезу захворювання виділяють повну форму ПСД (за якої спостерігається розвиток усіх вторинних статевих ознак і поява менструацій) та неповну. Повна форма ПСД зустрічається дуже рідко і становить до 9 % випадків. Найчастіше діагностують неповні (ізольовані) форми ПСД: телархе (ізольований розвиток молочних залоз) й адренархе (ізольований розвиток статевого оволосіння) за відсутності менструації.
Існує також самостійна група – гонадотропіннезалежна форма ПСД, за якої активація діяльності статевих залоз зумовлена генетичними порушеннями (синдром Мак-К’юна – Олбрайта).
Розрізняють ПСД за ізосексуальним (вторинні статеві ознаки відповідають статі дитини) або гетеросексуальним (вторинні статеві ознаки відповідають протилежній статі) типом.
ПСД за ізосексуальним типом
ПСД за ізосексуальним типом (рис. 1) найчастіше може бути зумовлене як органічною (асфіксія, пологова травма, перенесена нейроінфекція, пухлини), так і функціонально-органічною (токсичні, інфекційні чинники) патологією.
За наявності органічного характеру церебральної патології клінічні прояви ПСД відмічають на фоні вираженої неврологічної симптоматики: емоційної нестійкості, порушень обмінно-ендокринного характеру, можливої затримки інтелектуального розвитку. Об’єктивно найбільш типовими є такі синдроми: анізорефлексія, наявність патологічних рефлексів, ураження III, VIII, XII пар черепних нервів, порушення тонусу м’язів, ознаки внутрішньочерепної гіпертензії, що поєднується із застійними явищами на очному дні.
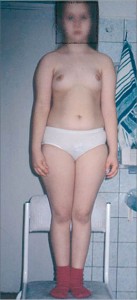 Рис. 1. Пацієнтка віком 5 років. ПСД церебрального генезу (Баисова Б. И. и др. Гинекология: учебник
Рис. 1. Пацієнтка віком 5 років. ПСД церебрального генезу (Баисова Б. И. и др. Гинекология: учебникпод ред. Савельевой Г. М., Бреусенко В. Г., 2011)
У разі функціонального характеру ураження ЦНС симптоми ПСД є первинними, виникають на фоні стертих неврологічних проявів, а інколи можуть бути єдиними ознаками порушення гіпоталамічних структур.
Причиною хибних периферійних форм ПСД за ізосексуальним типом може бути ураження гонад – гормональна пухлина (гранульозоклітинна, текаклітинна, тератобластома з елементами гормонально активної тканини, первинна хоріонепітеліома) або фолікулярна кіста яєчника. Такі патологічні стани характеризуються надлишковою продукцією естрогенів, що призводить до ПСД.
При ПСД яєчникового генезу неврологічна симптоматика відсутня, вторинні статеві ознаки незначно виражені. Маніфестують ациклічні кровотечі, наявні ознаки вираженої естрогенізації статевих органів (позитивний симптом «зіниці», збільшення розмірів матки). При ректоабдомінальному дослідженні виявляють пухлину яєчника. Рівень естрогенів у крові значно перевищує вікову норму при відповідному до віку дівчинки рівні секреції гонадотропінів та гонадотропного рилізинг-гормона.
ПСД за гетеросексуальним типом
Даний тип характеризується появою у дівчат ознак чоловічої статі і найчастіше зумовлений природженим АГС.
Проста вірилізуюча форма АГС – захворювання, причиною якого є недостатність ферментних систем кори наднирників, найчастіше 21-гідроксилази. Це призводить до дефіциту утворення кортизолу та збільшення секреції адренокортикотропного гормона (АКТГ) і, як наслідок, підвищення синтезу андрогенів і двобічної гіперплазії кори наднирників.
Відразу після народження відзначають збільшення клітора (від гіпертрофії до пенісоподібного), наявність урогенітального синуса, заглиблення присінка піхви, наявність високої промежини, недорозвиненість малих соромітних губ. При значно вираженій вірилізації виникають труднощі з визначенням статі дитини.
Характерним є прискорення росту хворих із 2-3-річного віку зі зміною пропорцій тіла в бік маскулінізації. Так, прискорюється ріст скелета (до 5-7 років кістковий вік випереджає календарний на 5-7 років). Він припиняється у віці 9-13 років внаслідок закриття зон росту. Кінцевий зріст пацієнток становить 130-150 см. При цьому скелет розвивається непропорційно: велика голова з грубими рисами обличчя, довгий тулуб і відносно короткі кінцівки. Відмічається атлетична будова тіла: широкі плечі, вузькі стегна, розвинуті м’язи грудної клітки та кінцівок унаслідок анаболічного впливу андрогенів на м’язову тканину.
ПСД при синдромі Мак-К’юна – Олбрайта – Брайцева
Синдром характеризується тріадою симптомів: пігментними плямами кольору кави з молоком з характерними «географічними» обрисами, поліостозною фіброзно-кістозною дисплазією та ендокринними порушеннями (рис. 2, 3).
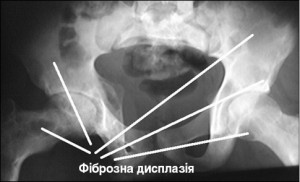 Рис. 2. Синдром Мак-К’юна – Олбрайта – Брайцева: рентгенологічна картина поліостозної фіброзної дисплазії
Рис. 2. Синдром Мак-К’юна – Олбрайта – Брайцева: рентгенологічна картина поліостозної фіброзної дисплазіїЗахворювання виникає спорадично, переважно в дівчаток. Відсутні дані щодо сімейних випадків патології. Відбувається раннє статеве дозрівання за чоловічим типом: характерне оволосіння, збільшення клітора, зниження тембру голосу, наявність перснеподібного хряща; розміри матки значно відстають від вікової норми; молочні залози та регулярні менструації відсутні.
Окрім ПСД, у пацієнток також відзначають інші ендокринні розлади: двобічну адреналову гіперплазію, тиреотоксикоз неімунного генезу, вузловий та дифузний еутиреоїдний зоб, гіперпаратиреоз, соматотропінпродукуючі аденоми гіпофіза. При цьому характерними є такі соматичні порушення: серцева тахіаритмія, гіпербілірубінемія, поліпоз, гіперплазія тимуса, селезінки та підшлункової залози.
Відмічається підвищення секреції 17-кетостероїдів (17-КС) та рівня тестостерону в крові (після проби з дексаметазоном знижується більш ніж на 50-75 %).
Неповні форми ПСД
Серед неповних (ізольованих) форм ПСД розрізняють передчасний розвиток молочних залоз (телархе), статевого оволосіння (адренархе) та передчасний початок менструацій (менархе).
Передчасне телархе – явище досить поширене і є найбільш доброякісним варіантом ПСД. Здебільшого передчасне телархе виникає в дівчаток віком до 3 років і нерідко є першим симптомом справжнього ПСД.
Етіологія транзиторного телархе не визначена, однак у цих пацієнток відмічено високу частоту гострих респіраторних вірусних інфекцій, після яких зазвичай і виникає клінічна маніфестація патології.
Причиною передчасного телархе є транзиторне підвищення рівня фолікулостимулюючого гормона (ФСГ), яке призводить до дозрівання яєчникових фолікулів та короткочасної естрогенної стимуляції. Вважається, що порушення локальної рецепторної чутливості молочних залоз також може бути причиною передчасного телархе. Збільшення молочних залоз часто спостерігається впродовж першого року життя, ступінь їх розвитку не перевищує ІІ стадії (за Таннером), ареоли не мають ознак естрогенізації.
У деяких дівчаток з передчасним телархе при УЗД в яєчниках візуалізуються фолікули більших за норму розмірів. Розвиток зовнішніх статевих органів гармонійний, завжди відповідає віку. Показники зросту також відповідають віковій нормі, кісткове дозрівання – календарному віку або може бути прискореним у межах 1-2 років. Пубертатний вік настає у звичні терміни, його перебіг не має ускладнень. Під час лабораторної діагностики цієї патології виявляють підвищений рівень ФСГ із широким індивідуальним діапазоном коливань його величин відповідно до препубертатних і пубертатних показників при незначному підвищенні рівня лютеїнізуючого гормона (ЛГ). Підвищення рівня пролактину та естрадіолу зазвичай не відмічається.
У 90 % дітей старших за 3 роки спостерігається регрес молочних залоз, і пубертат настає в нормальні терміни. Такі дівчатка не потребують гормональної терапії, але повинні протягом усього пубертатного періоду перебувати під наглядом дитячого гінеколога й ендокринолога.
Передчасне адренархе характеризується появою вторинного статевого оволосіння (частіше лобкового) у дітей віком до 8 років.
Патогенез: підвищення концентрації андрогенів (дегідроепіандростерону [ДГЕА]) у 3-4-річному віці, що призводить до маніфестації передчасного адренархе без проявів інших вторинних статевих ознак.
У дівчаток з передчасним адренархе найчастіше розвивається оволосіння лобка. Ступінь оволосіння незначний, відповідає II стадії (за Таннером). Швидкість росту скелета відбувається з незначним прискоренням, кістковий вік випереджає календарний на 1-2 роки. Кінцевий зріст дітей відповідає генетично запрограмованому. При УЗД малого таза розміри матки і яєчників не перевищують фізіологічних показників.
При гормональному дослідженні виявляють підвищення рівня ДГЕА відносно нормативів для пубертатного віку. Рівень тестостерону, показники ЛГ і ФСГ відповідають фізіологічному перебігу препубертатного періоду.
Передчасне адренархе часто є симптомом вродженого АГС, рідше – вірилізуючої пухлини яєчника, наднирника та інших наднирникових форм гіперандрогенії. Дівчата з передчасним адренархе не потребують гормональної терапії і повинні перебувати під наглядом ендокринолога та дитячого гінеколога впродовж усього пубертатного періоду.
Передчасне ізольоване менархе – досить рідкісна патологія, механізм розвитку якої, можливо, пов’язаний із наявністю підвищеної чутливості до естрогенів.
Лікування та спостереження за пацієнтками здійснюють, як при ізольованій формі телархе.
Діагностика
З метою виявлення та диференціальної діагностики ПСД необхідно провести ретельне візуальне обстеження з оцінкою статевого розвитку за класифікацією Таннера, оцінити розвиток зовнішніх статевих органів, вивчити динаміку росту дівчинки, визначити її кістковий вік, провести УЗД стану внутрішніх статевих органів, надниркових та молочних залоз, виконати вагіноскопію за показаннями.
Важливим критерієм оцінки стану пацієнтки з ПСД є визначення кісткового віку. За розвитком скелета можна не тільки встановити соматичний вік, а й передбачити час настання статевого дозрівання. Якщо кістковий вік відстає від календарного, то статеве дозрівання запізнюється, якщо ж він випереджає календарний, то статеве дозрівання настає раніше. Поява сесамоподібної кістки великого пальця кисті збігається з початком статевого дозрівання. Враховуючи загальну тенденцію акселерації, нині це спостерігається у більш ранньому віці, ніж раніше: у дівчаток приблизно у 10,5 року, у хлопчиків – у 13 (рис. 4).
 Рис. 4. Кістковий вік. Схема розвитку скелета кисті від народження до статевої зрілості (Schmid F., Moll H.): а – у момент народження: розвиток діафіза завершено, ядра скостеніння відсутні; б – 1 рік: епіфіз променевої кістки, головчаста кістка, гачкувата кістка; в – 3 роки: проксимальний епіфіз великого пальця кисті, тригранна кістка; г – 6 років: півмісяцева кістка, човноподібна кістка, кістка-трапеція, трапецієподібна кістка; ґ – 9 років: епіфіз ліктьової кістки; д – 12 років: сесамоподібна кістка ще відсутня; е – 14 років: сесамоподібна кістка великого пальця кисті (період статевого дозрівання); є – 19 років: зарощення лінії епіфізарного хряща
Рис. 4. Кістковий вік. Схема розвитку скелета кисті від народження до статевої зрілості (Schmid F., Moll H.): а – у момент народження: розвиток діафіза завершено, ядра скостеніння відсутні; б – 1 рік: епіфіз променевої кістки, головчаста кістка, гачкувата кістка; в – 3 роки: проксимальний епіфіз великого пальця кисті, тригранна кістка; г – 6 років: півмісяцева кістка, човноподібна кістка, кістка-трапеція, трапецієподібна кістка; ґ – 9 років: епіфіз ліктьової кістки; д – 12 років: сесамоподібна кістка ще відсутня; е – 14 років: сесамоподібна кістка великого пальця кисті (період статевого дозрівання); є – 19 років: зарощення лінії епіфізарного хрящаОскільки в основі справжньої форми ПСД часто є патологія ЦНС, для вивчення її стану виконують огляд очного дна, електроенцефалограму, комп’ютерну томографію, магнітно-резонансну томографію, призначають консультацію невролога і нейрохірурга.
Передчасну появу симптомів статевого дозрівання також може зумовлювати природжена або набута недостатність щитоподібної залози. Тому при обстеженні дівчаток з ознаками ПСД необхідно визначати функціональний стан щитоподібної залози (за даними УЗД і рівнем гормонів) для виключення його порушення.
З метою виключення ендокринної патології як етіологічного чинника ПСД проводиться вивчення гормонального профілю дівчат. Гормональна діагностика включає: визначення рівнів ЛГ, ФСГ, естрадіолу, пролактину, тестостерону, кортизолу, 17-гідроксипрогестерону, ДГЕА. Для встановлення форми захворювання проводять гормональні діагностичні проби з люліберином, аналогом АКТГ – синактеном, дексаметазоном.
При збиранні анамнезу необхідно також з’ясувати характер статевого розвитку у родичів.
Лікування
Якщо ПСД викликане церебральною патологією, широко використовують препарати, що знижують внутрішньочерепний тиск, та іншу симптоматичну терапію, направлену на нормалізацію функцій ЦНС. За наявності об’ємних утворень головного мозку здійснюють оперативне лікування в спеціалізованих стаціонарах нейрохірургічного профілю.
З метою зменшення симптомів ПСД, уповільнення темпів зростання та закриття зон росту проводять гормональну терапію, зокрема лікування антиестрогенами (андрокур, або ципротерону ацетат) добовою дозою 50-75 мг щоденно до 8-річного віку.
Ефективними в лікуванні ПСД є аналоги гонадоліберину, зокрема декапептил депо (трипторелін). Принцип терапії полягає у зниженні чутливості гіпофіза до гонадоліберину в результаті тривалої його стимуляції. На початку лікування препарат вводять внутрішньом’язово по одній ін’єкції на 0; 14 і 28-й день. Наступні введення проводять кожні 4 тиж, а у разі недостатньої ефективності ін’єкції можна робити кожні 3 тиж. Дозування препарату здійснюється залежно від маси тіла: < 20 кг – 1,875 мг (половина дози); 20-30 кг – 2,5 мг (2 / 3 дози); > 30 кг – 3,75 мг (повна доза). Лікування завершують після досягнення пацієнткою 8-9-річного віку.
Критеріями ефективності терапії вважається: припинення менструацій, значне зменшення, а з часом повне зникнення молочних залоз, оволосіння лобка та соромітних губ, зникнення фолікулів у яєчниках, зменшення розмірів яєчників, зниження базальних рівнів ЛГ та ФСГ, уповільнення зростання та темпів закриття зон росту кісток.
При ПСД яєчникового генезу застосовують оперативне лікування – видалення пухлини. Зазвичай симптоми ПСД зникають через 2-3 тиж після хірургічного втручання. Рекомендовано диспансерне спостереження у дитячого гінеколога протягом 1-2 років.
Нарушения полового развития у девочек
И. Б. Вовк, В. К. Кондратюк, В. Ф. Петербургская
В статье освещены современные аспекты проблемы нарушения полового созревания у девочек. Представлены клинические проявления основных форм патологии, возможности диагностики и лечения.
Ключевые слова: половое развитие девочек, преждевременное созревание, задержка полового развития.
Disorders of sexual development in girls
I. B. Vovk, V. K. Kondratiuk, V. F. Peterburgskaia
The article highlights the modern aspects of the problem of disorders of sexual development in girls. The clinical manifestations of the main forms of pathology, diagnosis and treatment are presented.
Keywords: sexual development of girls, premature puberty, delayed sexual development.
Продовження в наступному номері