4 серпня, 2020
Можливості покращення життя пацієнтів із персистуючою астмою: фокус на антагоністи лейкотрієнів
Проспективне відкрите дослідження ефективності монтелукасту в лікуванні астми легкого та помірного ступеня тяжкості показало, що, згідно з даними низки опитувальників з оцінки контролю самого захворювання і якості життя (ЯЖ) пацієнтів з астмою, застосування монтелукасту в дозі 10 мг допомагає успішніше контролювати астму й покращити ЯЖ пацієнтів. Астма – це хронічне запальне захворювання дихальних шляхів (ДШ), пов’язане з їхньою непрохідністю і гіперреактивністю. Це поліетіологічне захворювання, в основі його розвитку лежить як генетична схильність, так і вплив факторів довкілля, які грають взаємозамінну роль [1]. Безконтрольна та неадекватно керована астма значуще погіршує ЯЖ пацієнтів, а також може стати причиною передчасної смерті. За медичною статистикою, у 2018 р. кількість хворих на астму в усьому світі становила 339 млн осіб. При цьому бронхіальна астма (БА) посідає 16-е місце серед головних причин інвалідності і 28-е – у структурі провідних причин тягаря хвороб, який оцінюється роками життя, скоригованими з причини непрацездатності (disability-adjusted life year, DALYs) [2].
Запальний процес ДШ при астмі протікає із залученням надзвичайно великої кількості клітин та медіаторів запалення, які провокують ремоделювання ДШ, а також зумовлюють появу таких респіраторних симптомів, як кашель, хрипи й задишка. Еозинофіли, опасисті клітини, нейтрофіли, макрофаги, дендритні клітини, епітеліальні клітини ДШ, Т-хелпери 1 (Th1) і Т-хелпери 2 (Th2) залучені до запального процесу при астмі. Th2 генерують інтерлейкін (IL)-4, IL‑5 та IL‑13, які індукують вироблення імуноглобуліну Е та еозинофілів і призводять до гіперреактивності ДШ.
Опасисті клітини слизової синтезують гістамін, простагландини, а також лейкотрієн цистеїнілу (CysLT) – медіатори, які спричинюють звуження бронхів [3].
CysLT відіграє важливу роль у патогенезі астми, оскільки не тільки провокує скорочення гладкої мускулатури бронхів, а й викликає реконструкцію бронхів унаслідок стимулювання проліферації епітелію та збільшення відкладання колагену [4-5].
Наслідками впливу цього медіатора є посилення проникності судин, що веде до набряку слизової оболонки, зниження мукоциліарного кліренсу, збільшення вироблення слизу. Також CysLT активує міграцію лейкоцитів, чим провокує посилення запального процесу. Монтелукаст є потужним і селективним блокатором рецептора цього медіатора – CysLT1, який відіграє ключову роль у пригніченні бронхоконстрикції та запального процесу [8].
Міжнародний погоджувальний документ – Глобальна ініціатива з БА (The Global Initiative for Asthma, GINA) 2018 року рекомендує антагоністи лейкотрієнових рецепторів (АЛТР), до яких належить монтелукаст, як монотерапію при легкій персистуючій астмі та як доповнення або альтернативу збільшення дози інгаляційних кортикостероїдів (ІКС), а також замість додавання β2-агоністів тривалої дії (БАТД) [6]. АЛТР показали ефективність при тривалому контролі загострення астми, однак золотим стандартом для боротьби з астмою вважались ІКС [7].
Монтелукаст вивчався як додаткова терапія до ІКС для тривалого контролю персистуючої астми легкої та середньої тяжкості [9-11], але чи буде ефективною монотерапія монтелукастом? Саме на це питання намагалися знайти відповідь автори згаданого дослідження.
Матеріали та методи
Це проспективне відкрите інтервенційне дослідження проводилося протягом 3 міс (із січня по березень 2019 р.) у відділенні лікарні третинної допомоги в місті Лахор (Пакістан). У дослідженні брали участь пацієнти старше 15 років, хворі на БА не менше року.
Усім пацієнтам лікуючий пульмонолог призначав монтелукаст (10 мг 1 раз на день), без додавання ІКС чи БАТД. Усі учасники дослідження двічі заповнювали анкету – на початку дослідження (0-й день) та через місяць (30-й день).
Тест із контролю над астмою (Asthma Control Test, АСТ) був використаний для оцінки ефективності лікування [12]. При проведенні ACT середній бал <20 показує неконтрольовану астму, 20-24 бали – адекватний контроль захворювання, а оцінка 25 балів відповідає відмінному контролю астми.
У дослідженні було використано опитувальник загальної ЯЖ (ЗЯЖ) хворих на БА (Asthma Quality of Life Questionnaire-Standard, AQLQ-S) [13].
З дослідження були виключені: пацієнти з діагнозом астми <1 року; ті, хто вже приймав монтелукаст для контролю астми, а також пацієнти, які повідомили про будь-які побічні ефекти на тлі прийому монтелукасту протягом періоду дослідження.
Дані були оброблені та проаналізовані за допомогою SPSS для Windows версії 23.0 (IBM, США). Середнє та стандартне відхилення (СВ) обчислювалися для безперервних змінних, у тому числі вік та показник AQLQ-S та ACT. Частота й відсоток розраховували для категорійних змінних, включаючи стать, вік, тривалість астми та частоту загострень. Були порівняні бали AQLQ-S та ACT в 0-й та на 30-й день дослідження за допомогою залежного Т-тесту. Р-значення ≤0,05 вважалися статистично значущими.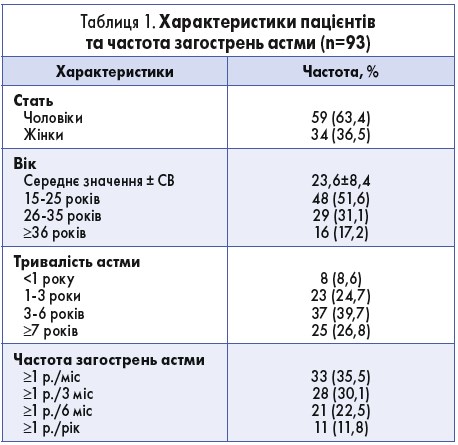
Результати дослідження
На початку дослідження участь у ньому взяли 112 осіб. Під час періоду дослідження 2 (1,8%) учасників виключили через побічні ефекти від прийому монтелукасту, 3 (2,7%) учасники вийшли з дослідження, не вказавши причину, а 14 (12,5%) осіб не пройшли друге опитування після закінчення лікування.
Дослідження завершили 93 (83,0%) учасники, з них 59 (63,4%) чоловіків, 34 (36,5%) жінки. Середній вік учасників становив 23,6±8,4 року (табл. 1).
Середні бали обох шкал – AQLQ-S та ACT – порівнювали в 0-й та на 30-й день. За оцінкою шкали AQLQ-S показник ЗЯЖ суттєво покращився за 1 міс терапії монтелукастом. Також спостерігалося поліпшення емоційного стану пацієнтів, покращення активності та полегшення симптомів астми. Показник контролю над астмою також значно покращився за місяць терапії монтелукастом (табл. 2). 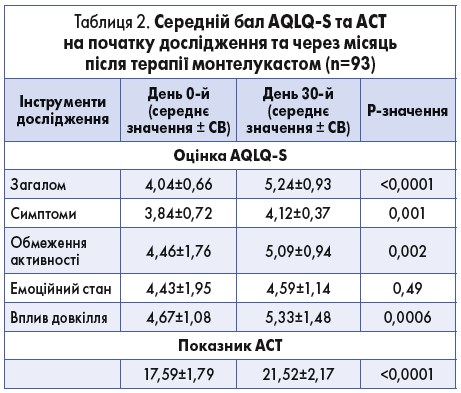
Обговорення
Це дослідження довело роль терапії монтелукастом у боротьбі з астмою та в покращенні ЗЯЖ пацієнтів. Однак воно має й свої обмеження. Оскільки дослідження було відкритим, воно не передбачало наявності контрольної плацебо-групи. Для більш детальної оцінки застосування монтелукасту в лікування астми рекомендуються довготривалі рандомізовані подвійні сліпі випробування.
Аналіз літератури показав, що в низці багатьох інших досліджень також показана ефективність монтелукасту. Наприклад, у дослідженні лікування хронічної астми MONICA (MONtelukast In Chronic Asthma) 10 мг монтелукасту щодня додавали до ІКС та/або БАТД протягом 6 міс, після чого спостерігалося значуще поліпшення стану пацієнтів – згідно з балами обох опитувальників: АСT і міні-AQLQ [9]. У метааналізі 50 випробувань ризик загострення астми був знижений до 0,60 в 6 дослідженнях при монотерапії АЛТР. У 4 випробуваннях, де АЛТР додавали до ІКС, коефіцієнт ризику загострення становив 0,80 [6]. Bozek та Biernacki також повідомили про виражене поліпшення стану пацієнтів при додаванні монтелукасту до ІКС [10, 11].
З іншого боку, у деяких дослідженнях суттєвого покращення контролю над астмою за допомогою терапії монтелукастом не було виявлено [14, 15].
У корейському дослідженні монтелукаст додавали до низьких доз ІКС, що дало кращі результати лікування при легкій та помірній персистуючій астмі, ніж лише збільшення дози ІКС [16]. У ще одному з досліджень монотерапію монтелукастом порівнювали з монотерапією ІКС при хронічній астмі. У 1-й і 3-й тиж показник пікової швидкості видиху (ПШВ) був кращим у групі, що отримувала монтелукаст (р<0,05), з 4-го по 8-й тиж цей показник був однаковим для обох груп [17]. А при порівнянні монотерапії монтелукастом з плацебо у пацієнтів, які отримували монтелукаст, не спостерігалося значного поліпшення за шкалою ACT, але показники згідно з AQLQ-S у цілому суттєво покращали [18].
У недавньому китайському дослідженні монтелукаст відіграв суттєву роль у регулюванні Th1/Th2 клітинного балансу та посилив експресію CD4+ CD25+ регуляторних Т-клітин. Це сприяло зменшенню запалення ДШ і допомагало поліпшити клінічні симптоми, а також легеневі функції в цих пацієнтів [19].
Показано, що монтелукаст є еквівалентним тіотропію як доповнення до ІКС/БАТД при астмі. Незважаючи на різний механізм дії препаратів, вони обидва зменшують обструкцію ДШ та покращують легеневу функцію [20].
У метааналізі 20 випробувань монтелукаст як доповнення до ІКС/ БАТД у дорослих із хронічною астмою значуще зменшив кількість загострень, а в пацієнтів із гострою астмою – статистично покращив ПШВ та зменшив потребу в системних кортикостероїдах [21].
Позитивний вплив монтелукасту в лікуванні легкої та середньотяжкої персистуючої астми, а також гострої астми підкріплено широкими літературними даними. Монтелукаст допомагає зменшити запалення ДШ та вираженість симптомів астми й частоту загострень, завдяки чому покращується ЯЖ пацієнтів.
Монтелукаст може бути використаний і в якості монотерапії астми, і як доповнення до ІКС/БАТД для забезпечення належного контролю астми.
Висновки
Монтелукаст відіграє важливу роль у боротьбі з астмою і сприяє покращенню якості життя пацієнтів із легкою та помірною персистуючою астмою. Він може бути перспективною альтернативою ІКС та БАТД або доповненням до цих препаратів у лікуванні хронічної астми з неконтрольованими симптомами.
Довідка ЗУ
Препарат Монтел (монтелукаст) ПАТ НВЦ «Борщагівський ХФЗ» (м. Київ), може застосовуватися для лікування в дітей і дорослих із БА та/або алергічним ринітом. Таблетки Монтел приймають перорально лише 1 раз на день, що дуже зручно, у разі якщо препарат призначений дітям. Монтел випускається у формі таблеток (жувальних і вкритих плівковою оболонкою) з різним умістом діючої речовини (4; 5 і 10 мг), це дає можливість ураховувати вікові особливості пацієнтів, спростити схему лікування й досягти максимальної ефективності терапії БА.
Реферативний огляд за матеріалом: A. Ikram, V. Kumar, M. Taimur et al. Role of Montelukast in Improving Quality of Life in Patients with Persistent Asthma. Cureus 11(6): e5046. DOI 10.7759/cureus.5046 (June 30, 2019).
Підготувала Анастасія Романова
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (51), 2020 р.


