4 серпня, 2020
Алергія під контролем: сучасні антигістамінні препарати в лікуванні алергічного риніту
3-5 квітня 2020 р. відбувся І Міжнародний конгрес «Від народження до зрілості: міждисциплінарний підхід у збереженні здоров’я нації», який через пандемію COVID‑19 був проведений в онлайн-форматі з трансляцією на всі регіони України. До заходу долучилася величезна кількість лікарів, які отримали можливість прослухати виступи провідних міжнародних фахівців з Іспанії, Польщі, Нідерландів та Словенії, а також вітчизняних опініон-лідерів. Представлені на конгресі доповіді та майстер-класи охопили різні галузі медицини. Особлива увага була приділена алергічним захворюванням (АЗ), зокрема алергічному риніту (АР), і передусім – вибору оптимальної тактики лікування, оскільки в реальній клінічній практиці нерідко трапляються помилки саме при призначенні відповідних лікарських препаратів.
.jpg) Пропонуємо вашій увазі одну з доповідей щодо призначення антигістамінних препаратів (АГП) у терапії АЗ, представлену заступницею керівника Центру алергічних захворювань верхніх дихальних шляхів та вуха ДУ «Інститут отоларингології ім. О.С. Коломійченка НАМН України», доктором медичних наук Інною Володимирівною Гогунською.
Пропонуємо вашій увазі одну з доповідей щодо призначення антигістамінних препаратів (АГП) у терапії АЗ, представлену заступницею керівника Центру алергічних захворювань верхніх дихальних шляхів та вуха ДУ «Інститут отоларингології ім. О.С. Коломійченка НАМН України», доктором медичних наук Інною Володимирівною Гогунською.
– Збільшення поширеності АЗ у країнах із високим економічним рівнем триває вже понад 50 років, і вже через 3-5 років ми можемо зіткнутися з епідемією АЗ, оскільки на сьогодні сенсибілізація до одного і більше алергену спостерігається в 40-50% дітей шкільного віку, а на АР страждає 10-30% населення.
Згідно з усіма міжнародними рекомендаціями, у тому числі ARIA (ВООЗ), першою лінією терапії АР і хронічної кропив’янки є АГП ІІ-го покоління (АГП‑ІІ) завдяки відсутності побічних ефектів (ПЕ), характерних для АГП І-го покоління (АГП‑І). Але, на жаль, у рутинній клінічній практиці досі пацієнтам призначають АГП‑І, незважаючи на їхню небезпеку і незадовільну ефективність. Бувають також випадки самостійного їх прийому пацієнтами протягом тривалого часу, що ставить під сумнів доцільність безрецептурного відпуску цих лікарських засобів.
Механізм дії АГП
АГП – це велика група препаратів, дія яких реалізується завдяки взаємодії з гістаміном – медіатором алергічних реакцій негайного типу, які вже понад 70 років використовують у симптоматичному лікуванні різних АЗ.
Останні 50 років традиційно вважалося, що АГП є антагоністами Н1-рецепторів, проте цей термін є застарілим і не відображає точного механізму дії цих препаратів. Сьогодні йдеться про те, що АГП працюють як зворотні агоністи, які стабілізують неактивну конформацію Н1-рецепторів, зміщуючи рівновагу на користь неактивного стану.
АГП – це найбільший клас препаратів, що застосовують у лікуванні АЗ. Сьогодні на світовому фармацевтичному ринку присутні понад 45 найменувань АГП‑І і АГП‑ІІ. Чим же вони різняться? АГП‑І характеризуються вільним проникненням крізь гематоенцефалічний бар’єр (ГЕБ) і заповненням Н1-рецепторів, розташованих на постсинаптичних мембранах гістамінергічних нейронів по всій центральній нервовій системі (ЦНС). Саме з цією особливістю пов’язаний негативний ефект АГП‑І, який перевищує потенційну користь, особливо при тривалому застосуванні.
Ризики, пов’язані з Н1-АГП‑І: позиційний документ GA2LEN
H1-АГП‑І:
- зменшують фазу швидкого сну;
- погіршують навчання та знижують ефективність праці;
- збільшують ризики авіакатастроф і дорожньо-транспортних пригод у разі керування літаком або автомобілем людиною, яка приймає ці препарати;
- асоційовані з випадками смерті внаслідок випадкового або навмисного передозування у немовлят та дітей раннього віку;
- використовуються деякими особами різного віку для здійснення суїциду;
- іноді проявляють кардіотоксичність у разі передозування.
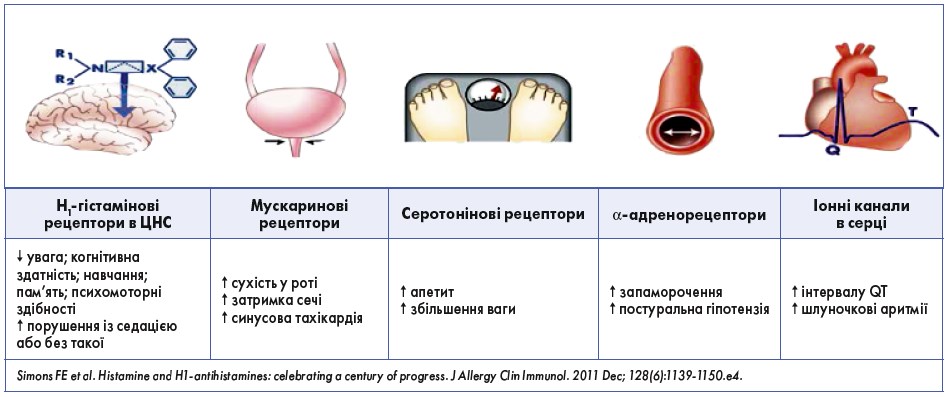
Широкий спектр і значна кількість ПЕ АГП‑І з боку різних органів і систем пов’язані з антимускариновою, антисеротоніновою і анти-α-адренергічною дією (рис.). Незважаючи на те що ці ПЕ добре відомі і значуще знижують якість життя, АГП‑І багатьма лікарями і пацієнтами сприймаються як безпечні внаслідок багаторічної історії застосування, що категорично неправильно, до того ж коли в арсеналі практикуючого фахівця є сучасні та безпечні АГП‑ІІ.
Рис. Побічні ефекти Н1-АГП‑І
Розподіл АГП залежно від седативного ефекту
АГП‑ІІ не проникають крізь ГЕБ, відповідно, вони позбавлені недоліків, характерних для АГП І-го покоління. Це було підтверджено за допомогою позитронно-емісійної томографії (ПЕТ) і показано, що ступінь окупації Н1-рецепторів у ЦНС (H1RO) може бути безпосередньо пов’язана з впливом на її функцію. За допомогою ПЕТ залежності від H1RO усі АГП було розділено на:
- неседативні (<20%);
- менш седативні (20-50%);
- седативні (≥50%).
Наприклад, у препараті кетотифен ступінь окупації Н1-рецепторів ЦНС сягає понад 80%, що зумовлює виражені ПЕ на тлі його застосування. Але, незважаючи на цей очевидний факт, деякі фахівці продовжують активно призначати цей препарат, зокрема і в педіатричній практиці. Це неприпустимо з огляду на наявність неседативних АГП, таких як біластин і олопатадин, які не проникають крізь ГЕБ, і H1RO у них становить 0%.
Варто наголосити, що біластин вигідно відрізняється і на фоні інших АГП‑ІІ, які мають здатність нехай незначного, але проникнення крізь ГЕБ. Так, у дезлоратадину і лоратадину, які належать до АГП‑ІІ, H1RO дорівнює 10% і 7% відповідно, що стає причиною седативного ефекту і сонливості при їх застосуванні. Це має неабияке значення в разі необхідності призначення подвійної дози препарату для досягнення швидкого ефекту або купірування тяжких проявів захворювання.
Різна ступінь проникнення крізь ГЕБ і окупація Н1-рецепторів у різних препаратів АГП залежать від низки факторів. Деякі речовини АГП‑ІІ потрапляють до ЦНС унаслідок мозкового кровообігу і пасивно переносяться в ендотелій ГЕБ. Однак, будучи субстратами gP, вони активно транспортуються ретроградно до мозкового кровообігу, і мінімальна кількість зв’язується з Н1-рецепторами в мозку. Коли препарати не є субстратами gP (наприклад, АГП‑І), вони потрапляють у мозковий кровообіг, проникають крізь ГЕБ і не видаляються з ЦНС, тісно зв’язуючись із Н1-рецепторами в мозку, та спричинюють свою побічну дію. Проте рівень вкладу P-глікопротеїну в здатність проникнення препаратів в мозок відрізняється залежно від хімічної структури молекули. Крім цього в процес проникнення речовини крізь ГЕБ залучені такі показники, як гідрофобність, молекулярна маса, електричний заряд і багато інших чинників, зокрема ферменти цитохрому P450, енантіомери та інше. Примітно, що в разі пасивної дифузії ступінь проникнення крізь ГЕБ тим вища, чим нижча молекулярна маса.
Деякі лікарські засоби з молекулярною масою <400 Da можуть проникати крізь ГЕБ завдяки пасивній дифузії, що пояснює різний седативний потенціал в окремих представників АГП‑ІІ. Так, молекулярна маса дезлоратадину становить 310 Da, лоратадину – 388 Da, біластину – 463 Da. При цьому треба зазначити, що при збільшенні молекулярної маси до 450 Da проникнення крізь ГЕБ зменшується в 100 разів. Таким чином, біластин має найменший ступінь дифузії та ймовірність проникнення крізь ГЕБ в порівнянні з дезлоратадином і лоратадином. Це обов’язково треба мати на увазі при виборі АГП для тривалого застосування, особливо за необхідності призначення більш високих доз, коли препарат накопичується в ЦНС. Так, під час розгляду залишкових явищ АГП на прикладі дифенгідраміну (50 мг) і кетотифену (1 мг) було доведено, що період напіврозпаду цих речовин у головному мозку приблизно вп’ятеро довший, ніж у плазмі, і становить 30 і 45 год відповідно. Звідси кумулятивний ефект і виражена седативна дія: порушення циркадного циклу сну й неспання, сонливість, порушення працездатності та уваги. Тому правильний вибір препарату забезпечує високий рівень якості життя пацієнта і хороший комплаєнс, оскільки більшість хворих на АЗ незадоволені результатами лікування.
Задоволеність пацієнтів лікуванням АР
Третина пацієнтів з АР незадоволені одержуваною терапією. З них 44% хотіли б більш швидкого полегшення симптомів, а 55% – тривалішої дії препарату. 2/3 хворих цікавляться найновішими препаратами для лікування алергії, які, можливо, були б ефективнішими і добре переносились, а 26% пацієнтів постійно шукають «свій» препарат, постійно їх змінюючи без рекомендацій лікаря.
З точки зору еволюції розвитку АГП, біластин є найновішою молекулою, яку було синтезовано в 2010 р. – останньою з цієї групи препаратів. Таким чином, біластин – це найновіший АГП‑ІІ з найбільшою кількістю властивостей із тих, що, відповідно до міжнародних рекомендацій ARIA, мають бути в сучасного антигістамінного засобу.
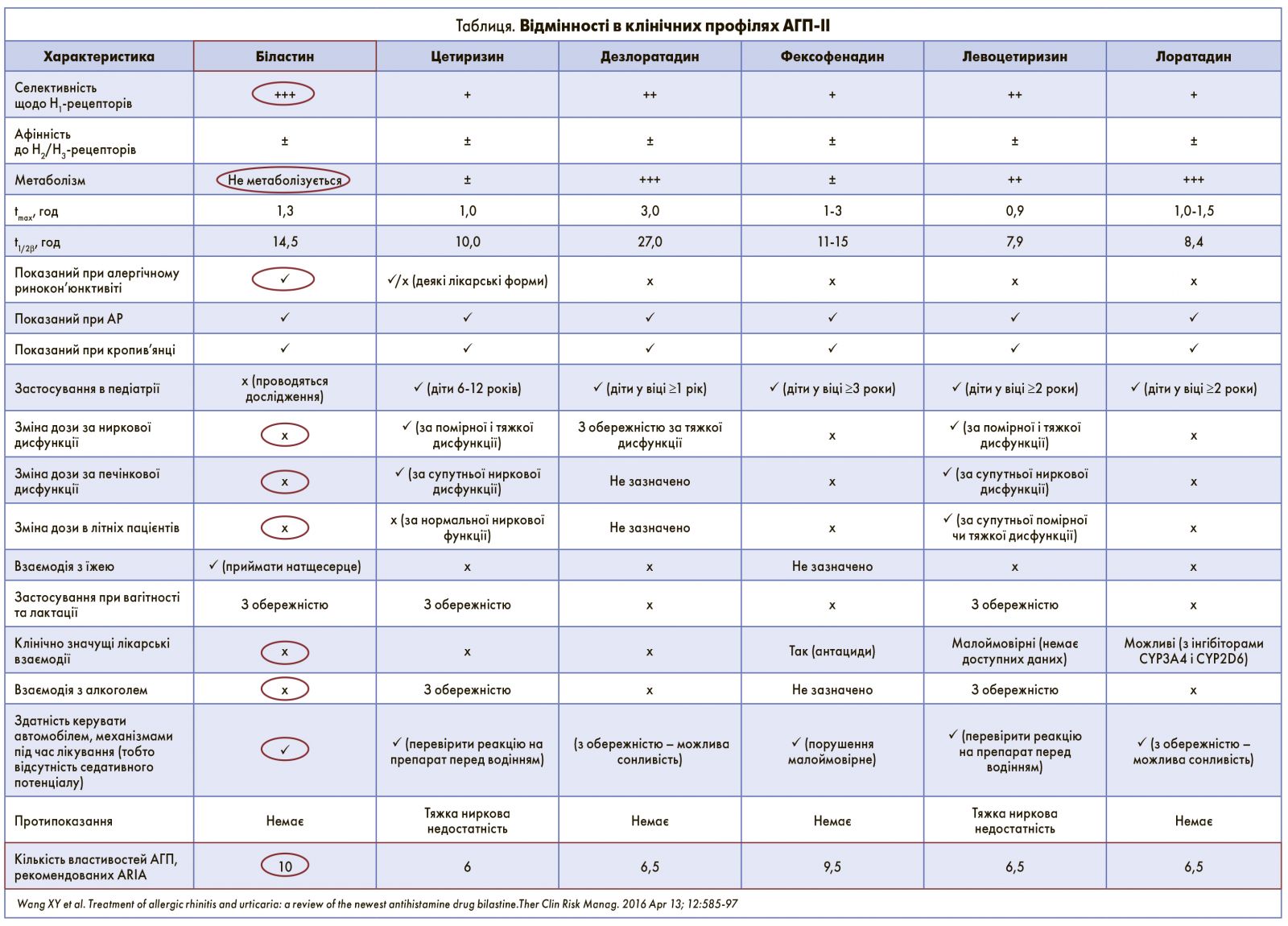
Експерти (Wang X.Y. et al., 2016) у своєму дослідженні визнали біластин відповідним критеріям ARIA. Автори порівняли кілька АГП між собою, нараховуючи їм по 0,5 бала за кожну відповідність критеріям ARIA. У результаті біластин отримав 10 балів, фексофенадин – 9,5 бала, дезлоратадин, ебастин, левоцетиризин і лоратадин – по 6,5 бала, цетиризин – 6 балів (табл.).
Згідно із зазначеними критеріями біластин має низку переваг:
- максимальна селективність Н1-рецепторів;
- не метаболізується в печінці, тому не взаємодіє з алкоголем, іншими лікарськими засобами, що дуже важливо для пацієнтів із супутньою патологією та при тривалому лікуванні алергічного захворювання;
- рекомендований при АР, кон’юнктивіті та кропив’янці;
- дозволений у педіатричній практиці;
- не потребує корекції дози при нирковій та печінковій недостатності, у літніх пацієнтів;
- не впливає на здатність керувати транспортним засобом і не має протипоказань.
При виборі найбільш оптимальних АГП‑ІІ необхідно враховувати багато факторів, зокрема безпеку та ефективність препарату, його вплив на психомоторні функції, наявність седативного ефекту. І як показали результати численних досліджень, біластин є кращим вибором завдяки своїй ефективності, безпеці, придатності для різних популяцій пацієнтів і відсутності седації.
Згідно з алгоритмом вибору АГП‑ІІ на підставі профілю пацієнта біластин може бути рекомендований пацієнтам із супутньою патологією, у разі порушення функції нирок або печінки, а також особам, професійна діяльність яких потребує високого рівня концентрації уваги.
За висновком експертів ARIA, біластин, завдяки своїм фармакологічним особливостям, результативності, безпеці та фармакодинамічним властивостям, відповідає критеріям EAACI/ARIA щодо лікарських засобів, які застосовуються в терапії АР.
Оригінальним препаратом біластину на фармацевтичному ринку України є Ніксар® . Він добре себе зарекомендував і відповідає всім критеріям вибору оптимального АГП, який дає можливість взяти під контроль найпоширеніші АЗ.
Ніксар® – оригінальний препарат біластину
- Відповідає вимогам ARIA і CONGA щодо сучасних АГП.
- Високоселективний щодо Н1-рецепторів.
- Ефективний для симптоматичного лікування АР, кон’юнктивіту і кропив’янки, що було доведено в ході низки клінічних досліджень.
- Швидке купірування симптомів – уже через 1 год, тривалий період дії – 24 год, що дає можливість використовувати його всього 1 раз на добу, тим самим підвищуючи прихильність пацієнтів до лікування.
- Не має седативної дії, негативного впливу на когнітивні функції та здатність керувати транспортом.
- Відсутні лікарські взаємодії.
- Можна застосовувати в дітей і літніх пацієнтів із супутньою патологією.
Підготувала Ірина Чумак
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (51), 2020 р.