12 серпня, 2020
Хвороба Паркінсона та поведінкові розлади при деменції
Наприкінці листопада 2019 р. у Києві відбувся грандіозний II Регіональний конгрес «Controversies in neurology» («Дебати в неврології»), акредитований Європейською радою з акредитації безперервної медичної освіти (EACCME). Представляємо до вашої уваги огляд виступів, що лунали на цьому форумі. Доповіді відображають сучасні погляди на контраверсійні питання сфери екстрапірамідних проявів та деменції у світі.
Чи є потреба додавати іМАО-Б пацієнтам із хворобою Паркінсона?
Відомо, що, на відміну від препаратів леводопи та агоністів дофамінових рецепторів (АДР), інгібітори моноаміноксидази типу Б (МАО-Б) є менш ефективними. З іншого боку, вони сприяють поліпшенню клінічної картини при виснаженні дози леводопи, скороченню періоду «вимкнення» та збільшенню періоду «увімкнення». Проте в деяких випадках ці препарати можуть викликати дискінезію, ортостатичну гіпотензію. Тож зазначене вище запитання є контраверсійним, тому в межах заходу були представлені дві протилежні точки зору.
 Провідний науковий співробітник відділу нейроінфекцій та розсіяного склерозу Інституту неврології, психіатрії та наркології НАМН України» (м. Харків), лікар-невропатолог, д. мед. н. Ірина В’ячеславівна Богданова акцентувала увагу на ролі МАО в організмі людини. Так, у разі дефіциту даного ферменту розвивається синдром Бруннера – порушення, що характеризується імпульсивною агресивністю та легкою олігофренією. Саме тому збалансована утилізація дофаміну є важливою складовою функціонування нервової системи. Однак за клінічно вираженого дефіциту дофаміну при хворобі Паркінсона (ХП) виникає потреба у гальмуванні такої утилізації. У цьому контексті були згадані іМАО-Б, що дозволяють посилити ефект леводопи при лікуванні ХП, а також зменшити утворення токсичних похідних амінів (Glover et al., 1993).
Провідний науковий співробітник відділу нейроінфекцій та розсіяного склерозу Інституту неврології, психіатрії та наркології НАМН України» (м. Харків), лікар-невропатолог, д. мед. н. Ірина В’ячеславівна Богданова акцентувала увагу на ролі МАО в організмі людини. Так, у разі дефіциту даного ферменту розвивається синдром Бруннера – порушення, що характеризується імпульсивною агресивністю та легкою олігофренією. Саме тому збалансована утилізація дофаміну є важливою складовою функціонування нервової системи. Однак за клінічно вираженого дефіциту дофаміну при хворобі Паркінсона (ХП) виникає потреба у гальмуванні такої утилізації. У цьому контексті були згадані іМАО-Б, що дозволяють посилити ефект леводопи при лікуванні ХП, а також зменшити утворення токсичних похідних амінів (Glover et al., 1993).
Найвідомішим представником групи іМАО-Б є селегілін, що призначають при ХП або симптоматичному паркінсонізмі як монотерапію на початкових стадіях чи в комбінації з препаратами леводопи при виникненні флуктуацій. У дослідженні DATATOP не вдалося підтвердити нейропротекторну дію селегіліну, додатковий симптоматичний ефект при моторних флуктуаціях виявився незначним. У зв’язку з появою дієвіших лікарських засобів, як-от АДР, інгібітори катехоламін-O-метилтрансферази (КОМТ), селегілін нечасто застосовують у клінічній практиці (Koller et al., 2007; Stocchi, 2006).
Важливим аргументом на користь обмеженого застосування селегіліну є ризик розвитку серотонінового синдрому (особливо при супутньому використанні інгібіторів зворотного захоплення серотоніну та/або норадреналіну, трициклічних антидепресантів, агоністів серотоніну – суматриптану, золмітриптану та ін.), а також гіпотензивних реакцій (при одночасному прийманні іМАО-А або неселективних інгібіторів МАО). Доповідачка навела дані, згідно з якими застосування комбінації леводопи та іМАО-Б у пацієнтів із початковою стадією ХП призводило до підвищення рівня смертності порівняно з монотерапією леводопою (28 та 18% відповідно, р=0,005). Така комбінація також сприяла розвитку помірної та тяжкої дискінезії з частотою 40 і 25% відповідно (р=0,04) (Lees, 1995).
Представником нового покоління із групи іМАО-Б є разагілін, ефективність якого у плані зменшення виразності основних симптомів паркінсонізму різної тяжкості при ХП було продемонстровано у дослідженнях TEMPO, PRESTO, LARGO. У клінічному випробуванні ADAGIO додатково виявлено нейропротекторний ефект і безпеку раннього та відтермінованого на шість місяців застосування разагіліну в дозі 1 мг/добу при ХП (Левін, 2010). Лекторка зазначила, що, завдяки зафіксованому хворобомодифікувальному впливу раннього призначення разагіліну, автори дослідження ADAGIO підкреслили виняткову актуальність ранньої діагностики ХП. Бажано проводити її на премоторній та преклінічній стадіях. Так, було показано кращий стан моторної функції протягом наступних шістьох років у пацієнтів, які розпочали приймання разагіліну на шість місяців раніше, що свідчило про безсумнівний вплив препарату на фундаментальні механізми патогенезу ХП. У додатковому аналізі в межах ADAGIO також виявлено, що застосування разагіліну сприяло сповільненню прогресування проявів втоми протягом дев’ятьох місяців лікування (Stocchi, 2014).
 Лікар-невропатолог Обласного клінічного центру нейрохірургії та неврології (м. Ужгород) Катерина Олегівна Карпінська виклала у своїй доповіді неоднозначні аргументи щодо ефективності препаратів для терапії ХП. Вона навела низку свідчень не на користь застосування селегіліну, приймання якого може супроводжуватися (Churchyard et al., 1997):
Лікар-невропатолог Обласного клінічного центру нейрохірургії та неврології (м. Ужгород) Катерина Олегівна Карпінська виклала у своїй доповіді неоднозначні аргументи щодо ефективності препаратів для терапії ХП. Вона навела низку свідчень не на користь застосування селегіліну, приймання якого може супроводжуватися (Churchyard et al., 1997):
- ризиком виникнення тирамінового синдрому, коли на тлі вживання сирів в організмі накопичується надлишок тираміну, механізм дії якого подібний до такого амфетамінових психостимуляторів; при підвищенні терапевтичної дози селегіліну утворюється більша кількість амфетаміну й метамфетаміну, що призводить до периферичного інгібування МАО-А серцево-судинної системи, вивільнення катехоламінів і, як наслідок, гіпертензивного кризу;
- ризиком розвитку серотонінового синдрому: на тлі супутнього приймання серотонінергічних препаратів може виникнути потенійно фатальний стан з галюцинаціями, лихоманкою, тахікардією, гастроінтестинальними симптомами;
- підвищенням показника летальності, пов’язаної з гострими серцево-судинними захворюваннями у пацієнтів, які отримують селегілін та леводопу.
Разагілін, на відміну від селегіліну, не метаболізується до амфетаміноподібних речовин і характеризується у десять разів вищою селективністю інгібування МАО-Б. Однак у дослідженні PRESTO виявлено, що разагілін суттєво подовжував період «вимкнення» із драматичними дискінезіями.
Сафінамід – некласичний іМАО-Б короткої дії, який не блокує рецептори N-метил-D-аспартату на відміну від амантадину. Сафінамід активує Na+ та Ca2+-канали, що сприяє зменшенню аномально високого вивільнення глутамату. У дослідженні SETTLE ефективність сафінаміду було підтверджено в аспекті зменшення періоду «вимкнення», збільшення періоду «увімкнення» та поліпшення бальної оцінки за уніфікованою рейтинговою шкалою оцінки хвороби Паркінсона (UPDRS). Загалом результати трьох ключових подвійних сліпих плацебо-контрольованих випробувань Study 016, Study 018 та SETTLE показали, що сафінамід у дозі 100 мг/добу сприяв скороченню моторних коливань та дискінезії у пацієнтів, які отримували леводопу (як монотерапію або в комбінації з іншими супутніми антипаркинсонічними препаратами). Крім того, за терапії сафінамідом зменшувалися прояви брадикінезії, ригідності та тремору, поліпшувалася хода. На додачу, сафінамід значно впливав на невропатичний біль. Ці результати можуть бути пояснені подвійним механізмом дії, який модулює змінену дофамінергічну та глутаматергічну нейротрансмісію.
Доповідачка наголосила також на необхідності виключення супутнього приймання декстрометорфану, опіоїдів, антидепресантів. Найчастішими побічними реакціями при застосуванні сафінаміду є дискінезія, падіння, нудота та безсоння. Результати дослідження MOTION підтвердили ефективність сафінаміду (при одночасному використанні з АДР) у пацієнтів із ранніми стадіями ХП.
Метааналіз C.D. Binde et al. (2018) дозволив оцінити ефект від застосування відомих іМАО-Б в осіб із ХП як монотерапії або в комбінації з леводопою/АДР. Було виявлено, що всі включені іМАО-Б були ефективними порівняно із плацебо як монотерапія та при застосуванні разом із леводопою. У разі поєднання з леводопою селегілін був найдієвішим, а разагілін – другим за ефективністю.
Підсумовуючи, К.О. Карпінська акцентувала увагу на тому, що при виборі тактики боротьби з дискінезіями та моторними флуктуаціями нині на перший план виходять більш ефективні та довготривалі методи корекції: підшкірне/сублінгвальне введення апоморфіну, застосування комбінації карбідопи/леводопи, а також препарату карбідопи та леводопи (дуопа) у формі гелю для дуоденальної інфузії.
Німецький підхід до застосування іМАО-Б
 Декан медичного факультету, голова кафедри неврології Дрезденського університету, президент Німецького неврологічного товариства, науковий співробітник Королівського медичного коледжу Великої Британії та Американської академії неврології, доктор медицини, професор Хайнц Райхманн (Heinz Reichmann) доповнив сателітний симпозіум фактами із власного досвіду та принципами універсальної тактики лікування пацієнтів у Німеччині. Так, селегілін ефективний у монотерапії та в комбінації з леводопою, але, на відміну від разагіліну, призводить до виникнення синдрому втоми та сонливості, а також побічних ефектів, пов’язаних з амфетаміноподібним ефектом (Olanow et al., 1992; Abu-Baya et al., 2002).
Декан медичного факультету, голова кафедри неврології Дрезденського університету, президент Німецького неврологічного товариства, науковий співробітник Королівського медичного коледжу Великої Британії та Американської академії неврології, доктор медицини, професор Хайнц Райхманн (Heinz Reichmann) доповнив сателітний симпозіум фактами із власного досвіду та принципами універсальної тактики лікування пацієнтів у Німеччині. Так, селегілін ефективний у монотерапії та в комбінації з леводопою, але, на відміну від разагіліну, призводить до виникнення синдрому втоми та сонливості, а також побічних ефектів, пов’язаних з амфетаміноподібним ефектом (Olanow et al., 1992; Abu-Baya et al., 2002).
Разагілін – єдиний затверджений лікарський засіб для монотерапії ХП у Німеччині, що характеризується високою ефективністю без явних побічних проявів. У протоколах терапії багатьох країн рекомендації щодо застосування препарату відповідають рівню доказовості А (таблиця).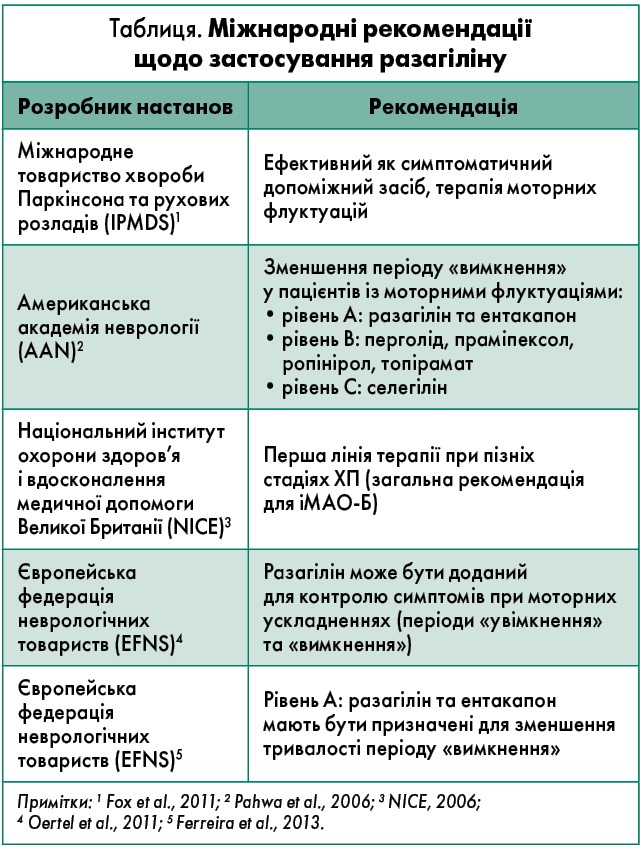
До того ж разагілін у дозі 1 мг/добу може чинити хворобомодифікувальний вплив, але даний факт наразі досліджується більш детально (Parkinson study group, 2005). Професор Х. Райхманн акцентував увагу на тому, що наслідки застосування разагіліну залежать від генетичних особливостей. Нині неможливо масово враховувати цей параметр індивідуальної чутливості, але слід брати його до уваги при формуванні висновків про ефективність разагіліну на підставі суперечливих клінічних результатів використання іМАО-Б. У даному контексті доповідач підкреслив, що в пацієнтів, які приймають разагілін, посилення дискінезії відсутнє. Основний беззаперечний результат застосування препарату є протилежним – це зменшення проявів дискінезії. Додатковим позитивним ефектом є послаблення проявів брадікінезії, тремору, ранкової акінезії та скорочення періоду «вимкнення» (Reichmann et al., 2013; Chapuis et al., 2012).
Своєю чергою сафінамід – препарат третього покоління іМАО-Б, що характеризується подвійним ефектом, а саме інгібуванням МАО-Б та антиглутаматергічним впливом. Він займає нішу препарату для успішної корекції дискінезій на тлі приймання леводопи й допомоги пацієнтові з немоторними проявами: невропатичним болем, тривогою, депресією, безсонням та зниженням якості життя (Bianchi et al., 2019).
Чи слід призначати леводопу як препарат ініціальної терапії при ХП?
 Завідувач кафедри неврології та нейрохірургії факультету післядипломної освіти Вінницького національного медичного університету імені М.І. Пирогова, к. мед. н., доцент Геннадій Сергійович Московко представив доповідь, присвячену золотому стандарту лікування ХП – леводопі, одному з варіантів початкової терапії ХП та єдиному оптимальному на розгорнутій стадії хвороби. Лектор навів дані, згідно з якими можливі опції стартової терапії ХП включають призначення (Warren, 2015; Olanow et al., 2004):
Завідувач кафедри неврології та нейрохірургії факультету післядипломної освіти Вінницького національного медичного університету імені М.І. Пирогова, к. мед. н., доцент Геннадій Сергійович Московко представив доповідь, присвячену золотому стандарту лікування ХП – леводопі, одному з варіантів початкової терапії ХП та єдиному оптимальному на розгорнутій стадії хвороби. Лектор навів дані, згідно з якими можливі опції стартової терапії ХП включають призначення (Warren, 2015; Olanow et al., 2004):
- леводопи;
- прямих АДР (ерготамінових/неерготамінових, праміпексолу, ропініролу, ротиготину, апоморфіну);
- іМАО-Б (разагіліну, селегіліну, сафінаміду);
- амантадину;
- блокаторів ацетилхолінових рецепторів (тригексифенідилу).
Тож виникає потреба у визначенні профілю ефективності та безпеки леводопи на початковому етапі ХП. Спершу, на думку Г.С. Московка, слід розглянути шлях метаболізму леводопи в організмі. Він включає декарбоксилювання у дофамін, який окиснюється з утворенням пероксиду водню, що надалі нейтралізується глутатіоном з утворенням неактивних речовин. За браку достатньої кількості глутатіону пероксид водню вступає у реакцію із двовалентним залізом, перетворюючи його на тривалентне (реакція Фентона), яке, своєю чергою, є токсичним для клітин (Spencer et al., 1998; Dexter et al., 1994). У чорній субстанції пацієнтів із ХП виявляють різке зниження вмісту глутатіону з відповідним зростанням кількості пероксиду водню та токсичного тривалентного заліза й розвитком закономірної нейродегенерації.
Таким чином, стають зрозумілими результати дослідження in vitro, за якими додавання великої дози леводопи до культури клітин викликало некроз та апоптоз (Basma et al., 1995; Ziv et al., 1997). Натомість застосування малої кількості сприяло нейропротекторному ефекту й виділенню антиоксиданту глутатіону (Mytilineou et al., 1993; Han et al., 1996). Цікавим є той факт, що додавання антиоксиданту блокувало як цитотоксичний, так і нейропротекторний ефекти (Mytilineou et al., 1993).
Однак дослідження in vivo на лабораторних тваринах (як здорових, так і з індукованим паркінсонізмом) не показало токсичного впливу леводопи на клітини чорної субстанції (Murer et al., 1998; Datla et al., 2001). За словами спікера, це можна пояснити тим, що в центральну нервову систему надходить 12‑15% леводопи, прийнятої пероральним шляхом, а тому доза є невеликою та нетоксичною. Проте навіть після зниження вмісту глутаміну (за рахунок введення бутіоніну сульфоксиміну) не було виявлено цитотоксичної дії леводопи на клітини чорної субстанції (Mytilineou et al., 2003).
Щодо клінічних випробувань, результати не продемонстрували відмінностей за кінцевими точками для пацієнтів із ХП, які почали отримувати леводопу на ранній або пізній стадії захворювання (Diamond et al., 1990). У дослідженні PD-MED через три роки спостереження не було виявлено різниці між ефектами леводопи, АДР та іМАО-Б, оцінених за 39-пунктовим опитувальником щодо імпульсивно-компульсивних розладів при ХП (PDQ‑39) (Gray et al., 2014). Проте у випробуванні ELLDOPA, присвяченому аналізу впливу раннього та відстроченого призначення леводопи, були отримані неоднозначні результати однофотонної емісійної томографії. У пацієнтів, які приймали леводопу, відзначався значний ступінь зниження поглинання радіоактивного аналога дофаміну пресинаптичними нігростріарними закінченнями, що може розцінюватися як результат скорочення їхньої кількості, а отже, нейротоксичного ефекту леводопи. Проте зміна показників поглинання аналога дофаміну, ймовірно, зумовлена не нейротоксичною, а фармакологічною дією леводопи на дофамінові транспортери (білки, які контролюють пресинаптичне захоплення дофаміну) (Fahn et al., 2004).
Доповідач навів дані щодо порівняння груп пацієнтів, які отримували терапію леводопою або АДР:
- Через 3‑5 років спостереження у групі леводопи спостерігалася вища частота рухових коливань та дискінезій, більш рання їхня поява, але краща ефективність терапії, а при використанні АДР – менше рухових ускладнень, пізніше виникнення, однак нижча дієвість лікування.
- Через більш ніж п’ять років спостереження частота рухових коливань та дискінезій зрівнялася, а ефективність терапії була вищою у групі приймання леводопи (Zhang et al., 2016).
Насамкінець доповіді Г.С. Московко зазначив, що питання стосовно призначення леводопи дійсно є контраверсійним і потребує прицільного розгляду.
Чому леводопу може бути призначено як препарат першої лінії?
.jpg) Професор Хайнц Райхманн нагадав присутнім, що згідно з сучасним підходом препарати леводопи призначають при помірній та тяжкій інвалідизації внаслідок ХП, пацієнтам віком від 70‑75 років або за наявності серйозної коморбідності, включно з виразним когнітивним дефіцитом. За помірного/значного рухового дефіциту та без проявів когнітивної недостатності слід віддати перевагу АДР, а за легкого моторного дефіциту без порушення когнітивних функцій – АДР або іМАО-Б (Schapira, 2007).
Професор Хайнц Райхманн нагадав присутнім, що згідно з сучасним підходом препарати леводопи призначають при помірній та тяжкій інвалідизації внаслідок ХП, пацієнтам віком від 70‑75 років або за наявності серйозної коморбідності, включно з виразним когнітивним дефіцитом. За помірного/значного рухового дефіциту та без проявів когнітивної недостатності слід віддати перевагу АДР, а за легкого моторного дефіциту без порушення когнітивних функцій – АДР або іМАО-Б (Schapira, 2007).
Однак безпека такої стратегії, особливо в осіб молодого віку, ставиться під сумнів, оскільки, за даними D. Weintraub et al. (2010), АДР підвищують ризик розвитку розладів імпульсного контролю (РІК), як-то схильність до азартних ігор, компульсивних купівель, розлади харчової поведінки, компульсивна сексуальна поведінка. Втім, слід враховувати, що кожний представник даного класу препаратів характеризується індивідуальними характеристиками. Так, показано, що терапія ротиготином супроводжується меншою вірогідністю появи РІК (Rizos et al., 2014). За даними D. Weintraub et al. (2010), приймання амантадину також асоціювалося з розвитком РІК.
З іншого боку, використання леводопи у 55% пацієнтів призводить до виникнення таких побічних явищ, як період «вимкнення», а у 23% спричиняє дискінезію (Lieberman et al., 2004). Ризик розвитку цих небажаних реакцій зменшується за призначення комбінації леводопи/карбідопи (Dhall et al., 2016). Професор Х. Райхманн також зазначив, що підбір оптимальної дози леводопи з урахуванням маси тіла хворого (4 мг/кг для чоловіків та 5 мг/кг для жінок), при розв’язанні питання щодо потреби у паралельному призначенні АДР, а також за потенційного використання помпи з підшкірним введенням леводопи/карбідопи (при ХП на пізній стадії) дозволяє уникнути несприятливих ефектів та успішно використовувати леводопу на ранніх термінах ХП, особливо у пацієнтів, що потребують повної компенсації рухових обмежень хвороби (піаністів, нейрохірургів тощо).
Чому не слід призначати леводопу як препарат першої лінії?
 Директорка Центру рухових розладів лікарні імені Св. Анни Університету Масарика (Брно, Чехія) Ірена Ректорова (Irena Rektorova) акцентувала увагу на ризику розвитку дискінезій у разі приймання леводопи в дозі понад 400 мг/добу. Запобігти появі пов’язаних із леводопою ускладнень можливо, якщо віддати перевагу АДР, які характеризуються дещо меншою ефективністю, але є зручними у використанні (1 раз на добу в таблетованій формі; є також форми для підшкірного введення) та дієві у плані корекції нерухових проявів ХП (Goetz et al., 2002; Horstink et al., 2006).
Директорка Центру рухових розладів лікарні імені Св. Анни Університету Масарика (Брно, Чехія) Ірена Ректорова (Irena Rektorova) акцентувала увагу на ризику розвитку дискінезій у разі приймання леводопи в дозі понад 400 мг/добу. Запобігти появі пов’язаних із леводопою ускладнень можливо, якщо віддати перевагу АДР, які характеризуються дещо меншою ефективністю, але є зручними у використанні (1 раз на добу в таблетованій формі; є також форми для підшкірного введення) та дієві у плані корекції нерухових проявів ХП (Goetz et al., 2002; Horstink et al., 2006).
Достовірно встановлено, що монотерапія АДР на 87% знижує ризик розвитку дискінезії порівняно з леводопою (р<0,001). Імовірність виникнення дискінезії не залежить від дози АДР, тривалості захворювання та курсу лікування. Саме тому доцільно використовувати монотерапію АДР на ранній стадії ХП у дозах, які забезпечують ефективність та відстрочують потребу в леводопі (Chondrogiorgi et al., 2014).
Відомо, що АДР можуть збільшувати ризик виникнення РІК (Voon et al., 2007; Weintraub et al., 2010; Rektorova, 2019). Спираючись на дані D. Weintraub et al. (2010), при виборі між леводопою та АДР слід враховувати такі фактори ризику розвитку РІК, як:
- молодий вік;
- чоловіча стать;
- ранній початок ХП;
- особистий або сімейний анамнез зловживання алкоголем (гемблінг, куріння);
- імпульсивність у характері;
- брак досвіду подружнього життя;
- генетична схильність.
На думку доповідачки, стосовно галюцинацій, які можуть бути спровоковані застосуванням АДР, не слід ігнорувати факт, що даний симптом може бути не лише побічним явищем терапії, але й типовим для захворювання проявом навіть на премоторній стадії (Pagonabarraga et al., 2015). Додатково було зазначено, що результати останніх досліджень свідчать про провідну роль у виникненні галюцинацій при ХП не дофаміну, а серотоніну (Ballanger, 2010). Такий погляд підтверджується успішним використанням новітнього препарату пімавансерину, що діє як зворотний агоніст і антагоніст рецепторів серотоніну 5-НТ2А і 5-НТ2С та ліцензований для лікування психозу й галюцинацій при ХП у США.
Загалом АДР можуть бути корисними за наявності депресії, апатії, безсоння, мікрогалюцинацій, порушень автономної регуляції, гіпоосмії, когнітивних порушень.
І. Ректорова підсумувала, що вибір лікувальної тактики має бути обґрунтованим з огляду на анамнез, симптоми та потенційний індивідуальний ризик у кожному клінічному випадку.
Чи може камптокормія бути проявом дистонії внаслідок застосування АДР?
Професор Х. Райхманн зазначив, що камптокормія (стійке збереження неприродної позиції тулуба) може бути проявом дистонії, побічним явищем приймання АДР, а також деяких міопатій (наприклад, лице-лопаткової форми прогресуючих м’язових дистрофій). За кожного виявлення даного симптому слід детально розглянути клінічний випадок для остаточного встановлення причини.
Камптокормія як поліетіологічний симптом
 Завідувач відділення неврології № 1 Обласної клінічної лікарні імені І.І. Мечникова (м. Дніпро) Вадим Іванович Пашковський перелічив нозології, за яких може спостерігатися феномен камптокормії. Це мультисистемна атрофія, ХП, м’язова дистонія, хвороба Альцгеймера (ХА), есенціальний тремор, синдром Туретта, вторинні міопатії (гіотиреоз, дерматоміозит, міозит), хронічна запальна демієлінізувальна поліневропатія, розсіяний склероз, травми, новоутворення; зустрічається також медикаментозно-індукована камптокормія (при терапії оланзапіном, донепезилом, вальпроатами, стероїдами, АДР).
Завідувач відділення неврології № 1 Обласної клінічної лікарні імені І.І. Мечникова (м. Дніпро) Вадим Іванович Пашковський перелічив нозології, за яких може спостерігатися феномен камптокормії. Це мультисистемна атрофія, ХП, м’язова дистонія, хвороба Альцгеймера (ХА), есенціальний тремор, синдром Туретта, вторинні міопатії (гіотиреоз, дерматоміозит, міозит), хронічна запальна демієлінізувальна поліневропатія, розсіяний склероз, травми, новоутворення; зустрічається також медикаментозно-індукована камптокормія (при терапії оланзапіном, донепезилом, вальпроатами, стероїдами, АДР).
Феномен камптокормії в осіб із ХП розвивається за певних умов, як-то похилий вік, чоловіча стать, раннє приєднання аксіальних симптомів (порушення мови, ковтання, постуральна нестійкість). Уперше медикаментозно-індукований феномен виявили у пацієнта, який приймав праміпексол; після скасування препарату він регресував. Подібний випадок описаний у хворого, що лікувався ропініролом.
 Професорка кафедри неврології № 1 Національної медичної академії післядипломної освіти імені П.Л. Шупика (м. Київ), д. мед. н. Тетяна Миколаївна Слободін додала до переліку можливих причин камптокормії бічний аміотрофічний склероз, деменцію з тільцями Леві, дистонію та міастенію. Особливу увагу доповідачка приділила мультистемній атрофії, за якої дофамінергічні препарати можуть бути пусковим фактором (а не причиною) для прояву камптокормії як поширеного симптому даної патології. Т.М. Слободін порекомендувала також не забувати про «паркінсонізм-дистонію».
Професорка кафедри неврології № 1 Національної медичної академії післядипломної освіти імені П.Л. Шупика (м. Київ), д. мед. н. Тетяна Миколаївна Слободін додала до переліку можливих причин камптокормії бічний аміотрофічний склероз, деменцію з тільцями Леві, дистонію та міастенію. Особливу увагу доповідачка приділила мультистемній атрофії, за якої дофамінергічні препарати можуть бути пусковим фактором (а не причиною) для прояву камптокормії як поширеного симптому даної патології. Т.М. Слободін порекомендувала також не забувати про «паркінсонізм-дистонію».
Додаткову інформацію про походження камптокормії можна отримати в результаті аналізу ефективних стратегій терапії за наявності симптому. Серед них глибинна мозкова стимуляція, спрямована на globus pallidus interna (підтверджує зв’язок камптокормії з дистонією), застосування леводопи (якщо камптокормія є проявом періоду «вимкнення» або хвороби Сегави), ботулінічного токсину (ефект виражений при сегментарній дистонії), холінолітиків, скасування АДР.
Фармакологічна корекція поведінкових розладів при деменції: бути чи не бути?
 Співробітник Королівського коледжу лікарів та хірургів Канади, спеціаліст із геріатричної та внутрішньої медицини Олег Весельський (Oleg Veselskiy) представив результати дослідження J.A. Schneider et al. (2006), в якому 421 пацієнт із ХА отримував терапію рисперидоном, оланзапіном, кветіапіном або плацебо. Це випробування зупинили через 40 тижнів у зв’язку з виникненням побічних ефектів лікарських засобів.
Співробітник Королівського коледжу лікарів та хірургів Канади, спеціаліст із геріатричної та внутрішньої медицини Олег Весельський (Oleg Veselskiy) представив результати дослідження J.A. Schneider et al. (2006), в якому 421 пацієнт із ХА отримував терапію рисперидоном, оланзапіном, кветіапіном або плацебо. Це випробування зупинили через 40 тижнів у зв’язку з виникненням побічних ефектів лікарських засобів.
У роботі V.A. Mittal et al. (2011) було виявлено, що приймання антипсихотиків підвищує ризик цереброваскулярних катастроф та показник летальності в осіб похилого віку.
Саме на підставі зазначених досліджень Управління з контролю за якістю харчових продуктів та лікарських засобів США (FDA) сформулювало застереження стосовно використання атипових антипсихотиків у пацієнтів із поведінковими та психічними проявами деменції. Однак, незважаючи на таку рекомендацію, світовий досвід свідчить, що препарати даної групи єдині в сучасному арсеналі та застосовуються за крайньої потреби.
Лектор представив перелік поведінкових розладів, що можуть піддаватися медикаментозній корекції:
- агресія;
- ажитація;
- психоз;
- депресія;
- тривога;
- апатія;
- проблеми зі сном.
Психіатри пропонують використовувати такі препарати: рисперидон, кветіапін; арипіпразол, карбамазепін, циталопрам, габапентин, празозин. У разі терапії ажитації та агресії рекомендовано віддавати перевагу празозину та лоразепаму, а для корекції проявів ХА – інгібіторам ацетилхолінестерази та мемантину (Davies, 2018).
О. Весельський акцентував увагу на новому атиповому антипсихотику пімавансерині, розробленому для терапії психозів (галюцинації, марення), асоційованих із деменцією (Cummings et al., 2018). Препарат характеризується ефективністю без порушення моторної функції. Це відрізняє його від інших антипсихотиків (арипіпразол, оланзапін, рисперидон), які посилюють прояви паркінсонізму (Jack et al., 2017).
Додатково доповідач навів оптимістичні дані стосовно результатів попереднього 10-тижневого рандомізованого клінічного дослідження ефективності комбінації декстрометорфану/хінідину в пацієнтів з імовірною ХА. Було показано її клінічно значущий вплив при збудженні та безпечний профіль. Тобто терапія не асоціювалася з когнітивними порушеннями, седацією або клінічно значущим подовженням інтервалу QT (Cummings et al., 2015).
Що стосується циталопраму, серед осіб з імовірною ХА та збудженням, які отримували психосоціальне втручання, додавання циталопраму порівняно із плацебо сприяло значному зменшенню збудження пацієнтів та дистресу доглядальників. Однак когнітивні та серцеві несприятливі ефекти циталопраму можуть обмежувати його практичне застосування у дозуванні 30 мг/добу (Porsteinsson et al., 2014).
M. Ruthirakuhan et al. (2019) дійшли висновку, що ефективність канабіноїдів при збудженні та агресії у пацієнтів із ХА лишається непереконливою, хоча може свідчити про потенційну користь синтетичних канабіноїдів. Тож слід ретельно контролювати безпеку, оскільки терапія канабіноїдами пов’язана з посиленням седативного ефекту. Для лікування ажитації також може бути ефективним препарат набілон. Однак потрібний всебічний моніторинг несприятливих явищ у вигляді седації та минущого когнітивного зниження (Herrmann et al., 2019).
Насамкінець О. Весельський зауважив, що при обережному застосуванні та контролі появи можливих побічних реакцій психофармакологічні підходи можуть бути корисними та потенціювати нефармакологічні методи корекції психічних і поведінкових розладів у пацієнтів із деменцією.
 У ролі опонента виступила асистент кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету, лікар-психіатр, к. мед. н. Ніна Василівна Софілканич. Лекторка зазначила, що при виникненні поведінкових симптомів насамперед слід визначити об’єктивну причину такого стану. Це можуть бути незадоволені потреби (голод, спрага, іммобілізація, біль, невдале позиціонування), медичний стан (біль, інфекція, вплив препаратів, дегідратація), проблеми зовнішнього оточення тощо (рівень освітлення, сусіди, гіперстимуляція/ізоляція).
У ролі опонента виступила асистент кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету, лікар-психіатр, к. мед. н. Ніна Василівна Софілканич. Лекторка зазначила, що при виникненні поведінкових симптомів насамперед слід визначити об’єктивну причину такого стану. Це можуть бути незадоволені потреби (голод, спрага, іммобілізація, біль, невдале позиціонування), медичний стан (біль, інфекція, вплив препаратів, дегідратація), проблеми зовнішнього оточення тощо (рівень освітлення, сусіди, гіперстимуляція/ізоляція).
Доповідачка нагадала присутнім, що використання галоперидолу (0,5‑2,0 мг), рисперидону (0,2‑1,0 мг), оланзапіну (2,5‑7,5 мг), кветіапіну (<50‑100 мг), арипіпразолу (<2‑10 мг) та зипразидону (20‑40 мг) характеризується підвищеним ризиком, що значно переважає користь. Так, у пацієнтів, пролікованих рисперидоном, частіше проявлялися екстрапірамідні побічні явища, сонливість, периферичні набряки, лихоманка порівняно із групою контролю. При використанні оланзапіну у хворих було виявлено порушення ходи, сонливість та лихоманку (Ballard et al., 2006).
На додачу, слід зазначити, що у межах дослідження L. Schneider et al. (2006) побічними ефектами приймання рисперидону або оланзапіну були переважно сонливість та інфекція сечовивідних шляхів, нетримання сечі, а також екстрапірамідні симптоми або порушення ходи. Результати когнітивних тестів теж виявили погіршення стану. Не було доказів зростання частоти травм, падінь чи синкопе, але підтвердився значний ризик виникнення цереброваскулярних подій, особливо у групі рисперидону. Повідомлялося про підвищену вірогідність загальної смертності.
Детально ризик летальних наслідків було розглянуто у дослідженні T. Gerhard et al. (2014). Згідно з отриманими результатами, при терапії рисперидоном, оланзапіном та галоперидолом було продемонстровано залежність ризику смерті від дози. Значні відмінності щодо вірогідності летальних випадків при лікуванні антипсихотичними препаратами свідчать про те, що вибір та дозування можуть вплинути на виживання літніх пацієнтів.
Враховуючи наведені тривожні дані про наслідки використання атипових антипсихотичних засобів, Н.В. Софілканич закликала застосовувати доступне нефармакологічне лікування, що є вибором першої лінії при поведінкових розладах. З-поміж них варто відзначити сенсорну стимуляцію, арома-, світло- та музикотерапію, а також поведінкові методи: гальмування небажаної поведінки, диференційне підкріплення, залучення тварин.
Підготувала Маргарита Марчук
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 2 (53) 2020 р.


