31 жовтня, 2020
Вплив цинку на розвиток інфекційної діареї у дітей
.jpg) В останні роки гострі захворювання кишечнику у дітей посідають друге місце серед усіх інфекційних хвороб, поступаючись лише захворюванням дихальних шляхів [1]. За даними Всесвітньої організації охорони здоров’я (ВООЗ), щорічно в світі реєструється близько 1,7 млрд випадків гострої діареї (ГД) у дітей, від якої помирають 525 тис. пацієнтів віком до 5 років [2]. За даними Міністерства охорони здоров’я, у 2017-2018 рр. в Україні було зареєстровано близько 120 тис. випадків діарейних захворювань [3].
В останні роки гострі захворювання кишечнику у дітей посідають друге місце серед усіх інфекційних хвороб, поступаючись лише захворюванням дихальних шляхів [1]. За даними Всесвітньої організації охорони здоров’я (ВООЗ), щорічно в світі реєструється близько 1,7 млрд випадків гострої діареї (ГД) у дітей, від якої помирають 525 тис. пацієнтів віком до 5 років [2]. За даними Міністерства охорони здоров’я, у 2017-2018 рр. в Україні було зареєстровано близько 120 тис. випадків діарейних захворювань [3].
Гострі кишкові інфекції (ГКІ) підвищують ризик розвитку невідкладних станів, тяжких форм захворювання та постінфекційних змін [4]. Спостерігається також і зміна етіології гострого гастроентериту у дітей. Структура ГКІ визначається епідеміологічною ситуацією в країні, соціально-економічними умовами життя населення, а також віком хворих [5]. Для ГКІ й раніше була характерна поліетіологічність. Але в останні роки відзначається зміна етіологічної структури ГКІ, особливо у дітей [5].
Найпоширеніша причина виникнення ГКІ – віруси. Кількість спровокованих ними хвороб значно перевищує ураження кишечнику, викликані сальмонелами, шигелами, патогенними штамами кишкової палички [1]. Сучасний стан епідеміологічної ситуації з кишковими інфекціями вимагає від лікарів усіх напрямків концентрації знань та досвіду для подолання цієї проблеми [9]. Необхідна модифікація принципів лікування: широке застосування антибіотиків вже залишається в минулому, противірусні препарати не розроблені. Тому основна увага приділяється симптоматичному лікуванню, а саме – призначенню сорбентів, про- і пребіотиків [1].
За рекомендаціями ВООЗ, важливим складником у лікуванні ГД є пероральна регідратація, проте така терапія спрямована лише на подолання наслідків зневоднення організму й не зменшує частоту, об’єм випорожнень та тривалість діареї [1].
У наукових публікаціях останніх років (що стосуються різних медичних галузей) велика увага приділяється питанням дефіциту макро- та мікроелементів і їх впливу на розвиток різних патологічних процесів [6]. Незважаючи на низький вміст мікроелементів в організмі, їх значення для нормального перебігу фізіологічних процесів важко переоцінити. Фізіологічне значення мікроелементів у першу чергу зумовлене їх роллю в складі ферментативних систем організму, оптимальне функціонування яких великою мірою залежить від надходження мікроелементів із навколишнього середовища. Особливу роль має цинк, який є одним із найбільш багатофункціональних мікроелементів [7].
Цинк являє собою незамінний мікроелемент, що міститься в усіх клітинах організму та бере участь у різних біологічних процесах, таких як синтез і стабілізація нуклеїнових кислот і білків, процеси енергетичного обміну, проліферації та диференціювання клітин, підтримка антиоксидантного статусу. Добова норма споживання цинку залежить від віку та становить: 2 мг для дітей від 0 до 6 місяців, 3 мг – для дітей від 7 місяців до 3 років, 5 мг –для дітей від 4 до 8 років, 8 мг – для дітей від 9 до 13 років та 9-11 мг – для підлітків старше 14 років [8]. Надходження цього мікроелемента до організму відбувається переважно з їжею й у значно меншій кількості – з водою. Серед продуктів, що містять цинк, найбільший його вміст мають устриці, менший – червоне м’ясо, м’ясо птиці, квасоля, горіхи, деякі види морепродуктів (такі як краби та омари), цільнозернові злаки, збагачені злакові сніданки і молочні продукти. Фітати, що присутні у цільнозерновому хлібі, крупах, бобових та інших продуктах харчування, зв’язують цинк і гальмують його засвоєння, через що біодоступність цинку з зерна та рослинної їжі нижча, ніж із продуктів тваринного походження [9].
Дефіцит цинку супроводжується комплексом порушень, що обумовлюються його різнобічними фізіологічними функціями. В організмі людини практично весь цинк (99,9 %) міститься у тканинах і лише 0,1% – у плазмі крові [10]. Цинк необхідний для каталітичної активності понад 200 металоферментів, задіяних у різних метаболічних шляхах, таких як ДНК- та РНК-полімераза, дегідрогеназа, карбоксипептидаза, фосфатаза, супероксиддисмутаза, алкогольдегідрогеназа, піруваткарбоксилаза. У молекулах металоферментів цинк може входити до складу активного центру. Крім того, він входить до складу великої групи неферментних металопротеїнів, у молекулах яких катіони мікроелемента беруть участь у стабілізації вторинної та третинної структур [11]. Цинк впливає на всі види обміну, сприяє стабільності клітинних мембран, бере участь у забезпеченні клітинного метаболізму, становленні та реалізації імунних реакцій [12]. На тлі запальних процесів у кишечнику всмоктування цинку зменшується, швидше за все, під впливом інтерлейкіну-1 [13].
Значення цинку як есенціального ростового фактора для нижчих грибів було вперше показане в 1869 році, але лише через 70 років було встановлено, що цинк входить до складу карбоангідрази і відіграє важливу роль у біохімічних процесах, які відбуваються в організмі людини. Таким чином, цинк – важливий компонент багатьох металоензимів, що беруть участь у різноманітних метаболічних процесах [3]. Оскільки загальний вміст цинку в організмі зберігається в основному в кістках, м’язах, шкірі (вільного цинку в організмі немає), потреби в ньому задовольняються постійним надходженням із продуктів харчування [14]. У людей із дефіцитом цинку виявляються специфічні ураження, такі як акродерматит, підвищена ламкість волосся, повільна регресія шкірних симптомів та загоєння ран [15]. Експериментальні дослідження на мишах показали, що дефіцит цинку може викликати подібні до ознак акродерматиту зміни шкіри, при цьому чим більший дефіцит цинку, тим ширші та серйозніші ураження шкіри. Враховуючи імунологічні ефекти цинку, можна припустити, що його дефіцит призведе до дисбалансу в імунній системі. Це припущення підтверджене в дослідженнях [16-21], які показали, що дефіцит цинку призводить до дисбалансу між Th1- і Th2-клітинами. Саме тому розвиток імунопатологічних реакцій, що лежать в основі алергії, пов’язаний із дефіцитом цинку.
Цинк є незамінним мікроелементом для людини. Цикл розвитку клітини потребує наявності цього мікроелемента. Проникність клітинних мембран також пов’язана з цинком. Цей мікроелемент має антиоксидантні властивості і затримує апоптоз (програмовану загибель) периферичних клітин. У період загострень запального процесу в слизовій оболонці кишечнику підвищується потреба в цинку (відбувається мобілізація мікроелемента з крові), чим забезпечується репарація й інтенсивне оновлення кишкового епітелію [23]. Від забезпеченості організму цинком залежить становлення імунітету, при його дефіциті має місце атрофія тиміко-лімфатичної системи. Цинк входить до складу інсуліну, прискорює регенерацію слизового шару кишечнику, підвищує активність ферментів щіткової облямівки слизової оболонки кишкового тракту, збільшує рівень секреторних антитіл і напруженість клітинного імунітету [24].
Отже, цинк – один з найважливіших мікроелементів, необхідних людині протягом усього життя, починаючи з внутрішньоутробного періоду і до глибокої старості. Він входить до групи так званих есенціальних або незамінних мікроелементів, до яких також відносяться залізо, йод, мідь, селен, марганець та ін. Запаси цинку в організмі людини досить малі – близько 1,5-3 г. Його кількість залежить від багатьох факторів: віку, статі людини, стану слизової оболонки шлунково-кишкового тракту, наявності супутніх захворювань, вагітності та ін. [22]. Цинк міститься практично в усіх органах і тканинах. За даними багатьох дослідників [22], в організмі людини цинк розподілений таким чином (мкг/г): шкіра, наднирники – 6, яєчники – 12, мозок – 13, лімфовузли – 14, шлунково-кишковий тракт – 21, серце – 27, нирки – 37, печінка – 38, м’язи – 48, кістки – 66, передміхурова залоза – 87, сперма – 125. Цілісна кров містить близько 2,5-5,3 мкг/мл цинку. У плазмі його менше – 0,7-1,2 мкг/мл (близько 0,2-1% від загального вмісту в організмі). У сироватці крові цинку міститься трохи більше (1,1-1,3 мкг/мл), ніж у плазмі, за рахунок зруйнованих тромбоцитів і більшої концентрації [22].
Дія цинку відбувається переважно в тонкій кишці, де він пригнічує індуковану 3-5-цАМФ-хлоридзалежну секрецію рідини [23]. Пригнічення цАМФ-індукованої секреції хлоридів пов’язують із пригніченням базолатеральних калієвих канальців, але без вираженого впливу на кальцій-опосередковані калієві канальці. Чутливі до цинку рецептори виступають тригерами вивільнення внутрішньоклітинного кальцію і регуляції іонного транспорту. Цинку притаманна бактеріостатична дія, яка реалізується через регуляцію експресії генів per і ler. Так, у дослідженнях in vitro цинк у концентрації 0,5-1 ммоль/л пригнічував ріст ентеропатогенних Escherichia coli, а через пригнічення експресії BFP і EspA знижувалася адгезія патогенної кишкової палички до епітелію кишечнику [25]. Відомо, що цинк необхідний для забезпечення бар’єрної функції мембран. Результати досліджень свідчать, що дефіцит цинку збільшує проникність міжклітинних сполук епітелію кишечнику, зокрема в ділянках щільних та адгезивних сполук. Це, у свою чергу, супроводжується посиленням міграції нейтрофілів, збільшенням продукції прозапальних цитокінів і надмірним прогресуванням запальної реакції. Така ситуація призводить до розвитку ускладнень, затяжного або хронічного перебігу запального процесу в кишечнику [26]. Аналогічним чином дефіцит цинку порушує гомеостаз шкіри. Нестача цього мікроелемента призводить до підвищення проникності, зокрема, рогового шару та щільних сполук. Одним із наслідків такого дисбалансу може бути розвиток атопічного дерматиту [27].
Також виявлений механізм негативного зворотного зв’язку під час розвитку запальної реакції, що реалізується наступним чином: активація NF-κB призводить до посилення активності мембранного транспортеру ZIP8, збільшуючи надходження цинку до клітини та забезпечення регулювання проінфламаторної відповіді [28].
На сьогодні існує багато підтверджень активної участі цинку в реалізації протимікробної функції клітинами макрофагального ряду. Ці клітини першими стають на шляху патогенів, їх завданням є фагоцитоз і передача сигналу подальшої активації імунної відповіді. На рівні макрофагів цинк відіграє важливу роль у механізмах захисту від внутрішньоклітинних збудників. Не менш важливою є його роль у реалізації протимікробного захисту іншою ланкою імунітету – нейтрофілами. Нейтрофіли відомі як головні клітини, що швидко мобілізуються в зоні вторгнення патогену. Вони здатні синтезувати різні захисні молекули, зокрема дефензини, катіонні антимікробні пептиди, протеолітичні ферменти та хелатори металів. Одним із найпоширеніших і потужних елементів серед них є кальпротектин (гетеродимер протеїнів S100A8 та S100A9). У нормальних умовах він представлений у цитозолі у вигляді неактивних мономерів і не реагує з цинком. При зустрічі з мікроорганізмом нейтрофіли створюють комплекси з молекул кальпротектину, що приєднують іони цинку та набувають активного біостатичного потенціалу [29]. Цинк також відіграє важливу роль у формуванні Т-клітинного імунітету. Мікроелемент є кофактором ферменту, що утворює активний тимулін, необхідний для дозрівання Т-лімфоцитів. Дефіцит цинку супроводжується зниженням кількості Т- та В-лімфоцитів у тимусі та кістковому мозку. Від забезпечення цинком залежить також баланс між Th1- та Th2-залежною імунною відповіддю. Відновлення дефіциту цинку призводить до зростання активності Th1-залежної функції [30]. Дефіцит цинку асоціюється з підвищенням продукції проінфламаторних цитокінів, зокрема IL-1β, IL-6 і TNF-α [31].
Сучасні теорії пов’язують розвиток багатьох захворювань із дефіцитом макро- та мікроелементів, а тяжкість перебігу діарейного захворювання – із вмістом цинку в організмі. Вивчення значення цього мікроелемента призвело до збільшення кількості досліджень його клінічного застосування. Сучасним обґрунтуванням призначення цинку для лікування захворювань, у тому числі інфекційного походження, є його дефіцит в організмі. Метою лікування в цьому випадку є відновлення балансу цього мікроелемента і, відповідно, покращення функції біологічних процесів, залежних від цинку. У випадку інфекційних захворювань зазвичай основний позитивний ефект очікується від поліпшення різних ланок імунологічної відповіді.
Препарати цинку застосовуються в медицині ще з давніх часів. Більше 3 тис. років тому людство застосовувало оксид цинку, відомий як каламін, для лікування ран. У подальшому різні солі цинку використовували при лікуванні епілепсії, хореї, як блювотний засіб при отруєннях і для зовнішнього застосування [25]. Досліджений у 60-х рр. минулого століття дефіцит цинку викликав інтерес у світлі клінічного застосування цього мікроелемента та сприяв проведенню численних досліджень у цьому напрямку.
Спектр захворювань інфекційної природи, при яких вивчалася ефективність препаратів цинку, є широким. Отримані переконливі дані щодо його ефективності при деяких захворюваннях, таких як інфекційні ураження шкіри, гострі респіраторні захворювання, кишкові інфекції. При цьому ефект цинку був продемонстрований не тільки для лікування, але й для профілактики окремих захворювань.
Препарати цинку показані при лікуванні та профілактиці інфекційної діареї у дітей. Хоча механізм їх позитивного впливу в таких випадках остаточно не з’ясований, встановлено, що цинк відновлює цілісність бар’єра слизової оболонки та активність кишечнику з ентероцитами, сприяє виробленню антитіл та циркулюючих лімфоцитів проти кишкових збудників і впливає на іонні канали, діючи як блокатор калієвих каналів аденозинової 3-5-циклічної монофосфат-опосередкованої секреції хлору [32].
Дотепер проведено багато клінічних досліджень ефективності препаратів цинку при кишкових інфекціях у дітей. Зокрема, він допомагає скоротити тривалість та тяжкість діарейного синдрому. В одному з досліджень (Бангладеш) вивчалася роль цинку при лікуванні холери. Серед 179 дітей із підтвердженим діагнозом холера 90 з них отримували 30 мг цинку в поєднанні зі стандартною терапією, інші 89 пацієнтів контрольної групи лікувалися стандартними засобами. В основній групі частіше, ніж у групі контролю, реєструвалися випадки одужання впродовж 2 (49 проти 32%; р=0,032) та 3 днів (81 проти 68%; р=0,03). Під час лікування цинком спостерігалося скорочення тривалості діареї на 12% (64,1 проти 72,8 год; р=0,028) та на 11% зменшувався об’єм випорожнень (1,6 проти 1,8 кг/день; р=0,039) [33].
Великий систематичний огляд, присвячений застосуванню препаратів цинку при діареї у дітей, був опублікований у 2016 р. Автори включили до нього 33 дослідження із загальною кількістю пацієнтів 10 841. За результатами, у дітей старше 6 міс додавання цинку скорочувало середню тривалість ГД на 11,46 год (95% ДI від -19,72 до -3,19), персистуючої діареї – на 15,84 год (95% ДІ від -25,43 до -6,24). Під час такої терапії кількість дітей із тривалістю діареї понад 7 днів зменшувалася (ВР 0,73; 95% ДI 0,61-0,88). Автори зазначають, що більший ефект щодо скорочення тривалості діареї спостерігався серед дітей із гіпотрофією (M 26,39 год; 95% ДI від -36,54 до -16,23). Водночас результати аналізу свідчать, що у дітей перших 6 місяців життя препарати цинку суттєво не впливали на скорочення тривалості діареї (M 5,23 год; 95% ДI -4,00 до -14,45) та кількість дітей із персистенцією діареї понад 7 днів (ВР 1,24; 95% ДI 0,99-1,54) [32].
У рекомендаціях ВООЗ та ЮНІСЕФ із клінічного ведення діареї наведені результати багатьох рандомізованих клінічних досліджень, присвячених цій проблемі [22]. Встановлено, що призначення цинку при діареї в дозі 5-20 мг на добу протягом 10-14 днів не тільки зменшує її тривалість і тяжкість, а й запобігає виникненню подальших випадків гастроентеритів протягом, принаймні, 2-3 місяців [1].
З метою демонстрації впливу дефіциту цинку на перебіг інфекційної діареї у дітей раннього віку наводимо дані власного спостереження.
Обстежено 82 дитини перших 2 років життя, госпіталізовано до Запорізької обласної інфекційної клінічної лікарні із діагнозом ГКІ. Етіологія захворювання встановлена за допомогою специфічних досліджень випорожнень за результатами імунохроматографічного тесту Citotestrota (ТОВ «Фармаско»). Бактеріальна етіологія була підтверджена бактеріологічним досдіжденням випорожнень на кишкову патогенну групу та групу умовно-патогенних мікроорганізмів. Під час госпіталізації в стаціонар усім пацієнтам робили загальний та біохімічний аналіз крові (рівні сечовини, креатиніну, калію, натрію у сироватці крові), загальний аналіз сечі. Оцінювалися клінічні симптоми (частота і характер випорожнень, ступінь дегідратації та її тривалість, частота і характер блювання, тривалість діареї і блювання на 1-шу, 3-тю та 5-ту добу). Для оцінювання тяжкості перебігу ГКІ використовувалася бальна шкала оцінки тяжкості гастроентеритів, запропонована T. Vezikari, в якій враховано основні клінічні ознаки захворювання: гарячка, її тривалість, кратність і тривалість блювання, частота випорожнень та тривалість цього симптому, ступінь ексикозу.
Усім пацієнтам був проведений аналіз крові на 1-й, 3-й та 5-й день перебування в стаціонарі. Був визначений рівень цинку методом колометричного тесту з 5-бром-PAPS за допомогою тест-системи Globalscientific. Референтні показники рівня цинку в сироватці крові дорівнювали 63,8-110 мкг/дл (9,8-16,6 мкмоль/л), у новонароджених – 49,54-110 мкг/дл (7,6-15,3 мкмоль/л).
Учасники дослідження були розділені на дві групи: до основної входили пацієнти, у яких вміст цинку в крові був нижче референтного значення, до групи порівняння – інші обстежені діти. У результаті дослідження було виявлено, що серед обстежених пацієнтів з інфекційною діареєю 21 дитина (25,6%) мала знижену концентрацію цинку в сироватці крові (основна група), а 61 – у межах референтних значень (група порівняння).
Порівняльний аналіз клініко-лабораторних даних пацієнтів груп порівняння показав, що в першу добу стаціонарного лікування у пацієнтів (переважно старших – 7-24 місяці), в яких було виявлено недостатній вміст цинку, підвищилася температура тіла (фебрильні та гіпертермічні показники; р=0,006), був наявний виразний діарейний синдром (р=0,01) із патологічними домішками (р=0,08). Більшість дітей цієї групи була на штучному вигодовуванні (р=0,01) та мала в анамнезі епізоди діарейного захворювання (р=0,07). Крім того, хоча достовірні зв’язки між рівнем цинку та видом збудника діареї (віруси чи бактерії) відсутні, у пацієнтів з дефіцитом цинку частіше мав місце нейтрофільоз крові із зсувом лейкоцитарної формули вліво (р=0,02), що свідчить про наявність бактеріальної інфекції.
При дослідженні впливу дефіциту цинку на перебіг захворювання було з’ясовано, що на 3-ю добу перебування в стаціонарі у дітей основної групи практично вдвічі частіше зберігалася підвищена температура тіла (у 54% проти 30% у групі порівняння; р=0,08) та в 4 рази – анемія (у 40% проти 9% відповідно; р=0,04). На 5-ту добу госпітального лікування спостерігалися більш суттєві клінічні відмінності (рис. 1-3). Так, у пацієнтів із інфекційною діареєю, які в дебюті захворювання мали дефіцит цинку, в пізні терміни хвороби достовірно частіше зберігалося блювання (р=0,05), діарея (р=0,03) та виявлялися патологічні домішки у калі (р=0,03). Крім того, такі симптоми супроводжувалися лейкопенією у 43% (проти 6% у групі порівняння; р=0,04), що може свідчити про виснаження імунологічної відповіді на інфекційний збудник діарейного захворювання.
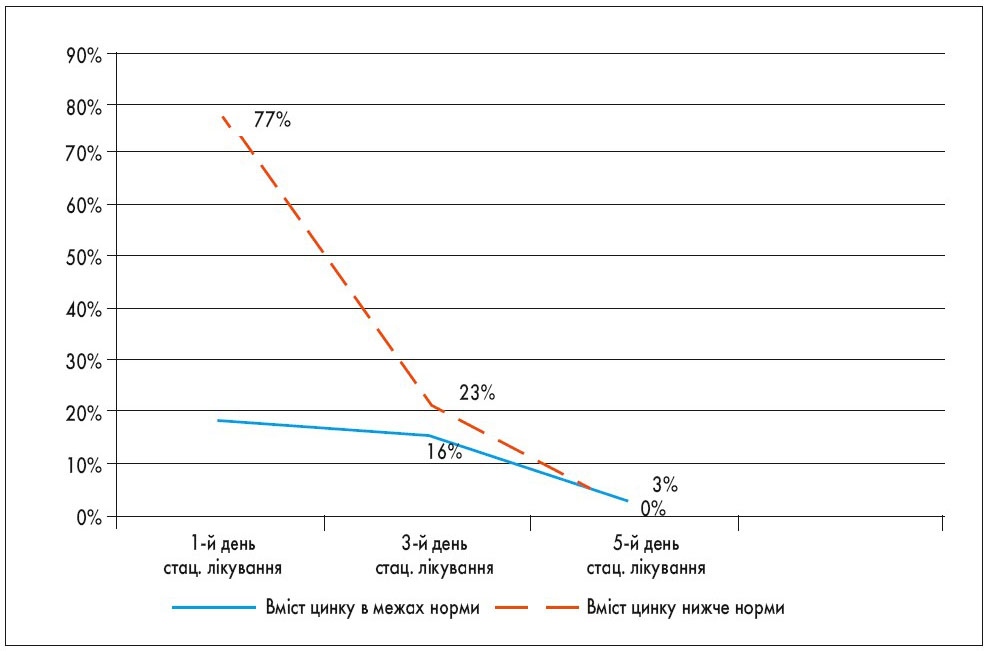 Рис. 1. Динаміка частоти блювання у пацієнтів групи спостереження
Рис. 1. Динаміка частоти блювання у пацієнтів групи спостереження
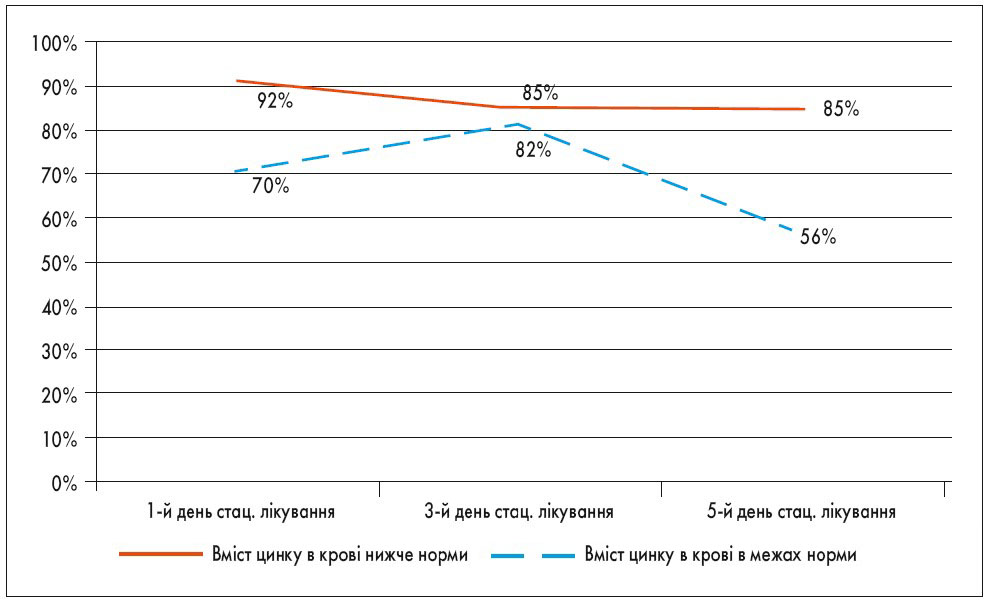 Рис. 2. Динаміка частоти діареї у пацієнтів групи спостереження
Рис. 2. Динаміка частоти діареї у пацієнтів групи спостереження
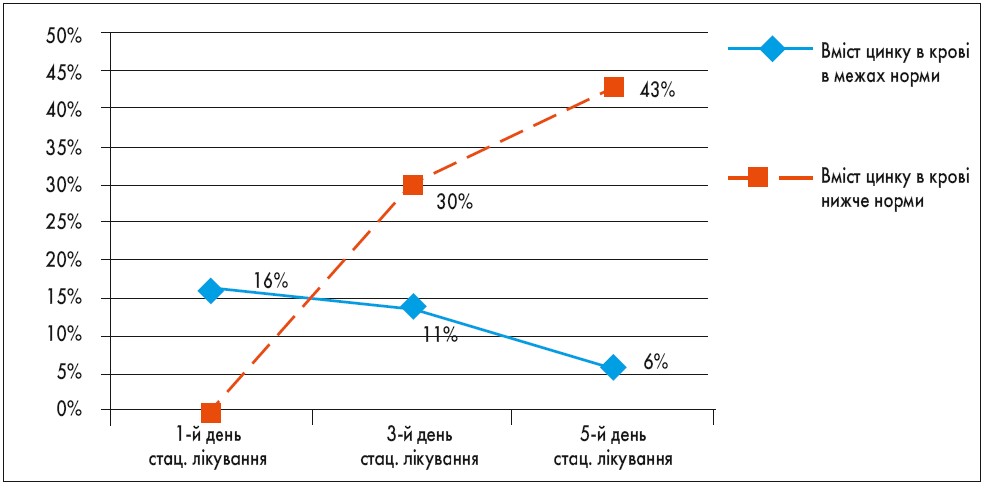 Рис. 3. Динамічні зміни частоти лейкопенії у дітей групи спостереження
Рис. 3. Динамічні зміни частоти лейкопенії у дітей групи спостереження
Підсумовуючи все вищесказане, можна зробити висновок, що цинк є важливим мікроелементом, необхідним для нормальної цілісності слизової кишечнику, транспорту натрію та води, для імунної функції [6]. На жаль, біля 30% населення планети має дефіцит цього мікроелемента [7], що підтверджено і нашими дослідженнями. Роль рівню цинку та його зв’язок із розвитком ГД у дітей вивчаються протягом останніх років у багатьох країнах, що розвиваються, а також у розвинених, що свідчить про потенційний ефект цинку в зменшенні ускладнень та смертності [7]. Наша робота також наочно демонструє взаємозв’язок між дефіцитом цинку та тяжкістю перебігу інфекційної діареї у дітей.
Сучасні рекомендації ВООЗ та UNICEF засвідчують необхідність використання цинку разом із пероральними регідратаційними солями та доглядом за пероральним годуванням [6]. При інфекційній діареї дітям до 6 місяців рекомендовано призначати цинку сульфат моногідрат у дозі 10 мг на добу, дітям з 6 місяців та дорослим – 20 мг на добу. Тривалість лікування становить 10-14 днів.
- У світі та в Україні зокрема кожна 4-та – 5-та дитина раннього віку з інфекційною діареєю має дефіцит цинку.
- Вірогідно до дефіциту цинку призводять особливості його всмоктування з їжі та його метаболізму: діти, що перебувають на ранньому штучному вигодовуванні, в анамнезі мають епізод діарейного захворювання, лабораторні ознаки анемії та дефіцит цинку.
- У дебюті діарейного захворювання недостатність забезпечення цинком асоціюється зі значним підвищенням температури тіла та виразним діарейним синдромом на тлі суттєвого нейтрофільозу крові із зсувом лейкоцитарної формули вліво.
- Дефіцит цинку в дебюті інфекційної діареї призводить до тривалої температурної реакції та тривалого (понад 5 діб) діарейного синдрому.
- До комплексу терапії інфекційної діареї у дітей слід включати препарати цинку у відповідних вікових дозах.
Література
- Надрага О.Б., Поцілуйко Н.М. Препараты цинка в комплексном лечении острых диарей у детей // Здоровье ребенка. – 2011. – 4 (31). – С. 104 -106.
- Хохлова Н.І, Краснова Є.І., Проворова В.В., Васюнин А.В., Патурина Н.Г. Острые кишечные инфекции вирусной и бактериальной этиологии у детей: современные возможности диагностики и терапии, роль метабиотиков//Лечащий врач. – 2018. – (06) https://www.lvrach.ru/2018/06/15437003/
- Голубовська О.А., Крамарьов С.О. Ротавирусная инфекция: современное состояние проблемы//Здоровье ребенка. – 2019. – Т. 14. – № 4 http://www.mif-ua.com/archive/article/4798124.
- Плоскірєва А.А. Пробиотическая терапия при острых кишечных инфекциях у детей//Лечащий врач. – 2018; (06). – https://www.lvrach.ru/2018/06/15436996/.
- Боровицька А.І., Беломеря Т.А., Данилюк А.Н., Думчева Т.Ю., Ткаченко І.М., Захарова Л.А., Заяц В.Ю. Актуальные вопросы острых кишечных инфекций в последние годы//Актуальна інфектологія. – 2014. – № 1 (2). – С. 21-26.
…
33. Roy S.K., Hossain M.J., Khatun W., Chakraborty B., Chowdhury S., Begum A. et al. Zinc supplementation in children with cholera in Bangladesh: Randomized controlled trial. BMJ. 2008 Feb 2. – 336 (7638). – Р. 266-8.
Повний список літератури знаходиться в редакції.
Тематичний номер «Педіатрія» №4 (55) 2020 р.



