1 листопада, 2020
Рецидивуючий ангіоневротичний набряк: сучасне розуміння та диференційна діагностика
Ангіоневротичний набряк (АНН) – це поліетіологічна патологія, яка характеризується набряком глибоких шарів шкіри, підшкірної або підслизової клітковини внаслідок збільшення проникності кровоносних судин та переходу плазми у міжклітинний простір. Локалізація набряку може бути різною: обличчя (повіки, губи), язик, кінцівки, статеві органи, шлунково-кишковий тракт, дихальні шляхи. В останньому випадку патологія є загрозливою для життя, адже ларингеальні напади, які призводять до асфіксії, є основною причиною смерті таких пацієнтів. Для клініцистів особливий інтерес становить рецидивуючий АНН, коли часті епізоди набряку чергуються із безсимптомними періодами.
Протягом останніх років уявлення про етіопатогенез рецидивуючого АНН суттєво змінилося. Так, нарешті вдалося спростувати тісний зв’язок АНН та алергії. Як результат, ефективність рутинної алергодіагностики, елімінаційної дієти та деяких методів лікування підпадає під сумнів. Розрізняють два види АНН: індукований медіаторами мастоцитів (анафілаксія, кропив’янка) та брадикінін-індукований (набутий та спадковий). В їх основі лежать абсолютно різні механізми, тому їх лікування потребує різних підходів. Проте в обох випадках основним інструментом лікаря є детальний збір анамнезу захворювання та спадкового анамнезу.
 За підтримки фармацевтичної компанії «Такеда» відбувся вебінар «Рецидивуючий ангіоневротичний набряк: сучасне розуміння та диференційна діагностика», у рамках якого професор Маркус Маґерль (відділення дерматології, венерології та алергології університетської клініки «Шаріте» у Берліні, Німеччина) на основі власного досвіду та знань про патогенетичні механізми обґрунтував принципи диференційної діагностики рецидивуючого АНН.
За підтримки фармацевтичної компанії «Такеда» відбувся вебінар «Рецидивуючий ангіоневротичний набряк: сучасне розуміння та диференційна діагностика», у рамках якого професор Маркус Маґерль (відділення дерматології, венерології та алергології університетської клініки «Шаріте» у Берліні, Німеччина) на основі власного досвіду та знань про патогенетичні механізми обґрунтував принципи диференційної діагностики рецидивуючого АНН.
– Основним клінічним критерієм для встановлення діагнозу рецидивуючий АНН є періодичність виникнення епізодів раптового набряку, між якими є проміжки часу, коли пацієнт не має жодних скарг. Складність своєчасного встановлення діагнозу полягає в тому, що на момент звернення таких пацієнтів до лікаря вони мають здоровий вигляд. Саме тому ретельний збір анамнезу захворювання у хворих на рецидивуючий АНН має дуже велике значення.
АНН характеризується появою локального, асиметричного (рідко – двостороннього) щільного набряку, без зміни кольору над патологічним вогнищем (інколи виникає незначна гіперемія) з/без свербежу. Деякі пацієнти відзначають поколювання, відчуття оніміння в зоні набряку. Симптоми АНН зникають самостійно протягом 72 годин без будь-яких залишкових явищ.
За патогенетичним механізмом АНН розрізняють індукований медіаторами мастоцитів та брадикінін-індукований.
АНН, індукований медіаторами тучних клітин
До цього типу АНН належать анафілаксія та кропив’янка (гостра/хронічна спонтанна, індукована кропив’янка). Пацієнтам із уртикарним висипом та набряком, які можуть виникати як одночасно, так і в різні проміжки часу, а також особам із ізольованим уртикарним висипом чи АНН встановлюється діагноз кропив’янка. В основі цих станів лежить дегрануляція мастоцитів та вивільнення медіаторів запалення, зокрема гістаміну, котрий і спричиняє появу симптомів.
Якщо у випадку гострої кропив’янки труднощів із діагностикою та лікуванням захворювання не виникає, то хронічна кропив’янка, яка триває понад 6 тижнів, є актуальною медичною проблемою. Раніше вважалося, що причинами хронічної кропив’янки можуть бути стрес, інфекції, непереносимість деяких продуктів чи ліків. Багатьом пацієнтам встановлювали діагноз хронічна ідіопатична кропив’янка через те, що не вдавалося ідентифікувати конкретну причину захворювання. Проте за останні роки накопичено багато нових знань, тому ця концепція вже застаріла та неактуальна.
Відомо, що у більшості пацієнтів в основі захворювання лежать аутоімунні або аутоалергічні процеси. У сироватці крові таких пацієнтів присутні антиIgE-IgG. Зв’язування IgG з IgE на поверхні рецептора або безпосередній вплив IgG на FCε-рецептори мастоцитів призводить до їх дегрануляції та вивільнення медіаторів запалення. Нещодавно стала відома аутоалергічна природа хронічної кропив’янки, що полягає у продукції аутоалергенспецифічних IgE проти власних клітин. Таким чином, стрес, інфекція, непереносимість продуктів харчування чи ліків є не причинами захворювання, а тригерами, які запускають аутоімунні чи аутоалергічні процеси.
Це відкриття внесло свої корективи в діагностику та лікування патології. Згідно з сучасними настановами, алгоритм діагностики хронічної кропив’янки включає загальний аналіз крові та визначення рівня С-реактивного білка (для виключення інших тяжких захворювань). Не рекомендоване рутинне призначення елімінаційної дієти, алергологічних тестів для пошуку конкретного чинника патології. Важливе значення також має контроль активності захворювання (за допомогою опитувальників у вигляді щоденника).
Брадикінін-індукований АНН
У просвіті судин, крім клітин крові та плазми, міститься група білків, об’єднаних у єдину кінінову систему. Каскад реакцій, які відбуваються в результаті поступової активації цих протеїнів, призводить до утворення брадикініну – пептиду з дуже короткою тривалістю дії, який за кілька секунд розщеплюється за допомогою 5 ензимів, серед яких – ангіотензинперетворюючий фермент (АПФ). Брадикінін впливає на судинну стінку шляхом зв’язування з брадикініновими рецепторами. Цей пептид у дуже малій кількості постійно синтезується в людському організмі та бере участь у регуляції артеріального тиску, процесах запалення, передачі больових сигналів тощо. Синтез брадикініну починається з активації фактору згортання крові ХІІ (ф. ХІІ), а далі відбувається каскад реакцій: активований ф. ХІІ – прекалікреїн – калікреїн (водночас активує ф. ХІІ) – кініноген – брадикінін – інактивовані метаболіти. Порушення функціонування кінінової системи призводить до розвитку патології (рис). Виділяють спадковий та набутий брадикінін-індукований АНН.
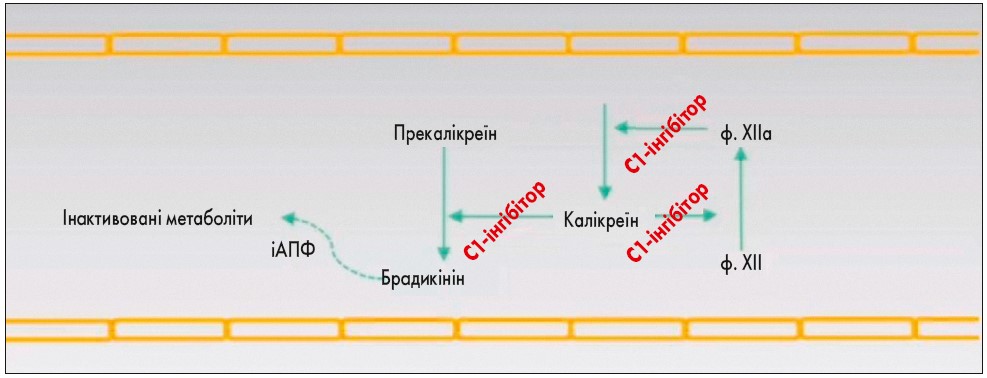 Рис. Патогенез брадикінін-індукованого АНН
Рис. Патогенез брадикінін-індукованого АНН
Набутий брадикінін-індукований АНН
Сьогодні частою причиною появи набутого брадикінін-індукованого АНН є застосування інгібіторів АПФ (іАПФ), котрі беруть участь в інактивації брадикініну. Це призводить до надлишку пептиду в крові, який підвищує проникність судинної стінки, через що відбувається перехід плазми з судинного русла у міжклітинний простір та розвивається місцевий набряк.
У більшості випадків АНН розвивається через 2 тижня після початку лікування іАПФ, проте існують випадки, коли патологія виникає через кілька років антигіпертензивної терапії, яку пацієнт раніше добре переносив. Типовими локалізаціями набряку, індукованого іАПФ, є обличчя (особливо губи та щоки), язик, м’яке піднебіння, увуля, горло, що робить цей стан небезпечним для життя.
Слід підкреслити, що іАПФ-індукований АНН – це не алергія на конкретний препарат, а побічний ефект усього фармакологічного класу в конкретного пацієнта.
Також виділяють набутий АНН внаслідок дефіциту С1-інгібітора, який зустрічається вкрай рідко і виникає здебільшого в осіб 50-70 років. Хворі мають такі ж клінічні прояви та лабораторні показники, що і пацієнти зі спадковим АНН І типу, проте спадковий анамнез у них не обтяжений.
Спадковий брадикінін-індукований АНН
Виділяють 3 типи спадкового брадикінін-індукованого АНН (табл.):
- І – пов’язаний із дефіцитом С1-інгібітора;
- ІІ – пов’язаний із дефектом С1-інгібітора;
- ІІІ – з/без мутації в генах ф. ХІІ, плазміногену, кініногену, ангіопоетину.
За різними даними, поширеність спадкового брадикінін-індукованого АНН становить від 1:10 тис. до 1:100 тис. За власними підрахунками, поширеність патології у Берліні складає 1:57 тис. У 90% хворих перші симптоми захворювання з’являються від народження і до 21-річного віку, маніфестація патології в старшому віці спостерігається рідко.
Спадковий брадикінін-індукований АНН – це аутосомно-домінантне захворювання (у 20% виникає внаслідок спонтанної мутації), пов’язане із понад 500 мутаціями гена С1-інгібітора, розташованого в 11-й хромосомі.
У здорових осіб С1-інгібітор пригнічує активований ф. ХІІ та калікреїн, що забезпечує синтез малої кількості брадикініну. Відповідно при дефіциті чи зниженні функції С1-інгібітора втрачається контроль над калікреїн-кініновим каскадом, що супроводжується надлишковою продукцією брадикініну та появою типових клінічних проявів АНН.
На відміну від гістамін-індукованого АНН (кропив’янки), клінічні прояви спадкового АНН мають ряд особливостей, що ускладнює діагностику захворювання. Зокрема, при спадковому АНН майже в усіх пацієнтів розвивається набряк у черевній порожнині, зокрема кишечнику. Набряк стінки кишечнику може бути настільки сильним, що суттєво перекриває його просвіт аж до повної обтурації. У таких випадках клінічні прояви спадкового АНН нагадують «гострий живіт»: виникає нудота, блювання, порушення дефекації, різкий абдомінальний біль. Ці епізоди можуть тривати 2-5 днів. Нерідко через помилково встановлений діагноз гострий живіт таким пацієнтам проводять безпідставні хірургічні втручання.
При спадковому АНН може уражатися шкіра. На відміну від кропив’янки, яка характеризується появою типового уртикарного висипу (поодинокі або множинні пухирі різного розміру та форми, які трохи виступають над поверхнею шкіри та супроводжуються свербежем), у хворих на спадковий АНН може виникати кільцевидна еритема, яка не виступає над поверхнею шкіри.
При кропив’янці немає продромального періоду, а АНН з’являється раптово без будь-яких передвісників. У хворих на спадковий АНН часто виявляють продромальні ознаки, такі як зміна настрою (сум, неспокій, дратівливість, загальна слабкість тощо) та висип у вигляді кільцевидної еритеми. Часто шкірні прояви спадкового АНН ідентифікуються лікарями як прояв алергії. Це призводить до призначення необґрунтованого лікування та відтермінованого встановлення правильного діагнозу.
Спадковий АНН може супроводжуватися так званим ларингеальним нападом, який становить небезпеку для життя пацієнта. Асфіксія внаслідок набряку гортані є основною причиною летального наслідку захворювання. Своєчасне встановлення діагнозу та призначення адекватного лікування суттєво знижує ризик смерті від дефіциту/порушення функції С1-інгібітора.
При обстеженні особи з підозрою на наявність спадкового АНН важливе значення має ретельний збір спадкового анамнезу. При виявленні у пацієнта хвороби необхідно обстежити усіх кровних родичів.
Що стосується спадкового АНН ІІІ типу з нормальним рівнем С1-інгібітора, сьогодні відома лише незначна частина мутацій генів, які можуть спричинити розвиток захворювання. Велика частина мутацій залишається «за завісою» ідіопатичного спадкового АНН. АНН ІІІ типу є рідкісним захворюванням і має певні особливості (частіше хворіють жінки, є естроген-чутливим станом, достеменно невідомий вплив спадковості на розвиток хвороби). Найперше була відкрита мутація гена ф. ХІІ, при якій спостерігалася інтенсивніша активація ф. ХІІ, а отже, збільшена продукція брадикініну. Нещодавно була виявлена мутація гена плазміногену, яка супроводжується продукцією гіперреактивного білка та сприяє активації більшої кількості ф. ХІІ. Механізм впливу мутації гена кініногену на розвиток АНН ІІІ типу до кінця не відомий. Причиною АНН ІІІ типу також може бути мутація гена ангіопоетину – білка, який у нормі пригнічує рецептори брадикініну. В осіб з мутацією цього гена синтезується ангіопоетин зі зниженою інгібуючою активністю до рецепторів.
Пацієнти з АНН ІІІ типу та нормальним рівнем С1-інгібітора мають схожі клінічні прояви, що і пацієнти з АНН І/ІІ типів (частіше мають набряк язика, рідше – тканин у черевній порожнині, немає уртикарного висипу), а лікарські засоби не є тригерами захворювання. Діагноз встановлюється на основі клінічних симптомів, наявності мутацій генів або обтяженого сімейного анамнезу та факту резистентності до антигістамінних препаратів.
Професор Маркус Маґерль продемонстрував багато власних спостережень та клінічних випадків різних варіантів АНН, а також відповів на поширені запитання. Повна версія онлайн-вебінару доступна за посиланням http://medical-space.com.ua/immunology/educational-materials/vebinar_retsidivuyuchiy_anginonevrotichniy_nabryak/.
Таким чином, АНН – це патологія, яка потребує особливої настороженості лікарів та проведення ретельної диференційної діагностики. Оскільки на момент звернення пацієнти з рецидивуючим АНН не мають жодних скарг, анамнестичні дані дають змогу проаналізувати тривалість захворювання, періодичність епізодів, наявність схожих симптомів у інших членів сім’ї. Хворі без встановленого діагнозу мають високий ризик смерті, тому необхідно своєчасно розпізнати хворобу та призначити адекватне лікування.
Підготувала Ілона Цюпа
Тематичний номер «Педіатрія» №4 (55) 2020 р.




